Кандидат химических наук, доцент
Тема 3. Дисперсные системы различных видов
Занятие 3. Микрогетерогенные системы. Заключение
Л е к ц и я
Саратов – 2010
СОДЕРЖАНИЕ
Введение
1. Эмульсии и суспензии.
2. Пены
3. Аэрозоли.
Заключение
ЛИТЕРАТУРА
основная
1. Фролов коллоидной химии. – М.: Химия, 1998. – С. 393-405.
2. Коллоидная химия. – СПб.: «Лань», 2003. – С. 194-310.
НАГЛЯДНЫЕ ПОСОБИЯ И ПРИЛОЖЕНИЯ
1. Слайды №№ 41-44
Пены.
Аэрозоли.
Эмульсии
ВВЕДЕНИЕ
Кроме рассмотренных уже коллоидных растворов, существуют другие классы дисперсных систем, свойства которых определяются поверхностными явлениями. К ним относятся суспензии, эмульсии, пены, аэрозоли и другие системы, средний размер частиц дисперсионной фазы которых достигает 100 нм и более, что может приводить к существенным различиям в некоторых свойствах систем. Остановимся на них более подробно.
1. ЭМУЛЬСИИ И СУСПЕНЗИИ
1.1. Эмульсии
Эмульсии – это дисперсные системы, образованные двумя взаимно нерастворимыми жидкостями.
Различают эмульсии неполярной жидкости в полярной (например, эмульсия масла в воде) – эмульсии первого рода, или прямые, и эмульсии полярной жидкости в неполярной (например, вода в масле) – эмульсии второго рода, или обратные.
Эмульсии первого рода часто обозначаются м/в, где под буквой «м» подразумевается масло или иная неполярная жидкость, а под буквой «в» - вода или другая полярная жидкость. Эмульсии второго рода обозначают соответственно в/м. В особый класс выделяются эмульсии жидких металлов (ртути, галлия) в воде, поскольку в этом случае и дисперсная фаза, и дисперсионная среда ведут себя как полярные жидкости.
Тип эмульсий устанавливается очень легко путем определения свойств ее дисперсионной среды. Для этого либо определяют способность эмульсии смачивать гидрофобную поверхность, либо испытывают способность эмульсии окрашиваться при введении красителя, растворяющегося в дисперсионной среде, либо проверяют возможность эмульсии растворяться водой, либо, определяют электропроводность эмульсии. Если эмульсия не смачивает гидрофобную поверхность, разбавляется водой, окрашивается при введении водорастворимого красителя и обнаруживает сравнительно высокую электропроводность, то это эмульсия типа м/в. Наоборот, если эмульсия смачивает гидрофобную поверхность, не окрашивается водорастворимым красителем и не обнаруживает заметной электропроводности, то это эмульсия типа в/м.
В зависимости от концентрации дисперсной фазы эмульсии делят на разбавленные, концентрированные и высококонцентрированные. Разбавленные эмульсии, имеющие концентрацию дисперсной фазы до 0,1% (об.), отмечаются высокой дисперсностью (размер капель может быть менее 100 нм), седиментационно устойчивы, в них наблюдается броуновское движение, эффект Тиндаля, электрофорез, электроосмос и т. п. Интересно отметить, что разбавленные эмульсии второго рода флуоресцируют при облучении ультрафиолетовыми лучами и фосфоресцируют при взаимном перемещении слоев системы (перемешивании, переливании и т. п.). Последним объясняется «свечение» воды морей.
Концентрированными считаются эмульсии, в которых суммарный объем фазы не превышает 74% от общего объема системы. Это максимальная концентрация, которая соответствует плотной упаковке сферических капель одинакового размера при отсутствии их деформации. Такие эмульсии являются типичными грубодисперсными системами. Они легко седиментируют, а если эмульсия недостаточно стабилизирована, то происходит слияние капель дисперсной фазы – коалесценция. Так происходит отстаивание сливок в молоке, расслоение майонеза при длительном хранении и т. п. Устойчивы такие эмульсии только в присутствии эмульгатора.
Если концентрация дисперсной фазы превышает 74%, то эмульсию называют высококонцентрированной. В таких эмульсиях движение капель почти отсутствует, они существенно деформированы, дисперсионная среда приобретает вид тонких прослоек – эмульсионных пленок. Частицы дисперсной фазы уже не сферической формы, а напоминают соты, отличаясь от них неправильной формой многогранников. Эти эмульсии склонны к обращению фаз, при механическом воздействии на них происходит смещение частиц дисперсной фазы и разрывание дисперсионной среды – образуется новая дисперсная фаза и новая дисперсионная среда. Этим объясняется наличие в природе множественных эмульсий – эмульсий в эмульсиях (типа м/в/м, в/м/в, м/в/м/в и т. п.). Высококонцентрированные эмульсии иногда называются желатинированными.
Получают эмульсии как конденсационными, так и диспергационными методами (на практике чаще используют диспергирование).
Конденсационный метод.
Пар одной жидкости (дисперсная фаза) инжектируется под поверхность другой, образующей внешнюю фазу (дисперсионную среду). В таких условиях пар остается пересыщенным и конденсируется в виде капель размерами порядка 1 мкм. Эти капли стабилизируются в жидкость, содержащую соответствующий эмульгатор. Жидкость, которая должна быть диспергирована, нагревают в отдельном сосуде. Для контроля нагрева температуру и давление пара поддерживают постоянными при определенных значениях. На размер образующихся капель существенным образом влияют давление инжектируемого пара, диаметр впускного сопла и эмульгатор. Чтобы создать неизменные условия, в течение всего периода нагревания под соплом держат какую-либо жидкость, выполняющую вспомогательную роль. Когда температура и давление достигнут требуемых значений, сосуд, содержащий эту вспомогательную жидкость, быстро заменяют сосудом с той жидкостью, которая должна быть дисперсионной средой в приготавливаемой эмульсии. Жидкость выдерживают при постоянной температуре, а также осторожно перемешивают, чтобы обеспечить равномерность распределения центров каплеобразования. Даже при не очень высоких концентрациях эмульсий этим методом легко получают капли с размером до 20 мкм.
Диспергационные методы.
Существуют три метода: смешения, гомогенизации и коллоидной мельницы. Обычно аппаратура для приготовления эмульсий этими методами характеризуется широким интервалом производительности – от малых лабораторных до больших промышленных установок.
Метод прерывистого встряхивания. Легко продемонстрировать образование эмульсии, если пробирку, в которую налиты две жидкости, энергично встряхивать.
Брин (1920 г.) установил, что прерывистое встряхивание с постоянными интервалами между толчками гораздо более эффективно, чем непрерывное. Например, для приготовления эмульсии 60% бензола в 1% растворе олеата натрия необходимо непрерывное встряхивание в течение 7 минут. Такая же эмульсия может быть приготовлена посредством только пяти встряхиваний вручную в течение 2 минут, если интервалы между каждыми двумя толчками составляют 20 – 30 секунд.
При ручном встряхивании капли имеют шаровую форму и размер порядка 50-100 мкм. Для получения капель меньших размеров применяют более энергичное перемешивание. Капли определенных размеров образуются, если ввести перемешивание со строго фиксированной скоростью. Таким путем можно получить и большие капли. Однако если соседние частички жидкости движутся с разными скоростями или обладают высоким градиентом скоростей, эти большие капли будут распадаться на мелкие.
Коллоидные мельницы. В коллоидной мельнице эмульгирование происходит при выдавливании жидкости в узкий зазор между ротором, вращающимся с большой скоростью, и неподвижным статором.
Смешивающиеся жидкости поступают сверху через соответствующую трубу в полость статора, протекают через узкий зазор между поверхностями статора и ротора и, наконец, вытекают из мельницы. Ротор отцентрирован и может развивать скорость, равную 10000 – 20000 об./мин. Зазор между поверхностями ротора и статора может быть уменьшен до 0,0025 см. Вследствие большой скорости и малого зазора возникают большие касательные напряжения, которые в сочетании с центробежными силами обуславливают почти мгновенный разрыв жидкой струи на капли. Жидкость течет в зазор либо под действием собственного веса, либо под небольшим избыточным давлением.
Гомогенизаторы. Гомогенизаторы – устройства, в которых диспергирование жидкости достигается пропускание ее через малые отверстия под высоким давлением. Их используют для получения эмульсий с размерами капель 1 мкм и менее.
Образование эмульсий также проводят методами: эмульгирование звуком и ультразвуком, получение эмульсий электрическими методами, самопроизвольное эмульгирование.
Чтобы получить устойчивые эмульсии, в систему добавляют стабилизаторы, называемые в данном случае эмульгаторами.
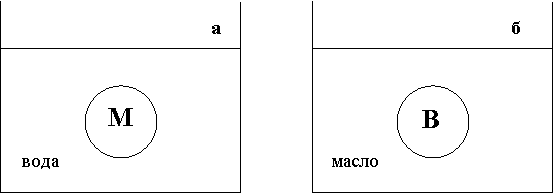
Эмульгаторами являются поверхностно-активные вещества, ВМВ, способные образовать на поверхности ориентированные абсорбционные слои с повышенной механической прочностью. Сюда относятся ионогенные и неионогенные мыла, белки, желатин, каучук и т. п. Тип образующейся эмульсии зависит, главным образом, от природы эмульгатора. Выбор эмульгатора определяется следующим положением: прямые эмульсии (м/в) стабилизируются водорастворимыми эмульгаторами, например желатином, мылами щелочных металлов, а обратные эмульсии (в/м) стабилизируются эмульгаторами, не растворимыми в воде, но растворимыми в маслах, например каучуком и другими высокополимерами, мылами с поливалентными катионами (Mg2+, Zn2+, Al3+) / На рисунке 1 представлена схема стабилизации прямых и обратных эмульсий с помощью поверхностно-активных веществ.
![]() << 1
<< 1
Рис. 1. Стабилизация прямых (а) и обратных (б) эмульсий
с помощью ПАВ
Стабилизаторами эмульсий могут быть не только вещества, растворимые в одной из фаз и способные понижать поверхностное натяжение, но и нерастворимые твердые эмульгаторы, порошки в состоянии большого измельчения. При этом гидрофильные порошки – мел, оксид железа, глина – стабилизируют эмульсии м/в, а сажа – в/м.
Если встряхивать минеральное масло с водой в присутствии глины, то можно допустить, что вначале образуются обе эмульсии – м/в и в/м. Однако частицы глины на границе раздела фаз для каждого типа эмульсии располагаются по-разному. В случае капелек воды частицы глины почти полностью втянутся внутрь капель, частицы не предотвращают слияния капель воды при столкновении (рис. 2.). На каплях же масла частицы глины, также почти полностью расположенные в воде, образуют броню – механически прочный слой, препятствующий слиянию капель.
 |
Рис. 2. Схема действия порошкообразных эмульгаторов
Эмульсию одного типа можно превратить в эмульсию другого типа. Такой переход называют обращением фаз или инвертированием эмульсий. Для обращения нужно изменить природу эмульгатора. Например, если к эмульсии бензола в воде, стабилизированной мылом щелочного металла, прибавить раствор хлорида кальция, то в результате реакции двойного обмена образуется нерастворимое в воде, но растворимое в бензоле мыло, которое стабилизирует эмульсию типа в/м.
В некоторых случаях возникает необходимость разрушения эмульсии или предупреждение ее образования. Для этой цели применяют различные способы, основными из которых являются: действие сильных минеральных кислот и их солей (высаливание); действие температуры; действие искусственного силового поля (седиментация); действие электрического поля (электрофорез) и действие низкомолекулярных ПАВ – деэмульгаторов. Например, полимер из латекса выделяют высаливанием или вымораживанием; для обезвоживания нефти и нефтепродуктов воздействуют электрическим полем, для этого используют центрифугирование; органические вещества при перегонке с водяным паром отделяют от воды высаливанием или действием деэмульгаторов и т. д.
В последнее время деэмульгаторы успешно используются для предупреждения образования эмульсии в процессах экстракции, в промышленных стоках, а также для удаления из сточных вод эмульгированных в них нефтепродуктов.
Эмульсии имеют большое практическое значение. Молоко, сливки, яичный желток, майонез, млечный сок растений, латекс – все это примеры типичных эмульсий. Жиры в кишечнике эмульгируются солями желчных кислот и всасываются через стенки кишечника в виде высокодисперсной эмульсии. В фармацевтической промышленности многие лекарства применяются в виде эмульсий, причем, как правило, для приема лекарств внутрь применяются эмульсии первого рода, а эмульсии второго рода используются для наружного применения.
1.2. Суспензии
Суспензии – это системы с твердой дисперсной фазой и жидкой дисперсионной средой. Можно дать и другое определение: суспензии – это взвеси порошков в жидкостях.
Суспензии разделяются по нескольким видам:
1.По размерам частиц дисперсной фазы: грубые суспензии (размер частиц более 1 ∙ 105 нм), тонкие суспензии (от 1 ∙ 105 до 500 нм), мути (от 500 до 100 нм).
2.По природе дисперсионной среды: органосуспензии (дисперсионная среда – органическая жидкость) и водные суспензии.
3.По концентрации частиц дисперсной фазы: разбавленные суспензии (взвеси) и концентрированные суспензии (пасты).
В разбавленных суспензиях частицы свободно перемещаются в жидкости, сцепление между частицами отсутствует и каждая частица кинетически независима. Разбавленные суспензии – это свободнодисперсные бесструктурные системы.
В концентрированных суспензиях между частицами действуют силы, приводящие к образованию определённой структуры (пространственной сетки). Таким образом, концентрированные суспензии – это связнодисперсные структурированные системы.
Суспензии могут быть получены диспергационными и конденсационными методами.
Наиболее простым и широко распространённым как в промышленности, так и в быту методом получения разбавленных суспензий является взбалтывание соответствующего порошка в подходящей жидкости с использованием различных перемешивающих устройств. Для получения концентрированных суспензий соответствующие порошки растирают с небольшим количеством жидкости.
При конденсационных методах необходимо помнить, что при небольших степенях пересыщения обычно образуются крупные частицы, при больших – мелкие. Предварительное введение в систему зародышей кристаллизации приводит к образованию практически монодисперсных суспензий. Уменьшение дисперсности может быть достигнуто в результате изотермической перегонки при нагревании, когда мелкие кристаллы растворяются, а за их счёт растут крупные. Дисперсность образующихся суспензий можно регулировать введением ПАВ.
Вследствие больших размеров частиц дисперсной фазы в суспензиях отсутствует броуновское движение, поэтому в них не происходит диффузия, и не наблюдается осмос и седиментационное равновесие.
В разбавленных суспензиях происходит быстрая седиментация (или флотация) с образованием слоя концентрированной суспензии и слоя просветленной жидкости.
Частицы дисперсионной фазы суспензии достаточно крупные (видны в обыкновенный микроскоп), поэтому лишь в сильно разбавленных взвесях можно наблюдать светорассеяние (эффект Тиндаля), а в концентрированных суспензиях это явление невозможно.
Так же, как для коллоидных растворов, для суспензий характерны электрические свойства. Следует заметить, что электрофорез и электроосмос впервые были обнаружены в глине (опыты Рейсса).
Интересным свойством суспензий является структурирование, выражающееся чрезмерно большой вязкостью системы и переходом при длительном покое в твердообразное состояние – гель. Структурирование объясняется вандерваальсовыми или электростатическими силами взаимодействия между частицами дисперсной фазы. Структуру такого геля можно разрушить встряхиванием или перемешиванием, тогда система вновь приобретает текучесть. Если систему оставить в покое, она опять перейдет в гель (потеряет текучесть). Это явление называется тиксотропией.
Тиксотропия имеет большое значение в промышленности и окружающей природе. Например, при бурении нефтяных скважин для предотвращения гелеобразования в промышленную воду вводят добавки, образующие с глиной тиксотропные системы, которые при движении инструмента остаются текучими. Краски и белила также должны быть тиксотропными: оставаться текучими и быстро «схватываться» после покраски.
Для суспензий характерен ряд процессов, не свойственных коллоидным системам или протекающим у последних иначе, чем у суспензий. К таким процессам относятся седиментация и флотации (о них мы говорили ранее), а также фильтрация и кольматация.
Фильтрация суспензий определяется дисперсностью и степенью агрегации частиц, а также образованием коагуляционной структуры и способностью ее к самоуплотнению в фильтрующем осадке. Поэтому фильтрация является сложным физико-химическим процессом, на который влияют все факторы, управляющие агрегированием частиц и развитием коагуляционных структур. Не менее сложен и процесс кольматации – «вмыв» мельчайших глинистых или илистых частиц в поры грунта для уменьшения водопроницаемости различных гидротехнических сооружений – дамб, плотин и т. д.
Для приобретения устойчивости суспензии необходим стабилизатор (чаще всего ПАВ или высокомолекулярные вещества, обладающие высокой вязкостью). В качестве примера рассмотрим процесс приготовления водной суспензии ДТС-ГК, стабилизированной жидким стеклом:
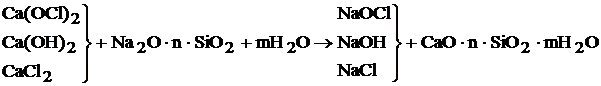
Образующийся гидросиликат кальция представляет собой гидратированный гель, достаточно устойчивый благодаря высокой вязкости системы.
Свойства этой системы зависят от концентрации жидкого стекла. При малой его концентрации (до 0,25%) образуется неустойчивое количество гидросиликата, а при повышенном содержании (более 2%) – из-за повышения вязкости – происходит потеря текучести. На практике берут на 100 л водного раствора ДТС-ГК 1 кг жидкого стекла. Нельзя нарушать последовательность растворения, т. к. нарушаются условия стабилизации.
В химической промышленности с суспензиями имеют дело при осаждении солей, их растворении, при выщелачивании, фильтрации. Суспензию образует твердый катализатор, если реакция проходит в жидкой фазе. Глинистые и известковые «растворы», красители, краски и многие другие материалы также представляют собой суспензии.
2. ПЕНЫ
Пенами называют дисперсные системы, в которых дисперсной фазой является газ, а дисперсионной средой жидкость (в случае жидких пен) или твердое тело (в случае твердых пен). Поскольку твердые пены получают застыванием жидких, т. е. они являются «продолжением» последних, остановимся на рассмотрении жидких пен. Так как разбавленные жидкие пены кинетически неустойчивы и не имеют практического значения, ограничимся рассмотрением только концентрированных пен.
Классификация пен основывается на такой важной характеристике как кратность пены:
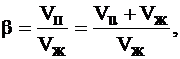
где Vп - объём пены;
Vж - объём жидкости, которая использована для получения пены.
Оба объёма легко измерить.
ГОСТ определяет условия, при которых следует определять кратность пены. В градуированный цилиндр ёмкостью 1000 мл следует налить 98 мл воды и 2 мл пенообразователя, закрыть пробкой и встряхивать в течение 30 секунд. Поставить на стол, вынуть пробку, измерить объём паны. Отношение объёма пены к объёму раствора (100мл) и есть кратность пены.
Таким образом, кратность пены показывает, сколько объёмов пены можно получить из одного объёма жидкости. Если кратность пены больше 10, пены называют жидкими, а если кратность пены в пределах от 01.01.01 – сухими.
В строительстве и производстве стройматериалов используют пену с кратностью от 5 до 10, в прачечных – с кратностью от 10 до 20. Для пожаротушения применяют пены с кратностью от 70 до 90. Известны также пены с кратностью до 1000.
Пена, как и любая дисперсная система, может быть получена двумя способами: объединением очень мелких (микроскопических) газовых пузырьков в более крупные (метод конденсации) или дроблением крупных воздушных пузырей и включений на более мелкие и устойчивые (метод диспергирования).
Конденсационный метод почти мгновенного вспенивания служит наглядной иллюстрацией закона газового состояния: при повышении давления или понижении температуры растворимость газа в жидкости увеличивается (закон Генри). Если снизить давление или повысить температуру, то газ сразу начнет выделяться и вспенит жидкость. На этом «эффекте открывания бутылки» основан один из методов вспенивания.
Диспергационный метод основан на получении пены в результате дробления и распределения воздуха или газа в растворе с пенообразователем. Обычно небольшие порции газа вводят в раствор и дробят их там до размеров мелких пузырьков.
В пеногенераторах вспенивание может происходить на сетках. Раствор пенообразователя под давлением выбрасывается из распылителя, попадает в виде капель на ячейки сетки и смачивает их. Поток воздуха, подаваемого вентилятором, выдувает на ячейках сетки пузырьки пены. Эти пузырьки отрываются от сетки и образуют пену с мелкими однородными парами – пену громадной кратности (1000 и более) и высокой стойкости. Такие пеногенераторы производят до 15000 л пены в секунду, а дальность полета струи достигает 8-12 м.
Устойчивость пены – это показатель, характеризующий продолжительность существования всего первоначального объема пены. Чтобы количественно оценить устойчивость пены, определяют скорость ее разрушения. Для устойчивых пен – это время, за которое разрушается 20% первоначального объема, для неустойчивых – время, за которое пена разрушается полностью. Во всех пенах происходит три основных процесса, приводящих постепенно к разрушению пены: перераспределение размеров пузырьков, уменьшение толщины пленки, разрыв пленки.
Эти процессы быстро разрушали бы пены, если бы не стабилизирующие факторы. Этих факторов три: кинетический, структурно-динамический и термодинамический.
Кинетический фактор замедляет процесс утончения пленок и способствует повышению жизнеспособности пен.
Структурно-механический фактор стабилизации пен связан со специфическим упрочнением тонких пленок за счет гидратации адсорбционных слоев, а также за счет повышения вязкости межпленочной жидкости.
Термодинамический фактор (расклинивающее давление) проявляется в тонких пленках, когда возникает избыточное давление, препятствующее их утончению под действием внешних сил. Совместными усилиями химиков, технологов и механиков созданы новые ПАВ и стабилизаторы, а также разработана технология пенообразования, позволяющая получать высокократные пены, «время жизни» которых измеряется многими сутками. Для специальных целей производят пены, которые живут без заметного разрушения 4 – 5 месяцев. Если использовать в качестве стабилизаторов полимерные смолы, можно создать пены, срок жизни которых составляют годы.
Мыльный пузырек или пена по своей природе не стабильны и склонны к самопроизвольному разрушению. Эта нестабильность объясняется избытком поверхностной энергии, пропорциональной поверхности раздела газ – жидкость. Таким образом, пузырьки пены и пленки пены лопаются потому, что площадь (и, следовательно, поверхностная энергия) полученной капли (или капель) меньше площади первоначальной системы.
Так, в пенах с толстыми стенками происходит интенсивное истечение жидкости из пленок, а в пенах высокой кратности (тонкостенных), а также в пенах, образованных вязкими жидкостями, разрушение вызывается в первую очередь диффузией газа.
Процесс истечения жидкости из пены под действием гравитационных сил называют дренированием. Если сосуд наполнить пеной и оставить на некоторое время, то постепенно на дне собирается слой жидкости, который будет расти до тех пор, пока в пленках пены не останется совсем мало жидкости (или пока пленки не лопнут). Наиболее простой и действенный, а потому и самый распространенный способ повысить жизнеспособность пен – стабилизация пен специальными добавками. Это глицерин, этиленгликоль, метилцеллюлоза, желатин, клей, крахмал, агар-агар и др., которые увеличивают вязкость жидкости в пленках более чем в 100 раз, а устойчивость пен возрастает при этом в 2 – 8 раз.
Пены находят широкое применение, в частности, в процессах флотации руд металлов, твердого топлива и других полезных ископаемых. Пенная флотация частиц минералов происходит вследствие их адгезии к пузырькам воздуха, которые вместе с частицами поднимаются на поверхность раствора. Порода хорошо смачивается водой и оседает во флотомашинах. Флотационные реагенты по характеру действия делят на три класса: собиратели, регуляторы и пенообразователи. Собиратели способствуют адгезии частиц к пузырькам газа. Их молекулы имеют полярную часть, обладающую специфическим сродством к данному минералу, и неполярную – углеводородный радикал, который гидрофобизирует поверхность частицы и обеспечивает ее «сродство» к пузырьку газа. Регуляторы применяют для увеличения избирательности флотационного процесса: они изменяют рН (кислоты, щелочи), подавляют смачиваемость минералов и активизируют их флотацию (соли с флотационно-активными ионами), улучшают смачиваемость породы, уменьшают вредное влияние находящихся в пульпе ионов и т. д.
Пены способствуют очистке поверхностей от различных загрязнений.
Пены применяются для тушения пожаров. Огнегасящее действие пен состоит в охлаждении горячих предметов водой, содержащейся в пене, а также в преграждении доступа кислорода к ним. Пена всегда находится наверху и поэтому очень эффективна при тушении горючих жидкостей.
В ряде производств пены мешают нормальному протеканию процессов. Например, специальное пеногашение приводят в целлюлозно-бумажной, сахарной и фармацевтической промышленности. Пены часто мешают на стадиях фильтрования, центрифугирования, при выпаривании, дистилляции органических жидкостей, очистке сточных вод и т. д.
Пены гасят путем введения в системы специальных пеногасителей или механическими методами. Пеногаситель препятствует стабилизации пены, поэтому он должен быть более поверхностно-активен, чем пенообразователь, чтобы вытеснить последний или растворить структурированную пленку пены. В качестве пеногасителей используют природные масла и жиры, органические кислоты, спирты, эфиры, некоторые кремнийорганические и фосфорорганические соединения.
Из нехимических методов разрушения пен применяют механические, термические и акустические. Механические методы заключаются в разбивании пены с помощью мешалок, циклонов, дисков. Термический метод основан на испарении жидкости, находящейся в пленках пены. В акустических методах для разрушения пены используется ультразвук частотой до 1000 кГц.
3. АЭРОЗОЛИ
Аэрозоли – дисперсные системы с газообразной дисперсионной средой и взвешенными твердыми или жидкими частицами. По агрегатному состоянию и размерам частиц дисперсной фазы аэрозоли делят на туманы – системы с жидкой дисперсной фазой, размер частиц 10 – 0,1 мкм; пыли – системы с твердыми частицами размеров больше 10 мкм; дымы – размеры частиц находятся в пределах 10 – 0,001 мкм.
Туманы имеют частицы правильной сферической формы (результат самопроизвольного уменьшения поверхности жидкости), а пыли и дымы содержат твердые частицы самой разнообразной формы. К типичным аэрозолям относятся: водяной туман (размер частиц 0,5 мкм), топочный дым (0,1-100 мкм), дождевые облака (10-100 мкм), дым из ZnO (0,05 мкм), сернокислотный туман (1-10 мкм), дым из P2O5 (1 мкм). Частицы высокодисперсных аэрозолей участвуют в тепловом движении газообразной дисперсной среды.
Различают аэрозоли, образующиеся в земной атмосфере в результате протекания различных природных процессов и получаемые в результате производственной деятельности человека. Первые называются естественными, вторые – техническими. Технические аэрозоли образуются в процессе добычи и переработки руд, угля, измельчения материалов, производства цемента, сжигания топлива (особенно с большим содержанием золы) и др. Промышленные аэрозоли в подавляющем большинстве случаев крайне нежелательны, т. к. они создают угрозу здоровью человека и наносят ущерб природе. По мере развития промышленного производства борьба с такими аэрозолями становится все более актуальной задачей.
Подобно системам с жидкой дисперсной средой аэрозоли получают двумя способами – конденсацией и диспергированием. Рассмотрим наиболее употребительные диспергационные способы.
1. Разбрызгивание в электрическом поле. По этому способу аэрозоли получают распылением вещества, например, из пульверизатора, соединенного с одним из полюсов источника электрического напряжения. Получающиеся аэрозоли достаточно устойчивы. В настоящее время выпускаются промышленные аппараты для получения аэрозолей лекарственных веществ таким способом.
2. Распыление раствора сжатым воздухом. Этот способ один из самых старых. Для его осуществления используются пульверизаторы различных конструкций.
3. Разбрызгивание с помощью ультразвука. Этот метод позволяет получать аэрозоли с высокой концентрацией дисперсной фазы. Его используют для генерирования в воде аэрозолей водных растворов антибиотиков.
4. Разбрызгивание жидкостей ультрацентрифугой. Таким способом можно получать аэрозоли различных водных растворов в значительных объемах.
Из конденсационных методов рассмотрим следующие:
1. Адиабатическое расширение газа. Таким путём образуются облака. Тёплые массы влажного воздуха поднимаются в более высокие слои атмосферы. Поскольку там атмосферное давление ниже, происходит адиабатическое расширение, сопровождающееся охлаждением воздуха и конденсацией водяного пара. На относительно небольшой высоте образуются кучевые облака, в которых вода находится в виде жидких капель. В верхних же слоях атмосферы, где температура более низкая, возникают перистые облака, содержащие кристаллики льда.
2. Смешение газов и паров, имеющих разные температуры. Так образуются атмосферные туманы. Чаще всего туман появляется при ясной погоде ночью, когда поверхность Земли, интенсивно отдавая тепло, сильно охлаждается. Тёплый влажный воздух соприкасается с охлаждающейся Землёй или с холодным воздухом вблизи её поверхности и в нём образуются капельки жидкости. То же происходит при смешении фронтов тёплого и холодного воздуха.
3. Охлаждение газовой смеси, содержащей пар. Этот случай можно проиллюстрировать на примере чайника, в котором закипела вода. Из носика вырывается водяной пар, который невидим, поскольку не рассеивает свет. Далее водяной пар быстро охлаждается, вода в нём конденсируется, и уже на небольшом расстоянии от носика чайника мы видим молочное облачко – туман, ставший видимым из-за способности рассеивать свет. Более прочный аэрозоль образуется, когда закипевшее на сковородке масло создаёт в помещении газ (масляный аэрозоль), удалить который можно, лишь хорошо проветрив помещение.
Кроме того, конденсационный аэрозоль может образовываться в результате газовых реакций, ведущих к образованию нелетучих продуктов.
Принципиальное отличие аэрозолей от систем с жидкой дисперсной средой заключается в том, что длина свободного пробега молекул в газе может быть больше размеров частиц дисперсной фазы.
Согласно молекулярно-кинетической теории газов длину свободного пробега молекулы, равную среднему пути между столкновением ее с другими молекулами, вычисляют по уравнению
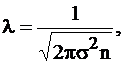
где ![]() – диаметр молекул;
– диаметр молекул;
n = P/kT – число молекул в единице объема (здесь k – диаметр молекул; T– температура, P - давление).
Следовательно, 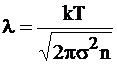
По порядку величины при атмосферном давлении длина свободного пробега молекул газа составляет около 10-7м. Длина свободного пробега молекул жидкости примерно равна их радиусу, т. е. по порядку величины близка к 10-10м.
При изучении молекулярно-кинетических свойств аэрозолей последние целесообразно разделить на два класса: аэрозоли с отношением длины пробега молекул к размерам частиц ![]() >> 1 и аэрозоли с
>> 1 и аэрозоли с ![]() << 1 удовлетворяет уравнению Стокса
<< 1 удовлетворяет уравнению Стокса

Уравнение Стокса не соблюдается при длине пробега, соизмеримой с размерами частиц. Для этого случая Кенингем предложил уравнение
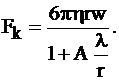
Значение постоянной A, входящей в это уравнение, было найдено Милликеном (A = 0,864).
Уравнение Стокса не соблюдается не только для очень малых аэрозольных частиц, но и для весьма крупных (больше 2030 мкм). Гидродинамическое сопротивление среды при оседании крупных частиц описывается уравнением Осеена:
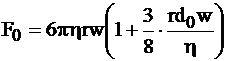 ,
,
где d0 – плотность среды.
Но эти формулы применимы только для описания движения твердых сферических частиц. Для аэрозолей с жидкой дисперсной фазой предложены уравнения, учитывающие вязкость дисперсионной среды.
Экспериментальные исследования подтверждают применимость теории броуновского движения Эйнштейна и Смолуховского. Однако и в этом случае необходимо учитывать отношение длины свободного пробега молекул к размерам частиц дисперсной фазы. При ![]() << 1 формула Энштейна-Смолуховского принимает вид
<< 1 формула Энштейна-Смолуховского принимает вид
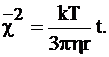
Для меньших частиц вводится поправка Кенингема, и формула приобретает вид
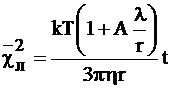
Аэрозольные частицы приобретают электрический заряд либо в процессе своего образования, либо находясь во взвешенном состоянии. Образование заряженных частиц наблюдается при разбрызгивании полярных жидкостей. Причина появления заряда у частиц, находящихся во взвешенном состоянии, - захват газовых ионов.
В атмосфере всегда присутствуют ионы, появление которых вызвано, в частности, действием естественной радиации. Для получения заряженных аэрозолей в промышленном масштабе концентрация атмосферных ионов недостаточна. В этих случаях ионизацию воздуха вызывают с помощью различных методов. Наиболее распространена ионизация с помощью коронного электрического разряда. Она положена в основу электроосадителей – аппаратов, предназначенных для очистки газов от частиц дисперсной фазы.
Промышленные установки, в которых применяется электростатическое поле для улавливания заряженных частиц, называются электрофильтрами. Катодом в них обычно служит металлический стержень. В зоне, примыкающей к катоду, происходит ионизация воздуха, и частицы заряжаются. Частицы, приобретающие заряд, осаждаются на поверхности металлической трубы, через которую пропускается аэрозоль. Эффективная работа электрофильтра требует весьма высокой разности потенциалов, достигающей нескольких сотен тысяч вольт.
Электризация аэрозолей в процессе получения придает им устойчивость, так как взаимное отталкивание одноименно заряженных частиц предотвращают коагуляцию. Аэрозоли, частицы которых имеют одинаковый по знаку заряд, называются униполярными. Униполярно заряженные аэрозоли применяются в медицине, сельском хозяйстве, промышленности (окраска в электростатическом поле и т. п.).
Оптические свойства аэрозолей подчиняются, в общем, тем же законам, что и оптические свойства лиозолей. Однако, вследствие большой разницы в плотностях и показателях преломления между фазами в лиозолях и аэрозолях, оптические свойства последних проявляются более интенсивно. Благодаря этому, аэрозоли применяются для создания дымовых завес, для защиты от теплового действия светового излучения при ядерном взрыве.
Аэрозоли – неустойчивые дисперсные системы, в которых интенсивное броуновское движение вызывает уменьшение концентрации частиц. Они не имеют факторов стабилизации, характерных для лиозолей. Однако во многих случаях скорость их естественной коагуляции недостаточна, а распределение частиц в пространстве нежелательно. Это в первую очередь относится к отходящим газам промышленного производства. Для очистки газов увеличивают число соударений частиц применяя звуковые колебания частотой 1-10 кГц. Иногда скорость коагуляции повышают, вводя в систему с газовой дисперсной фазой другой аэрозоль с более крупными частицами. Крупные частицы служат ядрами конденсации, на которых скапливаются мелкие частицы коагулируемого аэрозоля.
Коагуляция аэрозолей приводит к образованию в большинстве случаев довольно крупных агрегатов, образующихся при коагуляции, и крупных первичных частиц. Коагуляцию проводят в специальных камерах – пылеуловителях, в которых газовый поток с небольшой скоростью пропускается между двумя параллельными пластинами. Высоту камеры и скорость потока выбирают с таким расчетом, чтобы частицы определенного размера полностью оседали на нижней пластине.
Очистка от более мелких частиц достигается использованием центробежной силы. Широкое практическое применение нашли аппараты, называемые циклонами. Циклон – цилиндрический резервуар с коническим днищем. Газ, содержащий частицы дисперсной фазы, вводится в циклон по касательной к стенке цилиндра и, совершая вращательное движение в аппарате, выбрасывается в атмосферу или поступает на дальнейшую обработку. С помощью циклона удается осаждать частицы более 1 мкм.
Тонкая очистка газов от аэрозольных частиц достигается фильтрованием. Широко применяются бумажные, асбестовые и тканевые фильтры. Очень мелкие частицы отделяют от газовой фазы с использованием фильтров из пористых керамических материалов (поролитовые фильтры).
Одним из наиболее эффективных устройств для очистки газов является электрофильтр, в котором происходит прочное прилипание частиц к поверхности.
Следует отметить, что способность частиц прилипать к поверхности существенно влияет на работу очистного устройства. Смазки улучшают прилипание; влияют не только свойства смазочного материала, но и толщина его слоя на поверхности.
Осаждение жидких капель на поверхности, смоченной этой же жидкостью, приводит к слиянию капли с жидкостью. Однако столкновение жидких частиц с жидкой поверхностью или друг с другом может быть упругим. Отражение водных капель при столкновении наблюдал Релей, который установил некоторые особенности этого явления. На эффективность столкновений влияет, в частности, содержание газов, хорошо растворимых в воде. , показали, что слияние водных капель облегчается с повышением влажности газовой среды.
Эффективность использования аэрозолей в медицинской практике изучают в аэрозолях практически безвредных веществ (хлорида натрия, оксида железа и т. п.). С их помощью удалось установить степень осаждения частиц в дыхательной системе, как от размера частиц, так и от режима дыхания.
Частицы диаметром свыше 12 мкм практически полностью задерживаются в носовой полости. Степень осаждения в носовой полости частиц диаметром 4 мкм составляет около 50%. Поэтому для аэрозольной терапии легких оптимальная область размеров частиц 0,5 – 4 мкм.
Аэрозоли имеют большое практическое значение. Облака и туманы играют существенную роль в формировании климата; для здравоохранения актуальное значение имеют различные патогенные (бактерии и вирусы) и вредные аэрозоли, которые передают инфекционные и вызывают профессиональные заболевания; в биологии и сельском хозяйстве имеют значение перенос воздухом пыльцы растений, плесени, распыление удобрений препаратов для борьбы с вредителями растений, тепловая защита садов дымами: дымовые завесы применяются для маскировки и защиты от тепловых излучений при ядерных взрывах и т. д.
ЗАКЛЮЧЕНИЕ
Изучив основные закономерности и примеры, показывающие огромную роль дисперсных систем во многих научных направлениях и почти во всех отраслях народного хозяйства, можно более отчетливо и полно представить себе содержание курса. Изучение свойств реальных тел невозможно без разработки теории поверхностных явлений в самом широком смысле. С другой стороны, теория поверхностных явлений становится плодотворной лишь в том случае, если она приложена к реальным дисперсным системам. Эта неразрывная связь и лежит в основе предмета – химии и физики поверхностных явлений в дисперсных системах.
В нашем курсе сделана попытка изучения свойств дисперсных систем путем последовательного усложнения и конкретизации – от наиболее общих свойств поверхностного слоя, через учение о поверхностных силах и ориентации к явлениям адсорбции, электроповерхностным явлениям, необходимым для понимания устойчивости, и далее – к проблемам разрушения дисперсных систем и образования структур в системах различного типа. На основе этих позиций рассмотрены свойства важнейших классов дисперсных систем (золи, суспензии, эмульсии, пены, аэрозоли, ВМС и их растворы, коллоидные электролиты).
Мы старались установить связи и общие закономерности для различных явлений и систем с тем, чтобы выявить как можно полнее единство и цельность физико-химической дисциплины, изучающей дисперсионные системы и поверхностные слои. Эти слои на границе раздела фаз, обладающие особыми свойствами, являются той «почвой», где происходит взаимодействие реальных тел между собой и со средой, их окружающей.
Именно поэтому коллоидная химия является наукой, соединяющей различные отрасли знания. Каждый новый успех коллоидной химии способствует прогрессу в развитии других дисциплин, в том числе военно-химических наук и науки будущего – экологии.
Доцент кафедры ФОХ


