Решения заданий Всероссийской олимпиады школьников по химии (школьный этап) 2011 г.
Задание 1
Это элемент фосфор. Высший оксид - P2O5.
P2O5. + 3H2O =2H3PO4
P2O5 + 6 NaOH =2Na3PO4 + 3 H2O
Шкала оценивания задания:
- написание формулы высшего оксида – 1 б.
- составление уравнений реакций – 2б.+ 2=4б.
- расстановка коэффициентов – 0,5б.+2= 1б.
Всего: 6б.
Задание 2.
Ca + S = CaS
2 Ca + O2 = 2 CaO
Ca + 2H2O = Ca(OH) 2 + H2
Ca + H2 = CaH2
3Ca + N2 = Ca3H2
S + O2 = SO2
SO2 + CaO =CaSO3
Ca3N2 + 6H2O = 3Ca(OH) 2 + 2NH3
H2 +S = H2S
Шкала оценивания задания:
- написание реакций: 1б. x 9 = 9б.
- написание формул в-в: 0,25б. x 14 = 3,5б.
- расстановка коэффициентов: 0,5б. x 3 = 1,5б.
Всего: 14б. Задание 3.
Шкала оценивания задания:
- определён элемент: 0,5б. x 2 = 1б.
- изображены схемы строения атомов: 1б. x 2 = 2б.
- изображены электронно - графические формулы: 2б. x 2 = 4б.
№ 1 - это Аr – аргон +
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 3p
3p
3s
2p
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 2s
2s
1s
№ 2- это титан Ti +
4s
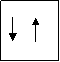 |
3d
![]()



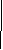

![]() 3p
3p
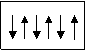 |
3s
![]()
![]()
![]() 2p
2p
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
 2s
2s
1s
Всего: 7б.
Задание 4. Шкала оценивания задания: 1-В 2-Е
3-А
4-Б
- определение степени окисления атомов в соединениях: 1б. x 4 = 4б.
- определение соответствия: 0,5б. x 4 = 2б.
Всего: 6б.
Задание 5
M(HO) =18 г/моль
m(H2O) =18 г.
18г. (H2O) :2г.(H) = 250г. (H2O) : X г.(H)
x= 27,7 г.(H)
18 г. (H2O) : 16 г. (O)=250 г. (H2O) : y г. (O)
y=222,3 г. (O) или
m(O) = 250 г. – 27,7 г.= 222,3 г.
Шкала оценивания задания:
- найдена масса воды: 1б.
- найдена масса водорода: 4б.
- найдена масса кислорода: 4б.
-оформление задачи: 1б.
Всего: 10б. Задание 6
А-С 1. C+O2=CO2
В-СO2 .2. 2C+O2 =2CO
C-CO 3. 2CO+O2 =2CO2
4. C+CO2 =2CO
Шкала оценивания задания:
- установлены вещества: А, В,С – 1б. x 3 = 3б.
- записаны уравнения реакций – 1б. x 4 = 4б.
Всего: 7б. Задание 7 Массовая доля неизвестного элемента = 100% - (6,33+ 15,19 +60,75)=17,72%
Для нахождения мольных долей разделим массовые доли элементов на их Аr:
H:C:O=6,33 : 15,19 : 60,76 =5:1:3
1 12 16
Пусть Аr неизвестного элемента Аr(x), тогда 17,72 =15.12
Аr(x) 12 (так как по условию число атомов неизвестного элемента равно числу атомов углерода) Аr(x) = 14 – это азот.
Простейшая формула NH5 CO3 или NH4HCO3 – это кислая соль – гидрокарбонат аммония.
Шкала оценивания задания:
- вычисление w четвёртого элемента – 2б.
- установление отношения w%(э)/ Аr(э) – 2б.
- вычисление атомного состава вещества – 2б.
- вычисление Аr азота – 1б.
- нахождение истинной формулы вещества – 2б.
- определение класса вещества – 1б.
Всего: 10б.
Задание 8
2 Me+ O2 = 2 MeO
12,71 + O2 = 15,91
2x 2x+32
2x x 15,91= (2x+ 32) x 12,71
31,82 x = 25,42 x +406,7
31,82 x - 25,42 x =406,7
x = 63,55 Это Cu – медь
2 Cu+ O2 =2 CuO
Шкала оценивания задания: - написана схема реакции - 1б.
- решение задачи – 7б.
- написание уравнения реакции - 1б. Всего: 10б
- оформление задачи -1б.
Суммарный балл: 70



