Государственное бюджетное образовательное учреждение
высшего профессионального образования
«Красноярский государственный медицинский университет
имени профессора -Ясенецкого»
Министерства здравоохранения и социального развития
Российской Федерации
Кафедра патологической физиологии
имени профессора
Патофизиология раневого процесса
учебное пособие для внеаудиторной работы студентов 2-го курса,
обучающихся по специальности 060201 – Стоматология
Красноярск
2012
УДК 616-
ББК 52.50
М 75
Патофизиология раневого процесса: учебное пособие для внеаудиторной работы студентов 2-го курса, обучающихся по специальности 060201 – Стоматология/сост. , , Ю, – Красноярск: КрасГМУ, 2012
Составители: к. б.н. ,
д. м.н. ,
д. б.н. Ю,
д. б.н.
Учебное пособие составлено в соответствии с образовательными стандартами подготовки специалистов высшего медицинского образования и предназначено для внеаудиторной работы студентов 2-го курса, обучающихся по специальности 060201 – Стоматология. Содержит информационные материалы, тестовые задания и ситуационные задачи по патофизиологии раневого процесса.
КрасГМУ
2012
Содержание
Травма. Определение. Классификация. 4
Раневой процесс: определение понятия, классификация. 5
Механизмы клеточно-гуморальной кооперации и морфологические основы раневого процесса (фазы раневого процесса) 7
Фаза воспаления 7
Фаза пролиферации 11
Фаза рубцевания 17
Общие реакции организма при раневом процессе 18
Классические типы заживления ран 19
Заживление первичным натяжением 19
Заживление вторичным натяжением 21
Заживление тканей под струпом 22
Рубцы и их осложнения 23
Регенерация: особенности регенерации соединительной, эпителиальной, мышечной и нервной ткани 24
Раны в стоматологической практике 27
Самоконтроль по тестовым заданиям 34
Самоконтроль по ситуационным задачам 37
Рекомендуемая литература 40
Травма. Определение. Классификация.
Травма – одномоментное воздействие внешнего фактора, вызывающего в тканях местные анатомические и функциональные нарушения, сопровождающиеся общими реакциями организма.
Травматология – наука о травмах.
Травматология представляет собой сводное понятие и состоит из многочисленных разделов, которые являются частью отдельных специальностей (офтальмологии, оториноларингологии, нейрохирургии, урологии и т. д.). Важным разделом травматологии является ортопедия, включающая распознавание и лечение нарушений развития, повреждений и заболеваний опорно-двигательного аппарата и их последствий. В отдельную дисциплину травматологии – комбустиологию – выделено лечение ожогов и отморожений.
Травматизм – совокупность травм на определенной территории (в стране, городе и т. д.) или среди определенного контингента людей (в сельском хозяйстве, на производстве, в спорте и т. д.).
Травматизм подразделяют на производственный и непроизводственный.
В зависимости от рода деятельности, места и обстоятельств, при которых была получена травма, выделяют бытовой, транспортный, промышленный (сельскохозяйственный, войсковой и пр.), спортивный виды травматизма. Отдельно следует выделять боевые повреждения, полученные военнослужащими и мирным населением во время войн и военных конфликтов.
Классификация травм.
По условиям возникновения травмы можно разделить на три группы: производственные, непроизводственные и военные.
• Производственный травматизм делят на: а) промышленный,
б) сельскохозяйственный.
• Непроизводственный травматизм: а) транспортный, б) уличный,
в) детский, г) бытовой, д) спортивный, е) умышленный.
• Военные травмы: а) огнестрельные повреждения, б) закрытые повреждения.
По виду повреждающего агента выделяют травмы: 1) механические,
2) химические, 3) термические, 4)лучевые, 5) огнестрельные,
6) комбинированные.
По механизму возникновения все травмы делят на прямые и непрямые, в зависимости от соотношения места повреждения и точки приложения силы.
В зависимости от целостности покровных тканей все повреждения могут быть закрытыми и открытыми. Открытые травмы или ранения в свою очередь подразделяют на огнестрельные (пулевые, осколочные, нанесенные стекловидными элементами и т. д.) и неогнестрельные (колотые, резаные, рубленые и др.).
С учетом выделения анатомических областей человека следует различать изолированные, множественные, сочетанные, а также комбинированные повреждения.
К изолированным закрытым травмам или ранениям относят одно повреждение одной анатомической области или ее сегмента (например, разрыв печени, перелом бедра, перелом плеча). В хирургии повреждений принято выделять семь анатомических областей: голова, шея, грудь, живот, таз, позвоночник, конечности.
К множественным травмам относят несколько однотипных повреждений в пределах одной анатомической области или ее сегментов (перелом бедра и предплечья, разрыв печени и мочевого пузыря и др.).
Под сочетанными повреждениями следует понимать закрытые травмы или ранения двух и более различных анатомических областей (перелом бедра и ушиб головного мозга, перелом плеча и разрыв печени и др.).
При сочетании разных по происхождению механических факторов (огнестрельное и колото-резаное ранения и др.) либо одновременного воздействия на человека механического и другого вида факторов (термического, радиационного, химического и др.) говорят о комбинированной травме (закрытая черепно-мозговая травма и отморожение конечностей).
Раневой процесс: определение понятия, классификация.
Раневой процесс – сложный комплекс биологических реакций, возникающих в ответ на повреждение органов и тканей, заканчивающийся обычно их заживлением. Раневой процесс является примером взаимоотношений клеточных элементов, действующих в ограниченной области и связанных с ними многочисленных реакций организма в виде нарушения функций нервной и эндокринной систем, развития шоковых состояний и т. д.
Процесс заживления раны всегда цикличен и характеризуется фазностью (периодами) в соответствии с функционально-метаболическими и структурными изменениями в очаге повреждения и окружающих тканях.
Изучение динамики раневого процесса имеет фундаментальное и прикладное значение. Только имея точное представление о функции каждой из клеток, участвующих в раневом процессе, можно разрабатывать рациональные патогенетически обоснованные методы лечения ран и предупреждать осложнения. Заживление ран протекает по общим закономерностям, но морфогенез варьирует в зависимости от характера повреждения, размера дефекта, наличия инфекции и вида поврежденной структуры. Поэтому представляется целесообразной информация об особенностях регенерации кожи, мышечной и костной ткани с позиций обсуждения механизмов нарушения репаративных процессов в различных тканях.
Раневой процесс – это патологический процесс, представляющий собой совокупность клинических, патофизиологических, биохимических, бактериологических и морфологических изменений, характеризующих динамику заживления раны.
Процесс заживления раны имеет важное значение для нормальной жизнедеятельности организма. Он представляет собой проявление биологической адаптации; а весь комплекс сложных биологических явлений в ране, завершающихся её заживлением, называется раневым процессом. Он всегда цикличен и более или менее четко может быть разделен на фазы (периоды) в соответствии с развитием функциональных и морфологических изменений в ране и окружающих тканях.
Раной называется любое повреждение, сопровождающееся нарушением целостности покровов тела (кожи, слизистых). Основными клиническими признаками ран являются наличие дефекта кожи или слизистых, кровотечение и боль.
По происхождению раны делят на операционные и случайные. Операционные раны наносятся с лечебной целью в особых условиях, сводящих к минимуму риск раневых осложнений. К случайным ранам относят все остальные: бытовые, производственные, боевые, криминальные. Общим является то, что все они наносятся вопреки воле раненого, контаминированы микроорганизмами, что определяет риск раневых осложнений.
По виду повреждающего фактора раны делят на: механические, термические, химические, лучевые, комбинированные (при наличии нескольких видов повреждающих факторов) и трофические язвы (возникают при нарушении артериального или венозного кровоснабжения - являются хроническими ранами).
По локализации выделяют раны головы, шеи, туловища и конечностей, внутренних органов и сочетанные - раны нескольких внутренних органов.
По характеру повреждения механические раны подразделяют на: резаные, колотые, ушибленные, размозженные, рваные, рубленые, укушенные, огнестрельные.
По степени обсемененности все раны делятся на три вида:
• асептические - это, как правило, только операционные раны при "чистых" оперативных пособиях. Они заживают первичным натяжением.
• контаминированные (свежеинфицированные) - это раны, обсемененные микрофлорой, но без признаков нагноения. К ним относятся все случайные раны за очень редкими исключениями и часть операционных ран.
• гнойные - раны с признаками гнойно-воспалительного процесса. Они подразделяются на первичные - образовавшиеся после операций по поводу острых гнойных процессов и вторичные - раны, нагноившиеся в процессе заживления.
Возникновение раны — это результат повреждений клеток и тканей, вызывающих локальный типовой патологический раневой процесс. Рану составляют: 1) некробиотически измененные клетки; 2) элементы межклеточного матрикса, разрушенных клеток и стенки микрососудов; 3) плазма и клетки крови, попавшие в интерстиций; 4) сгустки крови, образовавшиеся в результате высвобождения тканевого тромбопластина погибшими эндотелиоцитами.
Классификация динамики раневого процесса. 1) фаза воспаления — подготовительный период (1–6 суток); 2) фаза пролиферации или регенерации (грануляционная ткань — 6–12 суток); 3) фаза созревания и формирования рубца (12–13 суток).
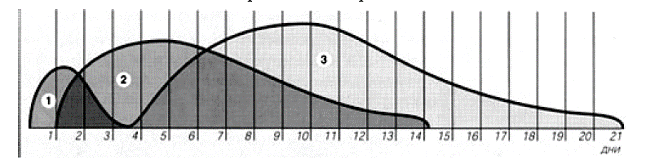
Рис.1. Схематическое представление временного взаиморасположения фаз раневого процесса. (1-фаза воспаления, 2-фаза регенерации и пролиферации, 3- фаза реорганизации рубца и эпителизации).
Патофизиологи характеризуют воспаление как типовой патологический процесс – реакцию целостного организма на локально действующий повреждающий фактор – объединяющий 3 последовательных стадии: альтерацию, экссудацию и пролиферацию. При наблюдении раневого процесса ученые стали рассматривать фазу пролиферации отдельно, в связи с особенностями образования грануляционной ткани при раневом повреждении. Но этот вопрос все еще остается дискуссионным.
Таким образом, комплекс биологических реакций организма в ответ на повреждение при раневом процессе можно рассматривать как три последовательные фазы.
Механизмы клеточно-гуморальной кооперации и морфологические основы раневого процесса
(фазы раневого процесса)
Фаза воспаления
Местной начальной реакцией организма на травму является спазм сосудов в области раны, сменяющийся их расширением, повышением проницаемости сосудистой стенки и быстро нарастающим отеком, получившим название «травматический отек». Спазм артериол, обусловленный выбросом адреналина из нервных окончаний, длится 10-15 сек. Далее формируется стадия артериальной гиперемии, связаная с действием на микрососуды гистамина, брадикинина, серотонина, кининокиназ и др. веществ, (медиаторов 1 порядка) вышедших из клеток в момент повреждения (первичная альтерация). Позже под влиянием тех веществ, которые образовались в момент первичной альтерации в результате активизации протеолитических и окислительных ферментов, из неповрежденных клеток высвобождаются и синтезируются медиаторы 2 порядка: гистамин, серотонин, брадикинин, гепарин, каллекриины, кинины, простагландины, лейкотриены, тромбоксан, Н2О2, пероксинитрит, оксид азота, TNF-a, IFN-g, которые вызывают вторичную альтерацию и оказывают влияние на сосудистую проницаемость и миграцию лейкоцитов и тромбоцитов. Происходит местное расширение сосудов и в связи с этим улучшение доставки к очагу повреждения новых порций крови – количества лейкоцитов, стимуляторов роста и других факторов, способствующих регенерации клеток и тканей. Освободившиеся при распаде лейкоцитов вещества (нуклеопротеиды и др.) стимулируют рост и усиливают митотическое деление восстанавливающих клеток.
В результате повреждений микрососудов и межклеточного матрикса, цитолиза эндотелиоцитов происходит прямой контакт высокомолекулярного кининогена, XII фактора свертывания крови и прекалликреина с субэндотелиальным и межклеточным коллагеном. Кроме того, происходит адгезия к субэндотелиальному коллагену тромбоцитов. Медиатором адгезии тромбоцитов является фактор фон Виллебранда. В результате контакта с коллагеном активируется XII фактор свертывания крови, что запускает действие плазменных механизмов гемостаза. При этом поврежденные эндотелиоциты высвобождают тканевой тромбопластин. Тромбопластин вызывает действие внешних по отношению к плазме крови механизмов свертывания. Высвобождение тканевого тромбопластина вызывает повышенное образование тромбина (второго фактора свертывания крови), что обусловливает повышенную агрегацию активированных тромбоцитов. Активированные тромбоциты высвобождают тромбоксан A2. В ответ активированные травмой и гипоксией эндотелиальные клетки высвобождают антагонист тромбоксана простациклин, который тормозит агрегацию тромбоцитов. Если повреждения тканей достигают определенной степени выраженности, то рост секреции простациклина не ограничивает спазма и тромбоза микрососудов, вызванных тромбоксаном. Стаз и тромбоз микрососудов становятся отправной точкой развития воспаления в очаге первичной травматической альтерации. Одновременно с активацией механизмов гемостаза происходит активация калликреин-кининовой системы. Это происходит через активацию прекалликреина активированным двенадцатым фактором свертывания крови.
В результате активации прекалликреина растет образование калликреина. Последний является хемоаттрактантом по отношению к нейтрофильным гранулоцитам. Активация калликреином нейтрофилов в просвете микрососудов обусловливает высвобождение полиморфонуклеарами эластаз. Действие эластаз служит одной из причин вторичной альтерации.
Действие калликреина на кининоген (высокомолекулярный) обусловливает образование брадикинина. Эффект брадикинина как медиатора воспаления складывается из дилятации артерий небольшого диаметра и артериол, а также из роста проницаемости стенок микрососудов и особенно венул. Рост проницаемости стенок микрососудов происходит посредством расширения пространств между клетками сосудистой стенки. Калликреин, повышая активность урокиназы, усиливает трансформацию плазминогена в плазмин. Кроме того, образование плазмина происходит в результате действия тканевого активатора плазминогена, который высвобождают активированные и поврежденные эндотелиоциты. Рост образования в очаге повреждения плазмина ограничивает в нем действие механизмов свертывания крови, вызывая фибринолиз.
Активация системы комплемента плазмином представляет собой ключевой момент в развитии локального раневого воспалительного процесса. Плазмин обладает свойством прямой и опосредованной активации системы комплемента.
Локальный раневой типовой патологический процесс создает предпосылки системной воспалительной реакции и раневой болезни.
Стадия артериальной гиперемии длится от 10-15 минут до часа и уступает место венозной гиперемии. Венозная гиперемия начинается с расширения прекапиллярных сфинктеров, происходит затруднение венозного оттока замедляется поступление крови в артериальное русло, что в дальнейшем способствует сгущению крови и стазу в посткапиллярных венулах, повышенной проницаемости сосудистой стенки. Следовательно, сосудистые изменения в области травмы имеют определенную динамику развития: кратковременный спазм, артериальная гиперемия, венозная гиперемия и стаз.
В очаге воспаления происходит активация эндогенных окислительно-восстановительных ферментов: сукцинатдегидрогеназы, гидролаз (фосфатазы, пептидазы, липазы), оксидаз, лизоцима, прежде всего, в рыхлой соединительной ткани, а затем в лейкоцитах, фибробластах. В последующем активируются такие ферменты как 5-нуклеотидаза, аденозинтрифосфатаза и др. Свое действие реализуют и ферменты бактериального происхождения (дезоксорибонуклеаза, катепсины, коллагеназа, стрептокиназа, гиалуронидаза и др.). В результате увеличивается распад белка, происходит активация процессов перекисного окисления липидов, освобождаются жиролипоидные вещества (жирные кислоты, лецитин), понижающие поверхностное натяжение в регенерирующих клетках. Наблюдается активирование аэробного и анаэробного гликолиза в регенерирующей ткани. Образование в условиях анаэробного гликолиза молочной и пировиноградной углекислоты, а также их накопление, вследствие нарушения микроциркуляции приводит к изменениям кислотно-основного состояния в очаге воспаления. В самом начале воспаления эти изменения за счет щелочных резервов тканей компенсируются, и рН тканей не изменяется (компенсированный ацидоз). Дальнейшее истощение щелочных резервов приводит к изменению рН и развитию декомпенсированного ацидоза. Оптимальное кислотно-щелочное равновесие в соединительной ткани равно 7,1, в гнойной ране 6,0-6,5 и даже 5,4. Ацидоз усиливает экссудативные изменения в ране, повышает проницаемость капилляров; миграцию лейкоцитов и макрофагов. При воспалении, особенно гнойном, изменяется состав электролитов в ране. В клетках накапливаются натрий и кальций, уменьшается содержание калия. При распаде клеток освобождение калия может увеличиваться в 50-100 раз, вследствие этого усугубляется нарушение соотношения калия и кальция, нарушается работа ионных насосов, что увеличивает степень ацидоза.
Изменения кислотно-основного состояния, состава электролитов, накопление в ране токсичных продуктов приводят к нарушению состава коллоидов, скоплению жидкости в межклеточных пространствах, набуханию коллоидов в клетках. Переход коллоидов из состояния геля в золь вызывает разрыв клеточной мембраны, разрушение клеток и развитие вторичного некроза (первичный некроз обусловлен действием травмирующего фактора). Таким образом, локальная альтерация тканей, обусловленная действием медиаторов 1-го и 2-го порядка и местное нарушение обмена веществ (ацидоз, гипериония, гиперосмия, гиперонкия, изменение состояния коллоидов и т. д.) значительно способствуют формированию отека.
В результате этого раневой канал суживается, а мертвые ткани, пропитанные кровью, могут выдавливаться наружу. Это так называемое первичное очищение раны.
В раннем периоде воспаления (первые 2-3 суток) в результате действия хемоаттрактантов (бактериальный липополисахарид, ИЛ-8, компоненты комплемента С-3а, С-5а, лейкотриен В-4, продукты протеолиза тканей, адениловые кислоты, аденозин и ряд других), в экссудате преобладают полиморфоядерные лейкоциты (нейтрофилы), позже в нем появляются мононуклеарные клетки (моноциты, макрофаги и лимфоциты). Нейтрофилы фагоцитируют микроорганизмы и в меньшей степени некротизированные ткани, лизируют нежизнеспособные ткани, выделяют биологически активные вещества (катионные белки, лактоферрин, лизоцим, миелопероксидазу) и флогогенные факторы модулирующего действия (супероксидный радикал, гидроксильный радикал, синглентный кислород), осуществляют внутриклеточный протеолиз. В зоне некроза значительно снижается содержание нуклеиновых кислот, выявляются деструктивные изменения коллагеновых волокон. Нейтрофилы после выполнения своих функций (фагоцитоз, экзоцитоз, синтез медиаторов 2 порядка, генерация эндогенных окислителей, индукция иммунного ответа, контактный лизис) распадаются или фагоцитируются макрофагами. Помимо фагоцитоза макрофаги выделяют ряд способствующих заживлению раны медиаторов, таких как: интерлейкины IL-1, IL-12 (активаторы клеточного и гуморального иммунного ответа, фактор роста эндотелия капилляров, трансформирующий фактор роста (GTF), фактор роста фибробластов (FGF) и др).
Лимфоциты в очаге воспаления – это источник плазматических клеток, синтезирующих антитела. Кроме того, лимфоциты переносят генетическую информацию, благодаря которой усиливается или поддерживается рост ряда клеток, в том числе, фибробластов, а также являются продуцентами цитокинов: IFN-g, IL-2, TNF-a (стимуляторов клеточного иммунного ответа), IL – 4, IL –5, IL – 6, IL – 10, IL – 13 (стимуляторов гуморального иммунного ответа).
Уже в 1-е сутки на границе жизнеспособных и омертвевших тканей формируется лейкоцитарный вал.
Фаза пролиферации
Фаза пролиферации или регенерации – начинается на 3-4 сутки после ранения, характеризуется развитием грануляционной ткани, постепенно заполняющей раневой дефект. Четких границ перехода между I и II фазами нет: продолжается активный воспалительный процесс, некролиз, очищение раны от нежизнеспособных тканей (подготовительная фаза), и в это же время начинается развитие и грануляционной ткани. Процесс пролиферации стимулируется действием цитокинов (фактора роста фибробластов (FGF)) и трансформирующего фактора роста (TGF), вырабатываемых активированными макрофагами и нейтрофилами. В эту фазу в ране резко уменьшается количество лейкоцитов, макрофаги сохраняются, но главную роль во время пролиферации играют фибробласты и эндотелий капилляров, продуцирующий большое количество ферментов. Наблюдается преобладание анаболических процессов, происходит превалирование синтеза белка над его распадом, формируется накопление в ране различных аминокислот (тирозина, лейцина, аргинина, гистидина, лизина, триптофана, лейцина, пролина и др.) Важная роль в регенерации принадлежит пролину, который превращается в оксипролин коллагеновых белков.
В начавшейся пролиферации основное значение имеет образование новых кровеносных сосудов. Оно может происходить путем почкования старых сосудов (1 тип новообразования сосудов), а также непосредственно в ткани без связи с предшествующими сосудами (2 тип новообразования). Второй тип новообразования сосудов заключается в том, что среди пролиферирующих клеток появляются щели, в которые открываются капилляры и изливается кровь, а прилегающие клетки получают признаки эндотелия. Присоединение гемодинамического фактора (давление крови, пульсация) упорядочивает общее направление растущих сосудов из глубины на поверхность, где, образуя крутой изгиб, капилляр вновь погружается вглубь грануляций. Места таких изгибов имеют вид небольших зернышек, усеивающих поверхность юной, незрелой соединительной ткани, которая выглядит как сочная ярко-красная масса с неровной зернистой поверхностью. Её называют грануляционной тканью (от granulum - зерно). Островки грануляционной ткани появляются в полностью еще не очистившейся ране на фоне участков некроза уже на 2-3-и сутки. На 5-е сутки рост грануляционной ткани становится весьма ощутимым. Рана, богатая грануляционной тканью, легко кровоточит. Кроме эндотелиальных клеток грануляционная ткань содержит большое количество фибробластов, число которых прогрессирующе увеличивается, и они быстро становятся основными клетками грануляционной ткани. Цитоплазма макрофагов и фибробластов содержит большое количество нуклеопротеидов, являющихся пластическим и энергетическим материалом, необходимым для регенерации. Фибробласты – важный компонент грануляционной ткани. Они, продуцируя коллаген, обеспечивают рубцевание раны. Ключевыми моментами в репаративной регенерации являются синтез ДНК в фибробластах, а также нейтральных мукополисахаридов и кислых гликозаминогликанов (гиалуроновая кислота, хондроитинсульфат) и связывание их с коллагеном. Гликозаминогликаны – основа межуточного вещества соединительной ткани. В синтезе мукополисахаридов принимают участие и тучные клетки, число которых учеличивается к 3-5 дню и достигает максимума к 5-7 дню. Активное участие в обменных процессах в ране в период формирования грануляционной ткани принимают плазматические клетки и гигантские многоядерные клетки, функция последних пока недостаточно ясна.
Строение и функции грануляционной ткани.В грануляционной ткани различают б слоев, каждый из которых имеет определенную функцию.
1. Поверхностный лейкоцитарно-некротический слой. Состоит из лейкоцитов, детрита и слущивающихся клеток. Он существует в течение всего периода заживления раны.
2. Слой сосудистых петель. Содержит помимо сосудов полибласты. При длительном течении раневого процесса в этом слое могут образоваться коллагеновые волокна, располагающиеся параллельно поверхности раны.
3. Слой вертикальных сосудов. Построен из периваскулярных элементов и аморфного межуточного вещества. Из клеток этого слоя образуются фибробласты. Этот слой наиболее выражен в раннем периоде заживления раны.
4. Созревающий слой — по существу, более глубокая часть предыдущего слоя. Здесь околососудистые фибробласты принимают горизонтальное положение и отходят от сосудов, между ними развиваются коллагеновые и аргирофильные волокна. Этот слой, характеризующийся полиморфизмом клеточных образований, остается одинаковым по толщине в течение всего процесса заживления раны.
5. Слой горизонтальных фибробластов. Непосредственное продолжение
предыдущего слоя. Он состоит из более мономорфных клеточных элементов, богат коллагеновыми волокнами и постепенно утолщается.
6. Фиброзный слой. Отражает процесс созревания грануляций.
Основными функциями грануляционной ткани являются:
· замещение раневого дефекта (является основным пластическим материалом, быстро заполняющим раневой дефект);
· защита раны от проникновения микроорганизмов и попадания инородных тел достигается содержанием в грануляционной ткани большого количества лейкоцитов, макрофагов и плотной структурой наружного слоя;
· секвестрация и отторжение некротических тканей (происходит благодаря деятельности лейкоцитов и макрофагов, выделению клеточными элементами протеолитических ферментов).
При нормальном течении процесса заживления одновременно с развитием грануляций начинается эпителизация. Путем размножения и миграции эпителиальные клетки «наползают» с краев раны по направлению к центру, постепенно покрывая грануляционную ткань. Вырабатывающаяся в нижних слоях фиброзная ткань выстилает дно и стенки раны, как бы стягивая ее (раневая контракция).
В результате полость раны сокращается, а поверхность — эпителизируется.
Грануляционная ткань, заполнившая раневую полость, постепенно трансформируется в зрелую грубоволокнистую соединительную ткань - формируется рубец.
Патологические грануляции тканей. При воздействии каких-либо неблагоприятных факторов, влияющих на процесс заживления (ухудшение кровоснабжения или оксигенации; декомпенсация функции различных органов и систем; повторное развитие гнойного процесса и т. д.), рост и развитие грануляций и эпителизация могут прекратиться. Грануляции приобретают патологический характер. Клинически это представляется в виде отсутствия сокращения раны и изменения внешнего вида грануляционной ткани. Рана становится тусклой, бледной, иногда синюшной, теряет тургор, покрывается налетом фибрина и гноя, что требует активных лечебных мероприятий.
Также патологическими считаются бугристые грануляции, выступающие за пределы раны, гипертрофические грануляции (гипергрануляции). Они, нависая над краями раны, препятствуют эпителизации. Обычно их срезают или прижигают концентрированным раствором нитрата серебра или перманганата калия и продолжают лечить рану, стимулируя эпителизацию.
Таблица 1
Ростовые факторы и цитокины участвующие в регенерации и заживлении ран
| Обозначение | Источник | Функции |
Epidermal growth factor | EGF | Тромбоциты, макрофаги, слюна, моча, молоко, плазма | Митогенный фактор для кератиноцитов и фибробластов; стимулирует миграцию кератиноцитов и формирование грануляционной ткани |
Transforming growth factor alpha | TGF-alpha | Макрофаги, Т-лимфоциты, кератиноциты и т. п. | Аналогично EGF: стимулирует деление гепатоцитов и некоторых эпителиальных клеток |
Hepatocite growth factoror | HGF | Мезенхимальные клетки | Усиливает пролиферацию эпителиальных и эндотелиальных клеток, гепатоцитов; увеличивает подвижность клеток |
Vascular endothelial cell growth factor | VEGF | Мезенхимальные клетки | Увеличивает сосудистую проницаемость; митогенный фактор для эндотелиальных клеток |
Platelet-derived growth factor | PDGF | Тромбоциты, макрофаги, эндотелиоциты, кератиноциты, ГМК | Хемотаксис нейтрофилов, макрофагов, фибробластов и ГМК; Активация нейтрофилов, макрофагов^и Фибробластов; митогенный эффект на фибробласты, эндотелиоциты и ГМК; стимулирует продукцию матриксных металлопротеиназ, фибронектина, гиалуроновой кислоты; стимулирует ангиогенез; ремоделирование; ингибирует аггрегацию тромбоците в; регулируетэ кспрессию интегринов |
Fibroblast growth factor | FGF | Макрофаги, тучные клетки, Т-лимфоциты, эндотелиоциты, фибробласты и т. п. | Хемотаксис фибробластов; митогенный эффект на фибробласты и кератиноциты; стимулирует миграцию кератиноцитов, ангиогенез, начальное заживление раны |
Transforming growth factor beta | TGF-beta | Тромбоциты, Т-лимфоциты, макрофаги, эндотелиоциты, кератиноциты, ГМК, фибробласты | Хемотаксис нейтрофилов, макрофагов, лимфоцитов, фибробластов и ГМК; стимулирует синтез тканевого ингибитора матриксных металлопротеиназ, миграцию кератиноцитов, ангиогенез; ингибирует продукцию матриксных металлопротеиназ и пролиферацию кератиноцитов; регулирует экспрессию интегрина и других цитокинов |
Keratinocite growth factor | KGF | Фибробласты | Стимулирует миграцию кератиноцитов, пролиферацию и дифференцировку |
Insulin-like growth factor 1 | IGF-1 | Макрофаги, фибробласты и другие клетки | Стимулирует синтез сульфатированных протеогликанов, коллагена, миграцию кератиноцитов, пролиферацию фибробластов; эндокринные эффекты подобные гормону роста |
Tumor necrosis factor | TNF | Макрофаги, тучные клетки, Т-л имфоциты | Активация макрофагов; регуляция продукции цитокинов и т. д. |
Interleukins | IL-1 и т. п. | Макрофаги, тучные клетки, кератиноциты, лимфоциты и т. п. | Множество функций, например: хемотаксис нейтрофилов (ИЛ-1) и фибробластов (ИЛ-4), стимуляция синтеза матриксной металлопротеиназы-1 (ИЛ-1), ангиогенеза (И Л-8), синтез тканевого ингибитора матриксных металлопротеиназ (ИЛ-6); регуляция цитоконов |
Interferons | IFN-a и т. п. | Лимфоциты и фибробласты | Активация макрофагов; ингибирование пролиферации фибробластов и синтеза матриксных металлопротеиназ; регуляция других цитокинов |
Таблица 2.
Эндотелиальные факторы роста (VEGF, VEGF-B, VEGF-C)
Продукция | В небольших количествах продуцируются многими клетками, сравнительно много VEGF образуется в подоцитах почечных клубочков и кардиомиоцитах |
Стимулирующие факторы | Гипоксия TGF-β PDGF TGF-α |
Рецепторы | VEGF-R1 VEGF-R2 |
Функции | Вызывает новообразование капилляров Увеличивает проницаемость микрососудов Стимулирует миграцию эндотелиальных клеток Стимулирует пролиферацию эндотелиальных клеток VEGF-С избирательно стимулирует гиперплазию лимфатических сосудов |
Фаза рубцевания
Формируется на 12-30 сутки. Происходит увеличение коллагеновых волокон, грануляционная ткань становится всё более плотной, снижается число микрососудов и клеточных элементов (макрофагов, тучных клеток, фибробластов). В клетках уменьшается содержание пластических (РНК, ДНК) материалов, снижается активность кислых фосфатаз. Идет процесс активного формирования эластических и коллагеновых волокон. Формирование эластических волокон начинается через 4-6 недель и заканчивается к 6-му месяцу, когда завершается окончательное формирование рубцовой ткани. Этим определяются сроки рациональной физической нагрузки больных в послеоперационном периоде. Синхронно с созреванием грануляционной ткани происходит процесс эпителизации раневой поверхности. Степень и скорость эпителизации определяются процессом образования грануляций. В случае нарушения синхронности возможно избыточное образование рубцовой ткани (когда процессы образования грануляций и образования рубца опережают процесс эпителизации); это приводит к образованию выступающих над кожей келлоидных рубцов. И, наоборот, если эпителизация начинается раньше выполнения раны грануляциями, формируются деформированные втянутые рубцы. Равновесие между данными процессами лежит в основе раневой контракции – равномерного концентрического сокращения концов и стенок раны. Раневая контракция сочетается с интенсивной эпителизацией, которая начинается с образования аргирофильных волокон. Эпителий надвигается на края раны, подвергаясь частичному разрушению. Новообразованный эпителиальный покров не содержит, в отличие от здоровой кожи, сальных и потовых желез, в нем отсутствуют волосяные луковицы. В дальнейшем эпителий подвергается дифференцировке. Восстановление иннервации происходит медленно. В краях раны регенерация нервных волокон начинается через 2-3 недели, а к 6-7 месяцу волокна определяются в рубце. Продолжительность заживления, как и количественные изменения при раневом процессе, определяются образованием рубцовой ткани, площадью эпителизации и зависят от ряда моментов, таких как размеры раны (чем больше рана, тем длительнее заживление), степень повреждения окружающих тканей (раны ушибленные, разможженные, рванные заживают медленнее), количество некротизированных тканей, количество, вид и вирулентность попавших в рану микроорганизмов; состояние организма человека (кровопотеря, шок, истощающие заболевания: туберкулез, сифилис, злокачественные новообразования, лучевая болезнь, авитаминозы и др. – замедляют заживление ран); возраст пострадавших (у молодых процессы заживления идут быстрее, чем у престарелых). На процесс заживления влияют также сопоставление и сближение краев раны, так ушивание раны приводит к более быстрому её заживлению с образованием небольших рубцов.
Приведенная схема заживления универсальна для всех видов ран, различия носят лишь количественный характер и касаются количества образованной грануляционной и рубцовой ткани, площади эпителизации, длительности заживления.
С учетом этого принято выделять заживление ран первичным и вторичным натяжением, а также заживление под струпом.
Общие реакции организма при раневом процессе
В течение 1-4-х суток от момента травмы отмечается возбуждение симпатической нервной системы, выделение в кровь гормонов мозгового слоя надпочечников, инсулина, АКТГ и глюкокортикоидов. В результате усиливаются процессы жизнедеятельности: повышаются температура тела и основной обмен, снижается масса тела, усиливается распад белков, жира и гликогена, снижается проницаемость клеточных мембран, подавляется синтез белка и др. Значение этих реакций состоит в подготовке всего организма к жизнедеятельности в условиях альтерации.
В ответ на повреждение, организм отвечает реакцией острофазового воспаления (РОФВ), в результате которой в организме происходит активизация иммунной системы, гипоталамо-гипофизарно-надпочечниковой и симпатико-адреналовой систем, стимулируется метаболизм. В процессе этой реакции повышается выработка активированными клетками: базофилами, нейтрофилами, моноцитами/макрофагами, натуральными киллерами и лимфоцитами интерлейкинов: интерлейкина-1(IL-1), интерлейкина-6 (IL-6), интерферона гамма (IFN-g), фактора некроза опухоли альфа (TNF-a). Действие интерлейкинов на нервную систему проявляется сонливостью, гиподинамией, лихорадкой. Вышеперечисленные интерлейкины стимулируют в печении, альвеолоцитах II типа и др. тканях продукцию белков острой фазы (30 различных белков). Белки острой фазы: С - реактивный белок (СРБ), a2– макроглобулин, a1– хемотрипсин, a1– антитрипсин, a1-кислый гликопротеин (орозомукоид), трансферрин, гаптоглобулин, церрулоплазмин и др. Вырабатываясь в 1-2 сутки после повреждения, они включают механизмы защиты. С - реактивный белок, например, усиливает фагоцитоз нейтрофилами и макрофагами, повышая выработку IL-1, IL-6, IL-8, и стимулирует клеточно-опосредованный иммунный ответ. При этом СРБ является модулятором воспаления, проявляет противовоспалительную активность, связывая и нейтрализуя избыточное количество цитокинов, таких как IL-8, TGF-b, IL-4.
a1-кислый гликопротеин (орозомукоид) способен связывать гистамин, ингибировать агрегацию тромбоцитов, взаимодействуя с фосфолипидами мембран. Белки с антипротеазной активностью a2–макроглобулин, a1– хемотрипсин, a1–антитрипсин способны ингибировать активность эластазоподобных протеаз из поврежденных тканей. Синтез белков острой фазы растет в острый период воспаления. Чем выше степень воспаления, тем выраженнее острофазный ответ.
В анализах крови отмечается повышение количества лейкоцитов, иногда имеет место небольшой сдвиг лейкоцитарной формулы влево; наблюдается увеличение скорости оседания эритроцитов, т. к образуются и адсорбируются на эритроцитах крупнодисперсные белки-реактанты острой фазы; отмечается увеличение концентрации пировиноградной кислоты и остаточного азота. В анализах мочи может появляться белок. При обильной кровопотере выявляется снижение количества эритроцитов, гемоглобина, гематокрита.
Начиная с 4-5-х суток, характер общих реакций обусловливается преобладающим влиянием парасимпатической нервной системы. Основное значение приобретают соматотропный гормон, альдостерон, ацетилхолин. В этой фазе повышается масса тела, происходит нормализация белкового обмена, мобилизуются репаративные возможности организма. При неосложненном течении к 4-5-м суткам купируются явления воспаления и интоксикации, стихает боль, прекращается лихорадка, нормализуются лабораторные показатели крови и мочи. Следует отметить, что подобная схема протекания общих реакций при раневом процессе возможна только при отсутствии осложнений.
Классические типы заживления ран
Заживление первичным натяжением
Заживление первичным натяжением (sanatio per primam intentionem) является наиболее экономичным и функционально выгодным, оно происходит в более короткие сроки с образованием тонкого, относительно прочного рубца.
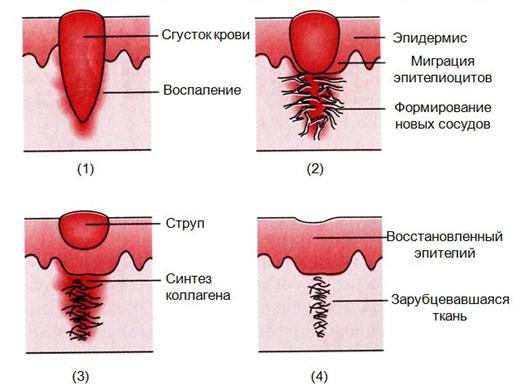
Рис. 2. Заживление раны первичным натяжением
Первичным натяжением заживают операционные раны, когда края и стенки раны соприкасаются друг с другом, (например, резаные раны), или если они соединены швами, как это наблюдается после первичной хирургической обработки раны, или ушивания операционных ран. В этих случаях края и стены раны склеиваются, слипаются между собой за счет тонкой фибринной пленки. Репаративная регенерация при этом проходит те же фазы, что и течение раневого процесса: воспаление, пролиферация и образование соединительной ткани, эпителизация. Количество некротических тканей в ране при этом небольшое, воспаление выражено незначительно.
Отпочковывающийся эпителий капилляров стенок раны и фибробласты проходят через фибринную склейку на противоположную сторону (как бы прошивая грануляции, выполняющие небольшие полости между стенками), подвергаются организации с образованием коллагеновых, эластических волокон, происходит формирование тонкого линейного рубца с быстрой эпителизацией по линии соединения краев раны. Случайные поверхностные раны небольшого размера с расхождением краев до 1 см также могут заживать первичным натяжением без наложения швов. Это происходит из-за сближения краев под воздействием отека окружающих тканей, а в дальнейшем их удерживает образующаяся «первичная фибриновая спайка».
При данном способе заживления между краями и стенками раны никакой полости нет, образующаяся ткань служит лишь для фиксации и укрепления срастающихся поверхностей. Первичным натяжением заживают только раны, в которых отсутствует инфекционный процесс: асептические операционные или случайные раны с незначительным инфицированием, если микроорганизмы погибают в течение первых часов после повреждения.
Таким образом, для того чтобы рана зажила первичным натяжением, необходимо соблюдение следующих условий:
- отсутствие в ране инфекции;
- плотное соприкосновение краев раны;
- отсутствие в ране гематом, инородных тел и некротических тканей;
- удовлетворительное общее состояние больного (отсутствие общих неблагоприятных факторов).
Заживление первичным натяжением происходит в кратчайшие сроки, практически не приводит к развитию осложнений и вызывает небольшие функциональные изменения. Это наилучший тип заживления ран, к которому всегда нужно стремиться, создавать необходимые для него условия.
Развитию инфекционного осложнения в ране способствует наличие субстрата для жизнедеятельности микробных агентов. Таковыми могут быть гематома, обилие некротических масс, наличие инородного тела. Гематома, кроме питательной среды для микроорганизмов, является также фактором, препятствующим плотному соприкосновению стенок раны. Инородное тело в ране может служить источником инфекции и вызывать реакцию отторжения, сопровождающуюся выраженным, длительно текущим воспалением и некрозом окружающих тканей.
Заживление вторичным натяжением
Заживление вторичным натяжением (sanatio per secundam intentionem) наблюдается в случаях, когда края и стенки раны не соприкасаются, отстоят друг от друга на то или иное расстояние (более 10 мм.). Склеивание краев и стенок раны в таких случаях невозможно. Заживление таких ран проходит те же фазы, но в этих случаях наблюдается выраженное гнойное воспаление, некротизированные ткани подвергаются некролизу. Это так называемое «заживление через нагноение». В этом случае заживление происходит после выраженного воспалительного процесса, в результате которого рана очищается от некроза. После очищения раны наступает процесс заполнения дефекта тканей грануляциями с последующим формированием коллагеновых, эластических волокон и образованием рубца.
Для заживления ран вторичным натяжением необходимы условия, противоположные тем, которые способствуют первичному натяжению:
- значительное микробное загрязнение раны;
- значительный по размерам дефект кожных покровов;
- наличие в ране инородных тел, гематом и некротических тканей;
- неблагоприятное состояние организма больного.
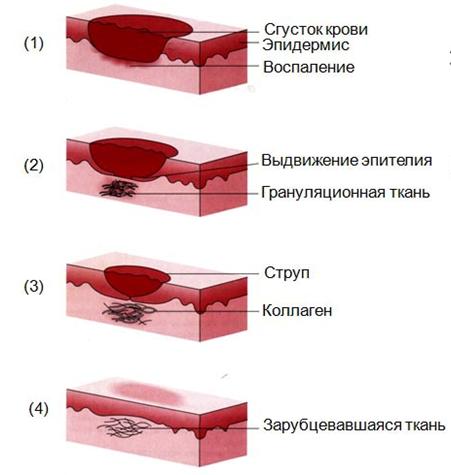
Рис. 3. Заживление раны вторичным натяжением
Заживление тканей под струпом
Заживление раны под струпом происходит при небольших поверхностных повреждениях типа ссадин, повреждений эпидермиса, потертостей, ожогов и пр.
Процесс заживления начинается со свертывания на поверхности повреждения излившейся крови, лимфы и тканевой жидкости, которые подсыхают с образованием струпа.
Струп выполняет защитную функцию, является своеобразной «биологической повязкой». Под струпом идет процесс заполнения дефекта тканей за счет образования грануляционной ткани, с краев надвигается на молодую соединительную ткань регенерирующий эпидермис до полного её закрытия, происходит быстрая регенерация эпидермиса, и струп отторгается. Весь процесс занимает обычно 3-7 дней. В заживлении под струпом, в основном, проявляются биологические особенности эпителия — его способность выстилать живую ткань, ограничивая ее от внешней среды. Струп не следует удалять, если отсутствуют явления воспаления. Если воспаление развивается и под струпом скапливается гнойный экссудат, показана хирургическая обработка раны с удалением струпа. Дискуссионным является вопрос, к какому типу заживления отнести заживление под струпом: первичному или вторичному? Обычно придерживаются мнения, что оно занимает промежуточное положение и представляет собой особый вид заживления поверхностных ран.
Описанные выше виды заживления ран не имеют между собой качественных различий: раневой процесс проходит все фазы своего развития, в регенеративных процессах принимают участие одни и те же клеточные элементы, заканчивается процесс заживления раны формированием соединительной (рубцовой) ткани. Различия носят лишь количественный характер и касаются выраженности воспалительной реакции (отёк, некроз), количества грануляционной ткани, размеров и формы рубца.
Рубцы и их осложнения
Исходом заживления раны является образование рубца. Характер и свойства рубца прежде всего зависят от способа заживления (первичное или вторичное натяжение). После заживления первичным натяжением рубец ровный, находится на одном уровне с поверхностью кожи, линейный, по консистенции не отличим от окружающих тканей, подвижный.
При заживлении вторичным натяжением рубец имеет неправильную звездчатую форму, плотный, часто пигментирован, малоподвижный. Обычно такие рубцы втянутые, расположены ниже поверхности кожи, так как грануляционная ткань замещается рубцовой соединительной тканью, имеющей большую плотность и меньший объем, что приводит к втяжению поверхностных слоев и эпителия.
Все рубцы делятся на обычные и гипертрофические. Обычный рубец состоит из нормальной соединительной ткани и обладает эластичностью. Прочность рубцовой ткани и устойчивость к повреждению приобретаются постепенно. Гипертрофические рубцы состоят из плотной фиброзной ткани и формируются при избыточном синтезе коллагена. Они носят характер грубых, тугих, уродливых рубцов, возвышаются над поверхностью кожи, имеют красноватый оттенок, чувствительны и болезненны, часто вызывают зуд. Среди них выделяют обычные гипертрофические рубцы и келоиды.
Обычный гипертрофический рубец никогда не распространяется за пределы области повреждения, соответствует границам предшествующей раны. В развитии такого рубца ведущую роль играют два фактора: большие размеры раневого дефекта и постоянная травматизация рубца.
Келоид — рубец, внедряющийся в окружающие нормальные ткани, до этого не вовлеченные в раневой процесс. В отличие от обычных гипертрофических рубцов, келоид нередко образуется на функционально малоактивных участках тела. Его рост обычно начинается через 1-3 мес. после эпителизации раны. Рубец продолжает увеличиваться даже после 6 месяцев и обычно не уменьшается и не размягчается. Келоидные рубцы возникают после любой, даже незначительной раны (укол иглой, укус насекомого), поверхностного ожога. Стабилизация рубца наступает в среднем через 2 года после его появления.
Морфологическую структуру келоида составляет избыточно растущая незрелая соединительная ткань с большим количеством атипичных гигантских фибробластов. Патогенез образования келоида остается неясным. Определенную роль играют механизмы аутоагрессии на собственную незрелую соединительную ткань. Нарушение синтеза коллагена, возможно, определяется генетическими отклонениями.
При развитии келоидов применяют электрофорез с лидазой, иссечение рубца с наложением косметического внутрикожного шва и с воздействием в течение всего процесса заживления лучевой терапией, стероидными гормонами, ферментами и пр.
Основными осложнениями рубцов являются: рубцовые контрактуры; изъязвления рубца; папилломатоз рубца; опухолевое перерождение рубцовой ткани (малигнизация).
Следует отметить, что наиболее часто все виды осложнений встречаются при рубцах после заживления вторичным натяжением.
Рубцовыми контрактурами называют стяжение рубцами окружающих тканей с ограничением и нарушением функций вовлеченных структур. Обычно этот процесс вызывают большие по площади и объему рубцы после обширных гнойных ран и ожогов. Часто возникает ограничение или даже отсутствие подвижности в суставах, нарушение деятельности органов (при рубцах на лице, шее, промежности), ухудшение кровоснабжения дистальных участков. Чаще всего рубцовые изъязвления возникают на участках, где кожа не закрыта: лицо, шея, руки.
Папилломатоз рубцов и малигнизация также чаще развиваются на фоне гипертрофических рубцов и постоянной травматизации.
Регенерация: особенности регенерации соединительной, эпителиальной, мышечной и нервной ткани
Регенерация (regeneratio – возрождение, возобновление) – обновление структур организма в процессе жизнедеятельности и восстановление тех структур, которые были утрачены в результате патологических процессов.
В процессе эволюционного развития в организме регенерация возникла как соответствующая приспособительная реакция. Она имеет большое значение не только для здорового организма, но и для больного.
Различают регенерацию физиологическую и патологическую. Физиологическая регенерация – постоянное восстановление отмерших клеток молодыми. Этот процесс происходит в течение всей жизни организма. Интенсивные процессы регенерации обнаруживают при восстановлении клеток крови, эпителия слизистых оболочек. К ним относят также линьку млекопитающих и птиц, рост резцов у грызунов и др. Патологическая регенерация – процесс восстановления поврежденных тканей и органов после действия чрезвычайных раздражителей.
Регенерация различных тканей имеет отличительные особенности, в зависимости от их структурного и морфологического строения: у животных, стоящих на более низкой ступени развития, регенеративные процессы идут более полно. У млекопитающих регенерировать могут клетки всех четырех видов тканей, но в разной степени. Большой регенераторной способностью обладают менее дифференцированные ткани, чем высокодифференцированные. Регенеративная способность оказывается более значительной в эмбриональном периоде жизни.
Регенерация соединительной ткани. Рыхлая соединительная ткань обладает особенно высокой способностью к регенерации. Наиболее активно регенерируют интерстициальные элементы, что очень важно при воспалении и при раневом процессе. В этих случаях идет формирование соединительно-тканного рубца, который замещает возникающий дефект.
Костная ткань обладает выраженной способностью к регенерации. Основными элементами, восстанавливающими поврежденную костную ткань, являются остеобласты (малодифференцированные клетки костной ткани). Заполнение альвеолы остеоидной тканью, организация кровяного сгустка и образование остеоидной ткани начинается в области её дна и особенно активно происходит там, где полость раны сообщалась с костномозговым пространством. Ведущая роль в реорганизации лунки зуба принадлежит эндосту окружающей костной ткани. Надкостница альвеолярного отростка в новообразованной ткани участия не принимает. Заживление рано инфицированных лунок протекает более медленно. В прилежащих костно-мозговых пространствах межзубных перегородок, сообщающихся с полостью лунки, кроме расширенных микрососудов и отека, отмечается воспалительная инфильтрация. Кровяной сгусток, заполняющий альвеолу, обильно инфильтрирован лейкоцитами. В альвеолах после удаления здоровых зубов образование остеоидных балок наблюдается на 6-8 сутки, а в первично инфицированных альвеолах - лишь на 12-е сутки. Весь костный дефект заполняется остеоидной тканью без инфицирования к 45-м суткам, а с инфицированием – через 60 суток.
Активно регенерируют сухожилия, фасции, менее активно – хрящи (регенерируют не клетки хрящевой ткани, а перихондрии) и очень слабо – жировая ткань.
Регенерация эпителиальной ткани. Выраженной способностью к регенерации обладают эпителиальные ткани – многослойный плоский эпителий кожи, роговая оболочка глаза. В процессе заживления ран важное значение имеет регенерация эпидермиса. Отмечается высокая регенераторная способность эпителия слизистой оболочки в полости рта, губ, носа, желудочно-кишечного тракта, мочевом пузыре и др. Процессы регенерации возможны в паренхиме печени, печек, слюнных желез и др.
Процесс регенерации развертывается на различных уровнях организма: системном, органном, тканевом, клеточном, внутриклеточном.
Различают две формы регенерации: клеточную и внутриклеточную (с единым феноменом ядерных и цитоплазматических структур). В зависимости от полноты восстановления, различают типичную и атипичную регенерацию. При атипичной регенерации восстановленная ткань, орган характеризуются значительным отклонением структуры или формы.
Регенерация кожи отличается от регенерации внутренних органов и состоит из следующих сложных взаимосвязанных процессов:
1) стягивание краев раны – контракция раны;
2) внераневой вставочный рост;
3) формирование новых тканей в дефекте и преобразование их в регенерат (комплекс незрелых пролиферирующих клеток в зоне повреждения).
Стягивание краев раны – это компенсаторный процесс, который обеспечивает сравнительно быстрое закрытие кожных дефектов. За счет этого процесса в зону дефекта входит неповрежденная кожа вместе с её специфическими структурами: волосами, железами и т. д. Важная роль в сокращении раневого дефекта принадлежит грануляционной ткани, заполняющей полость раны, и фибробластам, которые могут дифференцироваться в клетки, структурно и функционально сходные с клетками гладкой мускулатуры.
Внераневой вставочный рост – процесс разрастания кожи вокруг раны, направленный на восполнение утраченной массы кожи, связанной с её первичной контракцией.
В отдельных случаях на месте дефекта формируется регенерат со специфическими придатками кожи (волосами, железами, кожными складками). Формирование регенерата – долгий процесс, который продолжается еще длительное время после окончания эпителизации дефекта. Сформировавшийся регенерат всегда атипичен и неполноценен.
Перестройка соединительнотканного рубца, образовавшегося на месте дефекта, и покрывающего его эпителия в нормальную кожу невозможна. Грубая фиброзная ткань, состоящая из толстых пучков коллагеновых волокон, не может перестроиться в нормальную дерму.
На процессы регенерации кожи лица можно влиять гормонами. Кортизол и АКТГ снижает митотическую активность пролиферирущего эпителия, подавляют развитие воспалительного отека, угнетают фагоцитарную активность макрофагов, ограничивают развитие грануляционной ткани. Соматотропин, минералокортикоиды, тиреотропин и тироксин, наоборот, оказывают стимулирующее влияние на развитие соединительной ткани, размножение и дифференцировку клеток. Способствует регенерации кожи и витамин С.
Мышечная ткань регенерирует миобластическим и миосимпатическим способами. Регенераторная способность этой ткани выражена значительно слабее, чем у эпителиальной и соединительной тканей. Поперечно-полосатые мышечные волокна регенерируют путем амитотического деления клеток здоровой ткани, граничащих с поврежденным участком. В дальнейшем образовавшиеся на концах поврежденной мыщцы своеобразные колбовидные выпячивания (мышечные почки) сливаются. В результате происходит восстановление поперечной исчерченности в поврежденных мышечных волокнах. Гладкая мускулатура относительно слабо регенерирует и может происходить благодаря митотическому делению гладкомышечных клеток.
Регенерация нервной ткани. Нервная ткань обладает плохой способностью к регенерации. Эксперименты показали, что нервные клетки периферической и вегетативной нервной системы, двигательные и чувствительные нейроны спинного мозга весьма слабо поддаются регенерации. Наоборот, аксоны нервных клеток, (исключая кору, подкорковые узлы) регенерируют лучше. Кроме того, в процессе восстановления нерва существенное значение имеют шванновские клетки (леммоциты). Они формируют своеобразные трубочки, в которые и врастают регенерирующие волокна центрального конца поврежденного (перерезанного) нерва. В мозге, где роль шванновских клеток заменена клетками глии, регенерация нервных волокон отсутствует.
Раны в стоматологической практике
Раны в стоматологической практике имеют очень важное значение в связи с особенностями челюстно-лицевой области:
- обезображивание лица;
- нарушение функции речи и приема пищи;
- несоответствие вида пострадавшего тяжести повреждения;
- близость жизненно-важных органов (глаз, головного мозга, органа слуха, верхних дыхательных путей, крупных кровеносных сосудов);
- наличие зубов, которые, будучи кариозными, могут являться дополнительным инфекционным фактором, а иногда, и ранящим предметом;
- необходимость в специальном уходе и питании (из поильника, при крайне тяжелых состояниях – через зонд);
- повышенная регенераторная способность тканей лица, резистентность к микробному загрязнению, обусловленные богатством кровоснабжения и иннервации.
Особенности течения гнойных ран челюстно-лицевой области
В отличие от других областей тела, челюстно–лицевая область имеет более развитую сеть сосудов и нервов, за счет чего репаративные процессы в данной области осуществляются за более короткие сроки, но при нагноении раны эта область представляет большую опасность, нежели другие, по причине быстрого распростанения инфекции на головной мозг.
Расположение большого количества нервных окончаний характеризует челюстно-лицевую область как одну из наиболее «болезненных» областей при ранении. В стоматологии предупреждение и незамедлительное лечение гнойных ран имеет очень большое значение, т. к. в челюстно-лицевой области располагаются жизненно-важные органы, крупные кровеносные сосуды. Не стоит забывать, что даже при незначительных повреждениях лица и ротовой полости может развиться гнойный процесс. Если не принимать никаких мер по лечению гнойных ран, то гной может распространяться по клетчаточным пространствам и попадать от челюстно-лицевой области в область средостения.
Причинами раневого процесса челюстно-лицевой области могут являться травмы лица, воспалительные процессы (фурункулы), повреждения слизистой ротовой полости при употреблении грубой пищи, травмировании зубными щетками, столовыми предметами, прикусывание слизистой, ожоги, дерматиты, а также причины, связанные с осложнениями после удаления зубов.
Особенности патогенеза гнойных ран ротовой полости. В первой фазе явления воспаления выражены гораздо больше и очищение раны протекает намного длительнее. Фагоцитоз и лизис девитализированных (нежизнеспособных) в результате травматизации или действия микроорганизмов клеток вызывают значительную концентрацию токсинов в окружающих тканях, что усиливает воспаление и ухудшает микроциркуляцию. Рану с развившейся инфекцией характеризует не только нахождение в ней большого количества микробов, но и их инвазия в окружающие ткани. На границе проникновения микроорганизмов образуется выраженный лейкоцитарный вал. Он способствует ограничению инфицированных тканей от здоровых, демаркации, лизису, секвестрации и отторжению нежизнеспособных тканей. Рана постепенно очищается. По мере расплавления участков некроза и всасывания продуктов распада нарастает интоксикация организма. Об этом свидетельствуют все общие проявления, характерные для развития раневой инфекции. Длительность первой фазы заживления зависит от объема повреждений, характеристики микрофлоры, состояния организма и его сопротивляемости. В конце первой фазы после лизиса и отторжения некротических тканей образуется раневая полость и наступает вторая фаза - фаза регенерации, особенность которой заключается в наиболее мощном развитии грануляционной ткани. После второй фазы наступает фаза рубцевания, характеризующаяся более длительным интервалом течения.
Клинические признаки нагноения проявляются через 2-3 суток после ранения. Развитию гнойного процесса способствует обширность повреждения тканей, неполное удаление поврежденных тканей во время хирургической обработки, наличие в ране вирулентной микрофлоры. Бурное развитие нагноения, выраженная интоксикация, сильные боли в зашитой ране, высокая температура тела характерны для стафилококковой инфекции, при этом в ране отмечается умеренный некроз. Вялое течение воспаления, но с обширными очагами некроза наблюдается при инфицировании ран кишечной палочкой; гнойно-воспалительный процесс в этих случаях склонен к широкому распространению без четких границ воспаления. При стрептококковой инфекции наблюдается выраженный воспалительный инфильтрат с отчетливой гиперемией кожи. Развитие гнойно-воспалительного процесса в ране в первые 3-5 дней после ранения называется первичным нагноением, в более поздние сроки – вторичным нагноением, обусловленным появлением новых очагов некрозов в ране и вторичным инфицированием раны больничными штаммами микроорганизмов. При развитии нагноения усиливаются боли в ране, появляется отечность её краёв, изменяется цвет тканей. Сгустки крови, фибрина, становятся грязно-серыми, увеличивается раневое отделяемое, серозно-геморрагический экссудат меняется на серозно-гнойный, а затем гнойный. Окружающие ткани плотны на ощупь, гиперемированы. Регионарные лимфатические узлы часто увеличены, плотны на ощупь и болезненны. Часто встречается лимфангит.
По мере стихания воспаления уменьшается отек окружающих тканей и гиперемия кожи, отторгаются некротические ткани, стенки раны покрываются грануляциями, т. е. процесс переходит в фазу пролиферации. При неблагоприятном течении нарастают симптомы общей интоксикации: высокая температура тела, озноб, тахикардия; увеличивается отек окружающих тканей, усиливается гиперемия кожи, прогрессирует некроз тканей, увеличивается гнойное отделяемое. Температура тела повышается до 39-40 °С. В тяжелых случаях нарастают общее недомогание, слабость, потеря аппетита, головная боль. В крови нарастают лейкоцитоз и СОЭ, увеличивается сдвиг лейкоцитарной формулы влево. Цвет, запах, консистенция экссудата определяются видом микрофлоры. Ихорозный (специфический сладковатый), зловонный запах, грязно-серый цвет гноя характерны для гнилостной флоры, сине-зелёный цвет экссудата наблюдается в случае гнойного процесса, вызванного синегнойной палочкой, зеленый цвет – зеленящим стафилококком и т. д. Повторный озноб у больных с гнойными ранами при отсутствии болевых ощущений в ране относится к ранним признакам присоединения гнилостного распада тканей. При развитии гнилостной инфекции рана становится сухой, отсутствуют грануляции, нарастает некроз тканей, мышцы серые, тусклые. Отделяемое ран грязно-серого, бурого цвета, иногда с зеленоватым или коричневым оттенком, со специфическим запахом. Окружающие рану кожа и подкожная клетчатка покрыты грязно-зелеными пятнами в результате пропитывания их продуктами гемолиза. Регионарные лимфатические узлы часто увеличены и болезненны. Признакими неклостридиальной анаэробной инфекции являются неприятный запах экссудата, обилие некротических тканей в ране, наличие гнойного содержимого грязно-серого цвета с капельками жира. Выражены признаки тяжелой интоксикации: субиктеричность или желтушность склер и кожи, анемия, тахикардия и др. В отличие от анаэробной клостридиальной (газовой) гангрены местные проявления менее выражены, нет характерного изменения мышц - вида «вареного мяса», отсутствует бронзовая окраска кожи, очень редко отмечается скопление газа в тканях (отсутствие симптома крепитации (хруста)).
Ранения челюстно-лицевой области предполагают развитие одонтогенных воспалительных процессов. Под одонтогенными воспалительными заболева-ниями принято понимать большую группу инфекционно-воспалительных патологических состояний, локализующихся в челюстях, околочелюстных мягких тканях лица и шеи, включая лимфатический аппарат.
Возбудители одонтогенных воспалительных заболеваний – это микроорганизмы, которые обычно входят в состав постоянной микрофлоры полости рта – стафилококки, стрептококки, энтерококки, диплококки, грамположительные и грамотрицательные палочки e. coli, proteus и т. д. Кроме того, в очагах одонтогенной инфекции иногда обнаруживаются грибы, микоплазмы, простейшие из семейства трихомонад, спирохет. Нередко встречаются ассоциации стафилококка со стрептококком, стафилококка с диплококком, грамотрицательными палочками. Весьма часто в очаге воспаления присутствуют анаэробы и, если не вызывают заболевание, то, по крайней мере, утяжеляют течение заболевания. Характер течения инфекционно-воспалительного процесса зависит не только от видовой принадлежности возбудителей, но и от их культуральных свойств. При одонтогенной инфекции, вызванной патогенными штаммами стафилококка, чаще наблюдается развитие остеомиелита челюстей, тогда как непатогенные штаммы этого микроба обычно обусловливают возникновение околочелюстных флегмон и абсцессов. Поэтому результаты микробиологических исследований дают врачу не только ценную информацию о чувствительности микрофлоры инфекционного очага к тем или иным антибиотикам, но и позволяют в известной степени прогнозировать течение заболевания. Частой причиной развития раневых одонтогенных воспалительных процессов может быть механическое повреждение соединительнотканной капсулы очага хронической одонтогенной инфекции, что сопровождается повышением её проницаемости, Это может иметь место при удалении зуба по поводу хронического периодонтита, при резкой чрезмерной нагрузке его пародонта, во время разжевывания твердой пищи и др.
Механизмы распространения одонтогенной инфекции. Понимание механизма распространения одонтогенной инфекции исключительно как процесса поэтапного продвижения гноя по мере разрушения кости, надкостницы, фасций послужило основанием для ряда исследователей рассматривать любой одонтогенный воспалительный процесс как одонтогенный остеомиелит челюстей (, 1968 и др.). Однако существует и другой механизм развития одонтогенной инфекции – распространение бактериальных антигенов, которые сами по себе могут и не обладать повреждающим действием, по многочисленным питательным каналам компактного слоя челюсти в околочелюстные мягкие ткани. В сенсибилизированном организме вероятность встречи антигенов с антителами выше в тех тканях, где гуще сеть капилляров, где лучше условия для клеточной инфильтрации, то есть в рыхлых, хорошо васкуляризованных околочелюстных тканях (по сравнению с костной тканью). Образующийся при такой встрече комплекс антиген-антитело приводит к развитию иммунопатологических реакций, которые сопровождаются повреждением тканей и развитием воспаления.
Факторы, определяющие возникновение деструкции костной ткани и объем ее поражения. К числу таких факторов можно отнести вирулентность инфекционного начала, общую иммунологическую реактивность организма, состояние местного иммунитета и кровообращения (микроциркуляции) в тканях челюстно-лицевой области. Одной из причин нарушения микроциркуляции у больных с острой одонтогенной инфекцией может быть непосредственное повреждение эндотелия капилляров комплексами антиген-антитело, которые фиксируются на клеточных мембранах, а затем фагоцитируются нейтрофильными лейкоцитами. При этом в результате повреждения клеточной мембраны освобождаются лизосомальные энзимы – медиаторы воспаления – и происходит активация каллиреин-кининовой системы. Конечный продукт этой системы – брадикинин – влияет на тонус и проницаемость сосудов микроциркуляторного русла, реологические свойства крови, состояние свертывающей и фибринолитической системы.
Другая причина нарушения микроциркуляции связана с внесосудистым механизмом окклюзии. Сводится она к сдавливанию сосудов воспалительным инфильтратом периваскулярной клетчатки. Этому способствует то обстоятельство, что острый одонтогенный воспалительный процесс возникает в относительно замкнутом костномозговом пространстве, имеющем небольшой объем и ригидные стенки.
Известно, например, что остеомиелит с выраженной деструкцией кости нижней челюсти встречается в 4 раза чаще, чем верхней челюсти. Это обусловлено различием васкуляризации и структуры костного вещества челюсти. В частности, компактная пластинка верхней челюсти гораздо тоньше и более порозна за счет множества пронизывающих ее каналов, в которых проходят нервы, кровеносные сосуды. В связи с этим бактериальные токсины, микроорганизмы и продукты тканевого распада легче и быстрее проникают в околочелюстные ткани, рано вызывая там развитие воспалительного процесса. На нижней челюсти более мощная и менее порозная компактная пластинка препятствует распространению микроорганизмов и продуктов их жизнедеятельности в околочелюстные ткани. Поэтому их концентрация в кости может возрастать до такого уровня, при котором они вызывают повреждение тканевых структур, то есть развитие деструкции костной ткани. Кроме того, благодаря меньшей порозности, внутрикостное давление, связанное с экссудацией, быстрее достигает такой величины, при которой происходит окклюзия сосудов с последующим нарушением микроциркуляции.
Входными воротами для инфицирования могут являться дефекты твердых тканей зуба, зубодесневого прикрепления, эпителиального покрова десны над прорезывающимся (ретенированным) зубом.
Микроорганизмы, вегетирующие в полости рта, зубодесневых карманах, корневых каналах с погибшей пульпой, проникая в ткани пародонта, вызывают в них развитие инфекционно-воспалительного процесса. Поэтому при любой нозологической форме одонтогенной инфекции имеется воспаление костной ткани. Это воспаление может быть ограничено костным структурами пародонта одного зуба, либо распространяться на пародонт соседних зубов, основание челюсти, надкостницу, околочелюстные ткани и смежные анатомические области, а по путям лимфооттока – на регионарный лимфатический аппарат.
Анатомических границ между пародонтом отдельных зубов не существует. Однако с клинической точки зрения для оценки распространенности воспалительного или иного патологического процесса в челюсти определение таких границ целесообразно. Они соответствуют вертикальным плоскостям, проведенным через середину межальвеолярных перегородок.
На верхней челюсти верхняя граница пародонта передних зубов соответствует дну полости носа, боковых зубов – дну верхнечелюстной пазухи.
На нижней челюсти нижняя граница пародонта боковых зубов соответствует верхней стенке нижнечелюстного канала, а нижней границей пародонта передних зубов является горизонтальная плоскость, проходящая через подбородочные отверстия.
Инфекционно-воспалительный процесс, ограниченный пределами пародонта одного зуба, либо захватывающий часть пародонта двух соседних зубов, называют, в зависимости от локализации входных ворот для инфекции, периодонтитом, пародонтитом или перикоронитом:
-если входными воротами для возбудителей инфекционно-воспалительного процесса является дефект твердых тканей зуба, его называют периодонтитом;
-если такими воротами служит дефект зубодесневого прикрепления – пародонтитом,
-в случаях проникновения возбудителей инфекционного процесса через дефект десны над прорезывающимся, ретенированным зубом – перикоронитом.
Если наряду с поражением пародонта одного зуба наблюдается распространение гнойно-воспалительного процесса на надкостницу, десну, такая форма заболевания называется одонтогенным периоститом.
Острые инфекционно-воспалительные процессы в пределах пародонта одного зуба, сочетающиеся с ограниченным или разлитым гнойным воспалением околочелюстных мягких тканей, тканей шеи, являются самостоятельными нозологическими формами заболевания – одонтогенный абсцесс, одонтогенная флегмона той или иной локализации.
Инфекционно-воспалительные процессы в регионарных лимфатических узлах головы и шеи, обусловленные проникновением возбудителя заболевания лимфогенным путем из инфекционного очага в пародонте, называют одонтогенным лимфаденитом, одонтогенной аденофлегмоной.
Если инфекционно-воспалительный процесс распространяется на пародонт нескольких зубов, основание, ветвь нижней челюсти, такая форма заболевания называется одонтогенным остеомиелитом челюсти.
Острому остеомиелиту челюсти обычно сопутствует гнойное воспаление надкостницы (периостит) в пределах пораженного участка челюсти, гнойное воспаление околочелюстных мягких тканей – так называемая остеофлегмона.
Воспаление верхнечелюстной пазухи, обусловленное распространением инфекционно-воспалительного процесса из инфекционного очага в пародонте верхней челюсти, или инфицированием микрофлорой полости рта через перфорационное отверстие, возникшее при удалении зуба, называется одонтогенным синуситом (гайморитом).
Осложнения заживления ран лица. Заживление ран лица может осложняться различными процессами, основными из которых являются следующие:
- развитие инфекции. Возможно развитие неспецифической гнойной инфекции, а также анаэробной инфекции, столбняка, бешенства, дифтерии и пр;
- кровотечение. Может быть как первичное, так и вторичное кровотечение;
- расхождение краев раны (несостоятельность раны). Рассматривается как тяжелое осложнение заживления.
В 1-ю стадию раневого процесса необходимо осуществлять следующее:
1) подавлять микрофлору (общая терапия антибиотиками, местно – антисептики), осуществлять стимуляцию иммунной системы;
2) удалять эксудат из раны (промывание, дренаж);
3) удалять некротизированные ткани из раны (некроэктомия);
4) улучшать кровообращение в ране (физиотерапевтические процедуры и использование специальных препаратов для улучшения микроциркуляции, например, трентал, сермион);
5) улучшать трофику тканей, стимулировать анаболические процессы (витамино - и гормонотерапия);
6) применять протеолитические ферменты, повышающие проницаемость мембран для антибактериальных препаратов, обладающих антикоагуляционными свойствамии, способными ингибировать гиалуронидазу, коллагеназу и т. д.
Во 2-ю стадию раневого процесса при повреждении грануляций в ране воспаление может углубляться, и поэтому главными принципами ведения такого больного является следующее:
1) редкие и бережные перевязки (обработка ран);
2) использование антисептиков на мазевой основе для дальнейшего подавления микрофлоры в ране;
3) стимуляция роста грануляций, улучшение микроциркуляции и метаболических процессов с помощью биогенных стимуляторов;
4) стимуляция эпителизации раны;
5) профилактика формирования келоидного рубца.
В 3-ю стадию раневого процесса для рассасывания келоидного рубца назначаются биогенные стимуляторы (например, алоэ, фибс, стекловидное тело). Хороший терапевтический эффект оказывают физиотерапевтические процедуры (грязи, элекрофорез, фонофорез и др.) и стероидные гормоны.
Самоконтроль по тестовым заданиям
1. ЧТО НАЗЫВАЮТ РАНОЙ
1) любое повреждение, сопровождающееся нарушением целостности какого-либо органа и тканей
2)любое повреждение, сопровождающееся нарушением целостности кожных покровов
3) любое повреждение тканей организма, сопровождающееся нарушением целостности покровных тканей
4) все определения верны
2. КАКОВЫ СРОКИ ПРОТЕКАНИЯ ФАЗЫ РЕГЕНЕРАЦИИ
1) 1–2-е сутки
2) 1–5-е сутки
3) 6–14-е сутки
4) 1–14-е сутки
5) 1–2-я неделя
3. ПРИЗНАКАМИ ПАТОЛОГИЧЕСКИХ ГРАНУЛЯЦИЙ ЯВЛЯЕТСЯ
1) атрофичность, вялость
2) тусклый цвет
3) наличие гнойного или фибринозного налёта
4) избыточность
5) все перечисленное
4. К ОСНОВНЫМ ХАРАКТЕРИСТИКАМ РЕЗАНОЙ РАНЫ ОТНОСИТСЯ
1) ровные края
2) возможно повреждёние глубоко лежащих тканей
3) незначительное повреждение окружающих тканей
4) при отсутствии нагноения склонна заживать без образования грубых рубцов
5) все перечисленное
5. ГЕНЕРАЛИЗОВАННОЕ ОСЛОЖНЕНИЕ ФУРУНКУЛА НОСОГУБНОГО ТРЕУГОЛЬНИКА
1) образование гнойного свища
2) рожистое воспаление
3) образование карбункула
4) абсцедирование
5) синус-тромбоз
6. КЛИНИЧЕСКОЕ ЗНАЧЕНИЕ ВОЗНИКНОВЕНИЯ ВТОРИЧНОГО ИНФИЦИРОВАНИЯ РАНЫ
1) сокращается срок до начала гнойного осложнения
2) агравируется тяжесть инфекционного осложнения
3) удлиняются сроки фазы реорганизации рубца и эпителизации
4) резко возрастает вероятность гнойного осложнения раневого процесса
5) удлиняются сроки фазы регенерации
7. ЗАЖИВЛЕНИЮ РАНЫ ПЕРВИЧНЫМ НАТЯЖЕНИЕМ СПОСОБСТВУЕТ
1) активация фибринолиза
2) наличие в ране дренажа
3) адаптация краев раны
4) образование серомы
5) образование гематомы
8. ВТОРИЧНОЙ ГНОЙНОЙ РАНОЙ НАЗЫВАЕТСЯ РАНА, ОБРАЗОВАВШАЯСЯ
1) после некрэктомии
2) вследствие нагноения чистой операционной раны
3) после удаления инородного тела
4) вследствие иммунодефицита
5) после вскрытия гнойного очага
9. ЗАЖИВЛЕНИЕ РАН ВТОРИЧНЫМ НАТЯЖЕНИЕМ – ЭТО ЗАЖИВЛЕНИЕ
1) посредством гранулирования
2) без натяжения
3) с сосудистой реакцией
4) путем эпителизации
5) после хирургической обработки
10. ПРИНЦИП АКТИВНОГО ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГНОЙНЫХ РАН ОБЕСПЕЧИВАЕТ
1) сокращение фазы регенерации
2) перевод гнойной раны в заживление по типу первичного натяжения
3) нормализацию состояния больного
4) бактериостатический эффект
5) бактерицидное действие
11. АКТИВАЦИЯ КАКОЙ СИСТЕМЫ ЯВЛЯЕТСЯ КЛЮЧЕВОЙ В РАЗВИТИИ ЛОКАЛЬНОГО РАНЕВОГО ВОСПАЛИТЕЛЬНОГО ПРОЦЕССА
1) системы гемостаза
2) каллекреин-кининовой системы
3) системы комплемента
4) всех перечисленных
12. УХУДШАЕТ ТЕЧЕНИЕ РАНЕВОГО ПРОЦЕССА
1) наличие полирезистентной ассоциативной микрофлоры
2) высокая степень микробной контаминации
3) наличие инородных тел
4) нарушение оттока раневого отделяемого
5) все перечисленное
13. В НЕОСЛОЖНЕННОЙ РАНЕ НА ПОЗДНЕЙ ФАЗЕ РАЗВИТИЯ ВОСПАЛЕНИЯ ОБНАРУЖИВАЮТСЯ
1) макрофаги, фибробласты, клетки эндотелия
2) полиморфноядерные нейтрофилы, фибробласты
3) полиморфноядерные нейтрофилы, клетки эндотелия
14. ФУРУНКУЛ ВЕРХНЕЙ ГУБЫ ОПАСЕН
1) развитием перитонита
2) развитием воспаления плевры
3) тромбозом сагиттального венозного синуса
4) развитием подчелюстного лимфаденита
5) развитием паротита
15. КАРБУНКУЛОМ НАЗЫВАЕТСЯ ОСТРОЕ ГНОЙНО-НЕКРОТИЧЕСКОЕ ВОСПАЛЕНИЕ
1) нескольких волосяных мешочков и окружающих тканей
2) клетчаточных пространств
3) нескольких волосяных мешочков, сальных желез и окружающих тканей
4) сальной железы
5) волосяного фолликула, сальной железы и окружающей ткани
16. ОСЛОЖНЕНИЕ, ХАРАКТЕРНОЕ ДЛЯ КАРБУНКУЛА ВЕРХНЕЙ ГУБЫ
1) сепсис
2) некроз кожи
3) гнойный базальный менингит
4) остеомиелит верхней челюсти
5) тромбоз сонной артерии
17. АБСЦЕССОМ НАЗЫВАЕТСЯ
1) острое гнойное воспаление сальных желез
2) острое гнойное воспаление нескольких волосяных фолликулов
3) гнойное воспаление апокриновых желез
4) ограниченное скопление гноя в тканях или органах
5) разлитое воспаление подкожной жировой клетчатки
18. ЛИМФАНГИТОМ НАЗЫВАЕТСЯ ОСТРОЕ ВОСПАЛЕНИЕ
1) лимфатических узлов
2) собственно кожи
3) лимфатических сосудов
4) слизистой оболочки
5) стенок вен
19. ЛИМФАДЕНИТ – ЭТО ВОСПАЛЕНИЕ
1) лимфатических сосудов
2) потовых желез
3) лимфоузлов
4) вен
5) сосочкового слоя кожи
20. ВОСПАЛЕНИЕ КАПСУЛЫ ЛИМФОУЗЛА И ОКРУЖАЮЩЕЙ ТКАНИ НАЗЫВАЕТСЯ
1) абсцесс
2) аденофлегмона
3) карбункул
4) фурункул
5) тромбофлебит
Самоконтроль по ситуационным задачам
Задача №1.
50 лет, работая в мастерской, получил рваную рану левого предплечья, самостоятельно обработав которую (наложив повязку), продолжил работу. Обратился к врачу через 2 суток с жалобами на боли в области раны, повышение температуры тела до 38oС. При осмотре: края раны отёчны, отделяемое гнойное.
1. Какой патологический процесс развился у больного и какова стадия данного процесса?
2. Охарактеризуйте фазу раневого процесса у больного?
3. Каковы основные подходы в оказании помощи данному больному?
Задача №2.
49 лет, была выполнена первичная хирургическая обработка случайной раны тыла правой кисти, завершившаяся наложением первичных швов. Через 2 дня пациент отметил усиление болей в области операции, отёк кисти, повышение температуры тела, в связи с чем повторно обратился к врачу. При осмотре: состояние больного удовлетворительное. По органам без особенностей. Местно: отмечается выраженный отёк тыла правой кисти. Кожа вокруг швов резко напряжена, гиперемирована. Пальпация этой зоны резко болезненная. Функция кисти нарушена.
1. Какой патологический процесс развился у больного после первичной обработки раны?
2. Охарактеризуйте фазы раневого процесса. Какая фаза имеет место у больного?
3. Какое осложнение патологического процесса развилось у больгого К.?
Задача 3.
29 лет, через два дня после травматического удаления 6 зуба верхней челюсти справа температура тела в подмышечной впадине повысилась до 39,9°С.
Объективно: в области удаленного зуба края раны отечны, болезненны, открывание рта также болезненно; кожные покровы у больного бледные, сухие и холодные на ощупь. Состояние больного не удовлетворительное.
1. Какой патологический процесс развился у больного? Перечислите местные и общие признаки этого процесса.
2. Какая фаза раневого процесса имеет место у больного?
3. Какие элементы составляют рану?
4. Перечислите осложнения раневого процесса.
Задача 4.
15 лет, находится на стационарном лечении в клинической больнице по поводу острого лимфаденита правой подчелюстной области, возникшего после острого переохлаждения. В анамнезе у больного хронический тонзиллит, рекомендовано оперативное лечение. Состояние больного неудовлетворительное. Голова наклонена вправо. Справа в подчелюстной области пальпируется плотный инфильтрат, болезненный при пальпации. Температура тела в подмышечной впадине - 38,3ºС. Комплимент С-3 плазмы крови - 2,3 г/л (норма 1,3-1,7 г/л), НСТ - тест 40% (норма 15%), (тест восстановления тетразоля нитросинего отражает степень активации кислородзависимых механизмов бактерицидной активности фагоцитирующих клеток). С - реактивный белок в плазме крови (++), СОЭ - 35 мм/час.
1. Какому патологическому процессу присущи выявленные изменения?
2. Какие симптомы общих реакций организма на воспаление Вы выявили при анализе задачи?
3. Какие местные симптомы воспалительной реакции приведены в задаче?
4. Какие исходы воспалительной реакции Вы знаете?
5. Приведите пример общего анализа крови:
а) при остром воспалении;
б) хроническом.
Задача 5.
46 лет, поступил в стоматологическое отделение клинической больницы с жалобами на лихорадку (температура до 39סС), пульсирующую боль в подчелюстной области справа. Заболевание началось после резкого переохлаждения четыре дня назад. Объективно: в подчелюстной области справа инфильтрат красно-синюшного цвета с участком размягчения по центру. При неотложной помощи произведено вскрытие абсцесса. При лабораторном исследовании в экссудате обнаружено высокое содержание нейтрофильных лейкоцитов. В гемограмме выявлены: ядерный сдвиг влево, ускорение СОЭ. В плазме крови выявлены «белки острой фазы».
1. Для какого воспаления, острого или хронического, более типична указанная ситуация?
2. Что понимается под термином «белки острой фазы» при воспалении? О каких изменениях в организме свидетельствует нахождение «белков острой фазы» в крови и динамика их изменения в разных стадиях заболевания, значение для прогноза.
3. Как подразделяют раны по происхождению и по степени обсеменнености микрофлорой?
4. Какие факторы ухудшают и замедляют течение раневого процесса?
5. Причины возникновения хронического процесса в зубо – челюстной области.
Рекомендуемая литература
Основная:
1.Патофизиология (уч. для мед. вузов) / под ред , М.: ГЭОТАР-МЕД -200с.
2.Атлас по патофизиологии / под ред , МИА: Москва
Дополнительная:
1.Руководство к практическому курсу патофизиологи: учебное пособие / и др. // Р-на-Дону: Феникс
2.Барсуков физиология. Конспект лекций. - М.: ЭКСМО - 2007
3.Гормональная регуляция основных физиологических функций организма и механизмы её нарушения: учебное пособие /ред. . - М.: ВУНМЦ
4.Долгих патофизиология: учебное пособие.- Р-на-Дону: Феникс
5.Патологическая физиология: Интерактивный курс лекций / , , . – М.: информационное агентство» , 2007. – 672с.
6.Robbins S. L., Kumor V., Abbas A. K. et al. Robbins and Cotran pathological basis of disease / Saunders/Elsevier, 2010. – 1450P.
Электронные ресурсы:
1.Фролов патофизиология: Электронный курс по патофизиологии: учебное пособие.- М.: МИА, 2006.
2.Электронный каталог КрасГМУ
3.Электронная библиотека Absotheue
4.БД MedArt
5.БД Медицина
6.БД Гении медицины
7.Ресурсы Интернет





 Цитокин
Цитокин