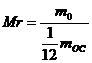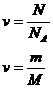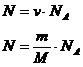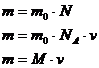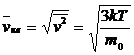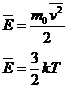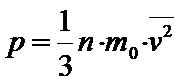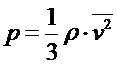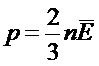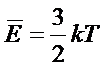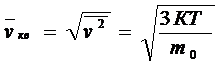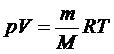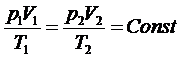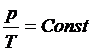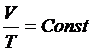Опорные конспекты по теме
«Молекулярная физика»
(10класс)
Основы молекулярно-кинетической теории (МКТ)
МКТ изучает свойства систем, состоящих из большого числа микроскопических частиц, характер движения и взаимодействия этих частиц.

Сформулированы на основе опытов
Основные положения МКТ | Доказательства |
Вещество состоит из частиц | Делимость вещества, растворимость, парообразование (котёл с маслом, спирт с водой) |
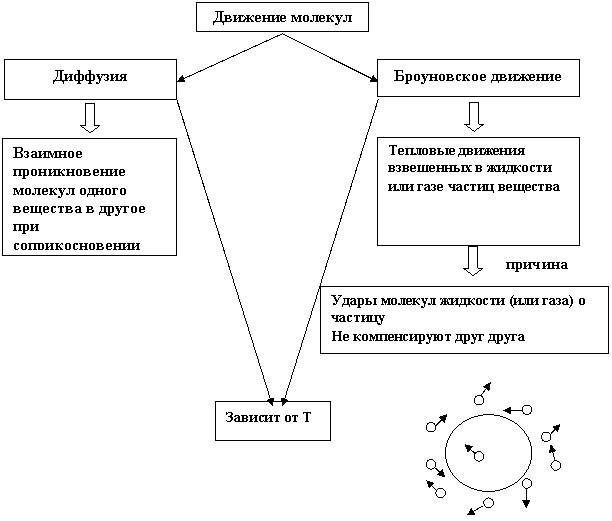
Частицы находятся в непрерывном хаотическом движении | Диффузия (распространение запахов), броуновское движение |
Частицы взаимодействуют друг с другом | Склеивание, смачивание, плохая сжимаемость жидкостей |
Приблизительные значения: размеры атомов D ~ 1010 м
масса атомов m0 ~ 1026 кг
Основные величины молекулярной физики
Наименование величины | Обозначение | Формула | Единица измерения | |
1 | Относительная молекулярная масса | Mr |
m0С-масса атома углерода | - |
2 | Количество вещества |
|
| Моль |
3 | Число молекул |
|
| - |
4 | Молярная масса | М |
|
|
5 | Масса молекулы | m0 |
| кг |
6 | Масса вещества | m |
| кг |
7 | Концентрация молекул | n |
|
|
8 | Средняя квадратичная скорость | Vкв |
|
|
9 | Средняя кинетическая энергия молекул |
|
| Дж |
NA = 6.022·1023 1/моль - постоянная Авогадро
k = 1,38·10-23 Дж/К - постоянная Больцмана
Тепловое движение
беспорядочное (хаотичные) движение молекул в твердых телах, жидкостях и газах.
Силы взаимодействия между молекулами
| |
 | |
| |
 |
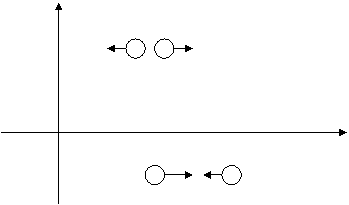
Модель взаимодействия между двумя молекулами
![]() При растяжении пружины шарики стремятся сблизиться
При растяжении пружины шарики стремятся сблизиться
![]() При сжатии отталкиваются
При сжатии отталкиваются
 |
|
|
При r = 2r0 силы притяжения и отталкивания уравновешены
При r > 2r0 преобладают силы притяжения
При r < 2r0 преобладают силы отталкивания
Строение газообразных, жидких и твердых тел
Газ | Жидкость | Твердое тело | |
Свойства вещества | Не сохраняет форму и объем, легко сжимаем | Сохраняет объем, не сохраняет форму, течет | Сохраняет объем и форму |
Структура вещества | Беспорядок (хаос) | Ближний порядок | Дальний порядок |
Характер теплового движения | Хаотическое движение | Сочетание колебаний молекул со скачком из одних временных положений равновесия в другие | Колебания частиц вблизи положений равновесия |
Силы взаимодействия между молекулами | Недостаточны, чтобы удержать молекулы друг около друга | Способствует упорядоченному расположению соседних молекул | Удерживают молекулы вблизи положений равновесия |
«Идеальный газ»
Газ (греч. chaos) - хаос.
Идеальный газ - это газ, взаимодействие между молекулами которого пренебрежительно мало.
«Идеальный газ»:
1. Число молекул в V велико
2. Размеры молекул << расстояний между ними (разреженные газы)
3. Распределение молекул в V равномерно
4. Соударения между молекулами абсолютно упругие
5. Молекулы взаимодействуют только в момент соударения
6. К движению молекулы применимы законы механики Ньютона
|
 | |
| |
Основное уравнение МКТ газа
МКТ устанавливает количественную связь между макроскопическими величинами, характеризующими состояние газа (давление, температура) и микроскопическими величинами, характеризующими движения молекул.
|
 |
Импульс, передаваемый всем молекулам при ударе о стенку сосуда и отскоке
|
F·Δt=2m0 ·VX·Z,
F=p·S
|
 |  | ||
 | 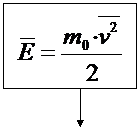 | ||
|
|
Термодинамическая система – это совокупность рассматриваемых микроскопических тел, которые могут взаимодействовать между собой и с внешней средой (обмениваться энергией и веществами).
Изолированная – это термодинамическая система, которая не взаимодействует с внешними телами
Макроскопические параметры – физические величины, характеризующие состояние макроскопических тел без учета молекулярного строения тел
Тепловое (термодинамическое) равновесие – это такое состояние системы, при котором все макроскопические параметры сохраняют свои значения с течением времени
Процесс – переход термодинамической системы из одного состояния в другое.
Термодинамическая система
 | |||||||||||||||||||||||
 | |||||||||||||||||||||||
|
| ||||||||||||||||||||||
 |  | ||||||||||||||||||||||
 | |||||||||||||||||||||||
|
| ||||||||||||||||||||||
|
| ||||||||||||||||||||||
| |||||||||||||||||||||||
Температура
Температура характеризует состояние теплового равновесия термодинамической системы (все тела системы имеют одну и ту же температуру)
![]() Измерение температуры
Измерение температуры
 |
| |||||||
|
|
|
| ||||
 |
|
|
|
|
|
0°C – температура таяния льда
100°C – температура кипения воды
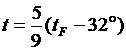
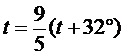
Абсолютная шкала температур (шкала Кельвина)
![]()
![]()
|
k – постоянная Больцмана
T – абсолютная (термодинамическая) температура
|
Tmin = 0 – абсолютный нуль температуры
(p = 0 при V = const или V → 0 при p = const)
|
|
Закон Авогадро | p = nkT |
Средняя квадратичная скорость (подтверждение – опыт Штерна) |
|
Уравнение состояния идеального газа
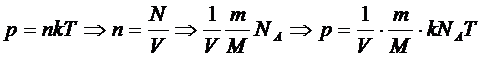
|
- уравнение Менделеева – Клапейрона
R = kNA = 8,31 Дж / моль ∙ К – универсальная газовая постоянная
|
- уравнение Клапейрона
|
Газовые законы (m = Const)
Название | З а к о н | Г р а ф и к и | I закон термодинамики | ||||||||||||||||||||
  T = Const | pV = Const (Бойль, 1662 г Мариотт, 1676 г) | ∆U = 0 Q = A | |||||||||||||||||||||
   V = Const |
(Шарль, 1787 г) | A = 0 Q = ∆U | |||||||||||||||||||||

  p = Const |
(Гей-Люссак, 1802) | Q = ∆U + A | |||||||||||||||||||||
4. Адиабатный Q = 0 | Q = 0 ∆U = A |