ИССЛЕДОВАНИЕ ЭКОЛОГИЧЕСКОГО СОСТОЯНИЯ
РЕЧНОЙ ВОДЫ РЕКИ ПИШЛЯ
Вода - одно из самых распространённых на Земле и необычных по своим свойствам химических соединений. Без воды невозможно существование самой жизни. Вода – носитель тепловой и механической энергии играет важнейшую роль в обмене веществом и энергии между геосферами и географическими районами Земли. Этому во многом способствуют и её аномальные физические и химические свойства. Один из основоположников геохимии, , писал: «Вода стоит особняком в истории нашей планеты. Нет природного тела, которое могло бы сравнится с ней по влиянию на ход основных, самых грандиозных геологических процессов. Нет земного вещества – минерала, горной породы, живого тела, которое её бы не заключало. Всё земное вещество – под влиянием свойственных воде частных сил, её парообразного состояния, её вездесущности в верхней части планеты – ею проникнуто и охвачено». (2)
К сожалению, в последнее время интерес исследователей к воде основан скорее не на изучении её необычных, уникальных и в то же время универсальных свойств, а на исследовании её экологического состояния, поиска путей её очищения, её защиты от бесцеремонного, безответственного отношения к ней человека. (2)
Результатом не всегда разумной хозяйственной деятельности человека стало увеличение безвозвратного водопотребления (до полного истощения водных источников) и угрожающее загрязнение природных вод, что вносит нередко необратимые изменения в водный баланс и экологические условия обширных районов. Это обусловило возникновение нового направления гидрологической науки – гидролого-экологическую, изучающего необратимые процессы и явления в природной среде и биосфере, возникающие в результате интенсивного антропогенного воздействия, а также близкие и отдалённые во времени последствия этих воздействий. (2)
Острейшей гидрологической проблемой стало изменение качества природных вод и состояния водных экосистем под влиянием хозяйственной деятельности человека. Стремительное распространение веществ антропогенного происхождения привело к тому, что на поверхности Земли практически не осталось пресноводных экосистем, качество воды которых не изменилось бы в той или иной степени. Следствием химических и физических воздействий антропогенного происхождения является изменение состава донных отложений и живого вещества водных объектов. (2)
Факторы, воздействующие на водные объекты посредством изменения поверхности речных водосборов, особо ощутимо сказываются на экологическом состоянии малых рек. Малые реки играют решающую роль в формировании водных ресурсов. (2)
Одна из основных особенностей малых рек – тесная связь формирования стока с ландшафтом бассейна. Это обуславливает необычайную уязвимость рек при интенсивном освоении водосбора. Увеличение распаханности земель, отставания почвозащитных мероприятий и распашка до уровня воды, вырубка лесов и осушение болот на их водосборах, строительство крупных животноводческих
комплексов, ферм и птицефабрик без проведения сопутствующих природоохранительных мероприятий и сброс в реки сточных вод без надлежащей очистки быстро приводит к нарушению экологической обстановки, ускорению старения малых рек. Рациональное комплексное использование ресурсов малых рек, их охрана от загрязнения и истощения требуют безотлагательных мер. (2)
Загрязнение речных вод может носить промышленный, бытовой характер, являться последствием сельскохозяйственных работ. Для выбранного нами объекта изучения, актуальными являются бытовое загрязнение и загрязнения, являющиеся следствием сельскохозяйственных работ, то есть вымывание из почвы в воду рек составных частей минеральных удобрений.
Значительным источником загрязнения водоёмов (малых рек) могут быть бытовые сточные воды, которые уносят с собой физиологические выделения человека, кухонные помои, загрязнения от умывания, стирки белья и мытья помещений, а также некоторые плотные отбросы: бумагу, обрывки тканей, сор. В этих стоках 60% составляют органические вещества. (4)
Весьма неблагоприятное влияние на водоёмы и водостоки оказывают поверхностно-активные вещества (ПАВ), которые содержатся главным образом в бытовых стоках, поскольку ПАВ всё больше используют как моющее средство. Водные растворы ПАВ имеют неприятный вкус и запах, дают стойкую пену, появление которой в водоёмах не только неприятно с точки зрения эстетики, но и препятствуют аэрации, ухудшая тем самым биохимическую очистительную способность водоёмов. Кроме того, в пене концентрируются другие органические загрязнения и различные микроорганизмы (в том числе вызывающие заболевания человека) в такой степени, что содержание их в пене может превышать концентрацию в воде в сотни раз. ПАВ имеют способность эмульгировать другие загрязняющие вещества, и делать их более стойкими к окислению; даже в небольших количествах прекращают рост водорослей и другой водной растительности. (2)
Кроме того, даже такие безобидные, казалось бы, гигиенические препараты, как шампунь от перхоти, и то могут повредить водоёму, так как действующим началом противоперхостных шампуней является, например, пиритионат цинка и дисульфид селена – вот вам уже два члена ряда токсичных металлов. (1)
Отличительной способностью бытовых сточных вод является их бактериальное загрязнение: в одном кубическом миллиметре воды могут содержаться десятки миллионов бактерий, в том числе болезнетворных, а также яйца глистов. Количество бытовых сточных вод примерно соответствует количеству потребляемой водопроводной воды. (4)
Чем дальше, тем более опасным источником загрязнений водоёмов становится сельское хозяйство. За последние несколько десятилетий, производство, а следовательно и использование минеральных удобрений в стране выросло в несколько десятков раз, выросло и производство средств защиты растений. Производство этих веществ будет увеличиваться и в дальнейшем. Это способствует урожайности сельскохозяйственных культур. Однако удобрения и особенно ядохимикаты, предназначенные для уничтожения сорняков и насекомых, при неправильном их применении смываются в водоёмы, а их растворы просачиваются в нижележащие водоносные слои грунта и тоже попадают в водоёмы.(4)
Сельскохозяйственные стоки также являются источниками многих металлов. Большинство тяжёлых металлов, естественно, не могут находиться в водной среде в растворимом виде, но присутствуют там в виде коллоидных частичек, а в смеси с другими органическими веществами часто выпадают на дно. Поэтому содержание металла в придонных осадках часто рассматривается как показатель степени загрязнённости воды металлами. (1)
Известное значение имеют также и ливневые стоки, которые смывают в реки загрязнения с поверхности земли: при сильных ливнях и затяжных дождях их количество может превышать бытовые стоки, а концентрация загрязняющих веществ в них оказаться высокой. Поэтому поддержание в чистоте верхних слоёв почвы и промышленных площадок и особенно предотвращения загрязнения их химическими отходами имеет существенное значение для охраны рек от загрязнений. (4)
Реки весьма чувствительны ко всем посторонним вмешательствам и необходимо бережное их сохранение и рациональное использование их вод. Задача, стало быть, заключается в том, чтобы всячески сохранять реки от загрязнения. (2)
Целью данной работы является изучение основных показателей воды реки Пишля, а также содержание в ней различных примесей.
В связи с этим я ставлю перед собой следующие задачи:
Определить основные показатели воды реки Пишля: цветность, запах, прозрачность воды и реакцию среды. Определить массу взвешенных в воде примесей. Определить массу растворенных в воде примесей. Определить содержание катионов калия, натрия, кальция, аммония, Fe2+, Fe3+ в речной воде реки Пишля. Определить содержание следующих анионов в речной воде: CO32 -,Cl -, SO42 -, NO3 -, PO43 -, HPO42 -, H2PO4 -.
6. Определить содержание органических веществ в воде реки Пишля.
Материалы и оборудование: универсальная индикаторная бумага со шкалой, цилиндры, фильтровальная бумага, воронка, химический стакан, лист белой бумаги, колба с притёртой пробкой, пробирки, технохимические весы с разновесами, фарфоровые чашки, водяная баня, часовое стекло, спиртовка, спички, скальпель.
Вещества: исследуемая и дистиллированная вода, растворы нитрата серебра AgNO3, хлорида бария BaCl2, соляной кислоты HCl, роданида калия KCNS или аммония NH4CNS, жёлтая кровяная соль, красная кровяная соль, перманганат калия, гексанитрокобальтиат (3) натрия, гексагидроксостибиат (5) калия, карбонаты натрия и калия, серная кислота, алюминий, гидроксид натрия, хлорид магния, хлорид аммония, аммиак.
1. Ход исследований.
1.1. Определение цветности воды.
Цветность природных вод обусловлена наличием, прежде всего гуматов железа (железных солей гуминовых кислот), а также сточными, бытовыми водами, которые попадают в реки. Повышенной цветностью обладает вода рек, имеющих болотный тип питания.
Мутную воду перед анализом на цветность следует отфильтровать.
В стеклянные цилиндры наливают отдельно исследуемую и дистиллированную воду. На фоне белого листа бумаги при дневном освещении воду рассматривают сверху и сбоку. На основе этого оценивают цветность, то есть указывают наблюдаемый цвет (бурый, жёлтый и т. д.). При отсутствии окраски вода считается бесцветной.(5)
1.2. Определение запаха воды.
Запахи воды могут быть связаны с жизнедеятельностью водных организмов (высших водных растений, водорослей и др.), а также появиться при их отмирании. Это естественные запахи. Бывает и так, что в реку попадают и производственные сточные воды, и бытовые воды с примесями определённого запаха (фенолы, формальдегид и др.). Это искусственные запахи. Силу запаха оценивают по пятибальной шкале.
Таблица 1. Шкала силы запаха воды.
Запах | Интенсивность | Оценка в баллах |
Отсутствие | Не ощущается | 0 |
Очень слабый | Обнаруживается только опытным исследованием | 1 |
Слабый | Обнаруживается потребителем только в том случае, если обратить внимание | 2 |
Заметный | Легко обнаруживается потребителем | 3 |
Отчётливый | Вода имеет сильный запах и непригодна для питья | 4 |
Очень сильный | Вода имеет резкий запах и непригодна для питья | 5 |
В колбу с притёртой пробкой наливают исследуемую воду (2/3 объёма) и сильно встряхивают в закрытом состоянии. Затем открывают и сразу же отмечают характер и интенсивность запаха.(5)
1.3. Определение прозрачности воды.
Наличие в природной воде грубодиспергированных примесей обуславливает её мутность. Часто в качестве косвенного показателя используют характеристику, обратную мутности – прозрачность. Определение прозрачности воды основано на нахождении максимальной высоты столба воды, через который можно прочитать стандартный шрифт.(5)
1.4. Определение реакции среды – рН.
Вода является слабым электролитом, она слабо диссоциирует по уравнению
Н2О = Н+ + ОН-
При 250 С в 1л воды распадаются на ионы 10-7 моль Н2О. Концентрация ионов Н+ и ОН - (в моль/л) будет равна
(Н+) = (ОН-) = 10-7
В этом случае среда нейтральная. Если же (Н+) > (ОН-) > 10-7 – среда кислая; в случае (Н+) < (ОН-) < 10-7 моль/л – среда щелочная. На практике для выражения кислотности и щёлочности вместо концентрации (Н+) используют её отрицательный десятичный логарифм, который называют водородным показателем рН:
рН = - lg (Н+)
Если рН = 7 – среда нейтральная, рН < 7 – кислая, рН > 7 – щелочная.
В пробирку налили на 2/3 объёма исследуемой воды и смачивают в ней кусочек универсальной индикаторной бумаги, затем сравнивают окраску бумаги со шкалой и устанавливают величину рН.(5)
1.5. Определение массы взвешенных в воде примесей.
На технохимических весах взвесили бумажный фильтр. Затем прифильтровали через него 500 мл воды. Высушенный на воздухе фильтр вместе с осадком снова взвешивают. По разности между массой фильтра с осадком и без него определяют массу осадка.
Расчёт массы взвешенных частиц ( г/л ) проводят по формуле:
mв= ![]() , где
, где
mв - масса взвешенных частиц, г/л;
m1 - масса чистого сухого фильтра, г;
m2 - масса высушенного фильтра с осадком, г;
V - объём воды, взятой для фильтрования, мл.
1.6. Определение массы растворённых в воде примесей (общей минерализации).
Мерным цилиндром отмеряют 100 мл отфильтрованной в предыдущем опыте воды и небольшими порциями выливали в большую фарфоровую чашку, предварительно взвешенную на технохимических весах. Выпаривание проводили на водяной бане.
После выпаривания чашка снова взвешивается, и разница показывает массу растворимых веществ. Умножив её на 10, получают содержание растворённых веществ в г/л (общая минерализация).
mр = (m2 – m1) • 10 ,где
mр – масса растворённых в воде примесей, г/л;
m1 - масса фарфоровой чашки, г;
m2 - масса чашки с сухим остатком, г.
Сухой остаток сохраняется для последующих анализов.
Если общая минерализация превышает 5 г/л, то целесообразно определить качественным путём наличие основных растворённых примесей.(5)
1.7. Качественное определение растворимых примесей в речной воде.
Химические компоненты природных вод условно делят на пять групп:
1) главные ионы (анионы: HCO3- , SO42- , Cl- , CO32-, HSiO3- и катионы: Na+, Ca2+, Mg2+, K+, Fe2+);
2) растворённые газы (O2, CO2, H2S);
3) биогенные вещества - неорганические соединения азота (NH4+, NO2-, NO3-) и минеральные формы содержания фосфора (H2PO4-, HPO42-) и др.
4) микроэлементы – это элементы, содержание которых в воде составляет менее 1 мг/л (типичные катионы Li+, Rb+, Cs+, Ba2+ и др.; ионы тяжёлых металлов Cu2+, Ag+, Cd2+ и др.; типичные анионы I-, F-, Br- и др.);
5) органические вещества, основная часть которых гумусовые соединения, образующиеся при разложении растительных остатков.(5)
В условиях школьной лаборатории возможно определить следующие ионы и вещества: карбонат-ионы, хлорид-ионы, сульфат-ионы, ионы кальция, ионы натрия, ионы калия, органические вещества, ионы железа Fe2+, Fe3+, ионы аммония.
1.7.1. Обнаружение ионов NH4+.
Ион аммония в дальнейшем может быть внесен в анализируемую смесь с групповыми реагентами, поэтому его следует обнаружить предварительно. Для этого используем специфическую реакцию выделения аммиака при действии щелочей. К анализируемому раствору нужно добавить 2-3 капли раствора NaOH или KOH. Щелочи (NaOH, KOH) при нагревании выделяют из солей аммония газообразный аммиак:
NH4+ + OH - = NH3↑ + H2O
Выделение аммиака подтверждаем по запаху, индикаторной бумагой (лакмусовая, фенолфталеиновая) или бумагой, смоченной раствором Hg2(NO3)2. Выделение мельчайших частиц свободной ртути вызывает почернение бумаги, смоченной раствором Hg2(NO3)2.(3)
1.7.2. Обнаружение карбонат-ионов.
Полученный сухой остаток после выпаривания пробы воды в предыдущем опыте испытывают на наличие в нём карбонат-ионов CO32-. Для этого на часть сухого остатка надо подействовать раствором соляной кислоты. Если при этом будет наблюдаться «закипание» с выделением пузырьков газа, не имеющего запаха (СО2), значит вода обладает гидрокарбонатной жёсткостью.
CaCO3 + 2HCl = CaCl2 + CO2 + H2O
MgCO3 + 2HCl = MgCl2 + CO2 + H2O
Если остаток не «вскипает», то в нём содержатся хлориды или сульфаты.(5)
1.7.3. Обнаружение хлорид-ионов.
Хлорид-ионы можно обнаружить с помощью 2% раствора нитрата серебра. Несколько капель раствора нитрата серебра добавляют в исследуемую воду. Помутнение будет тем значительнее, чем больше содержание хлорид-ионов в воде.
Ag+ + Cl - = AgCl (5)
1.7.4. Обнаружение сульфат-ионов.
Сульфаты определяют по помутнению воды в пробирке от раствора хлорида или нитрата бария. Воду предварительно подкисляют разбавленным раствором соляной кислоты.
Ba2+ + SO42- = BaSO4 (5)
1.7.5. Определение ионов кальция, калия, натрия.
На кончике чистого ножа из нержавеющей стали (или скальпеля) внести немного сухого остатка в наружный конус пламени спиртовки. Жёлтая окраска пламени укажет на соли натрия, фиолетовая – калия, кирпично-красная – кальция.
Совместное присутствие катионов мешает определению.
Так как речная вода, очевидно, содержит несколько из перечисленных ионов (K+ , Na+, Ca2+), то целесообразно прибегнуть к дробному методу определения катионов.(5)
1.7.5.1.Определение ионов калия.
С этой целью можно провести реакцию с Na3(Co(NO2)6). Мешающие ионы предварительно осаждаем в виде карбонатов, для чего к пробе анализируемой речной воды добавляем насыщенный раствор Na2CO3 до щелочной реакции. Осадок отделим. В растворе обнаружим ионы кальция.
К пробе полученного раствора добавим гексанитрокобальтат натрия Na3(Co(NO2)6). В присутствии ионов калия выпадает жёлтый кристаллический осадок.
2K+ + Na+ + (Co(NO2)6)3- = K2Na(Co(NO2)6) (3)
1.7.5.2.Определение ионов натрия.
Можно использовать реакцию с K(Sb(OH)6). Мешающие ионы осаждаем в виде карбонатов, как и в предыдущем этапе, только используем карбонат калия. Затем к раствору прибавляем равный объём реактива. В присутствии ионов Na+ выпадает белый кристаллический осадок.
Na+ + (Sb(OH)6)- = Na(Sb(OH)6) (3)
1.7.5.3.Определение ионов кальция.
В этом случае используют микрокристаллоскопическую реакцию образования гипса CaSO4*2H2O. Катионы второй группы и ионы свинца образуют малорастворимые сульфаты, затрудняя определение Са2+. Поэтому предварительно отделили мешающие ионы в виде сульфатов, используя сравнительно большую растворимость CaSO4 в воде.
К анализируемому раствору добавляем немного серной кислоты(1:4). Осадок отделяем. Каплю центрифугата помещаем на предметное стекло, выпариваем до появления белой каёмки и рассматриваем под микроскопом. В присутствии Са2+ образуются игольчатые кристаллы гипса.
Са2+ + SO42- = CaSO4 (3)
1.7.6. Обнаружение ионов Fe2+ и Fe3+.
Если сухой остаток после выпаривания исследуемой воды имеет жёлтый или желтоватый цвет, то это свидетельствует о наличие ионов железа в воде.
Для обнаружения ионов Fe2+ к нескольким миллилитрам исследуемой воды добавить немного раствора красной кровяной соли K3(Fe(CN)6).
В присутствии ионов Fe2+ появляется синий осадок турнбулевой сини:
3Fe2+ + 2(Fe(CN)6)3- = Fe3(Fe(CN)6)2.
Для обнаружения ионов Fe 3+ к исследуемой воде прилить раствор жёлтой кровяной соли K4(Fe(CN)6)3. В присутствии ионов Fe3+ образуется тёмно-синий осадок «берлинской лазури»:
4Fe3+ + 3(Fe(CN)6)4- = Fe4(Fe(CN)6)3. (5)
1.7.7. Обнаружение органических веществ.
Взять две пробирки, в первую налить несколько миллилитров дистиллированной воды, в другую - столько же исследуемой воды. В каждую пробирку прибавить по 2-3 капли 1% раствора перманганата калия. В пробирке с дистиллированной водой розово-фиолетовая окраска перманганата калия сохранится. Исчезновение окраски или побурение исследуемой воды указывает на присутствие в ней органических веществ (иногда неорганических восстановителей). Такая вода непригодна для питья.(5)
1.7.8. Обнаружение нитрат-ионов.
Активные металлы (цинк, алюминий) восстанавливают нитрат-ион в щелочном растворе до аммиака:
3NO3- + 2H2O + 8 AL + 5OH - = 8AlO2- + 3NH3.
В пробирку с исследуемой водой поместили 2-3 капли раствора гидроксида натрия и 1-2 гранулы цинка или алюминия. Пробирку неплотно закрыли кусочком ваты, на которую положена влажная лакмусовая бумага или фильтровальная бумага, смоченная раствором Hg2(NO3)2. Если выделение газа происходит слабо, пробирку слегка нагреем, не допуская бурного выделения водорода. В присутствии нитрат-ионов наблюдается посинение лакмусовой бумаги или появления чёрного пятна на бумаге, смоченной солями ртути.(3)
1.7.9. Обнаружение фосфат-ионов.
Магнезиальная смесь (раствор, содержащий MgCl2, NH4Cl, NH3) с фосфат-ионами и гидрофосфат-ионами образует белый кристаллический осадок MgNH4PO4*6H2O, растворимый в HCl, CH3COOH, но не растворимый в NH3.
НРО42- + Mg2+ + NH3 = MgNH4PO4.
К исследуемой воде прибавляем немного магнезиальной смеси и перемешайте. В присутствии фосфат-ионов образуется белый кристаллический осадок.(3)
2. Результаты и наблюдения.
2.1. Результаты исследований физических и некоторых химических параметров речной воды свели в таблицу:
Таблица 2.Физические параметры и некоторые химические свойства речной воды р. Пишля.
Объект исследо- вания | Цвет воды | Запах | Прозрачность, см | рН | Масса взвешенных в воде примесей mв, г/л | Масса растворённых в воде примесей mр, г |
Вода реки Пишля | Светло- серый | 3 | 25 | 5.0- 5.5 | 5,8 | 11 |
2.2. Рассчитаем массу взвешенных в воде частиц:
mв= 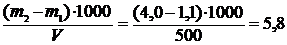 г/л
г/л
2.3. Рассчитаем массу растворённых в воде частиц:
mр= (m2 – m1) • 10 = (22,1 – 21,0) • 10 = 11,0г.
2.4. Результаты исследований качественного состава речной воды свели в таблицу:
Таблица 3.Качественный состав речной воды.
Объект исследо-вания | Определя- емый ион | Реагент | Наблюдения | Вывод |
Речная вода р. Пишля | NH4+ | NaOH, универсальная индикаторная бумага | Цвет индикаторной бумаги изменился на синий | Ионы аммония присутствуют |
CO32- | HCl | «Закипания» не произошло | Карбонат-ионы отсутствуют | |
Cl- | AgNO3 | Наблюдаем помутнение раствора | Хлорид-ионы присутствуют в исследуемой воде | |
SO42- | Ba2+ | Раствор помутнел | Сульфат-ионы обнаружены | |
K+ | Na3(Co(NO2)6) | Наблюдаем образование жёлтых кристаллов | Ионы калия обнаружены | |
Na+ | K(Sb(OH)6) | Образуются белые кристаллы | Ионы натрия присутствуют | |
Ca2+ | H2SO4 | Наблюдаем игольчатые кристаллы | Ионы кальция присутствуют | |
Fe2+ | K3(Fe(CN)6)2 | Синяя окраска не образовалась | Ионы Fe2+ не обнаружены | |
Fe3+ | K4(Fe(CN)6)3 | Наблюдаем образование осадка | Ионы Fe3+ обнаружены | |
NO3- | Al | Лакмусовая бумажка посинела | Нитрат-ионы присутствуют | |
PO43- HPO42- H2PO4- | MgCl2, NH4Cl, NH3 | Наблюдаем оброзование белых кристаллов | Предполагаем, что осадок обусловлен наличием дигидрофосфат- ионов | |
Органические вещества | KMnO4 | Раствор марганцовки обесцветился | Речная вода содержит органические загрязнения |
3. Выводы.
1. Проведены исследования физических параметров речной воды реки Пишля.
2. Исследования показали, что речная вода имеет светло-серый цвет, ярко выраженный запах, скорее искусственного происхождения, оцениваемый по шкале запахов в 3 балла. Вода имеет небольшую прозрачность, лишь порядка 25 см. Все эти показатели говорят о плохом качестве воды в реке, которые, естественно, делают её непригодной для питья и ограничивают употребление для хозяйственных целей.
3. Проведены исследования некоторых химических свойств.
4. Исследования показали, что среда речной воды слабо кислая (рН=5.0-5.5). Вода содержит взвешенные в воде примеси порядка 5,8 г/л. Кроме того, речная вода содержит растворённые в воде примеси порядка 11 г/л, что делает целесообразным проводить качественное определение растворённых примесей в речной воде.
5. Проведён качественный анализ речной воды р. Пишля.
6. Исследования показали, что речная вода содержит хлорид-ионы, сульфат-ионы, нитрат-ионы, дигидрофосфат-ионы, а также ионы калия, натрия, кальция, железа Fe3+, ионы аммония и органические вещества. Очевидно, содержание органических веществ в речной воде является следствием хозяйственной деятельности человека, то есть входящие в состав скорее бытовых отходов. А наличие в речной воде ионов К+, Fe3+, Na+ , NH4+, нитрат-ионов, дигидрофосфат-ионов, хлорид-ионов является следствием вымывания из почв минеральных удобрений и ядохимикатов.
4. Рекомендации.
1. В результате проделанных исследований рекомендуем не использовать речную воду реки Пишля для питья и по возможности ограничить её использование для хозяйственных нужд.
2. В целях улучшения качества речной воды рекомендуем жителям близлежащих районов не сбрасывать в реку бытовые отходы, а использовать для этих целей канализации для жидких отходов и мусорные контейнеры для твёрдых мусорных отходов.
3. Кроме того, для исключения попадания в реку компонентов минеральных удобрений и ядохимикатов соблюдать нормы, сроки и методы применения удобрений и особенно ядохимикатов. Обеспечить выявление факторов, влияющих на стекание и фильтрацию с полей загрязняющих вод и ограничить эти процессы, бороться с водной эрозией почв, оползневыми явлениями, разрушающие берега рек.
5. Литература.
1. О токсичности ионов металлов. М.: Знание, 1991. 32с.
2. Кушелев природы от загрязнений промышленными выбросами. – М.: Химия, 19с., ил.
3. , , Шегал обнаружения и разделения элементов: Лабораторный практикум. – Саранск, 1986. 63с.
4. Соросовский образовательный журнал, №5,12 1996 год.
5.Экологический практикум: Учебное пособие/ Сост. ; МО РМ, МРИПКРО – Саранск, 20с.



