ИССЛЕДОВАНИЕ ЭКОЛОГИЧЕСКОГО СОСТОЯНИЯ ПОЧВЫ НА ПРИШКОЛЬНОМ УЧАСТКЕ
Почва — верхний корнеобитаемый слой земной коры, из которого растения извлекают необходимые для их жизнедеятельности воду и элементы минерального питания. На поверхности земного шара сформировано множество различных почв, различающихся по внешнему виду, химическим и физическим свойствам. Только на территории бывшего СССР называют более 90 типов и 208 подтипов почв, не считая того, что выделяют и более мелкие единицы, различающиеся по содержанию песка и глины, содержанию гумуса и другим показателям. Существуют приемы, методы, показатели, чтобы почвы можно было различать и классифицировать. Создано несколько различных классификаций. Согласно , почвы различаются по условиям их образования, происхождению, внешнему виду. Академик предложил классификацию, основанную на химических свойствах почв. Используют при классификации особенности водного и теплового режимов, сочетания различных горизонтальных слоев (горизонтов) в толще почвы, наличие плотных прослоек и многое другое.
Целью данной работы является исследование экологического состояния почвы на территории пришкольного участка гимназии №1 в весенне-летний период 2009 года.
Задачи:
· Исследовать основные морфологические признаки и физические свойства почвы: структуру, водопрочность структурных агрегатов, окраску, плотность, влажность.
· Исследовать кислотность почвы.
· Определить качественный состав почвы.
· Сделать выводы о мерах повышения качественных характеристик почвы и повышения её плодородия.
Ход исследований.
1. ОПРЕДЕЛЕНИЕ ФИЗИЧЕСКИХ СВОЙСТВ ПОЧВ
Анализ почвенных образцов целесообразно начинать со знакомства с основными морфологическими признаками и физическими свойствами почвы непосредственно в полевых условиях.
1.1. Исследование структуры почвы. Под структурой почвы понимают способность распадаться на отдельные частицы, которые называются структурными отдельностями. Они могут иметь различную форму — пластинки, комки и т. д. Иногда структурные отдельности бывают выражены весьма слабо или вообще отсутствуют — такую почву называют бесструктурной.
Для определения структуры почвы на территории гимназии вырезали образцы почвы на разных участках, подбросили на лопате. При этом почва распадается на структурные отдельности в виде округлых комочков диаметром от 0,5 до 10 мм. Следовательно, для почвы на пришкольном участке типична комковатая структура.
1.2. Водопрочность структурных агрегатов — способность противостоять размывающему действию воды. Поместили несколько структурных отдельностей в стакан с водой. Лёгкими движениями взболтали содержимое сосуда. Почва сохранила комковатую структуру. Это свидетельствует о том, что почва обладает водопрочной структурой.
1.3. Окраска почвы. Одним из основных признаков, используемых при классификации и диагностике почв, остается цвет, который особенно удобен при проведении полевых исследований. Только само восприятие цвета у разных людей неодинаково. Оценка цвета почвы на глаз в полевых условиях не всегда однозначна. Влажные почвы обычно кажутся более темными, чем сухие, а оттенки цвета зависят от высоты стояния солнца над горизонтом, расположенной рядом растительности и других факторов. Следовательно, необходимы объективные способы понимания и оценки цвета почвы и ее горизонтов.
Важно, чтобы влажность и сила солнечного освещения при определении окраски почв были постоянными. Лучше всего окраску почв определять при высоком стоянии солнца. Правильность полевых определений цвета проверяют на образцах в воздушно-сухом состоянии.
Для унификации наименования цветовых оценок еще в 1927 году предложил треугольник почвенных окрасок (рис. 1). Он исходил из того, что гумус почвы окрашивает ее в серые и темно-серые тона, соединения железа — в бурые, красноватые и желтоватые, а многие компоненты почвы, такие, как карбонаты кальция СаСО3, сульфаты кальция CaSO4 и др., имеют белый цвет. Эта схема позволила понять, как формируется окраска почв, но она не вводила каких-то единых приемов измерений.
Рисунок 1. Треугольник почвенных окрасок .
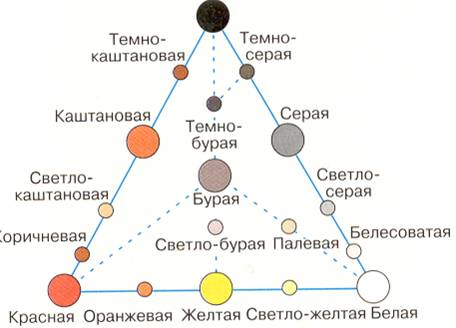
Оценку цвета почвы проводили три группы учащихся. Каждая группа состояла из двух человек. Группы исследователей пришли к единому мнению, что почва имеет тёмно-бурый цвет. Это позволяет предположить наличие достаточно большого количества гумуса и соединений железа в почве пришкольного участка. Более точные результаты возможны лишь при качественном определении компонентов в почве.
1.4. Определение плотности почвы. Различают 4 степени плотности почвы в сухом состоянии (табл. 1).
Таблица 1. Степени плотности почвы.
Степень плотности почвы | Почвенные характеристики |
Очень плотная | Лопата или нож при сильном ударе входят в почву на глубину не более 1 см |
Плотная | При большом усилии нож входит на 2 — 3 см |
Рыхлая | Нож входит на глубину 3 — 5 см, и почва легко разламывается руками |
Рассыпчатая | Лопата или нож легко погружаются в почву; без усилий рассыпается |
Исследования показали, что нож входит на глубину 5 см без особых усилий, почва легко разламывается руками, следовательно, почва на участке рыхлая.
1.5. Определения влажности почвы.
1.5.1. Полевой метод определения влажности. При изучении почв важно знать ее влажность, так как она оказывает влияние на цвет, структуру и т. д. В полевых исследованиях различают 5 степеней влажности (табл. 2).
Таблица 2. Степени влажности почвы.
Степень влажности | Почвенные характеристики |
Сухая | Пылит, не холодит руку, присутствие влаги в ней не ощущается |
Слегка увлажненная | Холодит руку, не пылит, при подсыхании немного светлеет |
Влажная | При подсыхании светлеет и сохраняет форму, при взятии почвы рука ощущает влагу, фильтровальная бумага становится влажной от комочка почвы |
Сырая | При сжатии в руке превращается в тестообразную форму, а вода смачивает руку, но не сочится по пальцам |
Мокрая | При сжимании выделяет воду, просачивающуюся между пальцам. |
Исследования почвы на различных участках пришкольной территории показали, что почва при подсыхании светлеет и сохраняет форму, при взятии почвы рука ощущает влагу, фильтровальная бумага становится влажной от комочка почвы.
1.5.2. Определение влажности почвы методом гравиметрии:
o взвесили пустой бюкс, записали его массу (а);
o взвесили массу бюкса с почвой, записали его массу (в);
o поместили бюкс с почвой на 5 часов в сушильный шкаф при температуре 110оС;
o достали образец из шкафа, охладили и взвесить (б);
o снова поместили образец в сушильный шкаф на несколько часов при температуре 110оС;
o вынули бюкс, охладили, повторно взвесили, чтобы убедиться в постоянстве веса (б), так как, если вес изменился, необходимо повторить операцию высушивания и взвешивания до постоянного веса (б);
o провели расчет процентного содержания воды от веса сухой почвы (влажность почвы — С) по формуле: С=((в-б) / (б-а)) * 100%
а = 60 г
в = 110 г
б = 95 г
С = ((110-95) / (95-60)) * 100% = 43 %
Следовательно, почве на пришкольном участке соответствует влажность 43 %
2. ОПРЕДЕЛЕНИЕ КИСЛОТНОСТИ ПОЧВЫ
Реакция почвы оказывает большое влияние на развитие растений и почвенных микроорганизмов, на скорость и направленность происходящих в ней химических и биохимических процессов. В природных условиях рН почвенного раствора колеблется от 3 (в сфагновых торфах) до 10 (в солонцовых почвах). Чаще всего кислотность не выходит за пределы 4 — 8. Кислые почвы занимают в нашей стране значительные площади. Связь между кислотностью почвы и величиной рН приведена в таблице 3.
Таблица 3. Зависимость кислотности почвы от рН
рН | Степень кислотности почв |
< 4,5 | Сильнокислые почвы |
4,5 – 5,0 | Среднекислые почвы |
5,1 – 5,5 | Слабокислые почвы |
5,6 – 6,0 | Близкие к нейтральным |
6,1 – 7,0 | Нейтральные почвы |
> 7,1 | Щелочные почвы |
Различают два основных вида почвенной кислотности — актуальную и потенциальную.
Актуальная (активная) кислотность — кислотность почвенного раствора. Такую кислотность определяют в водной вытяжке из почв. Актуальная кислотность оказывает непосредственное влияние на корни растений и почвенные микроорганизмы.
Потенциальная (скрытая) кислотность почвы обусловлена наличием поглощенных ионов водорода в почвенном поглощающем комплексе (ППК), который является совокупностью мелкораздробленных (коллоидных) частиц почвы: и органических веществ. Суммарный заряд ППК большинства почв отрицательный, и тем самым он удерживает на своей поверхности в поглощенном состоянии в основном положительно заряженные ионы — катионы Al3+, Ca2+, Mg2+, Na+, H+ . Кроме этих основных групп катионов, в поглощенном состоянии содержатся также ионы K+ и NH4 +; и ряд других катионов.
2.1 Определение актуальной кислотности
Актуальную (активную) кислотность определяли в водной почвенной вытяжке. Для этого поместили в колбу 2 г почвы, добавили 10 мл дистиллированной воды; полученную суспензию 1:5 хорошо встряхнули и дали отстояться осадку; в надосадочную жидкость внесли полоску индикаторной бумаги и сравнили ее цвет с цветной таблицей.
Таблица 4. Изменение цвета универсальной индикаторной бумаги в различных средах.
 |  |  |  |  |  |  |  |  |  |
рН=1 рН=2 рН=3 рН=4 рН=5 рН=6 рН=7 рН=8 рН=9 рН=10
Кислая среда | Нейтральная среда | Щелочная среда |
Подтвердили полученные данные повторным опытом и определением величины рН с помощью прибора Алямовского: к 3 мл почвенной вытяжки добавили 2 — 3 капли универсального индикатора и сравнить со шкалой (табл. 5).
Таблица 5. Шкала окраски раствора индикатора
рН | Окраска раствора индикатора | ||
3 |
| ||
4 |
| ||
5 |
| ||
6 |
| ||
7 |
| ||
8 |
| ||
9 |
| ||
10 |
|
В последнем случае кислотность может быть измерена как в вытяжках, так и в суспензии почвы (без предварительного фильтрования).
Исследования показали, что рН = 5 – 5,5, следовательно, реакция среды раствора слабокислая.
2.2. Определение обменной кислотности.
Обменную кислотность устанавливают в солевой почвенной вытяжке после взаимодействия почвы с раствором нейтральной соли (чаще всего хлорида калия). Для определения обменной кислотности использовали те же методы, что и для определения актуальной (индикаторная бумага, набор Алямовского). По показателям рН солевой вытяжки часто решают вопрос о необходимости известкования почв и о дозах извести (табл. 6).
Таблица 6. Дозы извести в зависимости от рН солевой вытяжки почв.
рН солевой вытяжки | Необходимость известкования | Доза извести, т/га | |
На лёгких почвах | На тяжёлых почвах | ||
<4,5 | Острая | 4,0 | 6,0 |
4,6 | Сильная | 3,4 | 5,5 |
4,8 | Средняя | 3,0 | 5,0 |
5,0 | Средняя | 2,5 | 4,5 |
5,2 | Слабая | 2,0 | 4,0 |
5,4 | Слабая | 2,0 | 3,5 |
>5,5 | Не требуется | - | - |
Исследования показали, что обменная кислотность почвы на пришкольном участке равна 5, значит, потребность в известковании средняя 2,5 - 4,5 т/га.
3. КАЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ В ПОЧВЕ
Любая почва состоит из трех главных составляющих частей, которые находятся между собой в тесном взаимодействии.
Твердая фаза почвы содержит основной запас питательных веществ для растений. Она состоит на 90% и более из сложных минералов и примерно на 10% и менее, из органических веществ, которые играют очень важную роль в плодородии почвы. Почти: половина твердой фазы почвы приходится на связанный кислород, одна треть — на кремний, более 10% — на алюминий, железо, и только 7% — на остальные элементы.
Почвенный раствор — наиболее подвижная и активная часть почвы, в которой совершаются разнообразные химические процессы и из которой растения непосредственно усваивают питательные вещества. Элементы питания, находящиеся в почвенном растворе, наиболее доступны для растений.
Почвенный воздух служит основным источником кислорода для дыхания корней растений. Он отличается от атмосферного повышенным содержанием углекислого газа и несколько меньшим — кислорода.
Определение химического состава почвы чаще всего начинают с анализа водной почвенной вытяжки, так как хорошо растворимые соединения почвы в первую очередь поглощаются растениями. Избыточные количества растворимых солей (более 0,2% от массы сухой почвы) создают повышенную концентрацию ионов в почвенном растворе, а это снижает плодородие почвы и ее экологическое состояние. С агрономической точки зрения наиболее вредными для растений считаются гидрокарбонаты, карбонаты и сульфаты натрия, а также хлориды (особенно магния и кальция). По степени экологической опасности химические вещества, попадающие в почву различными путями, делят на 3 класса (табл. 7).
Таблица 7. Степень экологической опасности веществ.
Класс экологической опасности | Перечень элементов и соединений |
1 | кадмий, ртуть, свинец, цинк, фтор, мышьяк, селен, бензаперен |
2 | кобальт, молибден, бор, медь, хром, никель, сурьма |
3 | ацетофенон, барий, вольфрам, марганец, ванадий, стронций. |
При анализе почв, прежде всего, следует обратить внимание на кислотность почвенной вытяжки. Помимо того, что кислотность почвы — один из наиболее важных агрохимических показателей, по ее величине можно предсказать наличие тех или иных микроэлементов в почве, а также оценить их подвижность (табл. 8).
Таблица 8. Подвижность микроэлементов в зависимости от кислотности почвы*
Реакция почвы | Pb | Cr | Ni | V | As | Co | Cu | Zn | Cd | Hg | S |
Кислые почвы | СП | СП | СП | СП | СП | СП | П | П | П | П | П |
Нейтральные | ПН | СП | СП | П | П | СП | СП | П | СП | СП | П |
Щелочные | ПН | ПН | ПН | П | П | ПН | СП | СП | СП | ПН | П |
*Примечание: ПН — практически неподвижные; СП — слабоподвижные; П— подвижные.
3.1. Определение сухого остатка почвенной вытяжки. Сухой остаток почвенной вытяжки — это общее содержание растворимых солей в водной почвенной вытяжке. Его определяют путем выпаривания в фарфоровой чашке некоторого объема фильтрата. Прокаливанием можно разделить сухой остаток на минеральный и органический.
В прокаленную и взвешенную фарфоровую чашку налили при помощи пипетки по 25 мл фильтрата водной вытяжки четыре раза (по мере выпаривания), чтобы в сумме получить от 100 мл вытяжки (чем выше засоленность, тем меньше объем вытяжки на анализ). После выпаривания жидкости чашку помещают в сушильный шкаф и высушивают ее содержимое при температуре 105оС в течение 3 — 4 ч. (до постоянной массы).
3.1.1.Содержание сухого остатка выражаем в процентах:
a) к воздушно-сухой почве:
X1= ((m1 – m2) * V1) / (m *V2 )) * 100%
где m1 — масса чашки с сухим остатком, г m1 = 56,5 г
m2 — масса пустой чашки, г m2 = 53 г
V1 — общий объем фильтрата, мл V1 = 180 мл
V2 — объем фильтрата для анализа, мл V2 = 100 мл
m — масса почвы для приготовления вытяжки, г m = 70 г
X1= ((56,5г – 53г) * 180мл) / (70г *100мл )) * 100% = 9%
б) к абсолютно сухой почве:
X2 = (((m1 –m2 ) * V1 ) / (m * V2 )) * 100/ 100 - y
у — влажность воздушно-сухой почвы, % у = 43 %
X2= ((56,5г – 53г) * 180мл) / (70г *100мл )) * 100%/ 100-43% = 0,16%
Если содержимое чашки после взвешивания озолить и прокалить, то потеря от прокаливания даст ориентировочное содержание в вытяжке органических веществ, а остаток в чашке — содержание минеральных солей. Озоление и прокаливание можно провести на газовой горелке или в муфельной печи при температуре не выше 525'С. Расчет ведут аналогично сухому остатку (минеральная часть); органический остаток узнают по разности между сухим остатком и минеральной частью.
Содержимое чашки после взвешивания озолили и прокалили на газовой горелке.
3.1.2.Содержание минерального остатка выражаем в процентах:
а) к воздушно-сухой почве:
X1= ((m1 – m2) * V1) / (m *V2 )) * 100%
m1 = 54,1 г
m2 = 53 г
V1 = 180 мл
V2 = 100 мл
m = 70 г
X1= ((54,1г – 53г) * 180мл) / (70г *100мл )) * 100% = 2,8 %
б) к абсолютно сухой почве:
X2 = (((m1 –m2 ) * V1 ) / (m * V2 )) * 100/ 100 - y
у = 43 %
X2= ((54,1г – 53г) * 180мл) / (70г *100мл )) * 100% /100 – 43% = 0,05%
По количеству минерального остатка судят о засоленности почвы (табл. 9)
Таблица 9. Взаимосвязь между содержанием солей в почве и степенью её засоленности
Содержание солей, в % от массы абсолютно сухой почвы | Степень засоления почвы |
Менее 0,3 | Не засолена |
0,3 – 1,0 | Слабо засолена |
1,0 –2,0 | Засолена |
2,0 – 3,0 | Сильно засолена |
Более 3,0 | солончак |
Следовательно, почва на пришкольном участке не засолена.
Рассчитаем содержание органического остатка.
3.1.3. Содержание органического остатка выражаем в процентах:
а) к воздушно-сухой почве:
X1= ((m1 – m2) * V1) / (m *V2 )) * 100%
m1 – масса сухого остатка, г m1= 3,5 г
m2 –масса минерального остатка, г m2 = 1,1 г
V1 = 180 мл
V2 = 100 мл
m = 70 г
X1= ((3,5г – 1,1г) * 180мл) / (70г *100мл )) * 100% = 6,2 %
б) к абсолютно сухой почве:
X2 = (((m1 –m2 ) * V1 ) / (m * V2 )) * 100/ 100 - y
у = 43 %
X2= ((3,5г – 1,1г) * 180мл) / (70г *100мл )) * 100%/ 100 – 43% = 0,1%
3.2. Определение карбонат-ионов. Небольшое количество почвы поместили в фарфоровую чашку и прилили пипеткой несколько капель 10% раствора соляной кислоты. Образующийся по реакции оксид углерода СО2, выделяется в виде пузырьков (почва "шипит"). По интенсивности выделения их можно судить о более или менее значительном содержании карбонатов. Почву, вскипающую от 10% раствора соляной кислоты, относят к группе карбонатных почв.
В результате проведённых исследований почвы с пришкольного участка, мы выяснили, что при внесении в почву 10%-ног раствора соляной кислоты выделение газа идет слабое. Можно сделать предположение о незначительном содержании карбонатов.
3.3. Определение хлорид-ионов. К 5 мл фильтрата, помещенного в пробирку, прибавили несколько капель 10%-ног раствора азотной кислоты и по каплям 0,1 М раствор нитрата серебра. Образующийся осадок в виде белых хлопьев указывает на присутствие хлоридов в количестве десятых долей процента и более. При содержании сотых и тысячных долей процента хлоридов осадка не выпадает, но раствор мутнеет.
Результатом проведённого эксперимента с почвой пришкольного участка является помутнение раствора. Следовательно, содержание хлорид-ионов в почве порядка 0,01 - 0, 001 %.
3.4. Определение сульфат-ионов. К 5 мл фильтрата добавили несколько капель концентрированной соляной кислоты и 2 — 3 мл 20 %-ног раствора хлорида бария. Если образующийся сульфат бария выпадает в виде белого мелкокристаллического осадка, это говорит о присутствии сульфатов в количестве нескольких десятых процента и более. Помутнение раствора также указывает на содержание сульфатов — сотые доли процента. Слабое помутнение, заметное лишь на черном фоне, бывает при незначительном содержании сульфатов — тысячные доли процента.
При проведении экспериментов по определению сульфат-ионов, образующийся сульфат бария выпадал в виде белого мелкокристаллического осадка, что говорит о присутствии сульфатов в количестве нескольких десятых процента и более.
3.5. Определение нитрат-ионов. К 5 мл фильтрата по каплям прибавляли раствор дифениламина в серной кислоте (0,05 г дифениламина растворить в 10 мл концентрированной серной кислоты). Раствор окрашивается в синий цвет, что свидетельствует о наличии нитратов и нитритов в почве пришкольного участка.
3.6. Определение кальция. К 10 мл фильтрата добавили несколько капель 10% раствора соляной кислоты и 5 мл 4%-ног раствора оксалата аммония. Белый осадок оксалата кальция свидетельствует о наличии нескольких процентов кальция. При незначительном содержании кальция (сотые и тысячные доли процента) наблюдается не осадок, а легкое помутнение раствора.
Результатом проведённого эксперимента с почвой пришкольного участка стало лёгкое помутнение раствора. Следовательно, содержание кальция в почве порядка 0,01 - 0, 001 %.
3.7. Определение ионов железа (II и Ш). В две пробирки внесли по 3 мл вытяжки. В первую пробирку прилилиь несколько капель раствора красной - кровяной соли К3 [Fe(CN)6), во вторую — несколько капель 10%-ного раствора роданида аммония или NH4SCN.
Появившееся синее окрашивание в первой пробирке и красное, во второй свидетельствует о наличии в почве соединений железа(II) и железа (Ш). По интенсивности окрашивания можно судить об их количестве.
В первой пробирке получили раствор с интенсивным синим окрашиванием, во второй окрашивание раствора менее интенсивно, но легко определяется наблюдателем красный цвет раствора. Следовательно, подтверждается предположение выдвинутое на основании исследования цвета почвы, то есть почва содержит железо.
3.8. Определение алюминия. К 5 мл солевой почвенной вытяжки прибавили по каплям 3% раствор фторида натрия до появления осадка. Чем быстрее и обильнее выпадает осадок, тем больше алюминия содержится в почве.
Обнаружено лишь незначительное помутнение раствора, что говорит о малой доли содержания алюминия в почве.
3.9. Определение натрия. О присутствии натрия в почве судят по ярко-желтому окрашиванию пламени горелки при внесении в него стеклянной палочки с каплей раствора почвенной вытяжки.
Внесение в пламя капли раствора почвенной вытяжки не изменило его цвет, следовательно, натрий в почве отсутствует.
3.10. Определение содержания азота
В химический стакан на 100 мл внесли 5 г (1 чайная ложка) почвы, прилили 50 мл 20 % - ного раствора хлорида калия, взболтали и через 3-4 мин отфильтровали через бумажный фильтр в колбу. Перенесли мерной пипеткой 2 мл фильтрата в пробирку на 10 мл и прилили 5 мл раствора дифенилового реактива. Через 1 ч жидкость изменила свою окраску. Сопоставили цвет раствора со шкалой (табл. 10)
Таблица 10. Определение потребности растений в азоте.
№ п/п | Концентрация NO3 –, мг/кг почвы | потребность в азоте |
1 | 100 | Слабая |
2 | 90 | |
3 | 80 | |
4 | 70 | |
5 | 60 | |
6 | 50 | Средняя |
7 | 40 | |
8 | 30 | |
9 | 20 | сильная |
10 | 10 |
Сопоставив с эталонной шкалой цвет раствора, сделали вывод, что содержание нитрат-ионов в почве 50 мг/кг. Значит, потребность растений данного участка в азоте средняя.
3.11. Определение содержания фосфора.
В колбу на 100 мл поместили 5 г (1 чайную ложку) почвы, прилили 25 мл 0,2 н. раствора хлороводорода и перемешали. Дали смеси отстояться в течение 15 мин. Затем раствор профильтровали через бумажный фильтр. Отберите пипеткой 5 мл фильтрата, перенесите его в химическую пробирку. Другой, чистой пипеткой отмерили 5 мл молибденового реактива и добавили его в пробирку. Слегка взболтали содержимое пробирки. Полученную окраску сравнили с эталонной шкалой (табл. 11).
Таблица 11. Определение потребности растений в фосфоре.
№ п/п | Содержание | Потребность в фосфоре |
1 2 3 4 5 6 7 8 | 1,25 2,5 3,75 5,0 6,25 7,5 8,75 10,0 | Сильная |
9 10 11 | 12,5 15 20 | Средняя |
12 | 25 | Слабая |
Сопоставив с эталонной шкалой цвет раствора, сделали вывод, что содержание фосфора в почве 10 мг/кг. Значит, потребность растений данного участка в фосфоре сильная.
3.12. Определение содержания калия
В стакан на 100 мл внесли 10 г почвы (2 чайные ложки) и прилили 40 мл 10%-ного раствора нитрата натрия, тщательно перемешали, через 1 ч отфильтровали.
Пипеткой взяли 5 мл фильтрата, поместили его в химическую пробирку и прилили мерной пипеткой 4 мл 10%-ного раствора нитрата натрия, влили в пробирку 1 мл раствора нитрата серебра и добавили медицинской пипеткой 5 капель раствора кобальтинитрита натрия. Через 1 ч раствор окрасился в желтый цвет.
Таблица 3. Определение потребности растений в калии.
№ п/п | Содержание К+ мг/кг почвы | Потребность в калии |
1 2 3 4 5 | 2 4 6 8 10 | Сильная |
6 7 8 | 15 20 40 | Средняя |
9 10 | 60 100 | Слабая |
Сопоставив с эталонной шкалой цвет раствора, сделали вывод, что содержание калия в почве 15 мг/кг. Значит, потребность растений данного участка в калии средняя.
Результаты.
1. ИССЛЕДОВАНИЕ ФИЗИЧЕСКИХ ПАРАМЕТРОВ почвы показало следующее:
1.1. Исследование структуры почвы.
Для определения структуры почвы на территории гимназии вырезали образцы почвы на разных участках, подбросили на лопате. При этом почва распадается на структурные отдельности в виде округлые комочков диаметром от 0,5 до 10 мм. Следовательно, для почвы на пришкольном участке типична комковатая структура.
1.2. Водопрочность структурных агрегатов.
Почва сохранила комковатую структуру после легкого взбалтывания в сосуде с водой. Это свидетельствует о том, что почва обладает водопрочной структурой.
1.3. Окраска почвы.
Группы исследователей пришли к единому мнению, что почва имеет тёмно-бурый цвет. Это позволяет предположить наличие достаточно большого количества гумуса и соединений железа в почве пришкольного участка.
1.4. Определение плотности почвы.
Исследования показали, что нож входит на глубину 3 см при большом усилии, следовательно, почва на участке плотная.
1.5. Определения влажности почвы.
Исследования почвы на различных участках пришкольной территории показали, что почва при подсыхании светлеет и сохраняет форму, при взятии почвы рука ощущает влагу, фильтровальная бумага становится влажной от комочка почвы. Это свидетельствует о том, что почва влажная.
Расчёты гравиметрическим методом подтвердили полевые исследования:
С = ((110-95) / (95-60)) * 100% = 43 %
Влажность почвы составляет 43 %
2. ОПРЕДЕЛЕНИЕ КИСЛОТНОСТИ ПОЧВЫ.
Исследования актуальной и обменной кислотности показали, что рН = 5, следовательно, реакция среды раствора слабокислая.
3. КАЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ В ПОЧВЕ дало следующие результаты:
3.1. Определение сухого остатка почвенной вытяжки.
3.1.1.Содержание сухого остатка:
а) к воздушно-сухой почве:
X1= ((56,5г – 53г) * 180мл) / (70г *100мл )) * 100% = 9%
б) к абсолютно сухой почве:
X2= ((56,5г – 53г) * 180мл) / (70г *100мл )) * 100%/ 100-43% = 0,16%
3.1.2.Содержание минерального остатка:
а) к воздушно-сухой почве:
X1= ((54,1г – 53г) * 180мл) / (70г *100мл )) * 100% = 2,8 %
б) к абсолютно сухой почве:
X2= ((54,1г – 53г) * 180мл) / (70г *100мл )) * 100% /100 – 43% = 0,05%
3.1.3. Содержание органического остатка:
а) к воздушно-сухой почве:
X1= ((3,5г – 1,1г) * 180мл) / (70г *100мл )) * 100% = 6,2 %
б) к абсолютно сухой почве:
X2= ((3,5г – 1,1г) * 180мл) / (70г *100мл )) * 100%/ 100 – 43% = 0,1%
3.2. Определение карбонат-ионов.
В результате проведённых исследований почвы с пришкольного участка, мы выяснили, что при внесении в почву 10%-ног раствора соляной кислоты выделение углекислого газа идет слабое. Можно сделать предположение о незначительном содержании карбонатов.
3.3. Определение хлорид-ионов.
Результатом проведённого эксперимента с почвой пришкольного участка является помутнение раствора после внесения нескольких капель 10%-ного раствора азотной кислоты и 2 капель 0,1 М раствор нитрата серебра. Следовательно, содержание хлорид-ионов в почве порядка 0,01 - 0, 001 %.
3.4. Определение сульфат-ионов.
При проведении экспериментов по определению сульфат-ионов, образующийся сульфат бария выпадал в виде белого мелкокристаллического осадка, что говорит о присутствии сульфатов в количестве нескольких десятых процента и более.
3.5. Определение нитрат-ионов.
При внесении раствор дифениламина в серной кислоте к почвенному фильтрату окрашивается в синий цвет, что свидетельствует о наличии нитратов и нитритов в почве пришкольного участка.
3.6. Определение кальция.
Результатом проведённого эксперимента с почвой пришкольного участка стало лёгкое помутнение раствора после внесения нескольких капель 10% раствора соляной кислоты и 5 мл 4%-ног раствора оксалата аммония. Следовательно, содержание кальция в почве порядка 0,01 - 0, 001 %.
3.7. Определение железа (II и Ш).
В первой пробирке внесение нескольких капель раствора красной - кровяной соли привело к появлению интенсивного синего окрашивания, во второй пробирке несколько капель 10%-ного раствора роданида аммония NH4SCN вызвало менее интенсивное окрашивание раствора, но легко определялся наблюдателем красный цвет раствора. Следовательно, подтверждается предположение, выдвинутое на основании исследования цвета почвы, то есть почва содержит железо.
3.8. Определение алюминия.
При добавлении 3%-ного раствора фторида натрия к почвенной вытяжке, обнаружено лишь незначительное помутнение раствора, что говорит о малой доли содержания алюминия в почве.
3.9. Определение натрия.
Внесение в пламя капли раствора почвенной вытяжки не изменило его цвет, следовательно, натрий в почве отсутствует.
3.10. Определение содержания азота.
Содержание нитрат-ионов в почве 50 мг/кг. Значит, потребность растений данного участка в азоте средняя.
3.11. Определение содержания фосфора.
Содержание фосфора в почве 10 мг/кг. Значит, потребность растений данного участка в фосфоре сильная.
3.12. Определение содержания калия.
Сопоставив с эталонной шкалой цвет раствора, сделали вывод, что содержание калия в почве 15 мг/кг. Значит, потребность растений данного участка в калии средняя.
Выводы.
1. Проведены исследования почвы на пришкольном участке гимназии №1 г. Рузаевка.
2. Почва рыхлая, тёмно-бурого цвета, имеет комковатую, водопрочную структуру. Влажность её составляет 43 %, реакция среды слабокислая.
3. Содержание сухого остатка в почве соответствует 9% к воздушно-сухой почве и 0,16 % к абсолютно сухой. Большая часть сухого остатка приходится на органическую составляющую.
4. Качественный анализ почвы показал, что содержание карбонатов, хлоридов, ионов кальция, алюминия и железа (Ш) в почве незначительно. Почва содержит сульфаты, нитраты, а также ионы железа (П). Исследования показали, что потребность растений пришкольного участка в азоте и калии средняя, в фосфоре сильная.
Рекомендации.
1. В результате проведённых исследований рекомендуем проводить известкование из расчёта 2,5 - 4,5 т/га.
2. Учитывая высокую потребность растений пришкольного участка в фосфоре, применять фосфорсодержащие удобрения (суперфосфат). А также из-за недостатка в почве калия и азота применять калий - и азотсодержащие удобрения (аммиачная селитра, натриевая селитра, сульфат аммония, калийная соль).
3. Увлажнять почву по мере её подсыхания.
Список литературы
1. Экологический практикум: Учебное пособие/ Сост. ; МО РМ, МРИПКРО – Саранск, 20с.
2. Кушелев природы от загрязнений промышленными выбросами. – М.: Химия, 19с., ил.
3. Человек в мире экологии. – М.: Дрофа, 20с., ил.
4. Соросовский образовательный журнал, № 5, 1998 г.
5. Земля – как экологическая среда. – М.: Просвещение, 19с., ил.
6. Что должен знать и уметь юный защитник природы.- М.: Прогресс, 19с.



