муниципальное образовательное учреждение
средняя общеобразовательная школа №37
с углублённым изучением английского языка
Методическая разработка
Приёмы технологии развития
критического мышления на уроках химии
Работу выполнила
учитель химии школы №37
Ярославль
2013 год
Аннотация
Приёмы технологии развития
критического мышления на уроках химии
(методическая разработка)
Автором представлена методическая разработка об использовании приёмов технологии развития критического мышления в процессе обучения химии. В работе рассмотрены основные положения данной методики, её основные методы и приёмы, приведены примеры использования автором на уроках химии некоторых приёмов данной технологии, даны методические разработки двух уроков химии в 8 классе. Методическая разработка предназначена не только для учителей химии, так как технология развития критического мышления относится к надпредметным, общепедагогическим современным образовательным технологиям.
Оглавление
1. Введение с. 4
2. Основные положения методики технологии
развития критического мышления с. 5
3. Некоторые приёмы использования технологии развития
критического мышления на уроках химии с. 8
4. Заключение с. 16
5. Список литературы с. 17
6. Приложение с. 18
Урок по химии 8 класс
Вычисления по химическому уравнению
7. Приложение с. 22
Урок по химии 8 класс
Химические свойства кислот в свете электролитической диссоциации
Введение
Российская школа вступила в сложный этап качественной перестройки содержания образования. Перед каждым учителем, педагогическим коллективом школ, органами народного образования поставлена задача - добиться коренного улучшения обучения и воспитания подрастающего поколения. В статье 66 «Начальное общее, основное общее и среднее общее образовании» закона об образовании говорится о том, что среднее общее образование направлено на становление и формирование личности обучающегося, развитие интереса к познанию и творческих способностей обучающегося, формирование навыков самостоятельной учебной деятельности, подготовку обучающегося к жизни в обществе, самостоятельному жизненному выбору, продолжению образования и началу профессиональной деятельности.
Развивающемуся обществу нужны современно образованные, нравственные, предприимчивые люди, которые могут самостоятельно принимать ответственные решения в ситуации выбора, прогнозируя их возможные последствия, способны к сотрудничеству, отличаются мобильностью, динамизмом, конструктивностью, обладают развитым чувством ответственности за судьбу страны. В концепции модернизации российского образования на период до 2010 г. в качестве одной из задач выдвигается формирование молодого человека с критическим, нестандартным мышлением, способного к поиску взвешенных решений, основанных на самостоятельном исследовании окружающего мира. Постоянное увеличение объема знаний, быстрое устаревание имеющихся сведений, необходимость ориентироваться во все возрастающем потоке информации заставляют нас искать источник новых знаний непосредственно внутри системы образования образовательных процессов. Выпускник школы должен самостоятельно мыслить, уметь увидеть возникающие в реальном мире трудности и искать пути рационального их преодоления, четко осознавать, где и каким образом приобретаемые им знания могут быть применены в окружающей действительности.
Школа - в широком смысле этого слова - должна стать важнейшим фактором гуманизации общественно-экономических отношений, формирования новых жизненных установок личности. Школе предоставляется право на творчество, на выбор методов обучения и организации учебно-воспитательного процесса, на отработку новаторских идей. Главное внимание надо уделить деятельностному обучению, развитию индивидуальных способностей учащихся. Очень важно научить школьников грамотно работать с информацией. Способствовать этому будут использование учителем различных педагогических технологий.
Одной из педагогических технологий, посредством которой обеспечивается более глубокое и более полное усвоение учебного материала по химии, является технология развития критического мышления. Она способствует совершенствованию качества обучения учащихся, закреплению приобретенных знаний, формированию умения переноса их в новые ситуации, установлению межпредметных связей. Развивает мыслительные навыки учащихся, делает образование личностно – ориентированным, помогает связи обучения с жизнью.
Поэтому цель моей работы:
показать использование различных приёмов технологии развития критического мышления учащихся общеобразовательных школ на примере уроков по химии.
Для реализации этой цели поставлены следующие задачи:
- раскрыть сущность технологии развития критического мышления показать структуру урока в рамках технологии развития критического мышления показать приёмы организации образовательного процесса, основанные на технологии развития критического мышления
Основные положения методики технологии
развития критического мышления
Технология развития критического мышления - разновидность личностно-ориентированного обучения, система формирования навыков работы с информацией, позволяющая развивать у школьников творческое, аналитическое, конструктивное мышление. Данная технология относится к общепедагогическим, надпредметным. (4)
Технология развития критического мышления - это совокупность разнообразных приёмов, направленных на то, чтобы сначала заинтересовать ученика, пробудить в нём исследовательскую, творческую активность, затем предоставить ему условия для осмысления материала и, наконец, помочь ему обобщить приобретённые знания. (3)
Особенности этой технологии заключаются в следующем:
- не объем знаний или количество информации является целью образования, а то, как ученик умеет управлять этой информацией: искать, наилучшим способом присваивать, находить в ней смысл, применять в жизни; не присвоение «готового» знания, а конструирование своего, которое рождается в процессе обучения; коммуникативно-деятельностный принцип обучения, предусматривающий диалоговый режим занятий, совместный поиск решения проблем, а также «партнерские» отношения между педагогом и обучаемыми; объективная оценка положительных и отрицательных сторон в познаваемом объекте. (3)
В ментальности русскоязычного человека понятие «критическое мышление» связано с поиском недостатков, недочетов. Когда мы говорим: «Он мыслит слишком критично», то подразумеваем излишнюю недоверчивость человека, его нежелание принимать что-либо на веру. Тем не менее, в российской образовательной системе, данный термин связывают с высоким уровнем осмысленности процесса обучения, причем не только со стороны учителя, но и со стороны ученика.
По мнению , критическое мышление - это один из видов интеллектуальной деятельности человека, который характеризуется высоким уровнем восприятия, понимания, объективности подхода к окружающему его информационному полю. (4)
Критическое мышление — это:
- способность ставить новые, полные смысла вопросы;
- вырабатывать разнообразные, подкрепляющие аргументы;
- принимать независимые продуманные решения.
Дж. Барелл выделяет следующие характеристики критически мыслящего человека:
- Проявляет настойчивость в решении проблем
- Открыт для других идей
- Слушает собеседника
- Рассматривает проблему с разных точек зрения
- Устанавливает множество связей между явлениями
- Умеет строить различные выводы
- Применяет свои навыки и знания в различных ситуациях
- Активно воспринимает информацию
- Любознателен
Что даёт ТРКМ ученику
- повышение эффективности восприятия информации
- повышение интереса как к изучаемому материалу, так и к самому процессу обучения
- умение ответственно относиться к собственному образованию
- умение работать в сотрудничестве с другими
- повышение качества образования
- желание и умение стать человеком, который учится в течение всей жизни
Что даёт ТРКМ учителю
- умение создать в классе атмосферу открытости и сотрудничества
- возможность использовать модель обучения и систему эффективных методик, которые способствуют развитию критического мышления и самостоятельности в процессе обучения
- стать практиками, которые умеют грамотно анализировать свою деятельность
- стать источником ценной профессиональной информации для других учителей (3)
Технология критического мышления по
Основы методики развития критического мышления включают в себя три стадии, которые должны присутствовать на уроке в процессе познания.
• Стадия вызова- На этой стадии происходит актуализация имеющихся знаний по теме.
• Вторая стадия – осмысление. Она даёт возможность познакомиться с новой информацией, понятиями, увязать их с уже имеющимися знаниями.
• Третья стадия – рефлексия или размышления. Она позволяет ученикам осмыслить всё, что они разобрали на уроке, выразить это своими словами.
Эти три стадии необязательно должны присутствовать на каждом уроке. Однако важно, чтобы какие-то приёмы и методы развития критического мышления использовались ежеурочно.
Этап урока | Деятельность учителя | Деятельность ученика | Приёмы работы |
I этап – стадия вызова - актуализация имеющихся знаний - пробуждение интереса к получению новой информации - постановка учеником собственных целей обучения | -вызов у учащихся уже имеющихся знаний по изучаемому вопросу - активизация их деятельности - мотивация к дальнейшей работе | - «вспоминает», что ему известно по изучаемому вопросу - делает предположения - систематизирует информацию до изучения нового материала - задает вопросы, на которые хочет получить ответы. | - рассказ-предположение по ключевым словам; - «толстые» и «тонкие» вопросы |
| направлена на сохранение интереса к теме при непосредственной работе с новой информацией постепенное продвижение от знания «старого» к «новому» | читает, слушает текст, используя активные методы чтения делает пометки на полях ведет записи по мере осмысления новой информации | методы активного чтения: |
III этап - рефлексия | - вернуть учащихся к первоначальным записям - внести изменения - дать творческие, исследовательские или практические задания на основе изученной информации | соотносят «новую» информацию со «старой», используя знания, полученные на стадии осмысления | -заполнение кластеров, таблиц - синквейн |
Все приёмы ТРКМ помогают формировать и развивать универсальные учебные навыки (УУД).
Познавательные УУД
Общеучебные универсальные учебные действия:
• поиск и выделение необходимой информации
• проявление познавательной инициативы
• знаково-символические действия, где выделены существенные характеристики объекта
• структурирование знаний
• постижение речевого высказывания в устной и письменной форме
• смысловое чтение
• контроль и оценка процесса и результатов деятельности
Логические универсальные действия
• анализ объектов с целью выделения признаков (существенных, несущественных)
• синтез – составление целого из частей, в том числе самостоятельное достраивание с выполнением недостающих компонентов
• выбор оснований и критериев для сравнения, классификации объектов
• установление причинно-следственных связей
Регулятивные УУД
контроль и коррекция – внесение необходимых дополнений и коррективов в план и способ действия в случае расхождения эталона, реального действия и его результата; внесение изменений в результат своей деятельности, исходя из оценки этого результата самим обучающимся, учителем, товарищами
оценка – выделение и осознание обучающимися того, что уже усвоено и что еще нужно усвоить, осознание качества и уровня усвоения; оценка результатов работы;
саморегуляция как способность к мобилизации сил и энергии к волевому усилию и преодолению препятствий.
Коммуникативные УУД
планирование учебного сотрудничества с учителем и сверстниками
инициативное сотрудничество в поиске и сборе информации
управление поведением партнера – контроль, коррекция, оценка его действий
умение с достаточной полнотой и точностью выражать свои мысли в владение монологической и диалогической формами речи
применение знаний в конкретной учебной ситуации
Личностные УУД
-личностное, профессиональное, жизненное самоопределение
- установление обучающимися связи между целью учебной деятельности и ее мотивом
-нравственно-этическая ориентация
-оценивание содержания изученного материала, исходя из социальных и личностных ценностей
-умение формулировать собственную позицию
Некоторые приёмы использования технологии
развития критического мышления на уроках химии
В ходе своей педагогической деятельности я стараюсь использовать различные методы и приёмы технологии развития критического мышления:
1. Кластер – это способ графической организации материала. Иногда такой способ называют «наглядным мозговым штурмом». Приём кластеров («гроздья») может применяться на стадии вызова для систематизации имеющейся информации. На стадии осмысления кластер позволяет фиксировать фрагменты новой информации. На стадии рефлексии понятия группируются и между ними устанавливаются логические связи.
Этапы работы над кластером:
1. В начале, посередине чистого листа (классной доски), написать ключевое слово или предложение, которое является «сердцем» темы.
2. Вокруг «накидать» слова или предложения, выражающие идеи, факты, образы, подходящие для данной темы. (Модель «планеты и ее спутники»)
3. По мере записи, появившиеся слова соединяются прямыми линиями с ключевым понятием. У каждого из «спутников» в свою очередь тоже появляются «спутники», устанавливаются новые логические связи.
В итоге получается структура, которая графически отображает наши размышления, определяет информационное поле данной теме.
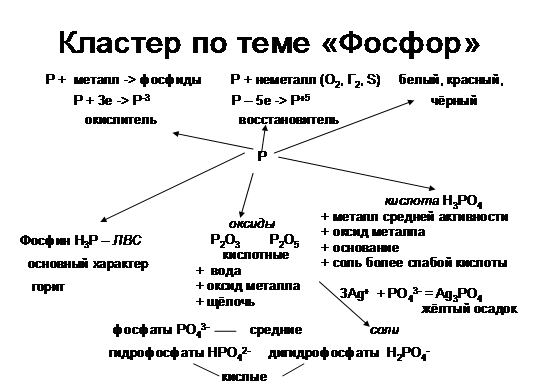
Я применяю кластер и при повторении основных вопросов темы на уроках обобщения, подготовки к контрольной работе, на первом уроке после каникул. Это позволяет быстро вспомнить основные вопросы изученного материала. Например, в 9 классе изучение неметаллов начинается во второй четверти, а заканчивается в третьей. Поэтому на первом уроке в третьей четверти ученики работают с кластером.
Вопросы | ответы | дополнения и исправления |
1.Какие особенности проявляют атомы неметаллических элементов в строении? | ||
2. Как изменяются окислительные свойства в ПС а) по периоду б) по главной подгруппе | ||
3. Как определить для атома неметаллла степень окисления а) минимальную б) максимальную | ||
4. С какой группой веществ обязательно взаимодействуют неметаллы? | ||
5. Какой характер проявляют высшие оксиды и гидроксиды неметаллов? | ||
6. Закончите уравнения реакций: Fe + Br2 à N2O3 + H2O à Mg(OH)2 + HclO4 à |
2. Инсерт – в дословном переводе означает интерактивную систему записи для эффективного чтения и размышления.
• 1этап: предлагается система маркировки текста
v «галочкой» помечается то, что уже известно ученикам
- «минусом» помечется то, что противоречит их представлениям
+ «плюсом» помечается то, что для них интересно и неожиданно
? «вопросительный знак» ставится, если что-то неясно, возникло желание узнать
больше
• 2 этап: учащиеся читают текст и делают соответствующие пометки
• 3 этап: последовательное обсуждение каждого маркированного фрагмента
Система обозначений может быть и другой.
Обсуждение: 1) Что в этом тексте знакомо «+»
2) Что увы узнали нового «v»
3) Что требует для вас пояснения «?»
4) Какие ошибки нашли «-»
Работать можно индивидуально и парами. На уроке по изучению водорода в 9 классе я предлагаю ученикам такой текст, где они тоже проводят соответствующую маркировку:
Молекула водорода состоит их двух атомов. Атомы в молекуле водорода соединены между собой ковалентной полярной связью. Вещество водород имеет молекулярную кристаллическую решётку. Водород можно собрать методом вытеснения воздуха. 1 моль водорода при нормальных условиях занимает объём 22,4 литра. В химических реакциях водород может проявлять себя только в роли восстановителя. Водород как неметалл взаимодействует со всеми металлами. Водород можно использовать в качестве сильного восстановителя при получении чистых металлов. Водород является экологически чистым топливом. Водород применяется в качестве пищевой добавки Е 949.3. Синквейн от французского слова «cing» – пять. Используется как способ синтеза материала. Он может быть предложен, как индивидуальное самостоятельное задание; для работы в парах; как коллективное творчество. Обычно синквейн используется на стадии рефлексии, хотя может быть дан и как нетрадиционная форма на стадии вызова.
План
1 строка – 1 слово - существительное - название темы
2 строка – 2-3 слова – прилагательные - свойства темы
3 строка – 2-3 слова – глаголы - действия темы
4 строка - 4-5 слов – ваше отношение к данной теме
5 строка – 1 –2 слова – философское понятие данной темы, синоним первой строки
Пример синквейна, составленного учениками 8 класса после изучения темы «Электролитическая диссоциация»:
Ионы
Отрицательные, положительные, устойчивые
Двигаются, взаимодействуют
Помогают понять свойства веществ
Заряженные частицы
Пример синквейна, составленного учениками 10 класса после изучения темы «Спирты»:
Этанол
жидкий, наркотический
опьяняет, дезинфицирует, растворяет, горит
правильно применять его в быту
-«огненная вода»
- этиловый спирт
- предельный одноатомный спирт
4. Мозговая атака используется с целью активизации имеющихся знаний на стадии «вызова» при работе с фактологическим материалом.
1 э т а п: Учащимся предлагается подумать и записать все, что они знают или думают по данной теме
2 э т а п: Обмен информацией
Рекомендации к эффективному использованию:
1. Жесткий лимит времени на 1-м этапе 5-7 минут;
2. При обсуждении идеи не критикуются, но разногласия фиксируются;
3. Оперативная запись высказанных предложений.
Возможна индивидуальная, парная и групповая формы работы. Как правило, их проводят последовательно одну за другой, хотя каждая может быть отдельным самостоятельным способом организации деятельности. Примечание: парная мозговая атака очень помогает учащимся, для которых сложно высказать свое мнение перед большой аудиторией. Обменявшись мнением с товарищем, такой ученик легче выходит на контакт со всей группой. Разумеется, работа в парах позволяет высказаться гораздо большему числу учащихся.
Мозговая атака всегда присутствует во время составления кластера.
5. Верные и неверные утверждения
Учащимся предлагается ряд высказываний, по поводу которых надо высказать своё мнение:
(+ ) верно или (–) неверно. Можно использовать на стадии вызова, как проверка подготовки к уроку. Или же на стадии вызова для настраивания на изучение новой темы. Тогда предлагается несколько утверждений по ещё неизученной теме. Дети выбирают «верные» утверждения, полагаясь на собственный опыт или просто угадывая. А затем по ходу урока формулируются правильные высказывания. Данный приём можно использовать и на стадии рефлексии для проверки усвоенного за урок материала.
Например, на стадии вызова в 9 классе при изучении раздела «Металлы» я предлагаю ученикам ответить на следующие вопросы:
На все вопросы ответьте «ДА» или «НЕТ» относительно КАЛИЯ
1. На ВЭУ атом содержит 1 электрон
2. Для завершения ВЭУ атом принимает электроны
3. Это восстановитель
4. Атом имеет степень окисления +1
5. Элемент проявляет валентность II
6. Элемент относится к щелочным металлам
7. Тип кристаллической решётки – металлическая
8. Металлические свойства выражены ярче у магния
9. Металл относится к тугоплавким металлам
10. Металл легко взаимодействует с хлором
11. При его реакции с водой получается оксид
12. Может реагировать со щёлочью
13. Его оксид проявляет основные свойства
14. Его гидроксид – щёлочь
15. Металл используется для получения других металлов в металлургии
При обобщении материала я тоже использую систему ответов «да-нет». Так, в 10 классе после изучения непредельных углеводородов ученики выполняют следующую работу.
Ответьте на вопросы « Да или Нет » ЭТЕН (6Б.) Вариант 1
В молекуле вещества тип гибридизации атома углерода sp3? Валентный угол в молекуле равен 1200 ? Каждый атом углерода образует по 2 сигма - связи с соседними атомами? В молекуле между атомами углерода присутствует пи - связь? Молекула имеет линейное строение? В молекуле атомы углерода могут вращаться вокруг своей оси? Длина связи между атомами углерода в молекуле составляет 0,134 нм? Длина связи между атомами водорода в молекуле составляет 0,109 нм? Связь С-Н в веществе менее прочная, чем связь между атомами углерода? Пи-связь между атомами углерода легче разорвать, чем сигма-связь? Связь между атомами углерода в вашем веществе тройная?12. Для вашего вещества характерны реакции замещения?
Ответьте на вопросы « Да или Нет » ЭТИН (6Б.) Вариант 2
В молекуле вещества тип гибридизации атома углерода sp3? Валентный угол в молекуле равен 1200 ? Каждый атом углерода образует по 2 сигма - связи с соседними атомами? В молекуле между атомами углерода присутствует пи - связь? Молекула имеет линейное строение? В молекуле атомы углерода могут вращаться вокруг своей оси? Длина связи между атомами углерода в молекуле составляет 0,134 нм? Длина связи между атомами водорода в молекуле составляет 0,109 нм? Связь С-Н в веществе менее прочная, чем связь между атомами углерода? Пи-связь между атомами углерода легче разорвать, чем сигма-связь? Связь между атомами углерода в вашем веществе тройная?12. Для вашего вещества характерны реакции замещения?
6. Концептуальная таблица. Приём используется, когда необходимо сравнить несколько объектов по нескольким позициям. Например, после изучения кислородсодержащих органических веществ в 10 классе ребята на уроке заполняют блок – схему, а домой получают задание составить 6 уравнений протекающих реакций.
Поставьте знак + там, где возможно протекание реакции
Вещество | Натрий | Гидроксид натрия | Лакмус | Окисление +(О) | Водород | Образование слож. эфира |
Этанол | ||||||
Этаналь | ||||||
Этановая кислота |
При подготовке к контрольной работе в 9 классе после изучения раздела «Металлы» ученики заполняют такую таблицу:
Поставьте знак + там, где возможно протекание реакции
Вещество | H2SO4 | CO2 | CuSO4 | KOH | фенолфталеин | Разложение при t0 |
NaOH | ||||||
Mg(OH)2 | ||||||
Al(OH)3 |
7. Таблица З-Х («Знаю – Хочу знать»)
Один из способов графической организации и логико-смыслового структурирования материала. Такие таблицы я использую на первом уроке в четверти, чтобы ученики вспомнили пройденный материал. А также такие таблицы помогают при подготовке к контрольным и проверочным работам. Например, в 11 классе после изучения темы «Химические реакции» учащиеся работают с таким заданием:
Основные вопросы темы «Химические реакции»Отметьте знаками: «+» знаю «-» хочу знать Химическая реакция - это… По составу и количеству участников реакции делятся на… Реакция является окислительно-восстановительной, если… Реакции ионного обмена протекают до конца, если… Уравнение реакции называют термохимическим, если а нём указан… Чтобы столкновение частиц было результативным, они должны обладать… Катализатор увеличивает скорость реакции потому, что он… Если реакция гетерогенная, то для увеличения её скорости обязательно надо… Химическое равновесие – это состояние реакционной системы, при котором … Концентрацию исходных веществ для увеличения скорости реакции и смещения равновесия вправо надо… Повышение давления сместит равновесие вправо в случае… |
Школьники в течение 5 минут выполняют задание индивидуально, затем в течение 2 минут обсуждают результаты с соседом по парте, а затем уже выясняют вопросы, помеченные знаком
«-», у учителя.
8. Чтение с остановками. Условное название методического приема организации чтения с использованием разных типов вопросов. Данный приём целесообразно использовать на стадии осмысления, дополняя эту методику другими приемами технологии на стадии вызова и рефлексии.
Подготовительная работа:
1. Учитель выбирает текст для чтения. Текст должен быть абсолютно неизвестным для данной аудитории (в противном случае теряется смысл и логика использования приема).
2. Текст заранее делится на смысловые части. Прямо в тексте отмечается, где следует прервать чтение и сделать остановку: «первая остановка», «вторая остановка» и т. д.
3. Учитель заранее продумывает вопросы и задания к тексту, направленные на развитие у учащихся различных мыслительных навыков.
Учитель дает инструкцию и организовывает процесс чтения с остановками, внимательно следя за соблюдением правил работы с текстом. (Описанная стратегия может использоваться не только при самостоятельном чтении, но и при восприятии текста «на слух»).
Такой приём я использую при изучении темы «Физические свойства металлов». Ученики вслух читают текст параграфа и мы совместно формулируем ответ на вопрос: «Какая особенность в строении металла объясняет данное физическое свойство?»
На уроке в 8 классе по теме «Виды ковалентной связи» ученики самостоятельно читают текст параграфа и выполняют следующее задание:
Используя текст учебника на странице 63-64, ответьте на вопросы: 1. В какой степени принадлежит атомам общая электронная пара в молекуле, образованной атомами одного и того же химического элемента? 2. В какой степени принадлежит атомам общая электронная пара в молекуле, образованной атомами различных химических элементов? 3. Какому атому общая электронная пара в такой молекуле будет принадлежать в большей степени? 4. Какие виды ковалентной связи выделяют? |
9. Групповая дискуссия. Дискуссия от лат. – исследование, разбор, обсуждение какого-либо вопроса. Учащимся предлагается поделиться друг с другом знаниями, соображениями, доводами. Обязательным условием при проведении дискуссии является:
А) уважение к различным точкам зрения ее участников;
Б) совместный поиск конструктивного решения возникших разногласий.
Групповая дискуссия может использоваться как на стадии вызова, так и на стадии рефлексии. При этом в первом случае ее задача: обмен первичной информацией, выявление противоречий, а во втором – это возможность переосмысления полученных сведений, сравнение собственного видения проблемы с другими взглядами и позициями. Форма групповой дискуссии способствует развитию диалогичности общения, становлению самостоятельности мышления.
10. «Продвинутая лекция».
Суть предлагаемой формы состоит в особой организации лекции с применением активной учебной модели вызов – осмысление – рефлексия. Учитель видоизменяет традиционную форму лекции, чтобы стимулировать учащихся к активному слушанию и критическому мышлению.
Алгоритм действий (возможны варианты):
1. Вызов. Подготовительная деятельность. Представление темы. Проблемный вопрос по содержанию лекции. (Работа в парах: обсуждение и запись имеющихся соображений для ответа, информационный прогноз, выступления от пар, фиксирование на доске высказанных идей).
2. Анонс содержания первой части лекции. Задание для учащихся (дл начала лекции): по ходу лекции один человек в паре кратко записывает новую информацию по проблемному вопросу, другой отмечает в первичных записях совпадения «+» и расхождения «-» услышанной в лекции информации со сделанным ранее прогнозом (аудированный вариант ИНСЕРТа)
3. Осмысление. Учитель зачитывает первую часть лекции.
4. Рефлексия. Предварительное подведение итогов.(Индивидуальное задание: выделение главного – письменный ответ. Работа в парах: обсуждение прогноза с услышанным материалом, обсуждение в паре, формулировка общего ответа, выступления от пар).
5. Повторный вызов. Анонс содержания второй части лекции. Проблемный вопрос. (Работа в парах: обсуждение и запись имеющихся соображений для ответа, информационный прогноз, выступления от пар, фиксирование на доске высказанных идей). Задание для учащихся (аналогичное пункту - 2).
6. Осмысление. Учитель зачитывает вторую часть лекции.
7. Рефлексия. Подведение итогов. (Работа в парах: обсуждение прогноза с услышанным материалом, выступления от пар).
8. Итоговая рефлексия. Задание классу: индивидуальная самостоятельная работа – письменный ответ на общий глобальный вопрос по материалу лекции. Форма – 10-минутное эссе.
9. Работы сдаются учителю. (Используются как показатель усвоения учащимися содержания лекции, а также как материал для подготовки следующего занятия.
11.Эссе.
Жанр критики и публицистики, свободная трактовка какой-либо литературной, философской, эстетической, моральной и социальной проблемы. Целесообразно использовать как небольшое письменное задание на стадии рефлексии.
Различают 5-минутное эссе, 10-минутное эссе, а также более продолжительные и трудоемкие сочинения.
10-минутное эссе. После чтения (прослушивания) и общего обсуждения текста учащимся предлагается организовать свои мысли с помощью 10-минутного эссе (по методике свободного письма). Для этого учитель просит в течение 10 минут писать на предложенную тему. Главное правило свободного письма – не останавливаться, не перечитывать, не исправлять. При затруднении можно письменно прокомментировать возникшую проблему и постараться писать дальше. Иногда текст свободного эссе предлагается использовать как подготовительный этап работы для более солидного сочинения.
5-минутное эссе. Этот вид письменного задания обычно применяется в конце занятия, чтобы помочь учащимся подытожить свои знания по изученной теме. Для учителя – это возможность получить обратную связь. Поэтому учащимся можно предложить два пункта:
1) написать, что они узнали по новой теме;
2) задать один вопрос, на который они так и не получили ответа.
12. Ключевые термины.
Учитель выбирает из текста 4-5 ключевых слов и выписывает их на доску.
Вариант «а»: Парам отводится 5 минут на то, чтобы методом мозговой атаки дать общую трактовку этих терминов и предположить, как они будут фигурировать в последующем тексте.
Вариант «б»: Учащимся предлагается в группе или индивидуально составить и записать свою версию рассказа, употребив все предложенные ключевые термины.
При знакомстве с исходным содержанием, учащиеся сопоставляют «свою» версия и версию «оригинального текста». Описанное задание обычно используется на стадии «вызова», однако на стадии «рефлексии» целесообразно вернуться к ключевым терминам и обсудить обнаруженные совпадения и выявленные разногласия.
13. Перепутанные логические цепочки.
На отдельные листы выписываются 5-6 событий из текста (как правило, историко-хронологического или естественно-научного). Демонстрируются перед классом в заведомо нарушенной последовательности. Учащимся предлагается восстановить правильный порядок хронологической или причинно-следственной цепи. После заслушивания различных мнений и придя к более или менее единому решению, учитель предлагает ученикам познакомиться с исходным текстом и определить: верны ли были их предположения.
14. «Толстые» и «тонкие» вопросы.
Толстый. | Тонкий. |
Объясните почему….? Почему вы думаете….? Предположите, что будет если…? В чём различие…? Почему вы считаете….? | Кто..? Что…? Когда…? Может…? Мог ли…? Было ли…? Будет…? Согласны ли вы…? Верно ли…? |
15. Ромашка Блума
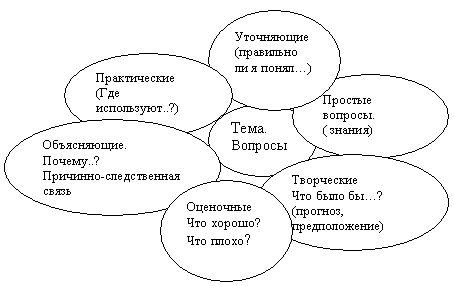
Вопросы по Блуму
- Простые вопросы (фактические вопросы) – требуют знания фактического материала, ориентированы на работу памяти
- Уточняющие вопросы – «насколько я понял….», «правильно ли я Вас поняла, что…»
- Интерпретирующие вопросы (объясняющие) – побуждая учеников к интерпретации, мы учим их навыкам осознания причин тех или иных поступков или мнений (почему?)
- Оценочные вопросы (сравнение) – необходимо использовать, когда вы слышите, что кто-либо из учеников выражает соседу по парте свое недовольство или удовольствие от произошедшего на уроке
- Творческие вопросы (прогноз) – «Как вы думаете, что произойдет дальше…?»
- Практические вопросы – «Как мы можем…?» «Как поступили бы вы…?»
16. Бортовой журнал.
Что я знаю по теме | Что нового узнал | Что не понял |
17. «Фишбоун» (рыбный скелет)
Голова - вопрос темы, верхние косточки - основные понятия темы, нижние косточки — суть понятии, хвост – ответ на вопрос. Записи должны быть краткими, представлять собой ключевые слова или фразы, отражающие суть.
Все эти методы и приёмы технологии развития критического мышления позволяют не только ученикам, но и учителю работать творчески.
Заключение
Современное общество заинтересованно в том, чтобы его граждане были способны самостоятельно действовать, принимать решения, гибко адаптироваться к изменяющимся условиям жизни. Технология развития критического мышления позволяет реализовать эти задачи через включение в урок разнообразных методов и приёмов, которые могут быть применены в различных предметных областях.
Использование технологии развития критического мышления делает уроки разнообразнее, обеспечивает деятельность учащихся на каждом этапе урока. Мне обычно в ходе урока удаётся применить 6-7 видов деятельности учащихся. При составлении кластера, синквейна, написании эссе школьники имеют возможность общаться через парную или групповую работу, проявлять своё творчество. Выполняя задания самоконтроля и самооценки, работая с инструктивными карточками, ученики развивают навыки самоорганизации и саморегуляции, навыки самоанализа, критического отношения к себе.
При работе в рамках этой технологии я столкнулась с тем, что на уроке тратится много времени на вычерчивание в тетрадях блок-схемы кластера. Чтобы ускорить этот процесс, я стала перед уроком набирать основу кластера и уже во время занятия выдавать её каждому ученику. Однако, не все дети бережно относятся к выданному им в личное пользование карточек. Поэтому, если позволяет время, я по ходу работы учеников сама вклеиваю или прикрепляю степлером карточки им в тетради. Ещё одна проблема при использовании данной технологии - большая подготовительная работа учителя, так как пока ещё нет пособий с готовыми заданиями.
Список литературы
1. ,
Технология развития критического мышления на уроках истории и краеведения. СПБ, 2001.
2. Гражданское образование.
Учебно – методическое пособие. СПБ, 2003.
3. , Заир-,
Учим детей мыслить критически. СПБ, 2003.
4. Селевко образовательные технологии. Учебное пособие. М., 1998
5.
Химия – 8 (9, 10,11). Учебник для общеобразовательных учреждений. Москва, 2010
6. Нечитайлова технологии развития критического мышления на уроках химии. Статья. Журнал «Химия в школе» № 6, 2011
Приложение
Урок по химии 8 класс
Вычисления по химическому уравнению
Цели урока.
Образовательные:
- начать формировать умение производить различные вычисления с использованием уравнения химической реакции; познакомить учащихся с алгоритмом решения задач.
Развивающие: (совершенствование у учащихся)
- умения работать с расчётными формулами, используя величину количество вещества, молярная масса; навыков аналитической мыслительной деятельности; навыков познавательной деятельности; навыков самоорганизации и самоконтроля при выполнении работы.
Воспитательные: (развитие у учащихся навыков)
- аккуратности, внимательности, точности в выполнении работы; настойчивости в достижении цели, в доведении начатого до конца; умения работать в парах.
Оборудование.
бланки для внесения ответов при составлении кластера, карточки – задания для самостоятельного решения и проверки задач.
Структура урока
по технологии развития критического мышления
Деятельность учителя | Деятельность учащихся | Приёмы и методы |
Стадия вызова | ||
Вызывает уже имеющиеся знания, задаёт вопросы по ранее изученному материалу, обсуждает полученную от учащихся информацию. | Вспоминают, анализируют, систематизируют уже имеющиеся знания по этой теме, демонстрируют свои знания с помощью устной речи. | Составление кластера. Совместное обсуждение полученных результатов. Корректировка записей в кластере. Работа ведётся индивидуально и парами. |
Стадия осмысления | ||
Рассказывает содержание нового материала, ведёт записи на доске, поддерживает интерес учащихся к теме, контролирует выполнение лабораторных опытов. | Слушают объяснение учителя, ведут записи в тетрадях, выполняют задание самоконтроля – решение задачи по образцу. | Ведение записей в тетради, ответы на поставленные вопросы, решение задачи по образцу – самоконтроль. Работа ведётся индивидуально, самоорганизация своей деятельности. |
Стадия рефлексии | ||
Помогает проанализировать изученную информацию, установить причинно - следственные связи между блоками информации. | Соотносят новую информацию с уже имеющимися знаниями. | Ответы на поставленные вопросы, возврат к ключевым словам и алгоритму решения задач. Работа ведётся совместно со всеми учащимися. |
Ход урока
Умение решать задачи есть искусство,
приобретенное практикой.
Д. Пойа.
I. Организационный момент. (1мин)
· подготовка аудитории к работе
· приветствие
· наличие учащихся
II. Мотивация учебной деятельности (1мин)
Итак, ребята, вы уже познакомились на предыдущих уроках с понятием уравнение химической реакции.
Сегодня мы начнем, а на следующем занятие продолжим разбирать вопрос о том, как при помощи уравнения химической реакции можно производить различные вычисления.
Сообщение темы и эпиграфа урока, постановка познавательных задач для учащихся.
Тема урока и эпиграф записаны на доске.
Задачи учащихся:
- понять, как производить вычисления с использованием уравнения химической реакции; научиться пользоваться алгоритмом решения задач.
III. Актуализация знаний учащихся. (13мин)
Сегодня мы начнём разбирать новый материал с воспоминания основных расчётных формул, которые использовали при вычислениях по химической формуле вещества. Для этого я вам приготовила специальные бланки, где вы внесёте свои ответы в течении 5 минут. Постарайтесь работать самостоятельно, проверяя себя и свою память.
Каждому ученику выдаётся бланк – кластер для внесения ответов. Кластер каждый ученик заполняет сам, а затем 2 минуты обсуждает результаты своей работы с соседним учеником по парте. После этого в течении 6 минут результаты работы обсуждаются совместно с учителем, а учащиеся класса вносят поправки в графу «дополнения, исправления».
Заполните таблицу
вопросы | ответы | дополнения и исправления |
| Запишите обозначения: А) молярная масса Б) количество вещества В) объем газа Г) масса вещества Д) число структурных частиц | А) Б) В) Г) Д) | |
| Составьте формулы для вычисления количества вещества, используя: А) массу вещества Б) объем газа В) число структурных частиц | А) Б) В) | |
3. Укажите числовое значение А) молярного объема Б) числа Авогадро | А) Б) | |
4. Напишите единицы измерения: А) количества вещества Б) молярной массы В) молярного объема | А) Б) В) | |
5.Что означают коэффициенты урав- нений химических реакций в макромире? |
IV. Изложение нового материала. (25мин)
1) Вы уже умеете производить вычисления по химической формуле вещества. А теперь начнём учиться производить вычисления с помощью химического уравнения. Делать это будем на конкретном примере.
Запись на доске и в тетрадях учащихся
Пример: Вычислите массу воды, которая образуется при сжигании 8г водорода.
m(H2O)-? Дано: m(H 2 )=8г M(H2)=2 г/моль M(H2O)=18 г/моль | Решение: 1. Составляем уравнение 8г m-? 2H2 + O2= 2 H2O 2 моль 2 моль |
Находим количество вещества, масса которого известна:
n (H2)= ![]() =
=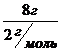 =4моль
=4моль
3. Находим количество вещества, масса которого неизвестна:
n (H2): n (H2O)=2:2; n (H2)= n (H2O); n (H2O)=4 моль
4. Находим неизвестную массу:
m(H2O) =n*M =4 моль*18 г/моль =72г
Ответ: образуется 72г воды.
То, что у вас, ребята, оказалось подчёркнутым, является основными шагами при решении задач, т. е. её план или алгоритм. Ещё раз проговорить алгоритм решения.
2) После разбора типовой задачи учащиеся класса решают аналогичную задачу в тетрадях, получая карточку – задание, составленное по принципу самоконтроля. Это своеобразные карточки, где на одной стороне листа написано условие задачи, а на другой - решение. Таким образом, учащиеся уже самостоятельно проверяют себя, насколько они усвоили материал.
Вариант 5. Какая масса серной кислоты получится при взаимодействии оксида серы VI массой 32г с водой? SO3 + H2O = H2SO4 | Найти: m(H2SO4)-? Дано: m(SО3)=32г M(SО3)= 80 г/моль M(H2SO4)= 98 г/моль | Решение: 1. 32г m-? SO3 + H2O = H2SO4 1 моль 1 моль 2.n (SO3)= 32 г : 80 г/ моль = 0,4 моль по уравнению реакции n (SO3): n (H2SO4)=1:1 n (H2SO4 ) = n (SO3)= 0,4 моль 5. m(H2SO4)= 0,4моль* 98 г/моль=39,2 г Ответ:39,2г |
3) Мы сейчас разобрали задачу, где коэффициенты веществ, используемых при решении, были равны. А как быть, если коэффициенты будут разными?
Запись на доске и в тетрадях учащихся
2А + 3В = А2В3 n (А) : n (В) = 2 : 3 n (А) = 2* n (В) : 3
V. Закрепление изученного материала, сообщение домашнего задания. (5мин)
Итак, сегодня на уроке мы начали выполнять большую и сложную работу по формированию умения производить различные вычисления с использованием уравнения химической реакции.
Вопросы учащимся:
Сколько этапов – шагов в решении подобных задач? На каком этапе решения используется уравнение химической реакции? Что определяют с помощью уравнения химической реакции? Как определить количество вещества, массу которого надо определить?Домашнее задание (заранее написано на доске):
Выучить план решения задач; решить задачу: Найти массу оксида серы IV, который образуется при взаимодействии 4,8г серы с кислородом. S + O2= SO2
Приложение
Урок по химии 8 класс
Химические свойства кислот в свете электролитической диссоциации
Цели урока.
Образовательные:
· актуализировать знания о составе и свойствах кислот;
- продолжить знакомство с основными химическими свойствами кислот в свете электролитической диссоциации.
Развивающие: (совершенствование у учащихся)
- умения составлять уравнения химических реакций с участием кислот в молекулярном и ионном виде; умения предсказывать химические свойства кислот; умения работать с реактивами и оборудованием; умения работать с текстом учебника, выделять главное, анализировать, формулировать выводы;
- навыков аналитической мыслительной деятельности; навыков познавательной деятельности; навыков самоорганизации, самоконтроля и самооценки при выполнении работы.
Воспитательные: (развитие у учащихся навыков)
- аккуратности, внимательности, точности в выполнении работы; настойчивости в достижении цели, в доведении начатого до конца; ответственности к выполнению полученного задания; умения работать в парах.
Оборудование. Реактивы.
Бланки для внесения ответов при составлении кластера, инструктивные карточки для проведения лабораторных опытов, карточки – задания для закрепления полученных знаний, учебники Химия-8 2008, пластины для проведения лабораторных опытов, шпатель, р-р гидроксида натрия, р-р сульфата меди II, р-р соляной кислоты, оксид кальция, р-р азотной кислоты, р-р серной кислоты, р-р карбоната натрия.
Структура урока
по технологии развития критического мышления
Деятельность учителя | Деятельность учащихся | Приёмы и методы |
Стадия вызова | ||
Вызывает уже имеющиеся знания, задаёт вопросы по ранее изученному материалу, обсуждает полученную от учащихся информацию. | Вспоминают, анализируют, систематизируют уже имеющиеся знания по этой теме, демонстрируют свои знания с помощью устной речи. | Составление кластера. Совместное обсуждение полученных результатов. Корректировка записей в кластере. Самопроверка и самооценка за ответы в кластере. Работа ведётся индивидуально и парами. |
Стадия осмысления | ||
Рассказывает содержание нового материала, ведёт записи на доске, поддерживает интерес учащихся к теме. | Слушают объяснение учителя, ведут записи в тетрадях, выполняют лабораторные опыты, работают с текстом учебника. | Записи в тетради, ответы на поставленные вопросы, лабораторная работа, работа с материалом учебника. Работа ведётся индивидуально и парами. |
Стадия рефлексии | ||
Помогает проанализировать изученную информацию, установить причинно - следственные связи между блоками информации. | Соотносят новую информацию с уже имеющимися знаниями. | Выбор из списка формул тех веществ, которые взаимодействуют с кислотами. Самопроверка и самооценка за работу в течение всего урока. Работа ведётся индивидуально. |
Ход урока
I. Организационный момент. (1мин)
· подготовка аудитории к работе
· приветствие
· наличие учащихся
II. Мотивация учебной деятельности (1мин)
Итак, ребята, вы уже познакомились на предыдущих уроках с понятием «кислота» и разобрали вопрос о взаимодействии кислот с металлами. Сегодня мы продолжим знакомство с химическими свойствами кислот и будем учиться составлять уравнения химических реакций с участием кислот в молекулярном и ионном виде.
Сообщение темы урока, постановка познавательных задач для учащихся.
Тема урока записана на доске.
Задачи учащихся:
- запомнить основные химические свойства кислот в свете электролитической диссоциации;
- научиться составлять уравнения химических реакций с участием кислот в молекулярном и ионном виде.
III. Актуализация знаний учащихся. (13мин)
Сегодня мы начнём разбирать новый материал с заполнения кластера, что позволит нам вспомнить основные вопросы по кислотам. Для этого я вам приготовила специальные бланки, где вы внесёте свои ответы в течении 5 минут. Постарайтесь работать самостоятельно, проверяя себя и свою память.
Каждому ученику выдаётся бланк – кластер для внесения ответов. Кластер каждый ученик заполняет сам, а затем 2 минуты обсуждает результаты своей работы с соседним учеником по парте. После этого в течении 5 минут результаты работы обсуждаются совместно с учителем, а учащиеся класса вносят поправки в графу «дополнения, исправления».
Заполните таблицу
вопросы | ответы | дополнения и исправления |
1. На какие ионы диссоциируют кислоты? | ||
2. Почему растворы кислот проявляют одинаковые свойства? | ||
3. Какой цвет приобретает лакмус в растворе кислоты? | ||
4. Закончите возможное уравнение реакции: Zn + HCl à Cu + HCl à | ||
5. При каких условиях реакции между ионами протекают до конца? |
Во время проверки ответов учащиеся ставят себе по 1 баллу за верно выполненное задание. Таким образом, они могут максимально получить 5 баллов.
IV. Изложение нового материала. (25мин)
Итак, продолжаем разбирать основные химические свойства кислот в свете электролитической диссоциации. Когда мы изучали реакции обмена между ионами, то я вам показывала, как происходит взаимодействие между кислотой и щелочью. Напомните себе ещё раз этот материал с помощью текста учебника на странице 205. Когда будете читать материал, отметьте те моменты, которые, на ваш взгляд, требуют комментариев.
В течение 2-х минут ученики работают с учебником, а затем учитель даёт ответы на их вопросы, ещё раз акцентируя внимание на порядке выполнения данного эксперимента.
Кислоты могут взаимодействовать не только со щелочами, но и с нерастворимыми основаниями.
Таким образом, мы переходим с вами к выполнению лабораторных опытов.
Учитель выдаёт учащимся инструктивную карточку и напоминает основные правила работы по технике безопасности. Работа проводится по следующему плану: выполнение опыта, запись уравнения проделанной реакции в молекулярном и ионном виде, определение смысла реакции по записи краткого ионного уравнения. По мере разбора материала учитель сам или с помощью учащихся ведёт записи на доске.
Инструктивная карточка
Исследования химических свойств кислот
Л. о. №1. В ячейку пластины поместите 2 капли гидроксида натрия и 1 каплю сульфата меди II. К полученному осадку добавьте 1 каплю соляной кислоты. Что произошло с осадком? Составьте уравнение реакции между гидроксидом меди II и соляной кислотой в молекулярном и ионном виде.
Л. о. №2. В ячейку пластины поместите шпателем немного оксида кальция и прилейте к нему 2 капли азотной кислоты. Что произошло с оксидом? Составьте уравнение реакции между оксидом кальция и азотной кислотой в молекулярном и ионном виде.
Л. о. №3. В ячейку пластины поместите 1каплю карбоната натрия и 1 каплю серной кислоты. Что произошло при этом? Составьте уравнение реакции между карбонатом натрия и серной кислотой в молекулярном и ионном виде.
После выполнения лабораторной работы учитель просит учеников ответить на вопрос:
С какими классами веществ могут взаимодействовать кислоты?
Вывод по уроку подводим с помощью схемы на 211-ой странице учебника.
V. Закрепление изученного материала, сообщение домашнего задания. (5мин)
Для закрепления полученных знаний учитель предлагает выполнить задание, которое записано на обратной стороне бланка – кластера. Задание выполняют 2 минуты, затем проверяют правильность его выполнения. Во время проверки ответов учащиеся ставят себе по 1 баллу за верно выполненное задание. Таким образом, они могут максимально получить 4 балла.
Вариант 1 | Вариант 2 |
Выберите формулы веществ, с которыми будет взаимодействовать раствор кислоты и реакции протекают до конца соляная кислота + Al, SO2, Fe(OH)2, Aq, K2O, CuSO4, AqNO3. | Выберите формулы веществ, с которыми будет взаимодействовать раствор кислоты и реакции протекают до конца серная кислота + Fe, K2CO3, CO2, Mq(OH)2, BaCl2, Cu, Al2O3. |
В конце урока ученики суммируют свои баллы. Учитель отмечает или оценивает работу тех учеников, которые по ходу урока были активны и набрали 8-9 баллов.
Домашнее задание (заранее написано на доске):
§ 38, выполнить упр. 4 на стр. 214




 Найти:
Найти:
