Лабораторная работа № 1
ОПРЕДЕЛЕНИЕ МОЛЯРНОЙ МАССЫ ЭКВИВАЛЕНТА МЕТАЛЛА
Цель работы: Определить молярную массу эквивалента цинка.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В лабораторной работе проводится определение молярной массы эквивалента неизвестного металла по объему водорода, выделившегося в реакции с хлороводородной кислотой образца этого металла известной массы.
Оборудование: эвдиометр (градуированный стеклянный сосуд для сбора газа); кристаллизатор; колба с газоотводной трубкой; штатив с лапкой; весы и разновесы; барометр; термометр.
Реактивы: раствор хлороводородной кислоты 1:2; исследуемый металл.
3.1. Ход работы
Собрать установку, схема которой приведена на рис. 1.
В кристаллизатор налить примерно ½ объема воды (используется в качестве гидрозатвора).

Рис. 1. Установка для измерения объема выделившегося водорода:
1 – штатив; 2 – кристаллизатор с водой; 3 – эвдиометр; 4 – газоотводная трубка; 5 – навеска металла; 6 – колба с раствором кислоты.
Набрать в стакан водопроводной воды и налить в эвдиометр. Закрыть его отверстие большим пальцем руки, опрокинуть и опустить открытый край эвдиометра в воду, налитую в кристаллизатор. Закрепить эвдиометр в штативе, на зажимая сильно лапку штатива.
Подвести под эвдиометр газоотводную трубку. Если уровень мениска воды в эвдиометре находится выше шкалы, необходимо немного приподнять эвдиометр и пустить в него небольшой пузырь воздуха.
На технических весах определить массу выданного образца металла (от 100 до 200 мг). Полученное значение записать в лабораторный журнал.
Отмерить цилиндром и перелить в реакционную колбу 10-15 мл раствора хлороводородной кислоты HCl (1:2).
Взвешенный кусочек металла положить в горлышко колбы, повернутой горизонтально, чтобы растворение металла не началось до полной сборки системы.
Колбу закрыть пробкой с газоотводной трубкой, обеспечив герметичность системы улавливания газа.
Записать значение объема воды в эвдиометре до начала опыта.
Колбу поставить в вертикальное положение, чтобы металл упал в кислоту.
После завершения выделения водорода записать конечное значение объема.
2. Оформление лабораторного отчета и расчет результата
Зарисовать схему прибора.
Написать уравнение реакции между металлом (Al, Fe, Sn или Zn) и хлороводородной кислотой.
Записать экспериментальные данные по следующей форме:
m – масса металла, г;
V1 – объем газа в эвдиометре до растворения металла, дм3;
V2 – объем газа в эвдиометре после растворения металла, дм3;
Vоэ(Н2) = 11,2 дм3/моль – объем моля эквивалентов водорода (н. у.);
Mэ(Н) = 1 г/моль – молярная масса эквивалента водорода;
t – температура в лаборатории, оС ;
Т – температура в лаборатории, К;
То – стандартная температура 273 К;
Ратм – атмосферное давление по барометру, мм. рт. ст. (перевести в кПа);
Ро – стандартное давление (760 мм рт. ст. = 101,325 кПа)
h1 – давление насыщенного водяного пара, при температуре проведения опыта (взять из табл. 3, перевести в кПа);
h2 – давление столба воды в эвдиометре по окончании опыта.
Для выбора значения h1 использовать данные табл. 1.
Величину h2 рассчитать по формуле:
h2 = ρ(H2O) ·g ·h(H2O),
где ρ(H2O) = 1000 кг/м3 – плотность воды;
g = 9,81 м/с2 – ускорение свободного падения;
h(H2O) – высота столба воды в эвдиометре, м.
3. Расчет молярной массы эквивалентов металла
Привести объем выделившегося водорода к нормальным условиям по уравнению :
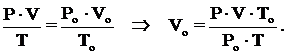
Парциальное давление водорода в эвдиометре P = Ратм – h1 – h2;
объем выделившегося водорода в условиях опыта V = V2 – V1.
Рассчитать массу выделившегося водорода, воспользовавшись следствием из закона Авогадро:
ν(Н2) = V / Vm;
m(Н2) = ν(Н2) · M(H2).
Рассчитать молярную массу эквивалента металла двумя способами.
Таблица 1
Давление насыщенного водяного пара при различной температуре
t, оС | Давление пара, мм рт. ст. | t, оС | Давление пара, мм рт. ст. |
15 | 12,79 | 21 | 18,65 |
16 | 13,63 | 22 | 19,83 |
17 | 14,53 | 23 | 21,09 |
18 | 15,48 | 24 | 22,38 |
19 | 16,48 | 25 | 23,76 |
20 | 17,54 | 30 | 31,32 |
4. Расчет погрешности определения Мэ(Ме)
После расчета величины Мэ(Ме) узнать у преподавателя, какой металл использовали в опыте.
По данным Периодической системы вычислить истинное значение Мэо(Ме).
Рассчитать относительную ошибку определения Мэ(Ме) по формуле
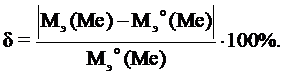
При относительной ошибке, превышающей 5%, в выводах указать предположительную причину значительного отклонения результата от истинного значения.
5. КОНТРОЛЬНЫЕ ВОПРОСЫ ДЛЯ ЗАЩИТЫ РАБОТЫ
1. Чьи идеи лежат в основе атомно-молекулярного учения? В чем их суть? Что является основным принципом атомно-молекулярного учения?
2. Назовите основные положения атомно-молекулярного учения.
3. Перечислите основные количественные законы химии.
4. Сформулируйте закон эквивалентов, закон кратных отношений.
5. Что такое эквивалент, фактор эквивалентности?
6. Как рассчитать молярную массу эквивалентов оксида, кислоты, гидроксида, соли (нормальной, основной и кислой)?
7. Сформулируйте закон Авогадро.
8. Какое следствие из закона Авогадро используют в расчете результата данной работы?
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
1. Глинка химия: Учеб. пособие для вузов. – 23-е изд. – Л.: Химия, 1984. – 704 с.
2. Фролов : Учеб. пособие для машиностроит. спец. вузов. – 3-е изд. – М.: Высш. шк., 1986. – 543 с.
3. , , Таперова работы по общей и неорганической химии: Учеб. пособие для вузов. – 3-е изд. – Л.: Химия, 1969. – 304 с.



