Муниципальное бюджетное образовательное учреждение
средняя общеобразовательная школа № 46 г. Тверь
Модуль по экологической составляющей производства серной кислоты из программы элективного курса для 10 класса (профильный уровень) «Химическая экология».
Автор:
Учитель химии высшей
квалификационной категории
МОУ СОШ № 46 г. Твери
Экологические проблемы, связанные с производством серной кислоты, и способы их решения.
Современное общество не может существовать без химических веществ. В частности, человек использует их для защиты своего здоровья, увеличения производства продуктов питания и облегчения повседневной жизни. Из более чем 6 млн. известных науке веществ в широком использовании находится от 60 до 70 тыс. из них, причем каждый год появляются еще от 500 до 1000 новых. Серная кислота – важнейший продукт химической промышленности. Она находит применение в производстве минеральных удобрений, волокон, пластмасс, красителей, взрывчатых веществ, в металлургии при получении меди, никеля, урана и других металлов. Используется и как осушитель газов. Много серной кислоты идет на очистку нефтепродуктов от вредных примесей. Большое практическое применение из солей серной кислоты имеют различные сульфаты. Медный и железный купоросы
CuSO4 ∙ 5H2O, и FeSO4 ∙ 7H2O
используются в сельском хозяйстве для борьбы с вредителями растений, в производстве красок, для пропитки древесины в качестве антисептического средства.
Купоросами называют кристаллогидраты сульфатов некоторых металлов (меди, железа, цинка и никеля).
Гипс CaSO4 ∙ 2H2O и сульфат кальция CaSO4 используют в строительстве, медицине и других областях.
Из гипса при прокаливании получают алебастр CaSO4 ∙ 0,5H2O:
CaSO4 ∙ 2H2O = CaSO4 ∙ 0,5H2O + 1,5H2O
Алебастр, смешанный с водой, быстро затвердевает, превращаясь в гипс:
CaSO4 ∙ 0,5H2O + 1,5Н2О = CaSO4 ∙ 2H2O
Сульфат натрия Na2SO4 используется в производстве стекла. Сульфаты
калия K2SO4 и аммония (NH4)2SO4 применяют как удобрения. Сульфат бария BaSO4 применяется в производстве бумаги, резины и минеральных красок.
Многие вещества оказывают вредное воздействие на здоровье людей и животных, на почву, растения, здания, в том числе памятники архитектуры. Выход из сложившейся ситуации специалисты видят в том, чтобы ожидания от использования этих веществ выгоды превышали заложенную в них опасность; для этого человек должен пользоваться ими разумно, т. е. предотвращать негативное влияние на окружающую среду.
Вместе с тем интенсивный рост химического производства, вызывает существенные негативные изменения в окружающей среде: отравление пресных вод, загрязнение атмосферы, истребление животных и птиц. В результате мир оказался в тисках экологического кризиса.
Вредные выбросы сернокислых заводов, содержащийся в них оксид серы (IV) , увеличивают количества случаев респираторных заболеваний человека, гибель животных и растительности, подавление её роста, разрушение конструкций из известняка и мрамора, повышение коррозионного износа металлов. Появляются «кислотные дожди».
Цель моего реферата – изучить влияние производства серной кислоты на биосферу.
Для этого я поставил следующие задачи:
· Изучить литературу по данному вопросу;
- Рассмотреть технологию производства серной кислоты; Выделить экологические проблемы, связанные с производством кислоты; Оформить рисунки, схемы, подготовить презентацию.
Широкое применение серная кислота находит в органическом синтезе, в производстве красок, пластмасс, взрывчатых веществ, различных медицинских препаратов. По мере расширения производства химических продуктов увеличивается производство серной кислоты.
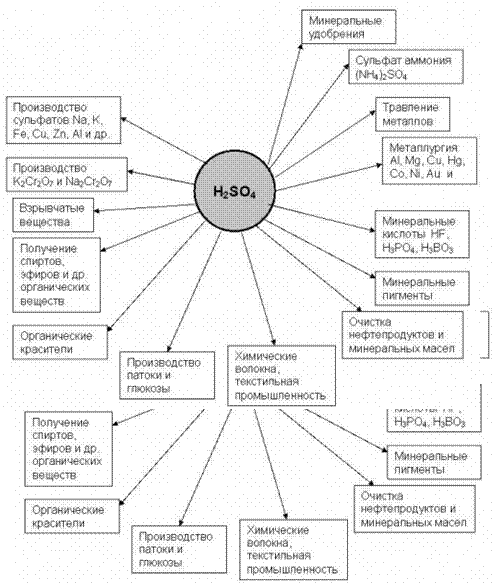 |
Серная кислота – бесцветная жидкость без запаха. Смешивается с водой во всех соотношениях, растворение сопровождается выделением значительного количества тепла, паров и газов. Чрезвычайно агрессивное вещество, поражает дыхательные пути, кожу, слизистые оболочки, вызывает затруднение дыхания, кашель, нередко – ларингит, трахеит, бронхит и т. д.
Прóлив отработанной серной кислоты на почву полностью уничтожает почвенную микрофлору, живые организмы, семена и корни растений и делает почву непригодной для роста и развития растений и живых организмов в будущем.
Воздействие серной кислоты на организм человека. Класс опасности II.
При вдыхании паров серной кислоты возникает раздражение и ожог глаз, слизистых оболочек носоглотки, гортани, носовые кровотечения, боль в горле, охриплость голоса из-за спазма голосовой щели, развивается отек голосовых связок, гортани, легких, вызывающий резкое затруднение дыхания. Лицо отравившегося человека становится синюшным, зрачки расширяются. Попадание серной кислоты в глаза грозит потерей зрения. При попадании серной кислоты на кожу возникают трудно поддающиеся лечению химические ожоги, при которых редко возникают пузыри, так как в своем большинстве они относятся к ожогам III и IV степени. Тяжесть поражения кожи и слизистых оболочек при химическом ожоге зависит от концентрации кислоты, длительности ее действия на ткани и площади ожога. Однако, при длительном воздействии, вызвать ожог может и слабый раствор серной кислоты. Ожог может существенно углубиться за 20-30 мин, если его распространению способствует пропитанная кислотой одежда.
Аэрозоль серной кислоты может образовываться в атмосфере в результате выбросов химических и металлургических производств, содержащих оксиды S, и выпадать в виде кислотных дождей.
1.Общая характеристика серной кислоты.
Безводная серная кислота – тяжелая бесцветная маслянистая жидкость, растворяющаяся в воде в любых соотношениях. Она гигроскопичная, нелетучая, без запаха, не проводит электрический ток. При температуре 10,3 °C затвердевает, образуя кристаллы, похожие на лёд. Температура кипения составляет 296,2 °С, при дальнейшем повышении температуры она разлагается.
Плотность 1,83 г/мл (200 °С). Это молекулярное вещество, относящееся к сильным двухосновным кислотам, структура которого соответствует модели, изображённой на рисунке (рис. 1).
Химические свойства серной кислоты во многом зависят от её
концентрации. В лабораториях и промышленности применяют разбавленную и концентрированную серную кислоту, хотя это деление условно (четкую границу между ними провести нельзя).
Взаимодействие с металлами.
Разбавленная серная кислота взаимодействует с некоторыми металлами, например с железом, цинком, магнием, с выделением водорода:
Fe + H2SО4 = FeSO4 + H2↑
Некоторые малоактивные металлы, такие как медь, серебро, золото, с разбавленной серной кислотой не реагируют.
Концентрированная серная кислота является сильным окислителем. Она окисляет многие металлы. Продуктами восстановления кислоты
обычно является оксид серы (IV), сероводород и сера (H2S и S образуется в реакциях кислоты с активными металлами - магнием, кальцием, натрием, калием и др.).
Примеры реакций:
Cu + 2H2SO4 = CuSO4 + SO2+ 2H2O
Mg + 2H2SO4 = MgSO4 + SO2+ 2H2O или
4Mg + 5H2SO4 = 4MgSO4 + H2S + 4H2O
Серная кислота высокой концентрации (практически безводная) не взаимодейст
вует с железом в результате пассивации металла. Явление пассивации связано с образованием на поверхности металла прочной сплошной пленки, состоящей из оксидов или других любых соединений, которая препятствует контакту металла с кислотой. Благодаря пассивации можно перевозить и хранить концентрирован ную серную кислоту в стальной таре. Концентрированная серная кислота пасси вирует также алюминий, никель, хром, титан.
Взаимодействие с неметаллами.
Концентрированная серная кислота может окислять неметаллы, например:
S + 2H2SO4 = 3SO2 + 2H2O
Окислительные свойства концентрированной серной кислоты могут также проявляться с некоторыми сложными веществами – восстановителями, например:
2KBr + 2H2SO4 = Br2 + SO2 + K2SO4 + 2H2O
Взаимодействие с основными оксидами и основаниями.
Серная кислота проявляет все типичные свойства кислот. Так, она реагирует с основными и амфотерными оксидами и гидроксидами с образованием солей. Как двухосновная кислота H2SO4 образует два типа солей: средние соли – сульфаты и кислые соли – гидросульфаты.
Примеры реакций:
Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O
сульфат алюминия
2KOH + H2SO4 = K2SO4 + 2H2O
сульфат калия
KOH + H2SO4 = KHSO4 + H2O
гидросульфат калия
Гидросульфаты образуются, когда кислота берётся в избытке. Многие соли сер ной кислоты выделяются из растворов виде кристаллогидратов, например:
Al2 (SO4)3 ∙18H2O
Na2SO4 ∙ 10H2O
Взаимодействие с солями.
С некоторыми солями кислота вступает в реакции обмена, например:
CaCO3 + H2SO4 = CaSO4 + CO2 + H2O
BaCl2+ H2SO4 = ВаSO4 + 2HCl
Последняя реакция является качественной на серную кислоту и ее соли: об их присутствии в растворе судят по образованию белого осадка BaSO4, который практически не растворяется в концентрированной азотной кислоте.
Взаимодействие с водой.
При растворении в воде серная кислота активно взаимодействует с ней образуя гидраты:
nH2O + H2SO4 = H2SO4 ∙ nH2O
Благодаря способности связывать воду серная кислота является хорошим осушителем.
2. Производство серной кислоты контактным способом.
Исходным сырьём для производства серной кислоты могут быть: сера, сероводо род, сульфиды металлов. Рассмотрим производство серной кислоты контактным способом, при котором исходным сырьём является пирит FeS2.
Весь процесс можно разбить на три последовательных стадии:
получение диоксида серы,
окисление его до триоксида
поглощение триоксида серы. (рис. 2)
Конструкция аппаратуры.
Для обжига колчедана применяются специальные печи. Наиболее эффективны печи со взвешенным («кипящим») слоем колчедана. В печах такой конструкции частицы колчедана находятся во взвешенном состоянии благодаря потоку воздуха, который подается противотоком (снизу через решетку в печи), а колчедан поступает через загрузочное отверстие в верхней части печи. (рис. 3)
Эффективность работы таких печей (1800 кг/м3 в сутки) намного выше, чем соответствующих аппаратов другой конструкции.
Обжиг пирита, получение диоксида серы. Очистка печного газа.
4FeS2 + 11O2 =2Fe2O3 + 8SO2 + Q
Измельчённый очищенный влажный (после флотации) пирит сверху засыпают в печь для обжига в "кипящем слое". Снизу (принцип противотока) пропускают воздух, обогащённый кислородом, для более полного обжига пирита. Температура в печи для обжига достигает 8000С. Пирит раскаляется до красна и находится в "подвешенном состоянии" из-за продуваемого снизу воздуха. Похоже это всё на кипящую жидкость раскалённо-красного цвета.
За счёт выделяющейся теплоты в результате реакции поддерживается температура в печи. Избыточное количество теплоты отводят: по периметру печи проходят трубы с водой, которая нагревается. Горячую воду используют дальше для центрального отопления рядом стоящих помещений.
Образовавшийся оксид железа Fe2O3 (огарок) в производстве серной кислоты не используют. Но его собирают и отправляют на металлургический комбинат, на котором из оксида железа получают металл железо и его сплавы с углеродом - сталь (2% углерода С в сплаве) и чугун (4% углерода С в сплаве). Таким образом выполняется принцип химического производства - безотходность производства.
В результате обжига пирита получается обжиговый газ, состав которого: SO2, O2, который, кроме диоксида серы, содержит кислород, азот, пары воды и другие примеси. Некоторые из этих примесей вредны для последующих процессов производства кислоты, поэтому обжиговый газ подвергают тщательной очистке от твердых частиц и влаги.
Очистка печного газа от твёрдых частичек огарка проводят в два этапа - в циклоне (используется центробежная сила, твёрдые частички огарка ударяются о стенки циклона и ссыпаются вниз) и в электрофильтрах (используется электростатическое притяжение, частицы огарка прилипают к наэлектризованным пластинам электрофильтра, при достаточном накоплении под собственной тяжестью они ссыпаются вниз). Для удаления паров воды в печном газе (осушка печного газа) используют серную концентрированную кислоту, которая является очень хорошим осушителем, поскольку поглощает воду.
Осушку печного газа проводят в сушильной башне - снизу вверх поднимается печной газ, а сверху вниз льётся концентрированная серная кислота. На выходе из сушильной башни печной газ уже не содержит ни частичек огарка, ни паров воды. Печной газ теперь представляет собой смесь оксида серы - SO2 и кислорода - О2.
3. Окисление SO2 в SO3 кислородом (получение триоксида серы).
2SO2 + O2 =2SO3 + Q
Протекает в контактном аппарате. Сложность второй стадии заключается в том, что процесс окисления одного оксида в другой является обратимым. Поэтому необходимо выбрать оптимальные условия протекания прямой
реакции (полученияSO3):
а)температура:
Прямая реакция является экзотермической (+Q), согласно правилам по смещению химического равновесия, для того, чтобы сместить равновесие реакции в сторону экзотермической реакции, температуру в системе необходимо понижать. Но, с другой стороны, при низких температурах, скорость реакции существенно падает. Экспериментальным путём химики-технологи установили, что оптимальной температурой для протекания прямой реакции с максимальным образованием SO3 является температура 400-500 °С. Это достаточно низкая температура в химических производствах. Для того чтобы увеличить скорость реакции при столь низкой температуре в реакцию вводят катализатор. Установили, что наилучшим катализатором для этого процесса является оксид ванадия(V) - V2O5.
б)давление:
Прямая реакция протекает с уменьшением объёмов газов: слева 3V газов (2VSO2 и 1VO2), а справа - 2V SO3. Раз прямая реакция протекает с
уменьшением объёмов газов, то, согласно правилам смещения химического
равновесия давление в системе нужно повышать.
Поэтому этот процесс проводят при повышенном давлении.
Прежде чем смесь SO2 и O2 попадёт в контактный аппарат, её необходимо нагреть до температуры 400-500°С. Нагрев смеси начинается в теплообменнике, который установлен перед контактным аппаратом. Смесь проходит ‑
между трубками теплообменника и нагревается от этих трубок. Внутри трубок проходит горячий SO3 из контактного аппарата. Попадая в контактный аппарат смесь SO2 и О2 продолжает нагреваться до нужной температуры, проходя между трубками в контактном аппарате.
Температура 400-500 °С в контактном аппарате поддерживается за счёт выделения теплоты в реакции превращения SO2 в SO3. Как только смесь оксида серы и кислорода достигнет слоёв катализатора, начинается процесс окисления оксида серы (IV) - SO2 в оксид серы (VI) - SO3.
Образовавшийся оксид серы SO3 выходит из контактного аппарата и через теплообменник попадает в поглотительную башню.
4. Поглощение триоксида серы. Получение H2SO4
Протекает в поглотительной башне, в которую поступает полученный оксид серы (VI).
А почему оксид серы SO3 не поглощают водой? Ведь можно было бы оксид серы растворить в воде:
SO3 + H2O =H2SO4
Но дело в том, что если для поглощения оксида серы использовать воду, образуется серная кислота в виде тумана, состоящего из мельчайших капелек серной кислоты (оксид серы растворяется в воде с выделением большого количества теплоты, серная кислота настолько разогревается, что закипает и превращается в пар). Для того, чтобы не образовывалось сернокислотного тумана, используют 98%-ную концентрированную серную кислоту. Два процента воды - это так мало, что нагревание жидкости будет слабым и неопасным. Оксид серы очень хорошо растворяется в такой кислоте, образуя олеум:
H2SO4 · nSO3.
Уравнение реакции этого процесса:
nSO3 + H2SO4 =H2SO4 · nSO3
Образовавшийся олеум сливают в металлические резервуары и отправляют на склад. Затем олеумом заполняют цистерны, формируют железнодорожные составы и отправляют потребителю.
Олеум может быть разбавлен водой до серной кислоты нужной концентрации.
5. Экологические проблемы, связанные с производством серной кислоты, и способы их решения.
Научно-техническая революция и связанный с ней интенсивный рост химического производства, вызывает существенные негативные изменения в окружающей среде. Например, отравление пресных вод, загрязнение земной атмосферы, истребление животных и птиц. В результате мир оказался в тисках экологического кризиса.
Важно подчеркнуть, что в сернокислотном производстве перерабатывают и получают такие вещества, как сероводород H2S, оксид серы (IV) SO2, оксид серы (VI) SO3, серную кислоту H2SO4. Эти вещества, присутствуя в воздухе, вредно отражаются на здоровье людей, губительно действуют на растения, разрушают постройки. Именно поэтому уделяется серьезное внимание проблеме охраны окружающей среды от загрязнения.
Можно выделить целый ряд экологических проблем, связанных с производ ством серной кислоты.
1. Связана с обжигом серного колчедана FeS2 и других сульфидных руд. При обжиге, протекающем в «кипящем слое», получающийся оксид металла, напри мер Fe2O3, выделяется в атмосферу:
4FeS2 + 11O2 = 2Fe2O3 + 8SO2
Это можно объяснить тем, что для аппаратов обжига в «кипящем слое» требует ся порошок руды, подвергшийся сильному измельчению. В результате обжига образуется оксид железа или другого металла с очень маленькими частицами. С улавливанием этих частиц фильтры могут не справиться. Частицы оксида могут попасть в атмосферу при выгрузке из печи. Попадание в атмосферу измельченных оксидов железа или других металлов называют
металлизацией атмосферы.
2. При производстве серной кислоты в атмосферу попадает много оксида серы (IV): 2SO2 + O2 = 2SO3
Это связано с тем, что производственные установки не всегда герметичны, а также с тем, что иногда автоматические системы управления не справляются с работой, что приводит к аварийным выбросам.
3. Для производства серной кислоты нередко используется сера, получаемая из сероводорода (это вещество является отходом ряда производств). Производится сера с помощью неполного окисления сероводорода. Эта технологическая схема несовершенна - около 20% серы идет на образование оксида серы (IV), который выделяется в атмосферу. В ходе производства возможны выбросы в атмосферу оксида серы (VI) и серной кислоты:
SO3+ H2O = H2SO4
4. Взаимодействуя с другими компонентами воздуха и атмосферной влагой, оксид серы (VI) образует мельчайшие частицы сульфатных солей. Вместе с капельками серной кислоты они при определенных условиях (дождях, бурях) образуют «кислотные осадки», которые губят лесные массивы, нарушают жизнедеятельность водных экосистем, вызывают серьезные нарушения здоровья животных и человека, особенно их дыхательной системы. (рис. 4)
Эти выбросы считаются аварийными, но они возможны и, к сожалению, случаются нередко.
Способы решения экологических проблем, связанных с производством серной кислоты:
1. Один из способов разрешения экологических проблем — использование технологических схем, сводящих к минимуму загрязнение атмосферы:
1) непрерывность процесса;
2) циркуляционные процессы (непрореагировавшие вещества возвращаются в сферу реакции);
3) принцип противотока (увеличивается площадь поверхности реагирующих веществ и скорость реакции);
4) комплексное использование сырья, безотходная технология;
5) выбор оптимального сырья и режима его переработки.
В мире около 80% серной кислоты производится из серы, а не из пирита FeS2. Это позволяет избежать металлизации атмосферы.
2. Еще один важный путь — это совершенствование технологического обо рудования, в частности различных фильтров и поглотителей. Большое значение имеет профилактический ремонт оборудования, а также установка современных автоматических систем управления производством.
Вредные выбросы сернокислых заводов следует оценивать не только по дейст вию содержащегося в них оксида серы (IV) на расположенные вблизи предпри ятия зоны, но и учитывать другие факторы - увеличение количества случаев рес пираторных заболеваний человека и животных, гибель растительности и подавле ние ее роста, разрушение конструкций из известняка и мрамора, повышение кор розионного износа металлов. По вине “кислотных” дождей повреждаются и памятники архитектуры.
В зоне до 300 км от источника загрязнения (SO2) опасность представляет серная кислота, в зоне до 600 км - сульфаты. Серная кислота и сульфаты замедляют рост сельскохозяйственных культур. Закисление водоемов (весной при таянии снега), вызывает гибель икры и молоди рыб. Помимо экологического ущерба налицо экономический ущерб - громадные суммы каждый год теряются при раскисление почв.
3. Рассмотрим химические методы отчистки: наиболее перспективны методы, основанные на:
- поглощение оксида серы (IV) известняком; поглощение раствором сульфита - гидросульфита аммония ; поглощение щелочным раствором алюмината натрия; интерес также представляют каталитические методы окисления оксида серы (IV) в присутствии оксида ванадия (V).
Мне кажется, что всем отходам должно быть придумано повторное применение, так как сложно представить полностью безотходное производство. Вклад химии в защиту окружающей среды может стать значительно больше, если будет изучен процесс взаимодействия человека и природы.
Наибольшей преградой на пути к безопасному использованию химических веществ является недостаточность знаний.
Этапы решения экологических проблем.
В начале важно подчеркнуть, что в сернокислотном производстве перерабатывают и получают такие вещества, как сероводород H2S, оксид серы (IV) SO2, оксид серы (VI) SO3, серную кислоту H2SO4. Эти вещества, присутствуя в воздухе, вредно отражаются на здоровье людей, губительно действуют на растения, разрушают постройки и т. п. Именно поэтому уделяется серьезное внимание проблеме охраны окружающей среды от загрязнения.
Далее можно выделить целый ряд экологических проблем, связанных с производством серной кислоты. Первая связана с обжигом серного колчедана FeS2 и других сульфидных руд. При обжиге, протекающем в «кипящем слое», получающийся оксид металла, например Fe2O3, выделяется в атмосферу:
4FeS2 + 11O2 = 2Fe2O2 + 8SO2
Это можно объяснить тем, что для аппаратов обжига в «кипящем слое» требуется порошок руды, подвергшийся сильному измельчению. В результате обжига образуется оксид железа или другого металла с очень маленькими частицами. С улавливанием этих частиц фильтры могут не справиться. Частицы оксида могут попасть в атмосферу при выгрузке из печи. Попадание в атмосферу измельченных оксидов железа или других металлов называют металлизацией атмосферы.
При производстве серной кислоты в атмосферу попадает много оксида серы:
2SO2 + O2 = 2SO3
Это связано с тем, что производственные установки не всегда герметичны, а также с тем, что иногда автоматические системы управления не справляются с работой, что приводит к аварийным выбросам. Для производства серной кислоты нередко используется сера, получаемая из сероводорода (это вещество является отходом ряда производств). Производится сера с помощью неполного окисления сероводорода. Эта технологическая схема настолько несовершенна, что около 20% серы идет на образование оксида серы, который выделяется в атмосферу.
В ходе производства возможны выбросы в атмосферу оксида серы и серной кислоты:
SO3 + Н2О = H2SO4
Эти выбросы считаются аварийными, но они возможны и, к сожалению, случаются нередко. Один из способов разрешения экологических проблем — использование технологических схем, сводящих к минимуму загрязнение атмосферы:
1) непрерывность процесса;
2) циркуляционные процессы (непрореагировавшие вещества возвращаются в сферу реакции);
3) принцип противотока (увеличивается площадь поверхности реагирующих веществ и скорость реакции);
4) комплексное использование сырья, безотходная технология;
5) выбор оптимального сырья и режима его переработки.
Так, например, в мире около 80% серной кислоты производится из серы, а не из пирита FeS2. Это позволяет избежать металлизации атмосферы.
Еще один важный путь —это совершенствование технологического оборудования, в частности различных фильтров и поглотителей. Большое значение имеет профилактический ремонт оборудования, а также установка современных автоматических систем управления производством.
Заключение.
Рассмотрение вопросов экологии, охраны природы, химической технологии, позволяет сформировать представление о роли химии в решении экологических проблем на современном этапе развития общества.
В заключении хотелось бы сказать, что в настоящее время находится широкое применение серной кислоты: в производстве минеральных удобрений, волокон, пластмасс, красителей и взрывчатых веществ; в металлургии при получении меди, никеля, урана; используется и как осушитель газов; серная кислота идет и на очистку нефтепродуктов от вредных примесей. Большое практическое применение получили и соли серной кислоты: их используют в сельском хозяйстве для борьбы с вредителями растений, в производстве красок, для пропитки древесины в качестве антисептического средства, в строительстве, медицине и других областях.
Вместе с тем рост химического производства, вызывает существенные негативные изменения в окружающей среде: отравление пресных вод, загрязнение атмосферы, истребление животных и птиц. Вредные выбросы сернокислых заводов увеличивают количества случаев респираторных заболеваний человека.
Можно сделать вывод о том, что любое производство обладает противоречивым характером: с одной стороны, это сырьё, товарная продукция, а с другой, - производственные отходы, загрязняющие природную среду. Поэтому современную химическую промышленность необходимо рассматривать как сложную социально-эколого-экономическую систему, участвующую в круговороте веществ всех оболочек Земли. Следующий вывод – что производство наносит ощутимый ущерб окружающей среде. И можно говорить о нескольких направления воздействия:
Экономический ущерб – снижение урожайности сельскохозяйственных культур в связи с выбросом загрязнителей и ускоренный износ оборудования за счёт усиления коррозии;
- Социальный ущерб – повышение заболеваемости населения и, как следствие этого, дополнительные затраты на лечение людей; Моральный ущерб – действие неблагоприятной санитарно-гигиенической обстановки на психику людей.
В данной работе рассмотрены вопросы производства серной кислоты, выделены экологические проблемы, связанные с её производством и способы их решения. Таким образом, можно сделать вывод, что цели, поставленные в начале работы выполнены. Данную работу можно использовать на уроках химии, при изучении серной кислоты.
Список литературы
1. http://*****/htnv/6-amelin-ag-yashke-ev-proizvodstvo-sernoj-kisloty;
1. ЭЛЕКТРОННЫЙ УЧЕБНИК ПО ХИМИИ_ПРОИЗВОДСТВО СЕРНОЙ КИСЛОТЫ КОНТАКТНЫМ СПОСОБОМ;
2. , , «Химия» учебник для учащихся 9 класса общеобразовательных учреждений. – М.: Вентана-Граф, 2004. – 320 с.: ил.;
3. Элективный курс. Химия и охрана окружающей среды. 10-11класс./Сост. . – Волгоград: ИТД «Корифей». – 112 с.;
4. Экологико-химический словарь-справочник, Урал-го. пед. ун-та., Екатеринбург, 1997. 66с.
Открытое занятие по теме
«Охрана среды обитания и техника безопасности при сернокислотном производстве»
ЦЕЛИ: 1. Формирование у учащихся экологических представлений и стратегий деятельности.
2. Освоение принципов взаимосвязей экологических позиций с промышленным производством.
3. Изучение воздействия выбросов сернокислотного производства
на организм человека и пути экологической коррекции.
4. Формирование моделей экологически правильного поведения.
ЗАДАЧИ:
1. Освоение представлений об экологической составляющей общественной жизни и экономики.
2. Определить проблемные точки взаимосвязи и взаимозависимости человека, его деятельности и природы.
3. Отношение к антропогенным влияниям на состояние биосферы.
4. Изучить варианты сернокислотного производства и производств, связанных с ним.
5. Презентировать учащимся материал о влиянии серной кислоты на организм человека.
6. Познакомить учащихся с путями экологической коррекции патогенных влияний производства серной кислоты.
Вид занятия: занятие по технологии развития критического мышления.
Оборудование: интерактивный комплекс, опорные схемы.
Ход занятия
Организационный момент:
За последние годы мир неузнаваемо изменился. Значительно увеличилось население, резко возросло промышленное производство, стала ощутимой нехватка различных ресурсов.
В окружающую среду выбрасывается огромное количество отходов, отравляющих воздух, воду, землю, вызывающих болезни у людей, животных и растений.
Изучив на уроках химии производство серной кислоты, мы не можем не говорить о процессах, происходящих в окружающей среде под воздействием этого производства, о влиянии этих процессов на человека, животных, растения.
Сообщается тема урока. Учащиеся записывают в тетрадь.
Введение учителя.
Человеческая деятельность в целом, так, как она формировалась до сих пор, способствует разрушению биосферы. Как остановить этот стихийный процесс? - Необходимо вооружаться экологическими знаниями.
1. Вызов: Объясните определение «экология».
После обсуждения записывается в тетрадь определение «экология (1886 год, Геккель, от греч. Oikos – жилище, Logos – наука). Эта наука о закономерностях взаимодействия человеческого общества и среды обитания, изучающая также проблемы охраны среды обитания».
Основоположником экологической теории явился Б. Коммонер. Им были разработаны законы экологии.
Обсуждение проблемы:
Законы экологии | Результаты обсуждения |
1. Все связано со всем. | 1.Воздействие какого-либо фактора нарушает взаимодействие всей экологической цепи. |
2. Все должно куда-то деваться. | 2. Все отбросы промышленной деятельности человека, попадая в окружающую среду, губительно скажутся на человеке. |
3. Природа «знает» лучше. | 3. Отбор жизнеспособных форм. Если в одном месте синтезировано одно вещество, то в другом – вещество, разрушающее первое. |
4. Ничто не дается даром. | 4.Взял – верни. К примеру, вырубка леса должна сопровождаться организацией дендрария. |
Ознакомившись с принципами экологической деятельности, возможно перейти к выяснению места человека в ноосферной общности в рамках эволюции. Представленная ниже схема объясняет влияние антропогенных и природных факторов наряду с их взаимосвязью на развитие самого человека и его интеллекта. В данной части урока обсуждаются связи «человек – природа» в «гуманистическом» и потребительском обществе
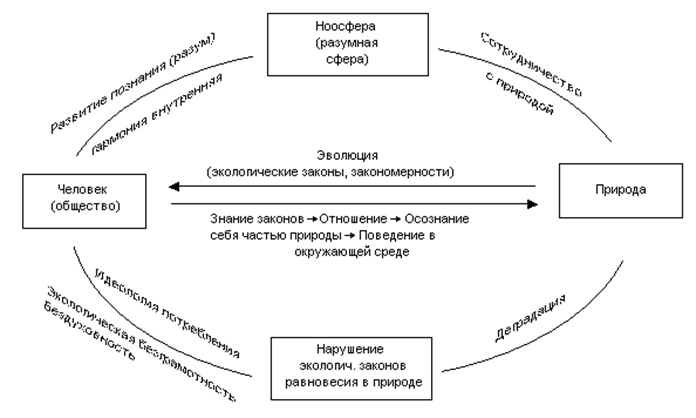
2. Второй вызов учителя: В XXI веке, в связи с интенсификацией развития человеческого интеллекта, значительно усиливается антропогенное воздействие на природу, и экология приобрела особое значение как научная основа рационального природопользования (табл. 3).
|
Происходит обсуждение с учащимися способов экологической природоохранительной деятельности.
3. В качестве примера организации экологического мониторинга и деятельности рассмотри вопросы экологической защиты на сернокислотном производстве.
Рассмотрим взаимосвязь сернокислотного производства с окружающей средой.
Учащиеся делают на доске записи предполагаемых выбросов производства и определяют точки воздействия в окружающей среде.
Выбросы сернокислотного производства
|
Комментарий учителя:
Как вы видите, образующаяся кислая среда закисляет почву, воду, выпадают кислотные дожди.
Вызов 3. Какое взаимодействие они оказывают?
Данный вопрос обсуждается после заслушивания короткого выступления ученика (1), сопровождаемого презентацией:
Кислотные дожди наносят огромный вред лесам. Леса высыхают, развивается суховершинность на больших площадях. Кислота увеличивает подвижность ионов алюминия в почвах, которые токсичны для мелких корней, что приводит к угнетению листвы и хвои, хрупкости ветвей. Чаще всего страдают пихта, ель, сосна. Снижается продуктивность почв, сокращается поступление питательных веществ. Меняется состав почвенных микроорганизмов.
Большой ущерб несут сельскохозяйственные культуры. Повреждаются покровные ткани растений, изменяется обмен веществ в клетках, нарушается рост и развитие растений, уменьшается сопротивляемость к болезням и паразитам.
Кислота разрушает сооружение из мрамора и известняка. Исторические памятники Греции, Рима, простояв тысячелетия, за последние годы разрушаются прямо на глазах. Такая же судьба грозит и Тадж-Махалу – шедевру индийской архитектуры периода Великих Монголов, в Лондоне – Тауэру и Вестминстерскому аббатству. На соборе Св. Павла слой портлендского известняка разъеден на 2,5 см. В Голландии статуи на соборе Св. Иоанна «тают как леденцы».
Конечно, страдает и здоровье людей, хотя действие кислотных дождей проявляется здесь, главным образом, косвенно. Возникает дополнительное загрязнение питьевых вод, так как кислота вытесняет из пород различные токсичные металлы – ртуть, свинец, кадмий, цинк и др. Установлена также связь кислотных дождей с повышенным уровнем содержания ртути в рыбе.
Спасать природу от закисления необходимо. Для этого придется резко снизить выбросы окислов в атмосферу, и в первую очередь, сернистого газа, так как именно серная кислота и ее соли на 70-80% обуславливают кислотность дождей, выпадающих на больших расстояниях от мест их выбросов. Выбросы сера на территории Европы превышают сейчас 30 млн т ежегодно.
Учащимся предлагается ситуация:
На расстоянии 2 км от сернокислотного завода ощущается сильный запах. Какие, на Ваш взгляд, причины имеются?
(разгерметизация оборудования, прорыв трубопровода в отдельных производствах, содержащих SO2 и H2S).
Вопрос учителя:
Какое воздействие на человека оказывают на человека выбросы сернокислого производства?
Выступление (с использованием презентации) ученика (2): (ученики делают записи условий безопасности работы – техники безопасности).
В производстве серной кислоты (Н2SO4) возможны случаи отравления сернистым газом, туманообразной серной кислотой.
Сернистый ангидрид (SO2) вызывает раздражение кожи. Слизистых оболочек носа, глаза и верхних дыхательных путей. При содержании воздухе 0,06 мг/л возможны острые отравления, сопровождающиеся отеком легких и расширением границ сердца. При отравлениях появляются головокружение, раздражение слизистых оболочек (щипание в носу, кашель). При сильных отравлениях наблюдается общая слабость. Предельно допустимая концентрация в воздухе рабочей зоны производственных помещений не должна превышать 10 мл/м куб.
Серный ангидрид(SO3) в свободном состоянии не содержится в воздухе; соединяясь с парами воды, он образует туман, состоящий из мелких капелек серной кислоты. Наличие в воздухе сернокислого тумана затрудняет дыхание. Предельная концентрация серного ангидрида и серной кислоты в воздухе рабочей зоны производственных помещений не должна превышать 1 мл/м куб.
Серная кислота (Н2SO4). Концентрированная серная кислота при попадании на кожу вызывает сильные, долга не заживающие ожоги. Ожоги на большом участке кожи очень опасны, а иногда и смертельны. Попавшую на кожу серную кислоту необходимо как можно быстрее смыть сильной струёй холодной воды, затем обожженную поверхность тела смочить 5%-м содовым раствором и смазать вазелином.
Сероводород. При больших концентрациях (выше 1 г/м) отравление происходит мгновенно, оно проявляется в судорогах и потерей сознания. В малых концентрациях сероводород действует раздражающе. ПДК – 10 мл/м куб.
Обсуждение представленного материала:
1) Специальная одежда (противогаз, перчатки, сапоги, очки)
2)Источники нейтрализации
3) Соблюдение инструктажа по технике безопасности.
Учащимся предлагается ситуация:
Человек случайно опрокинул на руку склянку с кислотой. Что необходимо сделать в первую очередь?
Варианты ответов:
1. Нейтрализовать содой – не правильно, так как образовавшийся комплекс оседает на ожоговой ране.
2. Промыть ожог большим количеством холодной воды, наложить стерильную повязку и отправить в ЛПУ – правильно.
Рефлексия
Вопрос к классу: Какие знания, полученные на уроке, Вы сможете применить в жизни? Варианты ответов:
1. Выполнение законов экологии.
2. Соблюдение техники безопасности в домашних условиях при работе с кислотными продуктами.
3. Правила оказания медицинской помощи.
Заключение учителя:
Глубокое знание законов природы, изучение взаимосвязи в биосфере и ноосфере могут стать основой хозяйственной деятельности, оптимальной для человека, общества и природы.
Экология – это не набор сведений. Это – особый взгляд на жизнь и особый образ мышления и жизни.
Используемая литература:
1. Стратегия защиты окружающей среды от загрязнений. М.: Мир, 1980.
2. , Чебан окружающей среды от химических выбросов промышленных предприятий. Кишинев, 1990.
3. , Ровинский атмосферу. М., 1987.
4. Опаловский Земля глазами химика. М.: Наука, 1990.
5. , , Третьякова и химическая технология в решении глобальных проблем. М.: Химия, 1988.
6. Гальперин основы природопользования. М.: форум-инфра-М, 2002
7. , , Экология и охрана биосферы при химическом загрязнении. М.: Высшая школа,1998
8. Будыко словарь, экономис,1995




