 Диффузия
Диффузия
простая диффузия: Простая диффузия представляет собой движение молекул незаряженного вещества по градиенту концентрации, т. е. от участков с более высоким содержанием данного вещества к участкам с более низким содержанием его.
![]() , а
, а ![]() , следовательно – общая скорость транспорта молекул будет:
, следовательно – общая скорость транспорта молекул будет: 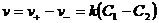 . Учтем, что k зависит от расстояния между участками 1 и 2 и запишем, что k = k0*1/∆x, где ∆x – расстояние между участками С1 и С2. Учтем также, что, чтобы перейти к потоку мы должны домножить выражение на V/S, т. е. перейти к другой размерности (если нужно – пояснить). Отсюда получим:
. Учтем, что k зависит от расстояния между участками 1 и 2 и запишем, что k = k0*1/∆x, где ∆x – расстояние между участками С1 и С2. Учтем также, что, чтобы перейти к потоку мы должны домножить выражение на V/S, т. е. перейти к другой размерности (если нужно – пояснить). Отсюда получим: 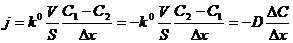 или
или 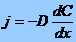 - уравнение Фика. (Первый
- уравнение Фика. (Первый
закон Фика отражает тот простой факт, что поток вещества J в направлении оси х
пропорционален движущей силе, т. е. градиенту концентрации dc/dx: J = - Ddc/dx,)
Отметим, что D – коэффициент диффузии, j – поток вещества, с размерностью D – можно найти, учитывая, что 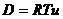 , где R и T – универсальная газовая постоянная и абсолютная температура, а u - подвижность вещества в рассматриваемой среде.
, где R и T – универсальная газовая постоянная и абсолютная температура, а u - подвижность вещества в рассматриваемой среде.
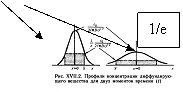 Через тонкую мембрану: . dC/dx = const =>
Через тонкую мембрану: . dC/dx = const => 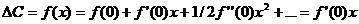 , если х – мало (или если x<h, а h – мало). =>
, если х – мало (или если x<h, а h – мало). => ![]() здесь γ – коэффициент пропорциональности между концентрацией диффундирующего вещества в растворе и внутри барьера (мембраны)=> . чтобы перейти от потоков к концентрации, нам нужно домножить выражение на S/V=S/(S* Δх)=1/Δх. =>
здесь γ – коэффициент пропорциональности между концентрацией диффундирующего вещества в растворе и внутри барьера (мембраны)=> . чтобы перейти от потоков к концентрации, нам нужно домножить выражение на S/V=S/(S* Δх)=1/Δх. => ![]() 2 закон Фика (описывает изменение концентрации растворенного вещества в зависимости от координаты х и времени. Методом подстановки можно убедиться в том, что решение дифференциального уравнения имеет вид
2 закон Фика (описывает изменение концентрации растворенного вещества в зависимости от координаты х и времени. Методом подстановки можно убедиться в том, что решение дифференциального уравнения имеет вид 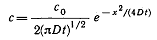 ) а для 3 мерной диффузии
) а для 3 мерной диффузии 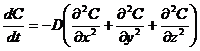
Коэффициент диффузии во многом зависит от размеров и форы молекул. Для сферических частиц используют уравнение Стокса-Эйнштейна:
![]() , где r – радиус частицы, η – вязкость среды. Если принять, что молекулярная масса частицы (М) пропорциональна объему (
, где r – радиус частицы, η – вязкость среды. Если принять, что молекулярная масса частицы (М) пропорциональна объему (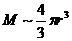 ), то при постоянной температуре и вязкости, D~M-1/3. Т. е.
), то при постоянной температуре и вязкости, D~M-1/3. Т. е. ![]() или
или ![]() . Последняя формула может быть использована для анализа зависимости lgD от lgM.
. Последняя формула может быть использована для анализа зависимости lgD от lgM.
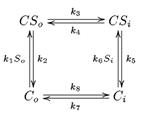
Облегченная диффузия:
![]()
![]() где Jmax – максимальная скорость переноса.
где Jmax – максимальная скорость переноса.
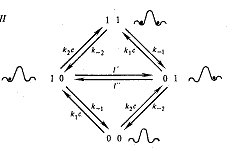
Ионный канал:
Ионная пора: белки фил, фоб группы. Селективный фильтр: специфический транспорт: по заряду //максикатионные каналы; по размеру. Воротный механизм; Сенсор; а) потенциало-чувствительный б) лигандо зависимым в) механочувствителный.
![]() где F(l 0) и F{0 1) — вероятности состояний 1 0 и 0 1 соответственно, а l’ u l’’— потенциалзависимые константы скорости перехода ионов через центральный барьер:
где F(l 0) и F{0 1) — вероятности состояний 1 0 и 0 1 соответственно, а l’ u l’’— потенциалзависимые константы скорости перехода ионов через центральный барьер:
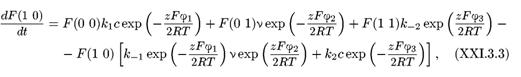
![]()
![]()
![]()
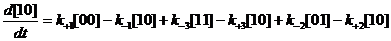
![]()
![]()
![]()
![]()
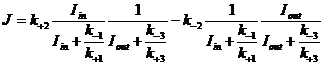
где I – концентрация ионов, а 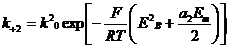 и
и 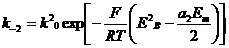 - потенциал-зависиые константы.
- потенциал-зависиые константы.
//Na u K канал для создания ПД.
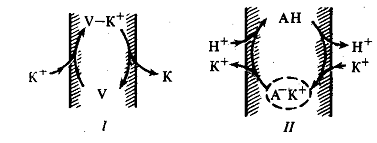
Транспорт ионов через неканальные системы пассивного транспорта
1 ) валиномицин (имеет полость = К 2) негирицин. (СООН – СОО + Н - перенос)
Пассивный транспотр ионов:
1фактор) Движущей силой для транспорта ионов является электрохимический потенциал: ![]() , где μ – химический потенциал, μ0 – стандартный химический потенциал, С – концентрация иона, z – заряд иона, F – постоянная Фарадея, φ – электрический потенциал.
, где μ – химический потенциал, μ0 – стандартный химический потенциал, С – концентрация иона, z – заряд иона, F – постоянная Фарадея, φ – электрический потенциал.
Электрохимический потенциал – мера работы, необходимой для переноса 1 моля ионов из раствора с данной концентрацией и данным электрическим потенциалом в бесконечно удаленную точку в вакууме. Эта работа складывается из затрат на преодоление сил химического взаимодействия (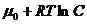 ) и работы по переносу зарядов в электрическом поле (
) и работы по переносу зарядов в электрическом поле (![]() ). Иногда работу по переносу ионов относят не к молю, а к одному иону. 2фактор) гидратация: . Эмпирически эффективный радиус гидратированного иона
). Иногда работу по переносу ионов относят не к молю, а к одному иону. 2фактор) гидратация: . Эмпирически эффективный радиус гидратированного иона ![]() форулы Стокса-Эйнштейна.
форулы Стокса-Эйнштейна.
две водные фазы, разделенные мембраной. 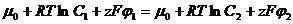 или
или 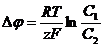 , такая разность потенциалов называется равновесным потенциалом или потенциалом Нернста, и С1 и С2 здесь – концентрации ионов с каждой из сторон мембраны в равновесии.
, такая разность потенциалов называется равновесным потенциалом или потенциалом Нернста, и С1 и С2 здесь – концентрации ионов с каждой из сторон мембраны в равновесии.
Доннановский потенциал: Он возникает в тех случаях, когда имеется фиксированный заряд, однако расположенный не на мембране, а в некотором объеме. В этом случае заряженные ионы будут поступать в фазу с фиксированными зарядами или уходить из нее, пока не потенциал, связанный с наличием фиксированных зарядов не будет уравновешен электрохимическим градиентом, связанным с транспортом ионов (Доннановское равновесие).
Пусть в системе из двух водных фаз растворен бинарный электролит А+В~. Предположим, что одна из фаз несет фиксированные положительные заряды и что значения стандартных химических потенциалов для обеих фаз одинаковы.
![]() =>
=> ![]() =>
=> ![]() =>
=> ![]() =>
=> ![]() =>
=>![]() =>
=> ![]() плотность фиксированных зарядов мала (Q << с), концен -
плотность фиксированных зарядов мала (Q << с), концен -
трации свободных катионов и анионов в заряженной фазе равны ![]() =>
=> ![]() или после разложения
или после разложения ![]() по формуле
по формуле 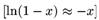
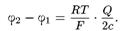
когда объемная плотность фиксированных зарядов велика по сравнению с концентрацией электролита во внешней среде (Q > с), получаем из уравнения 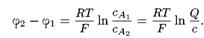
фиксированных поверхностных зарядов клеточных мембран приводит к образованию около мембраны двойного электрического слоя, который является важным фактором в протекании многих биоэлектрохимических процессов.
величину σ – плотность заряда на мембране, можно получить уравнение Гуи-Чэпмена:
![]()
Электродиффузия
Основное отличие электродиффузии от обычной диффузии – это учет влияния электрического потенциала на диффузионный процесс
подходе Гольдмана, развитым Ходжкиным и Катцем. Приняв это допущение, мы получаем для потока:
![]() , где hррррррр=Δx – например, толщина мембраны. Если принять, что J=const, т. е. что достигнуто стационарное распределение ионов в мембране, то можно получить:
, где hррррррр=Δx – например, толщина мембраны. Если принять, что J=const, т. е. что достигнуто стационарное распределение ионов в мембране, то можно получить:
![]()
Решая поучившееся уравнение, можно найти:
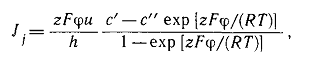
где c’ и c’’ – концентрации ионов в мембране с внешней и внутренней сторон. Удобно перейти от концентраций ионов в мембране, к их концентрациям в водной фазе, учитывая, что c’’=γcin, c’=γcout.
В этом случае мы можем перейти к уравнению Гольдмана-Хаджкина-Катца:

в котором P=uTγ/h – проницаемость мембраны для данного иона.
//Ʃ (Na, K,Cl) => ![]()
Усилка-Теорелла. Так если в уравнении Гольдмана-Ходжкина-Катца выделить два потока – наружу (jо) и внутрь (ji), то можно записать:
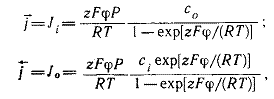
Как видно из приведенных уравнений, входящий поток линейно зависит от концентраций иона в наружном растворе и не зависит от концентрации во внутренней среде. В свою очередь, выходящий поток зависит только от концентрации во внутреннем растворе. Это и означает, что входящий и выходящий потоки в приближении постоянного поля являются независимыми.
Отношение таких потоков будет:
![]()
Выполнение уравнения Уссинга — Теорелла является критерием пассивного транспорта, при котором поток иона обусловлен только градиентом концентраций и действием электрического поля. Отклонение от такого равенства может указывать на участие системы активного транспорта в переносе ионов через мембрану или быть следствием нарушения независимости ионных потоков, например при диффузии через узкие каналы в мембране. В этом случае обычное электродиффузионное описание; основанное на представлении о диффузии точечных невзаимодействующих частиц, теряет силу.
Кинетика ферментативных процессов
Рассмотрим простейшую схему ферментативной реакции:
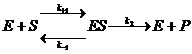
Здесь S – субстрат, Р – продукт, Е – фермент, ES – фермент-субстратный комплекс.
![]()
![]()
![]()
![]()
Сложим 2и3 уравнение Учтем, что [E]+[ES]=const=[E0], [S]+[P]=const=[S0]; d[E]/dt=d[ES]/dt и перейдем к системе из 2-х уравнений:
![]()
![]()
Замены переменных введем безразмерные величины:
![]() ,
, ![]() ,
, 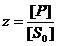 ,
, 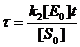 ,
, 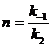 ,
, 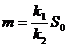
Разделив правую и левую части второго уравнения на величину ki[So]/k2 = m, получим: ![]() ;
; ![]()
=> ![]() , где
, где ![]() - константа Михаэлиса.
- константа Михаэлиса.
мы можем перейти от дифференциального равнения для х, к алгебраическому:
![]()
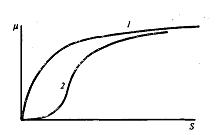
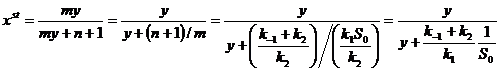
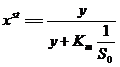
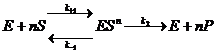 =>
=> 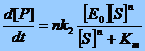
изолированные системы, которые не обмениваются с внешней средой ни энергией, ни массой, они полностью изолированы от влияния окружающей среды. Например – сосуд Дьюара.
закрытые системы, которые через свои границы обмениваются энергией с окружающей средой, но не могут обмениваться массой (веществом). Например – запаянная колба.
открытые системы, которые обмениваются с окружающей средой и энергией, и массой. К ним относятся, в частности, все живые организмы.
Равновесные, или обратимые, процессы протекают в системе таким образом, что вызванные ими изменения в состоянии системы могут произойти в обратной последовательности без дополнительных изменений в окружающей среде. Наоборот, неравновесные, или необратимые, процессы, к которым относятся реальные превращения в природе, не обладают этими свойствами, и их протекание в обратном направлении сопровождается остаточными изменениями в окружающей среде.
1-й закон термодинамики
который устанавливает общие закономерности взаимопревращения тепла и работы при изменении состояния системы и фактически эквивалентен закону сохранения энергии в применении к процессам преобразования теплоты.
![]() ,
,
где Q – количество теплоты, поступившее в систему, А – работа, совершенная системой над внешней средой и U – внутренняя энергия системы
В целом, приведенная запись первого закона термодинамики означает что теплота, поглощенная системой идет на увеличение внутренней энергии системы и на совершение работы против внешних сил.
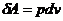 => p=const;
=> p=const; ![]() ; Энтальпия зависит только от U, p и v,
; Энтальпия зависит только от U, p и v, ![]() (p или v = const) закона Гесса, который гласит: тепловой эффект химической реакции не зависит от пути перехода от исходных веществ к конечным продуктам реакции, а определяется лишь разностью теплосодержания конечных и исходных продуктов.
(p или v = const) закона Гесса, который гласит: тепловой эффект химической реакции не зависит от пути перехода от исходных веществ к конечным продуктам реакции, а определяется лишь разностью теплосодержания конечных и исходных продуктов.
2-й закон термодинамики
Определяет направление распределения (протекания) энергии.
энтропии (S), которое определяется суммарной величиной поглощенных системой приведенных теплот Q/T. ![]() В том случае, когда система не совершает обмена с окружающей средой и δQ = 0, т. е. – в изолированной системе, становится верна формула
В том случае, когда система не совершает обмена с окружающей средой и δQ = 0, т. е. – в изолированной системе, становится верна формула ![]()
Отсюда второй закон термодинамики можно сформулировать следующим образом: в изолированных системах энтропия будет оставаться постоянной при равновесных процессах и будет возрастать при неравновесных.
1. 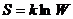 Закон возрастания энтропии (Н-теорема Больцмана).
Закон возрастания энтропии (Н-теорема Больцмана).
Энергия гемгольца и энергия Гиббса: ![]() ,=>
,=> ![]() ; 1yc). v, T = const, тогда соответственно
; 1yc). v, T = const, тогда соответственно 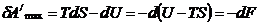 где F = U + TS– функция состояния, которая называется свободной энергией или энергией Гельмгольца. 2yc) 2. p, T = const, тогда соответственно
где F = U + TS– функция состояния, которая называется свободной энергией или энергией Гельмгольца. 2yc) 2. p, T = const, тогда соответственно ![]()
где G = U + pV – TS – функция состояния, которая называется термодинамическим потенциалом или энергией Гиббса.
F(v, T); G(p, T), если система = const;
Система не постоянная => + различные компоненты (n) F = F(v, T, n1, n2, … , nN), а G = G(p, T, n1, n2, … , nN).
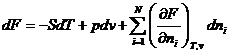 ;
; 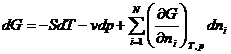
Химический потенциал описывается следующей формулой:
![]() ,
,
где сi – концентрация вещества, а μ0i – константа, зависящая от природы вещества и температуры.
Для условий равновесия:
![]() биохимические реакции протекают при p, V,T =const => F=G
биохимические реакции протекают при p, V,T =const => F=G
При анализе энергетики реакций обычно используют так называемую стандартную величину изменения термодинамического потенциала:
![]()
которая соответствует изменению энергии в условиях, когда концентрации всех реагентов равны 1, а температура равна 250С. vi – здесь стереометрический коэффициент вещества i, μi0 – его стандартный химический потенциал, K(T) – константа равновесия, описываемой реакции, которая зависит от температуры.
Отсюда можно получить формулу, описывающую изменение термодинамического потенциала в произвольной химической реакции:
![]()
Второй закон термодинамики в открытых системах^;
Допущение: 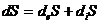
где dS – общее изменение энтропии, diS – изменение энтропии, связанное с внутренним процессами в системе, diS = 0 (для обратимых процессов) и diS > 0 (для необратимых), deS – это изменение энтропии, связанное с обменом энергии и вещества между системой и средой. В том случае, когда этот обмен отсутствует deS=0, => ![]() , (
, (![]() )>=0; (
)>=0; (![]() )><0;
)><0; ![]() , т. е. скорость возникновения энтропии внутри системы равно скорости изменения общей энтропии системы плюс – скорость оттока обмена энтропией с окружающей средой.
, т. е. скорость возникновения энтропии внутри системы равно скорости изменения общей энтропии системы плюс – скорость оттока обмена энтропией с окружающей средой.
Связь изменения энтропии, с протекающими в ней необратимыми процессами
Рассмотрим систему, в которой протекают необратимые химические реакции и которая находиться в частично-равновесном состоянии, а именно – в тепловом равновесии со средой.
![]() ;+
;+![]() =>
=> ![]() ;+
;+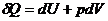 => =>
=> =>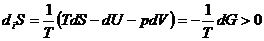 , что возрастание энтропии, связанное с протеканием необратимых процессов в системе пропорционально снижению ее свободной энергии. допущениями необратимыми в системе являлись только химические реакции, то можно записать следующее выражение:
, что возрастание энтропии, связанное с протеканием необратимых процессов в системе пропорционально снижению ее свободной энергии. допущениями необратимыми в системе являлись только химические реакции, то можно записать следующее выражение:
![]() где V – скорость реакции, A – химическое сродство или движущая сила химической реакции, которая описывается формулой
где V – скорость реакции, A – химическое сродство или движущая сила химической реакции, которая описывается формулой ![]() , где химический потенциал,
, где химический потенциал, ![]() Таким образом, производство энтропии в химической реакции пропорционально скорости реакции и ее химическому сродству.
Таким образом, производство энтропии в химической реакции пропорционально скорости реакции и ее химическому сродству.
Если в системе одновременно протекает несколько реакции, то можно записать: ![]()
Термодинамическое сопряжение процессов
Допустим, у нас в системе протекает две реакции с A1, V1 и A2, V2![]() или
или ![]() ;
; ![]()
реакция протекает с поглощением энергии – сопряженная реакция, а вторая – с выделением – сопрягающая реакция,![]()
диссипативная функция: ![]() где Х – некие обобщенные силы, а J – обобщенные потоки, вызванные действием этих сил.
где Х – некие обобщенные силы, а J – обобщенные потоки, вызванные действием этих сил. ![]()
Соотношения Онзагера
Рассмотрим случай, когда в системе имеется только одна сила и один поток. ![]() => J = J(X) в ряд Тейлора=>
=> J = J(X) в ряд Тейлора=> 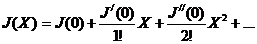 =>
=> 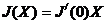 или
или 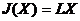 , где
, где 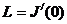 – постоянная величина.
– постоянная величина.
// закон Ома, где величина потока электричества (I) пропорциональна движущей силе — разности потенциалов (U), a ![]() – линейный коэффициент пропорциональности. То есть можно записать, что
– линейный коэффициент пропорциональности. То есть можно записать, что 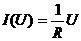 .
.
Рассмотрим случай, для двух взаимодействующих процессов потоками (J1 и J2) и силами (X1 и X2) => ![]() ;
;![]() - где L21 и L22 соответствуют возможной взаимосвязи двух потоков и носят название коэффициентов взаимности Онзагера. (
- где L21 и L22 соответствуют возможной взаимосвязи двух потоков и носят название коэффициентов взаимности Онзагера. (![]() ) => диссипативный вид:
) => диссипативный вид: ![]() ; а для 2 (
; а для 2 (![]() );
);![]() (см↑) Это так называемое соотношение взаимности Онзагера, которое показывает, что если поток j-того необратимого процесса испытывает влияние сродства Хk необратимого k-того процесса через посредство коэффициента Ljk, то и поток процесса k также испытывает влияние сродства Xj через посредство того же самого коэффициента Lkj = Ljk.
(см↑) Это так называемое соотношение взаимности Онзагера, которое показывает, что если поток j-того необратимого процесса испытывает влияние сродства Хk необратимого k-того процесса через посредство коэффициента Ljk, то и поток процесса k также испытывает влияние сродства Xj через посредство того же самого коэффициента Lkj = Ljk.
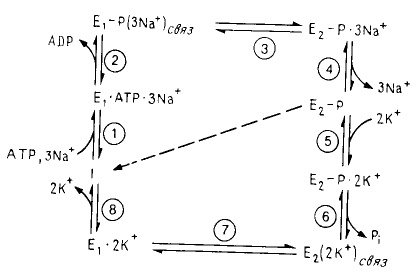
Активный транспорт:
1)Первичный активный транспорт// Na-К-АТФаза; , Са-АТФазы, Н-АТФаза
// Е1Е2 – АТФазы мат модель см ионные каналы.
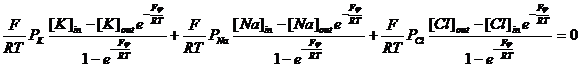
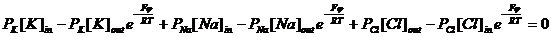
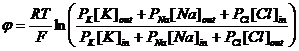
Поток через такую систему может быть задан как
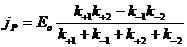
где k определяют тип АТФазы.
Для Н-АТФазы плазматической мембраны растений будут следующими:
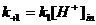 ;
; 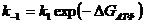 ;
;
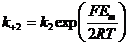 ;
; 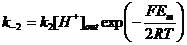
2 ый активный транспорт: систему транспорта сахарозы внутрь ситовидных трубок, которая работает за счет энергии электрохимического градиента протонов.
Потенциал покоя (диффуционная состовляющая ПП)
![]() или
или ![]() потенциалом Нернста
потенциалом Нернста
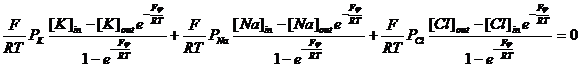
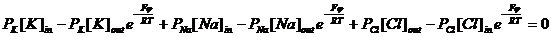
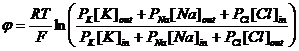 Гольдмана-Ходжкина-Катца для ионов каля, натрия и хлора:
Гольдмана-Ходжкина-Катца для ионов каля, натрия и хлора:
Эквивалентная схема ПП: K;Na;Cl ввести сопротивление, емкость, ЭДС. В этом случае, токи через каждый из элементов могут быть описаны как 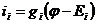 , где gi и Ei – проводимость и равновесный потенциал для иона i. Если учесть, что в стационарном состоянии сумма всех токов равна 0, то можно найти φ. Для калия, натрия и хлора это будет:
, где gi и Ei – проводимость и равновесный потенциал для иона i. Если учесть, что в стационарном состоянии сумма всех токов равна 0, то можно найти φ. Для калия, натрия и хлора это будет:
![]()
Для Н-АТФазы: Более прост для использования подход с описанием эквивалентных схем. В этом случае, в эквивалентную схему просто «вписывается» ЭДС, соответствующая активности АТФазы (РИС). Соответственно, для растений с Н-АТФазой общий вид уравнения принимает вид: 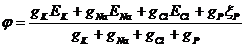 , где gP и ξР – собственная проводимость и ЭДС Н-АТФазы. Для расчета ЭДС можно использовать формулу
, где gP и ξР – собственная проводимость и ЭДС Н-АТФазы. Для расчета ЭДС можно использовать формулу 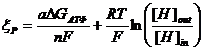 , где ΔGАТФ – энергия выделяющаяся при гидролизе 1 моля АТФ, а – КПД Н-АТФазы, т. е. доля энергии АТФ, идущая на перенос протонов, n - количество молекул протонов, переносимых при гидролизе 1 АТФ. Если принять, что а=1, n=1, рНin = 7 и рНout = 6, то ξР = -0.45 В.
, где ΔGАТФ – энергия выделяющаяся при гидролизе 1 моля АТФ, а – КПД Н-АТФазы, т. е. доля энергии АТФ, идущая на перенос протонов, n - количество молекул протонов, переносимых при гидролизе 1 АТФ. Если принять, что а=1, n=1, рНin = 7 и рНout = 6, то ξР = -0.45 В.

ПД Ходжкиным и Хаксли математическая модель генерации импульса.
В соответствие с ней, динамика потенциала на мембране определяется токами через нее, причем каждый из токов, зависит от состояния каналов:
![]()
где I – ток, действующий на мембрану, gNamax – максимальная проводимость для Na-каналов, gKmax – максимальная проводимость для К-каналов. m, h и n – это переменные, характеризующие состояние так называемых воротных частиц, которые модулируют проводимость натриевых и калиевых каналов.
n – это вероятность нахождения активационной частицы для калиевого канала в таком состоянии, которое способствует открытию канала.
![]() где αn и βn константы скорости для перехода в открытое и закрытое состояние канала =>
где αn и βn константы скорости для перехода в открытое и закрытое состояние канала => ![]() =>
=> 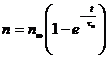
![]() =>
=> ![]() =>
=>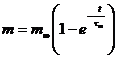
![]() =>
=> ![]() =>
=> ![]()
Зависимость величины вдоль волокна от расстояния вдоль нервного волокна может быть описано уравнением ![]() , где λ – кабельная постоянная:
, где λ – кабельная постоянная: 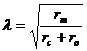 , где rm – это сопротивление мембраны, ro – сопротивление среды и rc –сопротивление цитоплазмы нервной клетки.
, где rm – это сопротивление мембраны, ro – сопротивление среды и rc –сопротивление цитоплазмы нервной клетки.
Для описания динамики потенциала, с произвольной зависимостью потенциала от времени можно использовать уравнение:
![]()
При решении полученного уравнения в общем виде, можно найти величину скорости ПД: ![]() , где Δφ – амплитуда ПД, dφ/dt – скорость изменения потенциала во время ПД.
, где Δφ – амплитуда ПД, dφ/dt – скорость изменения потенциала во время ПД.
Аналитическое решение:
// рост популяции бактерий в не лимитированных условиях.
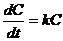 , где С-концентрация бактерий (или их количество), k - константа скорости, отражающая их деление. =>
, где С-концентрация бактерий (или их количество), k - константа скорости, отражающая их деление. =>![]() , где С0 – начальная концентрация бактерий
, где С0 – начальная концентрация бактерий
//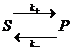 :
: 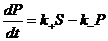 , где k+ - константа скорости прямой реакции, а k - - константа скорости обратной. Если учесть, что S+P=const=S0 – начальная концентрация субстрата, то можно записать уравнение как
, где k+ - константа скорости прямой реакции, а k - - константа скорости обратной. Если учесть, что S+P=const=S0 – начальная концентрация субстрата, то можно записать уравнение как ![]() . Решение этого уравнения (методом разделения переменных) имеет вид:
. Решение этого уравнения (методом разделения переменных) имеет вид: ![]()
//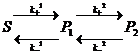 ; где k1>>k2 =>
; где k1>>k2 =>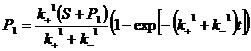 , (
, (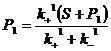 ;
;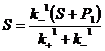 );для описания медленной реакции мы можем ввести новую переменную Х= S+Р1 и записать уравнение в виде:
);для описания медленной реакции мы можем ввести новую переменную Х= S+Р1 и записать уравнение в виде: 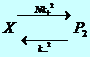 , где N – это доля Х способных к превращению в Р2 , т. е. NХ=Р1, отсюда
, где N – это доля Х способных к превращению в Р2 , т. е. NХ=Р1, отсюда 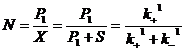 . =>
. => 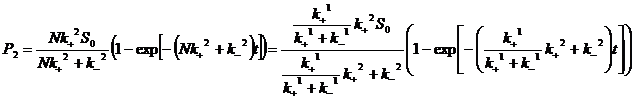
Качественное исследование кинетических систем
а достаточно найти стационарный состояния системы, оценить их устойчивость и определить каким путем происходит приближение системы к такому состоянию или ее удаление от него.
появление в системе нескольких стационарных состояний при изменении ее параметров называется бифуркацией, а значение параметра при котором происходит бифуркация – бифуркационное.
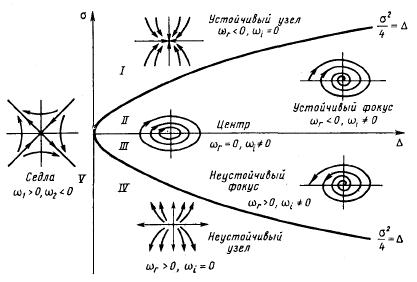
В качестве примера проведем качественный анализ модели Лотке-Волтерра – «хищник-жертва». Ее можно задать системой уравнений
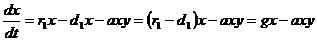
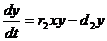
Здесь r – скорость размножения, причем для хищников (у) она зависит не только от числа особей данного вида, но и от количества пищи – жертв, d – коэффициент смертности (он пропорционален количеству особей), a - константа отражающая вероятность поедания хищником жертвы при встрече, g=r1-d1 – вводиться для упрощения системы и, по сути, отражает скорость прироста количества жертв.
Найдем стационарные значения х и у:
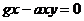 ,
, 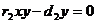 -
-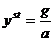 ,
, 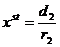 и
и ![]() ,
, ![]() , второй вариант нам не интересен, так как соответствует полному отсутствию и хищников, и жертв.
, второй вариант нам не интересен, так как соответствует полному отсутствию и хищников, и жертв.
Найдем а:
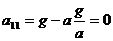 ,
, 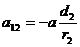 ,
, 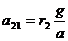 ,
, 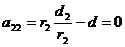
Отсюда:
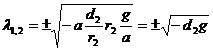
методе Эйлера. (численный метод) Опишем его.
Допустим нам известно значение функции y=f(t0), для того чтобы найти значение у=f(t0+Δt) мы можем разложить ее в ряд Тэйлора:
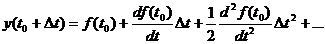
Если Δt достаточно мало, то в полученном выражении можно пренебречь членами со степенью выше 1, т. е.:
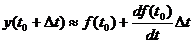
Таким образом, зная y(t0) и вид первую производную f(t) по времени, мы можем найти значение y(t=t0+Δt), если Δt достаточно мало. Однако ничего не мешает повторить эту процедур вновь, используя вместо y(t0) - y(t0+Δt). Отсюда повторяя подобную операцию, мы можем получить – численно - зависимость y от t. Причем подобная операция применима и для системы уравнений.
Преимуществом численного метода является его универсальность – он применим практически для всех моделей. Недостатками – ресурсоемкость и невозможность получить общую картину поведения системы: численные решения всегда реализуются лишь для определенных значений параметров.
Качественный анализ (примеры)
//1 уравнение: динамику количества клеток в проточном культиваторе:
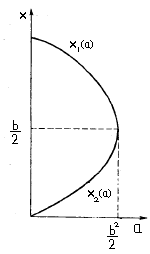
![]() , где x – концентрация клеток, а – скорость их притока, b и c – коэффициенты их гибели и размножения, соответственно. При этом учтем, что a, b, c > 0, также примем, что c = 1.=>
, где x – концентрация клеток, а – скорость их притока, b и c – коэффициенты их гибели и размножения, соответственно. При этом учтем, что a, b, c > 0, также примем, что c = 1.=> 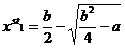 ,
, 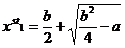 => При b2/4 = a – система имеет одно стационарное состояние, а при b2/4 > a – два.
=> При b2/4 = a – система имеет одно стационарное состояние, а при b2/4 > a – два.
// 2 уравнениями: Рассмотрим в качестве примера систему из 2-х уравнений:
![]() ;
; ![]() => Так если координаты особой точки данной ранее системы уравнений равняются xst и yst, то зададим малые смещения x и y из этой точки: ξ = xst – x и η = yst – y, причем | ξ / xst|<<1 и | η / yst| << 1. Если подставить в исходную систему уравнений вместо x и y – xst + ξ и yst + η, после чего разложить ее в ряд Тэйлора, отбросить нелинейные члены и принять P(xst, yst) = Q(xst, yst) = 0, то мы получим систему линенейных дифференциальных уравнений:
=> Так если координаты особой точки данной ранее системы уравнений равняются xst и yst, то зададим малые смещения x и y из этой точки: ξ = xst – x и η = yst – y, причем | ξ / xst|<<1 и | η / yst| << 1. Если подставить в исходную систему уравнений вместо x и y – xst + ξ и yst + η, после чего разложить ее в ряд Тэйлора, отбросить нелинейные члены и принять P(xst, yst) = Q(xst, yst) = 0, то мы получим систему линенейных дифференциальных уравнений:
![]() ;
; ![]() => Обозначим постоянные коэффициенты как a11, a12, a21, a22 => Примем, что аналитический общий вид решения будет
=> Обозначим постоянные коэффициенты как a11, a12, a21, a22 => Примем, что аналитический общий вид решения будет ![]() , а
, а ![]() , =>
, => ![]() ;
;![]() ;Или2;
;Или2;![]() ;
;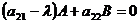 =>
=> 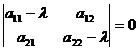
или – раскрыв определитель – 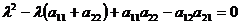
Отсюда:
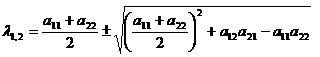
На основании этого мы можем записать уравнения для ξ и η:
![]()
1. λ1 > 0, λ1 > 0 – в этом особая точка будет представлять собой неустойчивый узел 2. λ1 < 0, λ2 < 0 – в этом особая точка будет представлять собой устойчивый узел 3. λ1 < 0, λ2 > 0 или наоборот – в этом особая точка будет неустойчивой – седло, однако в этом случае будут как траектории входящие в эту точку так и выходящие из нее
Системы с распределенными в пространстве параметрами
Системы, которые учитывают пространственный фактор, называются системами с распределенными в пространстве параметрами. Для одномерной системы такого типа, описывающие ее уравнения будут выглядеть как:
![]()
где i = 1, …, N, Q(r) – функция определяющая зависимость переменной (например – концентрации) от пространственной координаты. Полное решение такой системы будет выглядеть как xi = xi (t, r). В том случае, когда пространственное распределение задается диффузией, уравнения для х будут выглядеть:
![]()
Для анализа таких уравнений необходимо знать начальные условия - функцию x(r) при t = 0, и возможно – граничные условия. Такая система с распределенными параметрами может быть сведена к точечной при выполнении одного из 3-х условий (1) D = 0, что во многих случаях не имеет физического смысла, (2) D очень велико по сравнению со скоростями реакций – в этом случае равномерно частицы перемешиваются по всему реакционному объему и (3) все внешние и начальные условия абсолютно идентичны.
Брюсселятор это такая система, в которой протекает следующая совокпность химических реакций:
Его точечная модель выглядит следующим образом:
A → x; 2x + y → 3x ; B + x → y + D; x → E
Учитывая диффузию метаболитов в одномерном пространстве, система уравнений для брюсселятора:
![]() ;
; ![]()
![]()
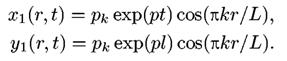
диссипативные структуры, т. е. неравномерное периодическое распределение концентрации реагентов вдоль брюсселятора
Биологические триггеры
 Система, обладающая двумя или несколькими устойчивыми стационарными состояниями, между которыми возможны переходы, называется триггерной.
Система, обладающая двумя или несколькими устойчивыми стационарными состояниями, между которыми возможны переходы, называется триггерной.
Теорема Пригожина
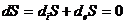 , рассмотрим случай двух необратимых процессов. Тогда приращение энтропии, отнесенное к единице времени, запишется в виде
, рассмотрим случай двух необратимых процессов. Тогда приращение энтропии, отнесенное к единице времени, запишется в виде ![]() , а феноменологические уравнения будут, соответственно:
, а феноменологические уравнения будут, соответственно:
![]() ;
;![]() => где L12 = L21 Пусть Ji = 0 =>
=> где L12 = L21 Пусть Ji = 0 =>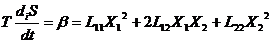 =>
=>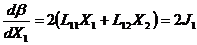
Отсюда следует, что при J1 = 0, 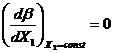 , то есть оба этих выражения эквивалентны в области линейной термодинамики, где применимы линейные соотношения. Отсюда условие
, то есть оба этих выражения эквивалентны в области линейной термодинамики, где применимы линейные соотношения. Отсюда условие 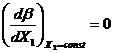 отражает минимальное значение функции
отражает минимальное значение функции ![]() . Аналогичные условия можно получить и для другого потока: J2 = 0,
. Аналогичные условия можно получить и для другого потока: J2 = 0,  Отсюда следует, что в случае двух процессов стационарное состояние соответствует минимальному β, т. е. минимуму производства энтропии.
Отсюда следует, что в случае двух процессов стационарное состояние соответствует минимальному β, т. е. минимуму производства энтропии.
если в системе протекает n процессов 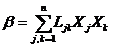 Допустим, что силы Х1, Х2,..., Xk — фиксированы, a Xk+1, Xk+2,..., Хn – варьируют так, что соответствующие им процессы переходят в стационарное состояние, где Jk+1 = Jk+2 = ... = Jn = 0 , тогда для стационарного состояния получим выражение:
Допустим, что силы Х1, Х2,..., Xk — фиксированы, a Xk+1, Xk+2,..., Хn – варьируют так, что соответствующие им процессы переходят в стационарное состояние, где Jk+1 = Jk+2 = ... = Jn = 0 , тогда для стационарного состояния получим выражение:
![]() ,
, ![]()
//Рассмотрим в качестве примера открытую химическую систему:
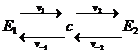 скоростями u1 = v1 – v-1 и u2 = v2 – v-2;
скоростями u1 = v1 – v-1 и u2 = v2 – v-2; ![]() Суммарное сродство реакции А – будет равно
Суммарное сродство реакции А – будет равно 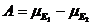 . В стационарном состоянии J = 0, а значит
. В стационарном состоянии J = 0, а значит ![]() . Из этого следует
. Из этого следует ![]() .
.
Вблизи равновесия А близко к нулю, а J = LA. Отсюда величина диссипативной функции ![]() . Условием минимума данной функции будет равенство ее первой производной по химическому сродству нулю, то есть
. Условием минимума данной функции будет равенство ее первой производной по химическому сродству нулю, то есть ![]() . Как мы уже вдели, это условие соответствует стационарному состоянию системы, когда u1 = u2. Следовательно, условие стационарности процесса оказывается эквивалентным условию минимума прироста энтропии. Т. е. это и является теоремой Пригожина о минимуме прироста энтропии в стационарном состоянии.
. Как мы уже вдели, это условие соответствует стационарному состоянию системы, когда u1 = u2. Следовательно, условие стационарности процесса оказывается эквивалентным условию минимума прироста энтропии. Т. е. это и является теоремой Пригожина о минимуме прироста энтропии в стационарном состоянии.



