Федеральное агентство по образованию
ГОУ ВПО
Тюменский государственный архитектурно-строительный университет
Кафедра Общей и специальной химии
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
к лабораторной работе по теме:
«ИОННЫЙ ОБМЕН»
для студентов специальности «Охрана окружающей среды
и рациональное использование природных ресурсов»
по курсу «КОЛЛОИДНАЯ ХИМИЯ »
Тюмень -2007
Ионный обмен: ст. преподаватель , методическое указание к лабораторной работе для студентов специальности ООС, дневное отделение, 2 курс, 4 семестр по курсу «Коллоидная химия». Тюмень: ТюмГАСУ, 2007г.
Рецензент: доцент, к. х.н.
(степень, звание, Фамилия, Имя, Отчество)
Учебно-методический материал утвержден на заседании кафедры общей и специальной химии,
протокол № от « » 2007г.
Учебно-методический материал утвержден УМС академии:
протокол № от « » 2007г.
Тираж экземпляров.
Введение
Данное методическое пособие предназначено для студентов специальности “Охрана окружающей среды и рациональное использование природных ресурсов”.
Ионный обмен широко применяется в технологических процессах и для аналитических целей. С помощью ионитов проводится очистка растворов от вредных и нежелательных примесей, концентрирование, извлечение веществ.
В методическом указании даны общие представления о ионитах. В ходе выполнения лабораторной работы студенты знакомятся с динамическим методом проведения сорбционных процессов, определяют ДОЕ ионита.
Правила техники безопасности.
1. Во время работы в лаборатории необходимо соблюдать тишину, порядок и правила безопасности.
2. Категорически воспрещается курить, пить воду, принимать пищу.
3. Нельзя приступать к выполнению опыта, пока не усвоена методика и не приготовлены все компоненты, необходимые для этого.
4. Опыты проводить только в чистой посуде. После проведения опытов всю использованную посуду чисто помыть.
5. При работе с кислотами, щелочами надо помнить, что это едкие, агрессивные вещества. Нужно следить, чтоб они не попадали на кожу рук, лица, одежду, т. к. возможен, химический ожег. При попадании вещества на кожу необходимо промыть пораженный участок большим количеством воды и обратится за помощью к преподавателю или лаборанту.
6. При отборе проб нельзя набирать растворы ртом, нужно пользоваться специальной грушей.
7. Необходимо соблюдать аккуратность и осторожность при работе со стеклянной посудой.
Теоретическая часть.
иониты
Некоторые сорбенты могут обменивать свои ионы на ионы раствора, в этом случае происходит обменная сорбция.
Материалы, способные к обмену ионов, получили название - иониты. Они могут быть в виде гранул, порошков, волокон, тканей, мембран. Большинство из них нерастворимо в воде.
Ионит условно состоит из трех частей: матрица (каркас), фиксированные ионы, противоионы. Например: ![]() «
« ![]() +
+ ![]()
R – матрица, ![]() - фиксированная группа,
- фиксированная группа, ![]() - противоион.
- противоион.
Противоионы подвижны и могут обмениваться на ионы раствора.
По природе матрицы различают неорганические (минеральные) и органические иониты. Например, структуру стекла составляет трехмерная сетка силикатных ионов, в пустотах которой содержатся катионы щелочных и щелочноземельных металлов, способные к обмену. В органических ионитах трехмерный каркас образован сеткой из углеродных атомов, с которой связаны группы, несущие заряд.
По происхождению иониты бывают природные, искусственные, синтетические. Синтетические органические иониты обычно называют ионообменными смолами. Некоторые примеры ионитов приведены в таблице 1.
Таблица 1
Классификация ионитов по природе и происхождению.
неорганические | природные | кристаллические силикаты типа цеолитов: глауконит, вермикулит; гидрослюды; апатит. |
синтетические | пермутиты (алюмосиликаты, подобные цеолитам; гетерополикислоты | |
органические | природные | каменные и бурые угли, торф, целлюлоза |
искусственные | сульфоуголь | |
синтетические | ионообменные смолы |
По строению иониты бывают гелевые и макропористые. Гелевые способны к обмену только после набухания.
В зависимости от знака заряда обменивающихся ионов различают: катиониты (обмен катионами), аниониты (обмен анионами), амфолиты (обмен и катионами, и анионами).
Катиониты могут быть в ![]() - форме, что по природе соответствует кислотам, и в солевой форме
- форме, что по природе соответствует кислотам, и в солевой форме ![]() и др.
и др.
Аниониты могут быть в ![]() - форме, что соответствует основаниям, и в солевой
- форме, что соответствует основаниям, и в солевой  и др.
и др.
По степени ионизации иониты могут быть сильно-, средне - и слабо-ионизированные, это аналогично обычным понятиям сильные и слабые электролиты. На примере ионообменных смол:
Сульфокатионит универсальный (КУ) RSO3H - сильнокислотный.
Фосфорнокислые иониты (КФП, КРФ) RPО3H2 - среднекислотные.
Карбоксильный ионит (КБ) RCOOH - слабокислотный.
Анионит АВ - высокоосновный.
Силу ионита можно охарактеризовать константой диссоциации. Средне - и слабокислотные иониты диссоциируют только в щелочных средах, а основные - только в кислых.
Слабые иониты перед работой обычно переводят в солевую форму и они становятся более сильными.
Ионный обмен
Ионный обмен происходит в равноэквивалентных количествах – сколько ионов поглощается из раствора, столько же их переходит обратно в раствор. Например:



Важнейшей характеристикой ионита является обменная емкость – количество поглощаемых им ионов [моль/г], [моль/м3]. Она зависит от числа активных групп на единицу массы или объема ионита и от степени диссоциации этих групп.
Общее число всех ионогенных групп, приходящееся на 1 г ионита характеризует его полную обменную емкость (ПОЕ). Методы определения ПОЕ стандартизованы. Обменная емкость ионита используется не полностью, а лишь на определенную величину (зависит от технологии процесса, гидродинамических условий, конструкции аппарата и т. д.), поэтому говорят о реальной емкости - рабочей (РОЕ). ПОЕ и РОЕ – главные показатели качества ионитов, т. к. являются мерой способности ионита к сорбции любых ионов, независимо от природы.
На обменную емкость ионитов влияют: структура ионита, набухаемость, рН (для сильных почти не влияет), концентрация, тип и размер ионов и др. Обменная емкость повышается с увеличением заряда иона, например:
![]()
А при одинаковой валентности – с ростом атомного радиуса, например:
для одновалентных катионов: ![]() ,
,
для одновалентных анионов: ![]() .
.
Процесс ионного обмена проводят в статических и в динамических условиях. Обменная емкость будет называться соответственно статическая обменная емкость (СОЕ) и динамическая обменная емкость (ДОЕ).
СОЕ соответствует ионообменному равновесию между ионитом и данной концентрацией электролита. В раствор, содержащий ион, который нужно извлечь (например, ![]() ), добавляют ионит в такой форме, которая соответствует целям процесса (например,
), добавляют ионит в такой форме, которая соответствует целям процесса (например, ![]() - форме) и выдерживают определенное время до установления равновесия. Затем смолу отделяют от раствора. При необходимости такую операцию производят повторно. После отделения смолу регенерируют, обрабатывая раствором, содержащим первоначальные ионы.
- форме) и выдерживают определенное время до установления равновесия. Затем смолу отделяют от раствора. При необходимости такую операцию производят повторно. После отделения смолу регенерируют, обрабатывая раствором, содержащим первоначальные ионы.
Для проведения процесса в динамических условиях, ионит загружают в колонну, через которую с определенной скоростью пропускают раствор.
Характеристикой адсорбента в динамических условиях являются выходные кривые - зависимость концентрации сорбируемого вещества в фильтрате от объема раствора, прошедшего через колонну (рис.1).

Рис.1 Выходная кривая сорбции в динамических условиях.
Сначала вещество поглощается полностью или почти полностью. Таким образом, в процессе продвижения раствора через слои ионита, происходит обмен ионов и из колонны вытекает раствор, не содержащий тех ионов, которые были в начальном растворе. В точке Р происходит появление вещества в фильтрате - проскок. Затем кривая поднимается вверх, т. е. поглотительная способность сорбента падает. В точке D происходит полное насыщение ионита, большее количество вещества поглотиться уже не сможет. Для дальнейшего использования сорбента нужна регенерация.
ДОЕ характеризуется динамической емкостью до проскока ДОЕр и полной динамической емкостью ПДОЕ– до полного извлечения данного иона из раствора. При этом обязательно указывают в каких условиях проводился процесс – толщина, высота слоя, размер, структура частиц адсорбента, скорость процесса, концентрация и др.
На выходной кривой ДОЕр определяется площадью OPEF, а полная ДОЕ – площадью OPDF. Так же эти величины можно определить, вычислив количество поглощенных ионов (а) для каждой порции фильтрата (1), а затем сложив их.
 (1)
(1)
где, ![]() - исходная концентрация компонента в растворе, моль/л; С
- исходная концентрация компонента в растворе, моль/л; С![]() - концентрация компонента в фильтрате, моль/л; V
- концентрация компонента в фильтрате, моль/л; V![]() - объем отдельной порции фильтрата, пропущенного через колонну, л; m – масса адсорбента, г.
- объем отдельной порции фильтрата, пропущенного через колонну, л; m – масса адсорбента, г.
Между величинами ДОЕ существует соотношение ДОЕр<ДОЕ<ПДОЕ.
Экспериментальная часть.
Ионообменная сорбция ионов никеля катионитом
в динамических условиях.
Цель работы:
1. Построить выходные кривые сорбции ионов никеля катионитом.
2. Определить динамическую обменную емкость катионита.
Для изучения процесса сорбции ионов никеля в данной работе используется катионит КБ (карбоксильный) в ![]() - форме,
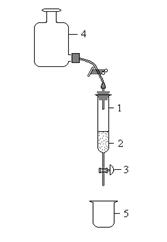
- форме, ![]() . Перед работой катионит помещают в колонку, заливают дистиллированной водой, и выдерживают 24 часа для набухания. На дно колонки помещается кусочек стеклянной ваты. Колонка должна быть закреплена строго вертикально (рис.2).
. Перед работой катионит помещают в колонку, заливают дистиллированной водой, и выдерживают 24 часа для набухания. На дно колонки помещается кусочек стеклянной ваты. Колонка должна быть закреплена строго вертикально (рис.2).
| 1. Колонка 2. Катионит 3. Кран 4. Напорная склянка с раствором 5. Стаканчик для сбора фильтрата |
Рис.2. Установка для проведения ионного обмена в динамических условиях.
Порядок выполнения работы работы. Постепенно спустить лишнюю воду через кран, оставляя слой воды над катионитом 3-4 см. Залить в колонку 0,1н раствор сульфата никеля.
Соединить верхнюю часть колонки с напорной склянкой для равномерной подачи раствора в колонку. В склянке должен быть налит 0,1н раствор сульфата никеля. (Точная концентрация раствора устанавливается титрованием).
Под колонку поместить мерный стаканчик на 25 мл, открыть кран, и начать пропускать раствор ![]() через слой катионита с постоянной скоростью 1 мл/мин, что соответствует 3 капли за 5 секунд, скорость регулируют краном.
через слой катионита с постоянной скоростью 1 мл/мин, что соответствует 3 капли за 5 секунд, скорость регулируют краном.
Собирать по 25мл вытекающего раствора (фильтрата), каждый раз подставляя под кран следующий стаканчик. В каждой пробе фильтрата определить концентрацию ионов никеля. Опыт закончить, когда концентрация ионов в фильтрате сравняется с исходной (в склянке).
Определение концентрации ионов Ni![]() . Пипеткой в коническую колбу отбирают пробу раствора сульфата никеля (5мл), прибавляют 5 мл аммиачного раствора буфера, несколько кристалликов индикатора мурексида. Титрируют раствором трилона Б до изменения окраски от желтой до сиреневой. Концентрацию ионов никеля рассчитывают по формуле:
. Пипеткой в коническую колбу отбирают пробу раствора сульфата никеля (5мл), прибавляют 5 мл аммиачного раствора буфера, несколько кристалликов индикатора мурексида. Титрируют раствором трилона Б до изменения окраски от желтой до сиреневой. Концентрацию ионов никеля рассчитывают по формуле:
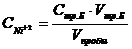 ; V
; V![]() = 5 мл.
= 5 мл.
Результаты заносят в таблицу 2. При расчете количества поглощенных ионов (а), учитывайте размерность.
Таблица 2.
Результаты сорбции ионов никеля катионитом в динамических условиях.
№ ст. | Vфильтрата, мл | Vтр. Б, мл |
моль/л | D моль/л |
моль/г |
1. 2. … | 25мл 25мл … |
Обработка результатов:
1. Построить выходную кривую сорбции, откладывая по оси абсцисс – объем фильтрата (мл) пропущенного через колонку, по оси ординат – концентрацию ионов Ni![]() (моль/л) в фильтрате.
(моль/л) в фильтрате.
2. Графически и аналитически определить динамическую обменную емкость до проскока (ДОЕр).
3. Определить полную динамическую емкость: считают сумму всех поглощенных ионов на единицу массы катионита.
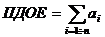 ,
,
где n – количество порций фильтрата, включая все порции, в том числе, в которых ![]() не был обнаружен.
не был обнаружен.
Выполнить задания и ответить на вопросы:
1. Записать уравнение ионного обмена для изучаемого процесса.
2. Объяснить, почему катионит взят в ![]() - форме.
- форме.
3. Проанализировать полученную выходную кривую.
4. Оценить адсорбционную способность катионита в данных условиях, используя справочные данные.
Контрольные вопросы.
1. Что такое иониты?
2. По каким признакам классифицируют иониты?
3. Приведите примеры ионообменных процессов.
4. Как проводят адсорбцию в статических и динамических условиях?
5. Какие величины используются для характеристики ионитов?
6. Лучше или хуже ионов Ni будут сорбироваться катионитом ионы 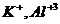 в тех же условиях эксперимента?
в тех же условиях эксперимента?
Литература
1. Воюцкий коллоидной химии. - М.: Химия, с.
2. Щукин E. Д., , «Коллоидная химия» - М.:ВШ,2006,444с.
3. А, Фельдман по физической и коллоидной химии. Учеб. пособие для нехимических вузов-М.: ВШ,с.
4. Айвазов по химии поверхностных явлений и адсорбции: Учеб. пособие для институтов. – М.:ВШ,1973,208с.
5. М, Ионный обмен в технологии и анализе неорганических веществ. – М. Химия, с.
Содержание | Стр. |
Введение | 3 |
Правила техники безопасности | 4 |
теоретическая часть | 5 |
экспериментальная часть | 10 |
контрольные вопросы | 12 |
Литература | 13 |