МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ
РОССИЙСКОЙ ФЕДЕРАЦИИ
федеральное государственное бюджетное образовательное учреждение
высшего профессионального образования
«МОСКОВСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
ПИЩЕВЫХ ПРОИЗВОДСТВ»
Мероприятие 41,1
Разработка научно-методических, информационных и лабораторных материалов с использованием научно-технического потенциала высшей школы для развития в средней школе в интересах города специализированных классов, лицеев и т. п., ориентированных на раннюю профессиональную ориентацию учащихся средних школ в части предоставления образовательных услуг
Научно-образовательный материал
«Разработка цикла лабораторных работ по химии для учащихся 10-11 классов»
Москва 2011
Классы химических соединений
Раздел "Классы химических соединений" является наиболее важным в курсе химии. Прежде чем выполнить экспериментальную работу по этому разделу, надо твердо усвоить на какие классы делятся неорганические вещества, как составляются названия веществ, принадлежащих различным классам соединений, какие основные реакции характерны для каждого класса химических соединений.
Химические соединения разделяются на классы по составу и по химическим свойствам, которые эти вещества проявляют в химических реакциях.
Один из классов неорганических соединений включает вещества, состоящие из двух элементов, один из которых кислород, такие соединения называются оксидами. Их названия образуются от корня латинского названия кислорода с окончанием - ид и русского названия второго элемента в родительном падеже. Если элемент может иметь разные степени окисления, то после его названия в скобках указывают римскими цифрами степень окисления. Например, С12О7 - оксид хлора (VII), Сu2О - оксид меди (I).
По химическим свойствам оксиды подразделяются:
 ОКСИДЫ
ОКСИДЫ
несолеобразующие солеобразующие
(безразличные) основные амфотерные кислотные
CO, NO, N2O Na2O, BaO ZnO, A12O3 CO2, N2O5
FeO, MgO и др. Cr2O3, Fe2O3 и др. SO3, C12O7 и др.
Несолеобразующие оксиды не взаимодействуют ни с кислотами, ни с основаниями.
Основными называются оксиды, которые образуют соли при взаимодействии с кислотами или кислотными оксидами. В основных оксидах для элемента, его образующего, характерна низкая степень окисления: +1, +2, редко +3.
Кислотными называются оксиды, которые образуют соли при взаимодействии с основаниями или с основными оксидами. В этом случае элемент, образующий оксид, имеет степень окисления +4 и выше.
Амфотерными называются оксиды, которые образуют соли при взаимодействии как с кислотами, так и с основаниями, т. е. проявляют двойственную природу.
Среди сложных соединений, состоящих из элемента, кислорода и водорода, важную группу образуют гидроксиды. Некоторые из них –основные гидроксиды - проявляют свойства оснований - NaOH, Ba(OH)2, Fe(OH)2 и т. п.
Другие - кислотные гидроксиды - проявляют свойства кислот - H2SO4, Н3РО4, НСlO4 и т. п. Существуют и амфотерные гидроксиды, которые в зависимости от условий проявляют как основные, так и кислотные свойства А1(OН)3, Zn(OH)2, Fe(OH)3, Cr(OH)3 и др.
Важный класс неорганических соединений, выделяемый по химическим свойствам, составляют кислоты. К ним относятся вещества, способные диссоциировать в растворе с образованием ионов водорода. Характерным свойством кислот является их способность взаимодействовать с основаниями, основными и амфотерными оксидами с образованием солей.
По наличию кислорода в своем составе кислоты делятся:
![]()
![]() КИСЛОТЫ
КИСЛОТЫ
бескислородные кислородсодержащие
HCl, HBr, HI, H2S H2SO4, HNO3, Н3РО4, Н2СО3 и т. п.
По числу содержащихся в молекуле кислот атомов водорода, способных замещаться атомами металла, различают кислоты одноосновные (НС1, HNO3), двухосновные (H2SO4, H2S), трехосновные (Н3РО4).
Названия кислот производят от элемента, образующего кислоту. Названия кислородсодержащих кислот зависят от степени окисления элемента, образующего кислоту. Максимальной степени окисления элемента, равной номеру группы в периодической системе элементов, соответствует суффикс "...н(ая)" или "-ов(ая)", например НС1О4 - хлорная кислота, Н2СгО4 - хромовая кислота. Для названия кислоты, соответствующей низшей степени окисления элемента, используется суффикс "-ист(ая)": НNО2 - азотистая кислота, H2SO3 - сернистая кислота.
Еще один важный класс неорганических соединений, характеризующийся общими свойствами, образуют основания. К ним относятся вещества, способные диссоциировать в растворе с образованием гидроксид-ионов.
Характерным свойством оснований является их способность взаимодействовать с кислотами, кислотными и амфотерными оксидами с образованием солей. Амфотерные гидроксиды образуют соли при взаимодействии как с кислотами, так и с основаниями.
Zn(OH)2 + 2НС1 = ZnCl2 + 2Н2О
Zn(OH)2 + 2NaOH = Na2ZnO2 + 2H2O
Рассматривая последнюю реакцию, следует обратить внимание, что ионы таких активных металлов, как натрий, калий в солях всегда стоят на первом месте.
По растворимости и по способу их получения основания делятся:
![]()
![]() ОСНОВАНИЯ
ОСНОВАНИЯ
растворимые нерастворимые, включая амфотерные
(щелочи)
NaOH, KOH, Ba(OH)2 Fe(OH)2, Mg(OH)2, Fe(OH)3, A1(OH)3
Растворимые основания можно получить:
1. 2Na + 2Н2О = 2NaOH + Н2.
2. Na2O + Н2О = 2NaOH.
Нерастворимые основания образуются действием щелочи на растворимую соль элемента. Например:
FeCl2 + 2NaOH = Fe(OH)2 + 2NaCl
Изучив такие классы неорганических веществ, как оксиды, основания, кислоты, следует запомнить, что в химических реакциях взаимодействие идет только между веществами с противоположными свойствами, т. е. между веществами основного и кислотного характера.
Самый большой класс неорганических соединений составляют соли.
Соли можно рассматривать как продукт полного или частичного замещения атомов водорода в молекуле кислоты атомами металла или как продукт полного или частичного замещения гидроксогрупп в молекуле основного гидроксида кислотными остатками. При полном замещении атомов водорода в молекуле кислоты образуются средние (нормальные) соли, при неполном - кислые соли.
При частичном замещении гидроксогрупп в молекуле основного гидроксида кислотными остатками образуются основные соли.
Следует запомнить, что кислые соли могут быть образованы только кислотами, основность которых равна двум или более, а основные соли — гидроксидами, содержащими две и более гидроксогруппы.
![]()
![]() СОЛИ
СОЛИ
кислые средние основные
NaHS, NaH2PO4 NaBr, K2S, Na3PO4 (ZnOH)2SO4, Fe(OH)2Cl
![]() Названия солей составляют из названия аниона кислоты в именительном падеже и названия катиона в родительном падеже. При этом название аниона производят qj корня латинского наименования элемента. Степень окисления металла, образующего катион, указывают, если это необходимо, римскими цифрами в скобках.
Названия солей составляют из названия аниона кислоты в именительном падеже и названия катиона в родительном падеже. При этом название аниона производят qj корня латинского наименования элемента. Степень окисления металла, образующего катион, указывают, если это необходимо, римскими цифрами в скобках.
В случае бескислородных кислот анион имеет окончание "ид" (NaBr - бромид натрия, K2S - сульфид калия).
В случае анионов кислородосодержащих кислот используются только два окончания; "-ат", если элемент имеет высокую степень окисления, и "ит", если элемент имеет более низкую степень окисления (Na2SO4 - сульфат натрия, Na2SO3 - сульфит натрия).
Если элемент, образующий кислоту, имеет более чем две положительных степени окисления (например, хлор, бром, йод), тогда в названии солей добавляются приставки; "гипо" - для самой низкой степени окисления, "пер" - для самой высокой степени окисления.
Названия кислых солей образуются также, как и средних, но при этом добавляют приставку "гидро", указывающую на наличие незамещенных ионов водорода, число которых обозначают греческими числительными (ди, три и т. д.). Например, Na2HPO4 - гидрофосфат натрия, КН2РО4 - дигидрофосфат калия.
Названия основных солей образуют подобно названиям средних солей, но при этом добавляют приставку "гидроксо", указывающую на наличие незамещенных гидроксогрупп, число которых обозначают греческими числительными. Так, (ZnOH)2SO4 - сульфат гидроксоцинка, Fe(OH)2Cl - хлорид дигидроксожелеза (III).
ЛАБОРАТОРНАЯ РАБОТА 1
КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Опыт 1. Свойства оксидов.
а) Взаимодействие оксидов с водой.
В две сухие чистые пробирки поместить на кончике шпателя в одну — оксид магния, в другую - оксид фосфора (V). Добавить в каждую пробирку приблизительно 5 мл дистиллированной воды. С помощью 2-3 капель фенолфталеина в первой пробирке и 2-3 капель метилоранжа во второй пробирке определить реакцию полученной среды. Написать уравнения соответствующих реакций, наблюдения, выводы.
б) Взаимодействие основного оксида с кислотой:
В сухую чистую пробирку поместить на кончике шпателя оксид магния. Добавить приблизительно 5 мл H2SO4. Растворился ли оксид магния? Какого цвета стал раствор? Написать уравнения соответствующих реакций, наблюдения, выводы.
в) Взаимодействие кислотного оксида с основанием.
В сухую чистую пробирку поместить на кончике шпателя оксид фосфора (V) и добавить приблизительно 5 мл NaOH. Растворился ли в щелочи оксид фосфора (V)? Написать уравнение соответствующей реакции, наблюдения, выводы.
Опыт 2. Получение и свойства оснований.
а) Получение нерастворимых оснований.
В сухую чистую пробирку налить приблизительно 5 мл раствора сульфата меди и добавить 1-2 мл раствора NaOH. Что Вы наблюдаете в результате реакции? Написать уравнение реакции, наблюдения, выводы.
б) Взаимодействие оснований с кислотами.
Половину полученного в пункте (а) осадка поместите в чистую пробирку и добавьте раствор H2SO4 до полного растворения осадка. Написать уравнение реакции, наблюдения, выводы.
в) Взаимодействие щелочей с растворами солей.
В чистую пробирку налить 3-5 мл раствора хлорида марганца (II) и добавить такой же объем раствора NaOH. Что Вы наблюдаете в результате реакции? Написать уравнение реакции, наблюдения, выводы.
Опыт 3. Получение и свойства солей.
а) Взаимодействие металла с кислотой.
В сухую чистую пробирку поместите кусочек цинка и добавьте приблизительно 5 мл раствора H2SO4. Какой газ при этом выделяется? Почему? Написать уравнение реакции, наблюдения, выводы.
б) Взаимодействие раствора соли с металлом.
В сухую чистую пробирку поместить кусочек цинка и добавить приблизительно 5 мл раствора CuSO4. Что Вы наблюдаете? Написать соответствующее уравнение реакции, наблюдения, выводы.
в) Взаимодействие раствора соли с кислотой.
В сухую чистую пробирку налить приблизительно 5 мл раствора Pb(NO3)2 и добавить такой же объем НС1. Что Вы наблюдаете? Написать соответствующее уравнение реакции, наблюдения, выводы.
г) Взаимодействие раствора соли со щелочью.
В сухую чистую пробирку налить приблизительно 5 мл раствора FеС13 и добавить приблизительно такой же объем NaOH. Что Вы наблюдаете? Написать соответствующее уравнение реакции, наблюдения, выводы.
д) Взаимодействие растворов двух солей друг с другом.
В сухую чистую пробирку налить приблизительно 5 мл раствора ВаС12 и добавить такое же количество сульфата натрия. Что Вы наблюдаете? Написать соответствующее уравнение реакции, наблюдения, выводы.
Скорость химических реакций
Химическое равновесие
Скорость химической реакции измеряется изменением концентрации участвующих в реакции веществ в единицу времени.
![]() ,
,
где ![]() С - изменение концентрации, моль/л;
С - изменение концентрации, моль/л;
![]() t - промежуток времени, за который произошло изменение концентрации, с.
t - промежуток времени, за который произошло изменение концентрации, с.
Закон действия масс (Гульдберг и Вааге, 1867 г.)
"Скорость химической реакции пропорциональна произвел концентрации реагирующих веществ, возведенных в степени, рае коэффициентам ".
Для химической реакции: А + В = С.
Скорость реакции V = к [А] × [В],
где [А] - концентрация вещества А, моль/л;
[В] - концентрация вещества В, моль/л;
к - константа скорости реакции.
Физический смысл константы скорости реакции
Если принять [А] = [В] = 1 моль/л или [А] × [В] = 1 моль/л, то V = к. Константа скорости численно равна скорости реакции при условии [А] × [В] = 1.
Для химической реакции:
nA + mB = С.
V = k[A]n × [B]m,
где n и m - стехиометрические коэффициенты уравнения реакции. Для гомогенной системы:
2Н2(г.) + О2(г.) = 2Н2О
V = k[H2]2 × [O2].
В гетерогенных системах реакция идет на поверхности раздела поэтому концентрация вещества, образующего твердую или жидкую фа остается постоянной и не влияет на скорость реакции. Следователе концентрации веществ, находящихся в конденсированном состоянии, не входят в выражение скорости реакции.
Для реакции: 4А1(т.) +ЗО2(г.) = 2А12О3
V = k[O2]3.
Влияние температуры на скорость реакции (эмпирическое правило Вант-Гоффа)
"При повышении температуры на каждые 10 градусов скорость химической реакции увеличивается в 2 – 4 раза".
Математически правило Вант-Гоффа выражается равенством
![]() ,
,
где ![]() и
и ![]() - скорости химической реакции при температурах t1 и t2;
- скорости химической реакции при температурах t1 и t2;
g - температурный коэффициент (число, показывающее во сколько раз увеличивается скорость данной реакции при повышении температуры на 10 градусов).
Ниже приведена таблица изменения времени протекания реакции получения воды из водорода и кислорода в зависимости от температуры:
Температура, °С | Скорость протекания реакции |
25 400 655 600 | Столетие 80 дней 2 часа Мгновенно, со взрывом |
Большинство химических реакций являются обратимыми, т. е. протекают одновременно в двух противоположных направлениях, например
N2 + ЗН2 = 2NH3.
Реакция, протекающая слева направо называется прямой (скорость ее обозначается через V1).
Реакция, протекающая справо налево называется обратной (скорость ее обозначим через V2).
Химическим равновесием называется такое состояние системы, при котором скорости прямой и обратной реакции равны (V1 = V2). При химическом равновесии концентрации веществ перестают изменяться называются равновесными концентрациями.
Химическое равновесие - состояние установления динамического равновесия.
|
|
|

Для обратимой реакции
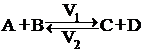
Согласно закону действия масс:
V1 = k1[A]×[B]; V2 = k2[C]×[D].
При равновесии V1 = V2
к1[А]×[В] = к2[С]×[D].
Разделив обе части равенства на произведение к2[А]×[В] получим
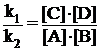 или
или ![]()
В обратимых реакциях равновесие наступает тогда, когда отношение произведения концентраций образующихся веществ к произведениию концентраций исходных веществ станет равным некоторой постоянной для данной реакции и при данной температуре величине, называемой константой равновесия кР.
Пример гомогенной системы: Н2 + С12 = 2НС1
Пример гетерогенной системы: 3Fe(т.) + 4Н2О(п.) = Fe3O4(т.) + 4Н2(г.)
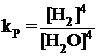
Физический смысл константы равновесия

Если концентрации участвующих в реакции веществ составляют 1 моль/л, то k1 = V1 и k2 = V2. Константа равновесия показывает во сколько раз прямая реакция идет быстрее обратной при данной температуре и концентрациях, равных единице.
кР зависит от температуры, для газовой системы и от давления.
Смещение (сдвиг) равновесия
Смещением равновесия называется процесс изменения концентраций участвующих веществ, вызванный нарушением равновесия:
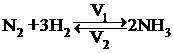
Если V1 > V2, то увеличивается концентрация аммиака, равновесие смещается в направлении прямой реакции (вправо).
![]() Если V1 < V2, то равновесие смещается в направлении обратной реакций (влево).
Если V1 < V2, то равновесие смещается в направлении обратной реакций (влево).
Принцип Ле-Шателье
"Если на систему у находящуюся в равновесии, оказывать внешнее воздействие (изменять температуру, давление, концентрации), то равновесие в системе смещается в направлении той реакции, которая противодействует произведенному воздействию, т. е. стремится восстановить прежние условия".
Влияние концентрации
Увеличение концентрации исходных веществ и уменьшение концентрации полученных веществ (отвод их из системы) приводит к смещению равновесия в направлении прямой реакции.
Влияние изменения температуры на смещение равновесия
При нагревании равновесие смещается в направлении протекания эндотермической реакции, при охлаждении - в направлении протекания экзотермической реакции:
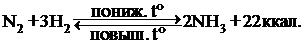
ЛАБОРАТОРНАЯ РАБОТА 2
ХИМИЧЕСКАЯ КИНЕТИКА. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
Опыт 1. Влияние концентрации реагирующих веществ на скорость реакции в гомогенной системе.
При взаимодействии раствора тиосульфата натрия Na2S2O3 и серной кислоты выпадает сера, вызывающая при достижении определенной концентрации помутнение раствора:
Na2S2O3 + H2SO4 = H2O + SO2 + S + Na2SO4
По промежутку времени от начала реакции до заметного помутнения раствора можно судить об относительной скорости этой реакции.
В три пробирки (одинакового диаметра) налить: в первую - 2,5 мл раствора Na2S2O3 и 5 мл Н2О, во вторую - 5,0 мл раствора Na2S2O3 и 2,5 мл Н2О, в третью - 7,5 мл раствора Na2S2O3. В каждую из трех пробирок добавить по 2,5 мл раствора H2SO4. Отмерять нужное количество реактивов следует либо с помощью бюреток, либо используя для этого мерные пробирки. С помощью секундомера отметить время, в течение которого появляется помутнение раствора в пробирках после добавления в них кислоты. Полученные результаты занести в таблицу.
Номер пробирки | Объем раствора, мл | Суммарный объем, мл | Время появления помутнения t, с | Относительная скорость, v = 1/t | ||
Na2S2O3 | Н2О | H2SO4 | ||||
1 | 2,5 | 5,0 | 2,5 | 10 | ||
2 | 5,0 | 2,5 | 2,5 | 10 | ||
3 | 7,5 | - | 2,5 | 10 |
Результаты эксперимента представить в виде графика зависимости относительной скорости реакции от концентрации Na2S2O3. Для этого на оси абсцисс откладывать три точки, отстоящие от начала координат на расстоянии а, 2а и За (где а - произвольно выбранный отрезок, соответствующий единице относительной концентрации Na2S2O3). На оси координат откладывать скорость реакции.
График зависимости относительной скорости реакции от концентрации реагирующих веществ
|
|
Опыт 2. Влияние температуры на скорость реакции в гомогенной системе.
Налить в пробирку 5 мл раствора Na2S2O3 и добавить в нее при комнатной температуре 5 мл H2SO4. Отметить время от начала реакции до помутнения.
В две другие пробирки налить по 5 мл тех же растворов и пробирки поместить на 5 минут в водяную баню, температура воды в которой на 10°С больше комнатной. Через 5 минут содержимое пробирок слить и отметить время от начала реакции до помутнения. Опыт повторить, повысив температуру водяной бани еще на 10°. Результаты опытов записать в таблицу.
Номер пробирки | Объем раствора, мл | t, °C | Время появления помутнения t, с | Относительная скорость, v = 1/t | |
Na2S2O3 | H2SO4 | ||||
1 | 2,5 | 2,5 | |||
2 | 2,5 | 2,5 | |||
3 | 2,5 | 2,5 |
По полученным данным построить график зависимости скорости реакции от температуры: на оси абсцисс отложить температуру, на оси ординат - относительную скорость реакции.
|
|
Смещение химического равновесия вследствие изменения концентрации реагирующих веществ.
Осуществить реакцию:
FeCl3 + 3KSCN = Fe(SCN)3 + ЗКС1
Роданид железа Fe(SCN)3 окрашен в яркий красный цвет. Изменение концентрации Fe(SCN)3 влияет на интенсивность окраски раствора. Это позволяет наблюдать, в каком направлении сдвигается равновесие при изменении концентрации реагирующих веществ.
К 5 мл разбавленного раствора хлорида железа (III) прилить 5 мл разбавленного раствора роданида калия. В результате получается раствор с характерной красной окраской. Полученный раствор разлить поровну в четыре пробирки. Первую оставить для сравнения, во вторую добавить 2-3 капли насыщенного раствора хлорида железа (III), в третью - 2-3 капли насыщенного раствора роданида калия, в четвертую - немного твердого хлорида калия. Содержимое второй и третьей пробирок перемешать, четвертую сильно встряхнуть. Результаты наблюдений записать в таблицу.
Номер пробирки | Вещество, добавляемое для смещеия равновесия | Изменение окраски | Смещение равнове5сия |
1 (контроль) 2 3 4 | FeCl3 (конц.) KSCN (конц.) КС1 (конц.) |
Пользуясь выражением константы равновесия для данной системы, дайте объяснения наблюдаемым процессам.



