На правах рукописи
якубов мухаммадходжа рахматджонович
стандартизация и контроль качества ПРОТИВОТУБЕРКУЛЕЗНЫХ лекарственных средств
15.00.02 – фармацевтическая химия, фармакогнозия
Автореферат
диссертации на соискание ученой степени
кандидата фармацевтических наук
Москва – 2007
Работа выполнена в ГОУ ВПО Московская медицинская академия имени
Росздрава.
Научный руководитель: доктор фармацевтических наук, академик РАМН, профессор Александр Павлович Арзамасцев
Официальные оппоненты:
доктор фармацевтических, профессор
доктор фармацевтических, профессор
Ведущая организация:
Институт стандартизации и контроля лекарственных средств ФГУ «Научный центр экспертизы средств медицинского применения».
Защита состоится «______»_________________2007 г. в _____ часов на заседании Диссертационного совета (Д 208.040.09) при Московской медицинской академии имени Москва, Никитский бульвар, 13.
С диссертацией можно ознакомиться в библиотеке ММА имени Москва, Нахимовский проспект, 49.
Автореферат разослан «______»_________________ 2007 г.
Ученый секретарь Диссертационного
совета Д 208.040.09
доктор фармацевтических наук
профессор
Общая характеристика работы
Актуальность темы. Несмотря на значительные успехи в области микробиологии проблема инфекционных заболеваний до настоящего времени не потеряла свою актуальность. Это обусловлено увеличением количества микроорганизмов, резистентных к большому числу противомикробных лекарственных средств. Особое значение в странах и регионах со сложной социально-экономической обстановкой приобретает, в частности, проблема туберкулеза, трудно поддающегося лечению. ВОЗ рекомендована стратегия борьбы с туберкулезом, известная под названием Directly Observed Treatment Short-course (курс ускоренной амбулаторной терапии, проходящий под непосредственным наблюдением). В основу стратегии DOTS положены пять основных элементов, в отсутствии каждого из которых она считается малоэффективной. Неотъемлемой частью программы является создание надежной системы поставки высококачественных противотуберкулезных лекарственных препаратов для учреждений здравоохранения. В первую очередь, это актуально для стандартных лекарственных средств «первого ряда» - изониазида, рифампицина, пиразинамида, этамбутола, используемых для лечения обычного (чувствительного) туберкулеза. Низкое качество даже одного из принимаемых больным препаратов на этом этапе нарушает всю систему и может привести к переходу легкоизлечимой чувствительной формы заболевания в туберкулез со множественной лекарственной устойчивостью (ТБ МЛУ). В этой ситуации важно не допустить распространения низкокачественных и особенно фальсифицированных лекарственных препаратов.
В Женеве Комитет экспертов ВОЗ по спецификациям для фармацевтических препаратов в 2006 году утвердил план разработки нормативной документации для противотуберкулезных лекарственных средств на следующие препараты:
- рифампицин таблетки
- рифампицин капсулы
- рифампицин + изониазид таблетки
- рифампицин + изониазид + пиразинамид таблетки
- изониазид + этамбутола гидрохлорид таблетки
- рифампицин + изониазид + пиразинамид + этамбутола гидрохлорид
таблетки.
При этом Комитет отметил, что перспективной является разработка методики теста «растворение» для этих противотуберкулезных лекарственных средств. В частности для препаратов, содержащих рифампицин, целесообразно строить кривые растворимости по рифампицину как по менее растворимому веществу.
Другой важной проблемой остается фальсификация лекарственных средств. Известно, что противомикробные средства подделываются чаще других – их доля среди фальсификатов составляет, по данным ВОЗ, до 30%. В мировой практике известны случаи фальсификации противотуберкулезных лекарственных средств. В Государственный реестр лекарственных средств входит несколько десятков индивидуальных и комбинированных противотуберкулезных лекарственных средств различных производителей. В то же время, в России и в Таджикистане отсутствует комплексный подход к выявлению поддельных противотуберкулезных лекарственных средств с использованием современных аналитических методов.
Учитывая вышеизложенное, разработка унифицированных подходов к стандартизации и контролю качества противотуберкулезных лекарственных средств с использованием современных физико-химических методов анализа является актуальной.
Цель и задачи исследования. Целью данной работы являлась разработка унифицированных подходов к стандартизации и контролю качества противотуберкулезных лекарственных средств с использованием современных физико-химических методов анализа. Для достижения поставленной цели решались следующие задачи:
- разработка унифицированной методики анализа субстанций и препаратов противотуберкулезных лекарственных средств методом ИК - спектроскопии;
- составление атласа ИК-спектров субстанций и препаратов противотуберкулезных лекарственных средств;
- разработка унифицированной методики анализа субстанций и препаратов противотуберкулезных лекарственных средств методом ТСХ;
- выбор условий теста «растворение» для сравнения препаратов рифампицина и выявления фальсификатов;
- разработка комплексного аналитического подхода к выявлению фальсифицированных противотуберкулезных лекарственных средств, не содержащих действующие вещества, указанных на этикетке, и содержащих действующие вещества, но изготовленные другим производителем.
Научная новизна исследования. Составлен атлас ИК-спектров субстанций и лекарственных препаратов противотуберкулезных лекарственных средств различных производителей. Впервые разработаны методики установления подлинности противотуберкулезных лекарственных средств в лекарственных формах «таблетки» и «капсулы» методом ИК-спектроскопии.
Разработана методика пробоподготовки субстанций и лекарственных препаратов противотуберкулезных средств для анализа методом ТСХ. Впервые разработана унифицированная методика установления подлинности индивидуальных и комбинированных противотуберкулезных лекарственных средств методом ТСХ.
Впервые показано, что тест «растворение» позволяет проводить сравнение препаратов рифампицина и выявлять фальсификаты.
Впервые разработан комплексный аналитический подход к выявлению фальсифицированных противотуберкулезных лекарственных средств с использованием методов ИК - и УФ- спектроскопии, ТСХ, качественных реакций и теста «растворение».
Практическая значимость исследования. В Республике Таджикистан принято Постановление Правительства № 000 от 01.01.01 года «Программа борьбы с туберкулезом в Республики Таджикистан на 2003 – 2010 годы», в котором, в частности, говорится об улучшении обеспечения населения качественными противотуберкулезными лекарственными препаратами.
Полученные ИК спектры могут быть использованы при стандартизации и контроле качества по разделу «подлинность» соответствующей НД на субстанции и препараты противотуберкулезных лекарственных средств и для выявления фальсификатов.
Методика установления подлинности методом ТСХ предлагается для стандартизации и контроля качества субстанций и лекарственных препаратов данной группы лекарственных средств с последующим их включением в соответствующие разделы НД, а также для выявления фальсификатов.
Выбранные условия теста «растворение» предлагаются для сравнения препаратов рифампицина различных производителей и для выявления фальсификатов.
Апробация работы. Основные положения диссертационной работы доложены и обсуждены на: XII и XIII Российских национальных конгрессах «Человек и лекарство» (Москва, 2005 г., 2006 г.). Апробация работы проведена на межлабораторной конференции кафедры фармацевтической химии фармацевтического факультета ММА им. 25 декабря 2006 г.
Публикации. По материалам диссертации опубликовано 4 печатные работы.
Связь исследования с проблемным планом фармацевтических наук. Диссертационная работа выполнена в рамках комплексной темы кафедры фармацевтической химии ММА им. «Совершенствование контроля качества лекарственных средств» (№ гос. регистрации 01.200.110545).
Объем и структура диссертации. Диссертация изложена на 105 страницах машинописного текста и состоит из введения, обзора литературы, экспериментальной части (материалы и методы, результаты исследования и их обсуждение), выводов, списка литературы, а также отдельно включает в себя 2 приложения. Работа иллюстрирована 15 таблицами и 9 рисунками. Библиографический указатель включает 125 источника, из них 40 – иностранные.
Основные положения, выносимые на защиту:
- результаты исследования противотуберкулезных лекарственных средств методами ИК - и УФ-спектрофотометрии;
- результаты изучения хроматографических характеристик противотуберкулезных лекарственных средств методом ТСХ;
- унифицированные методики установления подлинности противотуберкулезных лекарственных средств методом ТСХ;
- результаты биофармацевтического анализа рифампицина с использованием теста «растворение»;
- комплексный подход к выявлению фальсифицированных противотуберкулезных лекарственных средств;
Содержание работы
1. Объекты исследования
Объектами исследования являлись стандартные образцы, субстанции и препараты противотуберкулезных лекарственных средств (табл. 1).
Табл. 1. Изучаемые противотуберкулезные лекарственные средства.
МНН | Структурная формула | Химическое название, молекулярная формула, М. м., фарм. субстанции |
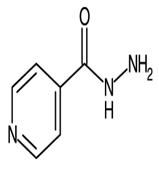
Изониазид |
| ГИНК–гидразид изоникотиновой кислоты. Гидразид 4-пиридинкарбоновой кислоты C6H7N3O, М. м. 134.14 Фарм. субстанция изониазид |
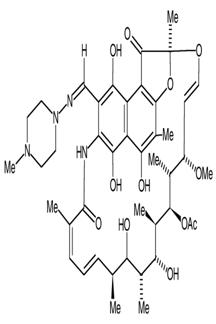
Рифампицин |
| 3-[[(4-Метил-1-пиперазинил)имино]метил]-5,6,9,17,19,21-гексагидракси-23-метокси2,4,12,16,18,20,22-гептаметил-8-[N-(4-метил–1-пиперазинил) формимидоил] -2,7-(эпиксипентадека[1,11,13] триэнимино) нафто [2,1-b] фуран-1,11-(2 H)-дион 21 ацетат C43H58N4O12 М. м 822,94 Фарм. субстанция рифампицин |
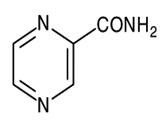
Пиразинамид |
| Пиразинкарбоксиамид. C5H5N3O, М. м 123.11 Фарм. субстанция пиразинамид |
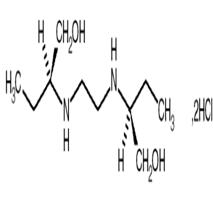
Этамбутол |
| S-(R, R*)-2,2-(1,2-Этандиилдиимино)бис (1-бутанол) (дигидрохлорид). C10H24N2O2 2 HCE М. м 277,23 Фарм. субстанция этамбутола гидрохлорид |
Амикацин |
| N-[4-Амино-2-(S)-гидроксибутил]-О-6-амино-6- дезокси-альфа-D-глюкопиранозил (1-4)]-O-[3-амино-3-дезокси-альфа-D-глюкопиранозил(1-6)] -2-дезокси-D-стрептамин С22Н43N5О13 2Н2SO4 М. м 781,76 Фарм. субстанция амикацина сульфат |
2. Оборудование и условия испытаний
2.1. ИК-спектроскопия
В работе использовали однолучевой интерференционный (с обратным преобразованием Фурье) ИК-спектрофотометр Инфралюм ФТ-02 (НПФ «ЛЮМЭКС», Россия). Параметры записи спектров: диапазон см–1, разрешение 1 см–1, циклическая запись с количеством сканов 20, аподизация стандартная. Фоновый спектр (воздух) получали непосредственно перед записью каждого спектра.
Управление прибором и обработку спектров осуществляли с использованием программы «Спектралюм» (НПФ «ЛЮМЭКС», Россия) и программы «ACD/SpecViewer», Freeware Version (Advanced Chemistry Development, Канада).
Пробоподготовку субстанций осуществляли в соответствии с требованиями ГФ XI. Навеску субстанции массой 15 мг измельчали в агатовой ступке и растирали с 1-2 каплями вазелинового масла качества «для ИК-спектроскопии». Полученную пасту наносили между двумя пластинками из KBr и получали ИК-спектр образца.
2.2. Тонкослойная хроматография
Хроматографирование проводили на пластинах для высокоэффективной ТСХ «Сорбфил» размером 10×10 см (, г. Краснодар), покрытых силикагелем с люминофорным содержимым. Пластины были представлены двумя видами, отличающимися между собой материалом подложки: алюминиевая фольга (ПТСХ-АФ-В-УФ) и полимер (ПТСХ-П-В-УФ).
Использовали стеклянную хроматографическую камеру размером 150×120×80 мм. Насыщение камеры парами подвижной фазы (ПФ) проводили в течение 20-30 мин.
В качестве подвижной фазы для изониазида, рифампицина, пиразинамида и этамбутола гидрохлорида использовали смесь: раствор аммиака 25% – ацетон – метанол – этилацетат (1:1:1:7), а для амикацина сульфата раствор аммиака 25% - метанол - ацетонитрил - ледяная уксусная кислота (7:10:12:1).
Для комбинированных противотуберкулезных лекарственных средств пробы наносились полоской 10 мм для четкости сравнения разделившихся веществ. Сушку проб противотуберкулезных лекарственных средств осуществляли с помощью нагревательного устройства для сушки пластин УСП–1 (, г. Краснодар) при температуре около 50˚С. Пробег фронта растворителя составлял 8 см. После хроматографирования пластину высушивали в сушильном шкафу при температуре 110° С в течение 5 минут.
После высушивания хроматографическую пластину помещали на 4-5 мин в камеру с парами йода (только для таблеток с этамбутолом) и с помощью раствора нингидрина 0,25%( для амикацина сульфата), а затем проявляли в УФ-свете облучателя хроматографического УФС 254/365 (, г. Краснодар) при 254 нм.
2.3. УФ-спектрофотометрия
В работе использовали однолучевой спектрофотометр СФ-103 (Аквилон, Россия). Управление прибором осуществляли с использованием программы «Спектр» (Аквилон, Россия).
Обработку спектров осуществляли с использованием программы «ACD/SpecViewer», Freeware Version (Advanced Chemistry Development, Канада)
2.4. Тест «растворение»
Тест «растворение» проводили в соответствии с ОФС «Растворение» на приборе SOTAX AT 7 smart (Швейцария), аппарат «вращающаяся корзинка».
Количественный анализ осуществляли методом УФ-спектрофотометрии по предложенным нами методикам.
3.1. ИК-спектроскопия
3.1.1. ик - спектры субстанций.
Было проведено исследование противотуберкулезных лекарственных средств с использованием метода ИК-спектроскопии. Пробоподготовку осуществляли путем диспергирования испытуемых лекарственных средств в вазелиновом масле.
На рис. 1 в качестве примера представлен ИК-спектр пиразинамида. В изучаемых спектрах полосы около 2955, 2924, 2855 см–1 соответствуют валентным колебаниям nС–Н, 1462, 1378 и 722 см–1 –деформационным колебаниям dС–Н вазелинового масла. Полосы с частотами около 2361, 2346, 2334 и 666 см–1 соответствует колебаниям присутствующего в атмосфере углекислого газа.
Соответствующая методика пробоподготовки может быть использована при фармакопейном анализе противотуберкулезных лекарственных средств и при накоплении их стандартных ИК - спектров.
Следует также добавить, что методика пробоподготовки с вазелиновым маслом является более экспрессной и удобной.
Рис. 1. ИК-спектр субстанции пиразиамида в вазелиновом масле

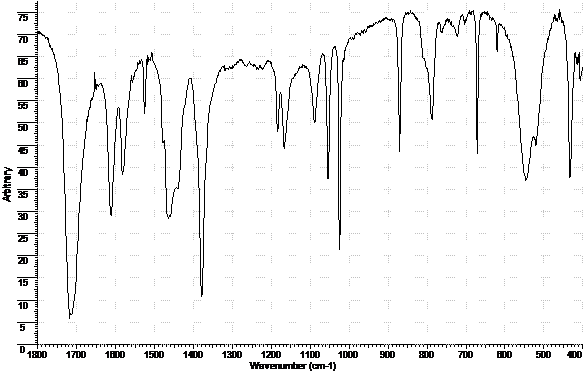
3.1.2. ИК-спектры противотуберкулезных лекарственных средств.
В данной работе также решалась задача получения ИК-спектров противотуберкулезных лекарственных средств в готовых лекарственных формах без предварительного извлечения действующего вещества. Нами было показано, что при содержании активной субстанции в лекарственной форме «таблетки» и «капсулы» на уровне не менее 30-40% можно получать ИК-спектр, на котором отмечаются практически все полосы, соответствующие полосам поглощения действующего вещества. Вспомогательные вещества не искажают картину и не маскируют полосы действующего вещества.
На рис. 2 в качестве примера представлен ИК - спектр таблеток пиразинамида.
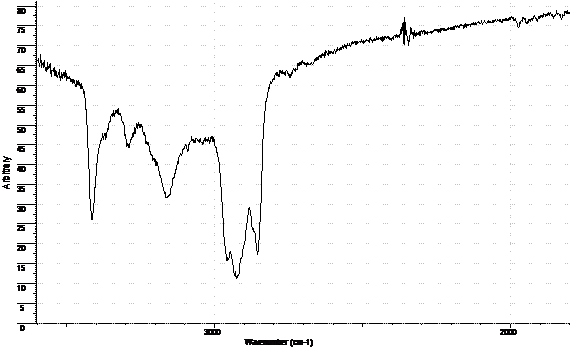

Из рис. 1 и 2 видно, что ИК - спектры субстанции и таблеток пиразинамида различаются крайне незначительно – практически совпадают. Аналогичная ситуация наблюдается и для других противотуберкулезных лекарственных средств.
В настоящей работе был составлен атлас ИК - спектров субстанций и препаратов противотуберкулезных лекарственных средств с целью их дальнейшего использования в качестве стандартных.
3.2. Тонкослойная хроматография
3.2.1. общий подход.
По нашему мнению, интерес могут представлять унифицированные методики установления подлинности противотуберкулезных лекарственных средств методом ТСХ. В последующем они могут быть включены в общий план исследований по разработке комплексного подхода к обнаружению фальсифицированных лекарственных средств, а также в раздел НД «подлинность» для субстанций и лекарственных препаратов.
Нами было исследовано влияние подвижных фаз (ПФ) различного состава на подвижность противотуберкулезных лекарственных средств и селективность хроматографической системы. Элюирующую силу ПФ оценивали по полярности входящих в ее состав растворителей, а для оценки селективности последних использовали классификацию Снайдера. Полярность ПФ ориентировочно оценивали по диэлектрической проницаемости растворителей. Для этого рассчитывали среднее взвешенное значение диэлектрической проницаемости фазы с учетом содержания каждого растворителя.
3.2.2. Препараты, содержащие изониазид, рифампицин, пиразинамид, этамбутола гидрохлорид.
Были изучены ПФ содержащие следующие растворители в различных соотношениях (в порядке увеличения полярности): тетрахлорметан, диэтиловый эфир, хлороформ, этилацетат, ледяная уксусная кислота, изоамиловый спирт, бутанол, изопропиловый спирт, пропанол, ацетон, этанол, метанол, ацетонитрил, вода, раствор аммиака 25%, формамид.
При увеличении содержания в ПФ высокополярных компонентов (раствор аммиака 25%, формамид) резко повышается подвижность изучаемых веществ, но снижается селективность хроматографической системы, и все пятна на хроматограмме имеют значения Rf более 0,8, в том числе оказываются на уровне фронта растворителя. При использовании в ПФ тетрахлорметана пятна имеют значения Rf менее 0,2, либо остаются на линии старта.
Показано, что для снижения эффекта размывания пятен испытуемых веществ следует включать в состав ПФ раствор аммиака 25%. Установлено, что оптимальное содержание раствора аммиака 25% в ПФ для комбинированных противотуберкулезных лекарственных средств составляет 10%.
Для увеличения селективности хроматографической системы необходимо использовать метанол. Оптимальное содержание метанола в ПФ составило 10%. ПФ также должна включать в себя другие растворители, которые хорошо смешиваются с раствором аммиака 25% и метанолом и имеют сильно различающихся между собой значениями диэлектрической проницаемости. Последнее обстоятельство позволяет, меняя их соотношение, регулировать полярность ПФ, и следовательно, выбирать оптимальную подвижность изучаемых лекарственных веществ. В качестве таких растворителей после ряда исследований были выбраны этилацетат и ацетон (значение диэлектрической проницаемости, соответственно, около 6 и 20).
Таким образом, было установлено, что оптимальные подвижность и разделение пятен изониазида, рифампицина, пиразинамида и этамбутола гидрохлорида наблюдаются в ПФ с промежуточной полярностью (значение диэлектрической проницаемости смеси составляет около 17) следующего состава: раствор аммиака 25% – ацетон – метанол – этилацетат (1:1:1:7). При этом значения Rf находятся в пределах 0,2-0,8, что является оптимальным. (Рис. 3.)

Рис. 3. ТСХ комбинированного противотуберкулезного лекарственного препарата содержащего изониазида, рифампицина, пиразинамида и этамбутола гидрохлорида в ПФ раствор аммиака 25% – ацетон – метанол – этилацетат (1:1:1:7). Рядом с пятнами указаны значения Rf.
Для детектирования всех пятен использовали комбинирование обработки парами йода и облучения УФ-светом с длиной волны 254 нм. Пятна рифампицина вследствие его естественной окраски видны на хроматограмме без какой-либо предварительной обработки при естественном освещении. Пятна изониазида и пиразинамида проявляются при облучении светом УФ-лампы при длине волны 254 нм (темные пятна на люминесцирующем фоне пластины). Для проявления пятен этамбутола гидрохлорида требуется обработка парами йода. На рис. 3 представлена схема соответствующей хроматограммы.
Для всех комбинированных противотуберкулезных лекарственных средств используется одна подвижная фаза, в которых препараты разделяются отчетливо в пределах значения Rf.
Детектирование в УФ - свете с использованием разработанной методики позволяет различать пятна при нанесении на линию старта изониазида около 2,7 мкг действующего вещества, пиразинамида около 1,45 мкг действующего вещества, рифампицина около 0,55 мкг действующего вещества и этамбутола около 0,1 мкг действующего вещества. При проведении детектирования было отмечено, изониазид и пиразинамид при длине волны 254 нм детектируются в виде темных пятен на светящемся (люминесцирующем) фоне пластины.
3.2.3. Препараты, содержащие амикацина сульфат.
На линию старта пластин с помощью микрошприца наносили:
· амикацина сульфата - 6 мкг:
Установлено, что оптимальная подвижность пятен амикацина сульфата наблюдаются в ПФ содержащей следующие растворители: ледяная уксусная кислота, метанол, ацетонитрил, раствор аммиака 25%. При этом значения Rf находятся в пределах 0,2 – 0,8, что, согласно современным представлениям, является оптимальным. Для подбора конечного состава ПФ учитывались следующие факты и предположения.
Показано, что для снижения эффекта размывания пятен амикацина сульфата следует включать в состав ПФ растворы аммиака 25% и одновременно ледяной уксусной кислоты. Установлено, что оптимальное содержание раствора аммиака 25% в ПФ для амикацина сульфата составляет 23,3 %, а ледяной уксусной кислота 3,3 %.
Для увеличения селективности хроматографической системы необходимо использовать метанол. Оптимальное содержание метанола в ПФ для амикацина сульфата составляет 33,3 %.
ПФ также должна в себя включать растворители, которые хорошо смешиваются с растворами аммиака 25%, ледяной уксусной кислотой и метанолом. В качестве такого растворителя после ряда исследований был выбран ацетонитрил. Для проявление пятен амикацина сульфата пластину опрыскивают 0,25% раствором нингидрина, после высушивают хроматографическую пластину сушат при температуре 110 °С 5 минут и проявляются пятна.
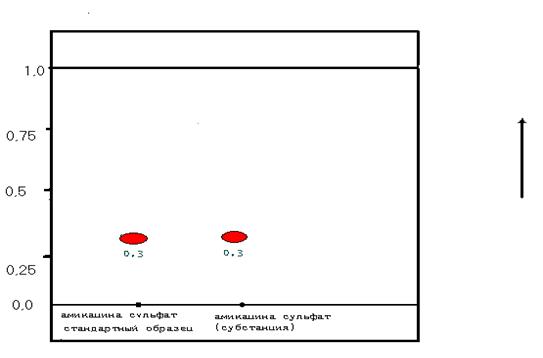 |
В результате был подобран оптимальный состав ПФ, для амикацина сульфата раствор аммиака 25% - метанол - ацетонитрил - ледяная уксусная кислота(7:10:12:1). (Рис. 4.)
На рис. 4 представлена схема соответствующей хроматограммы.
3.3. УФ-спектрофотометрический анализ
препаратов рифампицина
Молекула рифампицина содержит различные функциональные группы, обладающие кислотно-основными свойствами и вступающие друг с другом в сложное взаимодействие.
![]()
![]()


|

|

Рис. 5. Структура и кислотно-основные свойства рифампицина
В первую очередь, необходимо отметить наличие в структуре рифампицина (рис. 5) сложной системы p, p - и p, p-сопряжения, включающей нафталиновое ядро, имино-группу, амидную группу, систему кратных связей и ряд доноров и акцепторов электронов, в том числе фенольные гидроксилы. Также в молекуле присутствует пиперазинильный радикал и сложноэфирная группа.
Малую растворимость рифампицина в воде можно объяснить, в частности, наличием в составе молекулы имино-группы (основание Шиффа).
Наличие развитой системы сопряжения в структуре рифампицина обусловливает сильный батохромный сдвиг в электронном спектре поглощения и, соответственно, красно-коричневую окраску вещества, а также значительную величину удельного показателя экстинкции в максимумах поглощения. Это позволяет использовать для количественного определения данного вещества метод УФ спектрофотометрии. Поскольку количественное определение высвободившегося вещества проводили по методике, описанной в разделе «растворение» для капсул рифампицина (BP 2005), то есть без использования стандартного образца, нами проводилось количественное определение содержания действующего вещества в каждом из испытуемых препаратов.
При УФ спектрофотометрическом анализе прибор дает наименьшую ошибку при оптической плотности (А) испытуемого раствора, близкой к значению 0,4343. Зная удельный показатель экстинкции А(1%,1см) для раствора рифампицина в 0,1 М HCl, определяли требуемую концентрацию раствора С(мкг/мл):
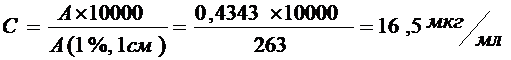
На примере анализа препарата: «Капсулы Рифампицина» (150 мг) производства Белмедпрепараты ОАО, Республика Беларусь. Из 7 капсул испытуемого препарата извлекали содержимое. Взвешивали на аналитических весах. Средняя масса содержимого 1 капсулы составила 0,212 г. Исходя из номинального содержания рифампицина (0,15 г), рассчитывали его долю в составе извлеченного порошка. Она составила около 49,6%.
Исходя из того, что прибор дает наименьшую ошибку при концентрации испытуемого раствора, близкой к значению 16,5 мкг/мл, а также учитывая долю рифампицина в составе порошка, извлеченного из капсул, рассчитывали массу точной навески:
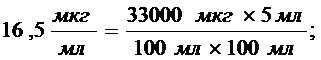
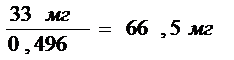
Порошок измельчали в ступке, брали среднюю пробу, из которой получали точную навеску по массе, близкую к рассчитанной.
Извлечение действующего вещества осуществляли 0,1 М HCl.
Около 66,5 мг (точная навеска) порошка содержимого капсул помещали в мерную колбу вместимостью 100 мл, растворяли в 0,1 М кислоте хлористоводородной и доводили объем раствора до метки тем же растворителем. 5,0 мл полученного раствора помещали в мерную колбу вместимостью 100 мл и доводили объем раствора до метки кислотой хлористоводородной 0,1 М. Полученный раствор фильтровали через фильтр типа «белая лента», отбрасывая первую порцию фильтрата.

Рис. 6. Спектр в УФ и видимой областях раствора содержимого капсул
рифампицина (Белмедпрепараты ОАО). Концентрация рифампицина
около 16,5 мкг, мл.
Расчет содержания рифампицина (мг) в капсулах осуществляли по формуле:
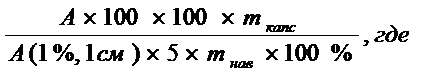
А – оптическая плотность испытуемого раствора;
А(1%, 1 см) – удельный показатель экстинкции;
mкапс – средняя масса содержимого одной капсулы, мг;
mнав – масса точной навески измельченного содержимого капсул, мг;
100×100/5 – разведение, мл.
Для проверки правильности выбранного максимума поглощения на используемом приборе нами был получен УФ спектр раствора содержимого капсул в среде 0,1 М HCl (рис. 6). В данной среде наблюдаются максимумы 233 нм, 269 нм, 336 нм и 473 нм. Максимум 336 нм достаточно хорошо выражен и совпадает с максимумом поглощения, указанным в BP 2005 при количественном определении высвободившегося рифампицина.
3.4 Тест «Растворение»
Для создания условий, в которых можно дифференцировать профили высвобождения различных препаратов, содержащих одно и то же действующее вещество, подбирали среду растворения, в которой высвобождение вещества будет несколько затруднено.
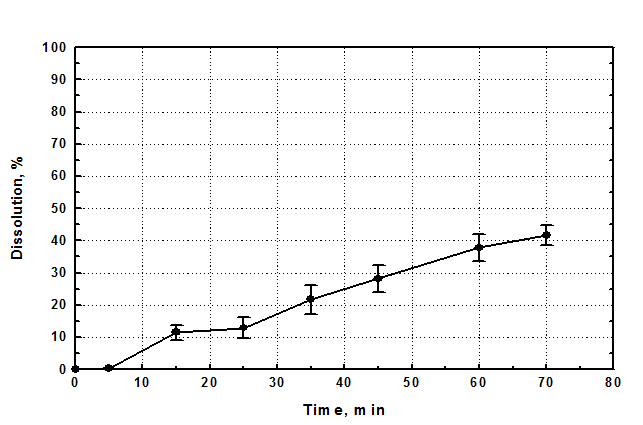 Рис. 7. Профиль высвобождения капсул Рифампицина производства
Рис. 7. Профиль высвобождения капсул Рифампицина производства
.
На рисунке 7 представлен профиль высвобождения препарата Рифампицин капсулы 150 мг производства Белмедпрепараты ОАО, Республика Беларусь, в следующих условиях:
- вращающаяся корзинка со скоростью вращения 100 об/мин,
- среда растворения 0,01 М раствор HCl (pH 2,0),
- объем среды растворения 900 мл,
- температура среды 37°С.
При использовании в качестве среды растворения 0,01 M HCl рифампицин высвобождается незначительно и очень медленно. Это можно объяснить нарушением так называемых «условий раковины» («sink conditions»), которые подразумевают использование таких условий растворения, дозировок и объемов среды, при которых не происходит образование насыщенного раствора действующего вещества. Это могло произойти и в данном случае. Видимо, в среде 0,01 М HCl происходит слабое протонирование основных центров. Растворимость рифампицина вследствие этого снижена и высвобождение затруднено. В этой ситуации дальнейшее использование данной среды растворения нецелесообразно.
Для создания дифференцирующих условий растворения, которые, в то же время, не приводили бы к преждевременному насыщению раствора, было решено использовать 0,1 М HCl (pH 1.06 с учетом поправки на ионную силу раствора). При таком значении pH растворимость рифампицина должна увеличиться. На рис. 8 представлены профили высвобождения рифампицина из испытуемых препаратов.
В табл. 2 представлены данные по высвобождению испытуемых препаратов в точке 45 мин. Из рис. 8 и табл. 2 видно, что в данной среде рифампицин высвобождается практически полностью. Препараты Р-цин (Люпин Лтд) и Рифампицин производства Белмедпрепараты требованиям как BP 2005 (не менее 70%), так и ОФС (не менее 75%).
Профиль высвобождения препарата Рифампицин (150 мг), «БИОС» (фальсификат) отличается резким снижением концентрации испытуемого вещества в растворе после точки 35 мин. Такое же явление наблюдается и для других испытуемых препаратов, но в значительно меньшей степени. Мы предполагаем, что это может быть связано со снижением стабильности рифампицина в ходе проведения испытания, в частности, с окислением с образованием рифампицина-хинона, что, несомненно, сказывается на удельном показателе экстинкции и положении максимума поглощения ввиду резкого изменения хромофора. Стабильность субстанции зависит, в том числе, от технологии ее получения и чистоты. Меньшую стабильность субстанции в составе фальсифицированного препарата можно объяснить ее низким качеством.
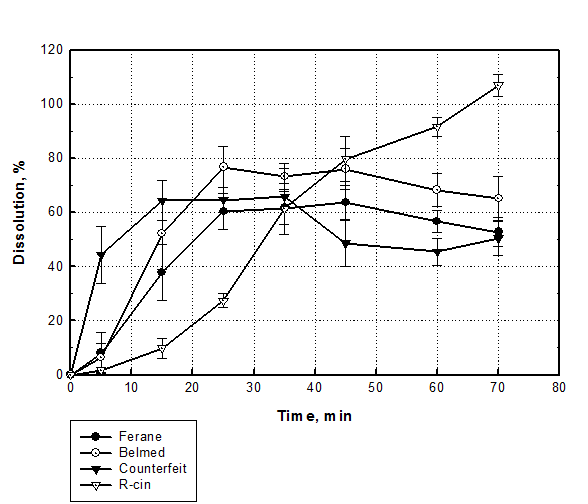
Рис. 8. Профили высвобождения препаратов рифампицина в 0,1 М HCl.
Препарат | Высвобождение в точке 45 мин. (%) | Фармакопейные требования | ||
BP 2005 | USP 29 | ОФС
| ||
Капсулы Рифампицин-Ферейн (150 мг) | 63,6 | не менее 70% | не менее 75% | не менее 75% |
Капсулы Рифампицин Белмедпрепараты ОАО (150 мг) | 76,1 | |||
Капсулы Рифампицин «БИОС» (150 мг), (фальсификат) | 48,7 | |||
Капсулы Р-цин (300 мг) | 79,8 |
Таблица 2. Высвобождение испытуемых препаратов в точке 45 мин.
На основании полученных данных была проанализирована возможность диффиренцировки исследуемых препаратов по профилям растворения. По рекомендации FDA для этого рассчитывали факторы различия и подобия. Различие между кривыми отсутствует, если:
- фактор различия (f1) принимает значения от 0 до 14;
- фактор подобия (f2) принимает значения от 51 до 100.
В табл.3 представлены значения фактора различия и фактора подобия в 0,1М HCl, полученные для каждой пары препаратов.
Таблица 3. Значения фактора различия (f1) и фактора подобия (f2) в 0,1 М HCl для препаратов рифампицина.
Р-цин | Рифампицин (Белмедпрепараты ОАО) | Рифампицин-Ферейн | |
Рифампицин (Белмедпрепараты ОАО) | f1 = 42,3 f2 = 25,5 | __ | __ |
Рифампицин-Ферейн | f1 = 50,7 f2 = 26,1 | f1 = 23,7 f2 = 45,4 | __ |
Рифампицин (фальсификат) | f1 = 71,1 f2 = 18,7 | f1 = 32,3 f2 = 33,2 | f1 = 30,4 f2 = 36,3 |
Каждая пара кривых отличается по параметрам FDA. Для установления статистически достоверной разницы можно также применять расчет по отдельным временным точкам с использованием теста Стьюдента для независимых выборок – двусторонняя критическая область (с предварительной проверкой гипотезы о равенстве генеральных дисперсий). Покажем это на примере двух наименее различающихся по высвобождению кривых (табл. 4).
Из представленных в табл. 4 данных видно, что два выбранных препарата различаются в 5 временных точках, что подтверждает результаты, полученные при использовании параметров FDA.
Таблица 4. Тест Стьюдента. 0,1 М HCl. Рифампицин-Ферейн – Рифампицин (Белмедпрепараты ОАО).
15 мин | 25 мин | 35 мин | 45 мин | 60 мин | 70 мин | |
Критерии Стьюден-та | t эксп. = - 2,219 t критич. = 2,262 | t эксп. = - 4, 096 t критич. = 2,228 | t эксп. = - 3,764 t критич. = 2,228 | t эксп. = - 3,146 t критич. = 2,228 | t эксп. = - 3,811 t критич. = 2,262 | t эксп. = - 3, 130 t критич. = 2,262 |
Вывод | |t эксп.| < t критич., генераль –ные средние равны | |t эксп.| > t критич., генераль - ные средние различают-ся | |t эксп.| > t критич., генераль - ные средние различают-ся | |t эксп.| > t критич., генераль - ные средние различают-ся | |t эксп.| > t критич., генераль - ные средние различают-ся | |t эксп.| > t критич., генераль - ные средние различают-ся |
Анализ полученных данных свидетельствует о возможности использовать тест «растворение» для определения различий между воспроизведенными лекарственными средствами, а также для выявления фальсифицированных препаратов рифампицина.
Выводы
1. Разработана унифицированная методика анализа субстанций и препаратов противотуберкулезных лекарственных средств методом ИК- спектроскопии и составлен атлас соответствующих ИК-спектров, которые предлагаются для использования в качестве стандартных при анализе по разделу нормативной документации «подлинность» и для выявления фальсификатов, не содержащих указанное на упаковке действующее вещество.
2. Разработаны условия метода ТСХ и методики пробоподготовки субстанций и препаратов противотуберкулезных лекарственных средств. Подобран унифицированный состав подвижной фазы для изониазида, рифампицина, пиразинамида и этамбутола гидрохлорида: раствор аммиака 25% - ацетон – метанол - этилацетат (1:1:1:7). Оптимальная подвижность пятен амикацина сульфата наблюдается в системе растворителей: раствор аммиака 25% - метанол – ацетонитрил - ледяная уксусная кислота (7:10:12:1). Разработанные методики предлагаются для выявления фальсификатов, не содержащих указанные на упаковке лекарственные вещества, и для включения в раздел нормативной документации «подлинность» для субстанций и лекарственных препаратов противотуберкулезных лекарственных средств.
3. Показано, что для капсул рифапицина возможен подбор условий теста «растворения», позволяющих дифференцировать дженерики. В среде 0,1 М кислоты хлористоводородной наблюдаются значимые различия между профилями растворения всех изученных препаратов рифампицина. Это свидетельствует о возможности использовать тест «растворение» для определения различий между воспроизведенными препаратами рифампицина.
4. Разработан комплексный подход к выявлению фальсифицированных противотуберкулезных лекарственных средств, не содержащих действующие вещества, указанные на этикетке. Для обнаружения таких подделок следует использовать простые качественные реакции, ТСХ и ИК - спектроскопию в средней области.
5. Для выявления фальсифицированных противотуберкулезных лекарственных средств, содержащих действующие вещества, указанные на этикетке, но изготовленных другим производителем, возможно использование теста «растворение» в комплексе с другими аналитическими методами при условии параллельного испытания в дифференцирующих условиях подлинного лекарственного средства.
Список работ, опубликованных по теме диссертации
1. , , . Разработка методик экспресс-анализа противотуберкулезных лекарственных средств с использованием метода ТСХ // Человек и лекарство: Тез. докл. ХII Росс. нац. конгр. – М., 2005. – С. 8-9.
2. , , . Установление подлинности комбинированных противотуберкулезных препаратов с использованием метода ТСХ // Человек и лекарство: Тез. докл. ХII Росс. нац. конгр. – М., 2005. – С. 9.
3. , , . Установление подлинности монокомпонентных противотуберкулезных препаратов методом ИК - спектроскопии. // Человек и лекарство: Тез. докл. ХIII Росс. нац. конгр. – М., 2006. – С. 44.
4. , , . Экспресс-анализ комбинированных противотуберкулезных средств методом ТСХ // Вестник Воронежского государственного университета. Серия: Химия. Биология. Фармация. – 2006.- №1. - С. 230-232.