На правах рукописи
КЛИНКОВА АСЯ СТАНИСЛАВОВНА
ОСОБЕННОСТИ СОСТОЯНИЯ МИКРОЦИРКУЛЯЦИИ СТЕНОК РАЗЛИЧНЫХ КАМЕР СЕРДЦА У БОЛЬНЫХ С АОРТАЛЬНЫМ СТЕНОЗОМ ДО И ПОСЛЕ КОРРЕКЦИИ ПОРОКА
14.03.03- патологическая физиология
Автореферат диссертации на соискание ученой степени
кандидата медицинских наук
Новосибирск – 2010
Работа выполнена в Федеральном государственном учреждении «Новосибирский научно-исследовательский институт патологии кровообращения имени академика » Министерства здравоохранения и социального развития РФ
Научный руководитель:
доктор медицинских наук
Официальные оппоненты:
доктор медицинских наук
доктор медицинских наук
Ведущая организация: Учреждение Российской академии медицинских наук Научно-исследовательский институт клинической и экспериментальной лимфологии Сибирского отделения РАМН.
Защита состоится « 14 » Декабря 2010г. в 12 часов на заседании диссертационного совета Д 001.048.01 в Научном центре клинической и экспериментальной медицины СО РАМН по адресу:
ул. Тимакова, д. 2, г. Новосибирск, 630117.
Тел/
С диссертацией можно ознакомиться в библиотеке НЦКЭМ СО РАМН.
Автореферат разослан «___» Ноября 2010 г.
 Ученый секретарь
Ученый секретарь
диссертационного совета, д. б.н.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы исследования. В настоящее время аортальные пороки сердца входят в число самых распространенных заболеваний среди приобретенных пороков. В свою очередь, это представляет большую социальную значимость, так как пороки аортального клапана поражают людей трудоспособного возраста и являются одной из причин ранней инвалидизации и смертности. Среди всех сердечно-сосудистых заболеваний аортальный стеноз по частоте занимает третье место после артериальной гипертензии и ишемической болезни сердца. При естественном течении клинически выраженного аортального стеноза уровень смертности в течение 10 лет составляет 80-90% (, 2008.).
По мере нарастания нарушений обменных процессов в гипертрофированном сердце возникают дистрофические изменения, а затем необратимые изменения – гибель клеток с разрастанием на их месте соединительной ткани. В дальнейшем происходит ослабление функции и, в конечном счете, когда адаптационные механизмы исчерпаны, наступает декомпенсация органа. Применительно к сердцу – развивается систолическая дисфункция левого желудочка и сердечная недостаточность. Все вышесказанные патологические изменения развиваются на фоне снижения количества капилляров на единицу площади миокарда, где происходит нарушение соотношения между доставкой кислорода и потребностью в нем гипертрофированного левого желудочка, что приводит к снижению энергетического обеспечения миокарда (Zingone B. et al., 2008.; Sanjiv K. et al., 2008.).
Изучение гемодинамики в системе микроциркуляции, особенно в капиллярном звене, где осуществляются транспортные и метаболические функции кровообращения на фоне гипертрофических изменений миокарда становится наиболее актуальным. Поскольку при аортальном стенозе в патологический процесс вовлечены не только левый желудочек, но и левое предсердие, а также, опосредованно правый желудочек, то изучение микроциркуляторного кровотока в стенках всех камер сердца представляет наибольший интерес. В известной нам литературе не приводятся данные по интраоперационному изучению МЦК непосредственно до и после замены аортального клапана у пациентов с аортальным стенозом. Изучение этого вопроса определяет актуальность настоящего исследования.
Цель исследования. Изучить особенности состояния микроциркуляторного кровотока в стенках различных камер сердца интраоперационно у больных с аортальным стенозом до и после хирургической коррекции порока.
Задачи исследования:
1. Изучить особенности состояния микроциркуляторного кровотока в стенках предсердий и желудочков у пациентов с аортальным стенозом до хирургической коррекции порока.
2. Оценить изменения состояния микроциркуляторного кровотока в стенках предсердий и желудочков по мере прогрессирования процессов увеличения наружных размеров и объемов камеры левого желудочка при аортальном стенозе до хирургической коррекции порока.
3. Провести оценку состояния микроциркуляции в стенках всех камер сердца в зависимости от сократительной способности левого желудочка у пациентов с аортальным стенозом до хирургической коррекции порока.
4. Оценить изменения состояния микроциркуляторного кровотока в стенках предсердий и желудочков у пациентов с аортальным стенозом после хирургической коррекции порока.
Научная новизна. Впервые проведен анализ особенностей состояния микроциркуляторного кровотока в стенках предсердий и желудочков у пациентов с аортальным стенозом (интраоперационно) методом лазер-допплер-флоуметрии до – и после хирургической коррекции порока, что позволяет выявить нарушения системы микроциркуляции на фоне развившегося аортального стеноза.
Определена стадийность изменений состояния микроциркуляторного кровотока в стенках предсердий и желудочков по мере прогрессирования патологических изменений структурно-геометрических параметров левого желудочка при аортальном стенозе:
1-ая стадия характеризуется наиболее высокой объемной скоростью микроциркуляторного кровотока в стенках предсердий и желудочков (выше 70 мл/100г/мин) при нормальных размерах и объемах левого желудочка (стадия компенсации),
2-ая стадия проявляется снижением объемной скорости кровотока в стенке левого предсердия (ниже 60 мл/100г/мин), при умеренной дилатации полости левого желудочка (до 25 % выше нормы) (стадия субкомпенсации),
3-я стадия характеризуется снижением объемной скорости микроциркуляторного кровотока в стенке левого желудочка (ниже 70 мл/100г/мин), а также правого предсердия (ниже 60 мл/100г/мин) и наибольшим снижением уровня микроциркуляции в стенке левого предсердия (ниже 40 мл/100г/мин) при выраженной дилатации полости левого желудочка (до 80 % выше нормы) (стадия декомпенсации).
Проведен сравнительный анализ состояния микроциркуляции в стенках всех камер сердца при различных показателях сократительной способности левого желудочка у пациентов с аортальным стенозом. Выявлено снижение объемной скорости микроциркуляторного кровотока при низкой фракции выброса левого желудочка, что указывает на взаимосвязь между уровнем микроциркуляторного кровотока и сократительной способностью левого желудочка.
Практическая значимость. Измерение объемной скорости микроциркуляторного кровотока методом лазер-допплер-флоуметрии в стенках предсердий и желудочков позволяет выявить нарушение микроциркуляции на фоне прогрессирования патологических изменений структурно-геометрических параметров левого желудочка при аортальном стенозе и дифференцировать стадии состояния микроциркуляторного кровотока для прогнозирования возможности возникновения ранних послеоперационных осложнений в сердечно-сосудистой системе.
Положения, выносимые на защиту:
1. Микроциркуляторный кровоток в стенках камер сердца у пациентов с аортальным стенозом характеризуется наиболее низкой объемной скоростью в стенке левого предсердия по сравнению с остальными камерами сердца. Снижение уровня микроциркуляции в стенке левого предсердия имеет обратную зависимость от степени выраженности гипертрофии миокарда левого желудочка.
2. Состояние микроциркуляции в стенках предсердий и желудочков у пациентов с аортальным стенозом взаимосвязано с фракцией выброса левого желудочка, что выражается снижением объемной скорости микроциркуляторного кровотока при низкой сократительной способности левого желудочка.
3. Изменения состояния микроциркуляторного кровотока в стенках предсердий и желудочков по мере прогрессирования патологических изменений структурно-геометрических параметров левого желудочка при аортальном стенозе характеризуются стадийностью:
1-ая стадия характеризуется наиболее высокой объемной скоростью кровотока в стенках предсердий и желудочков (выше 70 мл/100г/мин) при нормальных размерах и объемах левого желудочка (стадия компенсации),
2-ая стадия выражается снижением объемной скорости кровотока в стенке левого предсердия (ниже 60 мл/100г/мин), при умеренной дилатации полости левого желудочка (до 25 % выше нормы) (стадия субкомпенсации),
3-я стадия характеризуется снижением объемной скорости микроциркуляторного кровотока в стенке левого желудочка (ниже 70 мл/100г/мин), а также правого предсердия (ниже 60 мл/100г/мин) и наибольшим снижением уровня микроциркуляции в стенке левого предсердия (ниже 40 мл/100г/мин) при выраженной дилатации полости левого желудочка (до 80 % выше нормы) (стадия декомпенсации).
Апробация диссертационного материала. Основные положения диссертационной работы были доложены и обсуждены на 13 Всероссийском съезде сердечно-сосудистых хирургов, Москва (2007г.), на 14 Всероссийском съезде сердечно-сосудистых хирургов, Москва (2008г.).
Внедрение результатов исследования. Результаты проведенных исследований по интраоперационному определению уровня микроциркуляторного кровотока в стенках различных камер сердца у больных с аортальным стенозом до и после хирургической коррекции порока внедрены в практическую деятельность Центра хирургии приобретенных пороков сердца и биотехнологий ФГУ «ННИИПК им. акад. » Минздравсоцразвития России.
Публикации. По материалам диссертации опубликовано 14 научных работ, из них 5 статей, 4 из которых в журналах, рекомендованных ВАК.
Структура и объем диссертации. Диссертация изложена на 145 страницах машинописного текста и состоит из введения, обзора литературы, глав с описанием материала и методов исследования, собственных результатов, обсуждения полученных результатов, выводов, практических рекомендаций и списка литературы, который включает в себя 234 источника (66 отечественных и 168 зарубежных). Работа иллюстрирована 18 таблицами и 22 рисунками.
Весь материал данного исследования получен и проанализирован лично автором.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Исследование микроциркуляторного кровотока (МЦК) проведено у 61 пациента с диагнозом: приобретенный порок сердца, аортальный стеноз (АС) III-IV ст., хроническая сердечная недостаточность 2 А-Б ст., II-IV функциональный класс по Нью-Йоркской классификации до и после хирургической коррекции аортального порока (АП) с имплантацией в аортальную позицию механических протезов. Все операции выполнялись в условиях искусственного кровообращения. Все пациенты до хирургического лечения давали добровольное письменное согласие на исследования.
В общей группе пациентов мужчины составили 50 человек (82%), женщины –%). Больные были в возрасте от 33 до 70 лет, средний возраст составил 54,2±1,2 года.
Критерием включения были пациенты с изолированным АС либо с преобладанием стеноза, которым было выполнено протезирование аортального клапана механическим протезом. У всех пациентов использовалось идентичное анестезиологическое пособие, применялись методы защиты миокарда на фоне антеградной кардиоплегии Custodiol. Инотропная поддержка в интраоперационном периоде не использовалась. Критерием исключения было наличие сопутствующей органической клапанной патологии, наличие ишемической болезни сердца с хирургически значимым поражением коронарного русла. Диагноз верифицировался на основании клинических и инструментальных методов исследования специалистами ФГУ «ННИИПК им. акад. » Минздравсоцразвития России.
Метод лазер-допплер-флоуметрии. Всем пациентам с АС проводилось интраоперационно измерение объемной скорости МЦК на субъэпикарде стенки каждой камеры сердца методом лазер-допплер-флоуметрии (ЛДФ). Исследование проводилось на аппарате фирмы «Transonic Systems Inc» (США): BLF-21D – двухканальный в инфракрасном диапазоне лазерного излучения.
Первое измерение МЦК производилось на работающем сердце до подключения аппарата искусственного кровообращения после перикардотомии в стенках: центральной части левого и правого предсердий (ЛП, ПП), боковой поверхности левого желудочка (ЛЖбп), верхушки левого желудочка (ЛЖв) и передней поверхности правого желудочка (ПЖ). Повторное измерение МЦК проводилось в постперфузионный период – после хирургической коррекции АП и отключения аппарата искусственного кровообращения на тех же участках стенок камер сердца. Записи МЦК производились поверхностным датчиком с определением величины перфузии крови в мл на 100 г ткани в мин.
Во время измерений микроциркуляции до и после хирургической коррекции АП фиксировался показатель Hb артериальной крови, а также регистрировались основные показатели гемодинамики: систолическое артериальное давление (АДС), диастолическое артериальное давление (АДД), частота сердечных сокращений (ЧСС).
Методика эхокардиографии. Эхокардиографическое исследование проводили на аппаратах «Vivid» S6 и S7 (США) по стандартным методикам, включающих одномерную и двухмерную эхокардиографию (ЭхоКГ). В анализе использовались данные ЭхоКГ до операции и в ближайшие сроки после хирургического лечения (на 7-10-е сутки). Анализировались показатели: фракция выброса левого желудочка (ФВ ЛЖ, %), рассчитанная в модификации по Тейххольцу, конечный систолический размер ЛЖ (КСР, см), конечный диастолический размер ЛЖ (КДР, см), конечный систолический объем ЛЖ (КСО, мл), конечный диастолический объем ЛЖ (КДО, мл), толщина задней стенки ЛЖ (ТЗСЛЖ, см) и толщина межжелудочковой перегородки (ТМЖП, см) в диастолу, продольные размеры правого и левого предсердий. Для определения величины гипертрофии ЛЖ (ГЛЖ) рассчитывалась масса миокарда ЛЖ (ММЛЖ, г) по формуле R. Deveruex (1986).
Статистическая обработка полученных данных. Статистический анализ проводился с помощью программы Statistica 6.0. Для проверки соответствия вида распределения признака закону нормального распределения применяли критерий Шапиро-Уилка. Количественные данные представлены в виде среднее значение ± ошибка среднего (M±m). Распределение всех изучаемых признаков не соответствовало закону нормального распределения, поэтому для сравнения групп применяли методы непараметрической статистики. Сравнение двух зависимых групп проводили с помощью критерия Вилкоксона, двух независимых групп – критерия Манна-Уитни, трех и более несвязанных групп – методом Краскела-Уоллиса. Для проведения корреляционного анализа использовали коэффициент Спирмена. Уровень отклонения нулевой гипотезы об отсутствии различий между группами (p) принимали равным 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Известно, что у больных с АС происходит нарушение коронарного кровотока на уровне микроциркуляции (Rajappan K. et. al., 2008.). При этом в настоящее время недостаточно детально изучено состояние МЦК в стенках предсердий и желудочков у больных с АС до и после хирургической коррекции порока.
В таблице 1 представлены интраоперационные данные МЦК в стенках различных камер сердца у пациентов с АС общей группы до и после хирургической коррекции АП.
Таблица 1.
Динамика показателей МЦК в стенках различных камер сердца у пациентов общей группы до и после хирургической
коррекции аортального стеноза (M±m)
Участок измерения | До операции (n=61) | После операции (n=61) | ∆ МЦК мл/(мин*100г) |
Микроциркуляторный кровоток, мл/(мин*100г) | Микроциркуляторный кровоток, мл/(мин*100г) | ||
Правое предсердие | 75,2±3,2 | 62,4±3,5* | -12,8 |
Правый желудочек | 83,0±2,6 | 75,8±2,8 | -7,1 |
Левое предсердие | 57,0±3,9 | 60,5±3,8 | 5,5 |
Боковая поверхность левого желудочка | 74,7±2,6 | 71,2±2,5 | -4,2 |
Верхушка левого желудочка | 82,3±4,2 | 76,4±4,5 | -5,4 |
Примечание: *- статистически значимые различия с показателями до операции (p<0,05); ∆ МЦК - разность МЦК (МЦК после операции – МЦК до операции)
До коррекции АС в общей группе наиболее высокая объемная скорость МЦК отмечалась в стенке ПЖ и в области ЛЖв, что составило выше 80 мл/100г/мин, а наиболее низкий уровень микроциркуляции был отмечен по ЛП – чуть ниже 60 мл/100г/мин. Средние значения МЦК всех камер сердца кроме ЛП колебались от 74 до 83 мл/100г/мин.
Наибольшая разница по уровню микроциркуляции была выявлена между ЛП и ПЖ, где в среднем градиент МЦК составил 26 мл/100г/мин. Статистически значимые отличия по МЦК были выявлены между ЛП и остальными камерами сердца (p<0.05), а также между ЛЖбп и ПЖ за счет наиболее высокого МЦК последнего.
После коррекции АС отмечалась тенденция к снижению объемной скорости МЦК в стенках всех камер сердца, кроме ЛП, где имеет место небольшая тенденция к повышению уровня микроциркуляции. Достоверное снижение МЦК было зарегистрировано только по ПП (р<0,01). После операции происходило частичное выравнивание уровня микроциркуляции в стенках камер сердца с сохранением градиента МЦК между предсердиями и желудочками.
Таким образом, при развитии АС, наиболее высокий уровень микроциркуляции был выявлен в стенках обоих желудочков и ПП. Необходимо выделить ЛП, в стенке которого отмечался наиболее низкий уровень МЦК, по сравнению с другими камерами.
В ходе исследования были выявлены достоверные обратные корреляционные связи МЦК в стенках всех камер сердца до хирургической коррекции порока с абсолютными и индексированными показателями размеров и объемов ЛЖ по данным ЭхоКГ. То есть, с увеличением размера и объема ЛЖ происходит снижение уровня микроциркуляции в стенках предсердий и желудочков (таб. 2).
Таблица 2.
Величины корреляционных связей между микроциркуляцией в стенках камер сердца и параметрами эхокардиографии левого желудочка.
Показатели, ед. измерения | КДР ЛЖ, см | КСР ЛЖ см | КДО ЛЖ мл | КДИ ЛЖ мл/м2 | КСО ЛЖ мл | КСИ ЛЖ мл/м2 |
МЦК по ЛП мл/(мин*100г) | -0,17 | -0,33* | -0,18 | -0,07 | -0,32* | -0,25 |
МЦК по ПП мл/(мин*100г) | -0,40* | -0,36* | -0,33* | -0,28 | -0,39* | -0,35* |
МЦК по ПЖ мл/(мин*100г) | -0,32* | -0,30* | -0,31* | -0,18 | -0,28* | -0,18 |
МЦК по ЛЖбп мл/(мин*100г) | -0,37* | -0,42* | -0,35* | -0,31* | -0,40* | -037* |
Примечание: *- статистически значимая корреляционная связь до операции (p<0,05); МЦК-микроциркуляторный кровоток; ПП-правое предсердие; ПЖ-правый желудочек; ЛП - левое предсердие; ЛЖбп-боковая поверхность левого желудочка; ЛЖв-верхушка левого желудочка
Таким образом, было установлено снижение объемной скорости МЦК в стенках всех камер сердца по мере прогрессирования патологических изменений структурно-геометрических параметров ЛЖ при АС.
При корреляционном анализе не было выявлено статистически значимых взаимосвязей между гемодинамическими параметрами (АДС, АДД, АДср) и уровнем МЦК в стенках различных камер сердца до и после коррекции АС.
Было установлено, что у пациентов общей группы при снятии повышенной функциональной нагрузки с левого желудочка (после хирургической коррекции АС) происходит изменение распределения уровня микроциркуляции в стенках различных камер сердца. Это выражается в тенденции к снижению объемной скорости МЦК в стенках всех камер, кроме ПП, где средний уровень МЦК достоверно снижался. При этом МЦК по ЛП имел небольшую тенденцию к повышению на фоне его сниженного уровня до коррекции порока. Такое перераспределение уровня микроциркуляции отражает выявленную в нашем исследовании закономерность изменения МЦК после хирургической коррекции АС. Было отмечено, что величина объемной скорости МЦК после хирургической коррекции в стенках всех камер сердца находится в прямой линейной зависимости от исходного значения микроциркуляции:
МЦК (после операции) =аi +bi *МЦК (до операции).
Разность (∆) между величиной кровотока после хирургической коррекции находилась в обратной линейной зависимости от исходного фона микроциркуляции:
∆ МЦК=ci–di*МЦК (до операции)
Был определен уровень устойчивого равновесия МЦК для каждой камеры сердца, при котором кровоток после коррекции порока не изменялся.
МЦК (устойчивый уровень).=МЦК (до операции)= ci/di.
Если МЦК до операции в какой либо камере сердца был ниже найденной точки устойчивого равновесия, то после коррекции порока, наблюдалось его увеличение и наоборот.
На рисунке 1 представлена зависимость разности между объемной скоростью МЦК по ЛЖбп до и после коррекции порока от исходной величины МЦК до операции.
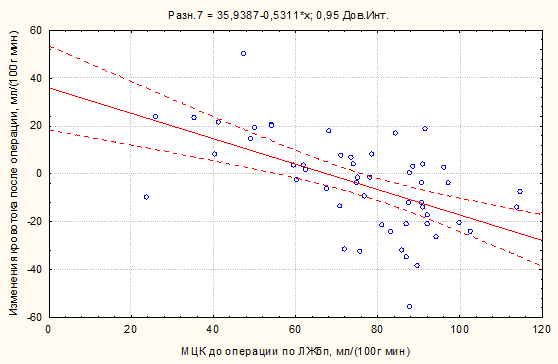
Рис.1. Закономерность изменения микроциркуляторного кровотока по боковой поверхности левого желудочка после хирургической коррекции аортального стеноза в зависимости от его исходных значений
Примечание: МЦК-микроциркуляторный кровоток; ЛЖбп-боковая поверхность левого желудочка
Таким образом, в результате проведенных исследований было выявлено, что у пациентов с АС при снятии повышенной функциональной нагрузки с ЛЖ после хирургической коррекции порока происходит тенденция к снижению объемной скорости МЦК в стенках всех камер сердца, кроме ПП, где средний уровень микроциркуляции достоверно снижался. По ЛП МЦК имел небольшую тенденцию к повышению на фоне его низкого уровня до коррекции порока. При этом по данным ЭхоКГ в раннем послеоперационном периоде происходило уменьшение размеров и объемов левых камер сердца, а также ММЛЖ и индекса ММЛЖ (ИММЛЖ) на 35%.
Фракция выброса наиболее часто применяется в качестве критерия глобальной сократимости миокарда ЛЖ. Нижняя и верхняя границы нормального значения ФВ ЛЖ, по данным различных исследований, колеблются от 50 до 70%. Снижение ФВ ЛЖ ниже 45%, а также увеличение КСР ЛЖ более 55 мм указывает на существенное снижение сократительной функции ЛЖ, где авторы считают данные показатели достоверным прогностическим критерием повышенного риска плохого исхода операции ( с соавт. 1987., Персиянов- с соавт. 2004., Carabello BA., Crawford FA. 1997., Fei H. W. et al. 2004.).
Проанализировав взаимосвязь между МЦК по ЛЖбп и ФВ ЛЖ было установлено, что у пациентов с ФВ ЛЖ от 70% до 45% МЦК по ЛЖбп был наиболее стабильным и не был связан с сократительной функцией ЛЖ. В свою очередь у пациентов с ФВ ЛЖ выше 70% при возрастании МЦК по ЛЖбп отмечалось увеличение ФВ ЛЖ, в то время как в группе с ФВ ниже 45% при снижении МЦК по ЛЖбп отмечалось снижение ФВ ЛЖ.
В зависимости от показателя ФВ ЛЖ все пациенты были разделены на три группы: 1-ю группу (15 человек-24%) составили пациенты с ФВ ЛЖ более 70% (среднее значение – 74,1±0,7%), 2-ю группу составили 31 человек – 52% с ФВ ЛЖ от 70 до 45% (среднее значение - 57,6±1,4%), в 3-ю группу (15 человек-24%), были включены пациенты с низкой сократительной функцией ЛЖ у которых по данным ЭхоКГ сердца ФВ ЛЖ составила ниже 45% (среднее значение – 39,2±1,0%).
В 1-й группе пациентов с изначальной ФВ ЛЖ выше 70%, был выявлен наиболее высокий МЦК не только по ЛЖбп, где уровень микроциркуляции был в пределах 82 мл/100г/мин, но и в стенках остальных камер сердца, включая ПП, ПЖ. Наибольший уровень МЦК был отмечен по ЛЖв и ПЖ. Микроциркуляторный кровоток в стенках всех камер сердца за исключением ЛП составил от 82 до 90 мл/100г/мин, что соответствует увеличению ФВ ЛЖ в ответ на повышенную постнагрузку, которая в среднем составила 74,4+1,7%. В стенке ЛП МЦК был наиболее низким по сравнению с другими камерами сердца, но при этом его значения были выше 70 мл/100г/мин (рис.3).
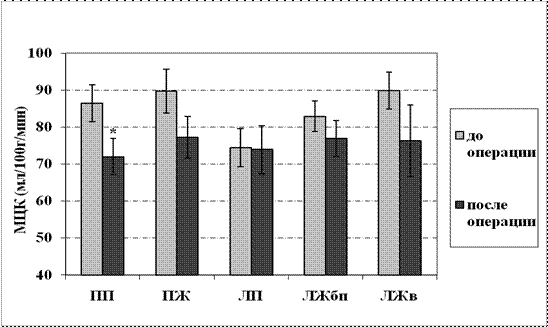
Рис.3. Показатели МЦК (M±m) в стенках различных камер сердца у пациентов с АС 1-ой группы (ФВ ЛЖ выше 70%) до и после хирургической коррекции порока
Примечание: *- достоверность различий с данными до операции (р<0,05); МЦК-микроциркуляторный кровоток; ПП-правое предсердие; ПЖ-правый желудочек; ЛП - левое предсердие; ЛЖбп-боковая поверхность левого желудочка; ЛЖв-верхушка левого желудочка
После хирургической коррекции АС в данной группе наблюдалась тенденция к снижению объемной скорости МЦК по желудочкам с выравниванием МЦК в стенках всех камер сердца. В стенке ЛП уровень микроциркуляции оставался на прежнем уровне (в пределах 74 мл/100г/мин). По ПП происходило достоверное снижение МЦК (рис 3). При этом в ранний послеоперационный период у пациентов 1-ой группы происходило достоверное снижение средних показателей ФВ ЛЖ (с 74,1 до 66,5%) и падение градиента систолического давления между полостью ЛЖ и аортой после снятия повышенной функциональной нагрузки с ЛЖ.
Таким образом, в 1-ой группе пациентов с ФВ ЛЖ выше 70% на фоне развившегося АС выявлен высокий уровень микроциркуляции в стенках всех камер сердца, которое можно объяснить гиперфункцией миокарда ЛЖ в ответ на повышенную нагрузку. Исходя из выше изложенного, можно говорить о компенсированном функциональном состоянии микроциркуляции стенок всех камер сердца на фоне развившегося АС в данной группе.
Во 2-ой группе пациентов с ФВ ЛЖ от 70 до 45% (среднее значение ФВ ЛЖ 57,6±1,4) до коррекции АС отмечался наиболее высокий уровень микроциркуляции в области ЛЖбп – в пределах 75 мл/100г/мин, а также по ПЖ и ЛЖв (выше 80 мл/100г/мин), наиболее низкая объемная скорость МЦК была выявлена в стенке ЛП (p<0.05) по сравнению с остальными камерами сердца. В данной группе наблюдался наибольший градиент МЦК между ЛП и ПЖ, а также между ЛП и ЛЖв (рис. 4).
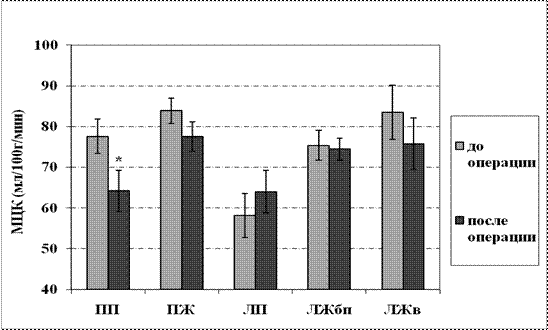
Рис.4. Показатели МЦК (M±m) в стенках различных камер сердца
у пациентов с АС 2-ой группы (ФВ ЛЖ от 70 до 45%) до и после хирургической коррекции порока
Примечание: *- достоверность различий с данными до операции (р<0,05); МЦК-микроциркуляторный кровоток; ПП-правое предсердие; ПЖ-правый желудочек; ЛП - левое предсердие; ЛЖбп-боковая поверхность левого желудочка; ЛЖв-верхушка левого желудочка
После хирургической коррекции АС у данной группы пациентов выявлялась тенденция к снижению МЦК по ЛЖв, ПЖ и выравнивание уровня микроциркуляции в стенках желудочков. Микроциркуляторный кровоток по ЛЖбп практически не менялся и составлял выше 70 мл/100г/мин. Было отмечено достоверное снижение уровня микроцируляции по ПП, а в области ЛП на фоне изначально умеренного снижения МЦК выявлена тенденция к его повышению, в результате чего уровень МЦК по обоим предсердиям был в пределах 64,2мл/100г/мин (рис. 4). Максимальный градиент МЦК между ЛП и ПЖ, а также между ЛП и ЛЖв после коррекции АС снизился и составил в среднем 13,6 и 11,8 мл/100г/мин соответственно.
Таким образом, в результате развившихся структурно-функциональных изменений ЛЖ на фоне АС во 2-ой группе пациентов с ФВ ЛЖ от 70 до 45% до коррекции порока было выявлено умеренное снижение уровня микроциркуляции в стенке ЛП по сравнению с остальными камерами сердца; в стенках ПП и желудочков МЦК был на высоком уровне. После хирургической коррекции порока наблюдалось сохранение градиента МЦК между предсердиями и желудочками, где уровень микроциркуляции сохранялся на высоком уровне в области ЛЖбп, ЛЖв и ПЖ.
В 3-ей группе пациентов с ФВ ЛЖ ниже 45% до коррекции АС было выявлено умеренное снижение МЦК по ЛЖбп (ниже 70 мл/100г/мин) и значительное снижение уровня микроциркуляции в стенке ЛП (ниже 40 мл/100г/мин) по сравнению с пациентами из 1-ой и 2-ой групп с более высокой ФВ ЛЖ. При этом в данной группе МЦК по ЛЖв и ПЖ сохранялся достаточно высоким – чуть выше 70 мл/100г/мин (рис.5).
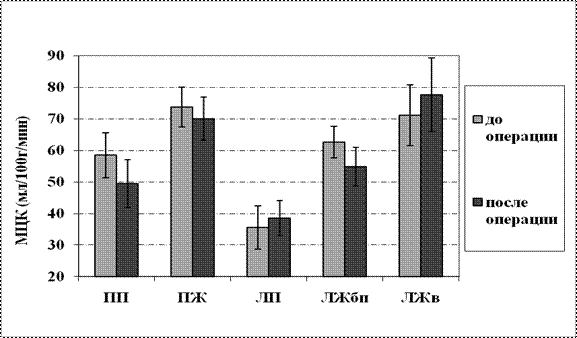
Рис.5. Показатели МЦК (M±m) в стенках различных камер сердца
у пациентов с АС 3-ей группы (ФВ ЛЖ ниже 45%) до и после хирургической коррекции порока
Примечание: МЦК-микроциркуляторный кровоток; ПП-правое предсердие; ПЖ-правый желудочек; ЛП - левое предсердие; ЛЖбп-боковая поверхность левого желудочка; ЛЖв-верхушка левого желудочка
Низкий уровень микроциркуляции в стенках левых отделов сердца сопровождался выраженной гипертрофией ЛЖ со значительным увеличением абсолютных и индексированных его размеров и объемов, а также выраженным увеличением ММЛЖ, ИММЛЖ и размеров обоих предсердий по сравнению с нормой.
После коррекции АС в стенках левых отделов сердца в данной группе МЦК оставался сниженным. Уровень микроциркуляции в области ЛЖбп имел тенденцию к снижению по сравнению с данными до операции и составил около 55 мл/100г/мин.
Таким образом, в 3-ей группе пациентов с низкой ФВ ЛЖ после коррекции АС и снятия повышенной функциональной нагрузки с ЛЖ не происходило выравнивания МЦК в стенках камер сердца с сохранением высокого градиента уровня микроциркуляции между предсердиями и желудочками: средние показатели МЦК составившие от 70 мл/100г/мин и выше отмечены только по ПЖ и ЛЖв, уровень микроциркуляции в стенках предсердий и ЛЖбп оставался невысоким с наиболее резким его снижением по ЛП.
Сниженной в ближайшие сроки после коррекции порока оставалась и ФВ ЛЖ, что соответствовало сохранению увеличенных размеров и объемов левых отделов сердца в ближайший послеоперационный период.
Сравнительный анализ трех групп пациентов в зависимости от ФВ ЛЖ показал, что МЦК до коррекции порока в стенках всех камер сердца был наиболее низким в 3-ей группе с ФВ ЛЖ ниже 45%. В области верхушки ЛЖ во всех группах уровень микроциркуляции был высоким – более 70 мл/100г/мин (рис.6).
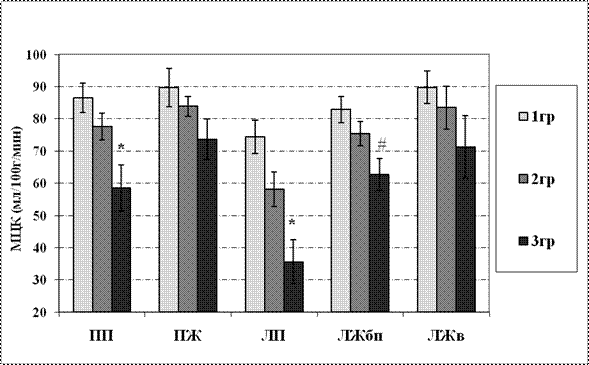
Рис.6. Микроциркуляторный кровоток (M±m) в стенках различных камер сердца до хирургической коррекции аортального стеноза
в 1-ой, 2-ой и 3-ей группах
Примечание: * – достоверность различий с 1-ой и 2-ой группами; # – достоверность различий с 1-ой группой; МЦК-микроциркуляторный кровоток; ПП-правое предсердие; ПЖ-правый желудочек; ЛП - левое предсердие; ЛЖбп-боковая поверхность левого желудочка; ЛЖв-верхушка левого желудочка
После коррекции АС наиболее низкий уровень МЦК в стенках всех камер сердца также был отмечен у пациентов 3-ей группы, кроме ЛЖв (рис.7). Статистически значимые различия уровня МЦК были отмечены по ЛП и ЛЖбп между 3-ей группой и двумя другими (p<0.05). Микроциркуляторный кровоток в стенке ПП в 3-ей группе статистически значимо был ниже, чем в 1-ой группе с высокой ФВ ЛЖ (p<0.05).
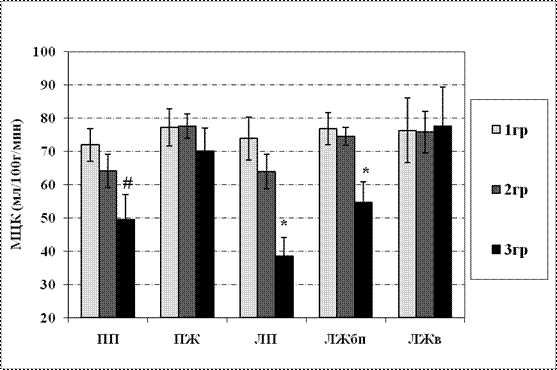
Рис.7. Микроциркуляторный кровоток (M±m) в стенках различных камер сердца после хирургической коррекции аортального стеноза
в 1-ой, 2-ой и 3-ей группах
Примечание: * – достоверность различий с 1-ой и 2-ой группами; # – достоверность различий с 1-ой группой; МЦК-микроциркуляторный кровоток; ПП-правое предсердие; ПЖ-правый желудочек; ЛП - левое предсердие; ЛЖбп-боковая поверхность левого желудочка; ЛЖв-верхушка левого желудочка
На фоне развившегося АС ремоделированию подвергаются не только ЛЖ, но и остальные камеры сердца. Миогенная дилатация ЛЖ вовлекает в патологический процесс ЛП, в котором происходит повышение давления и увеличение размеров данной камеры. При этом следует выделить изменение уровня микроциркуляции после коррекции порока в стенке ЛП, где он изначально был умеренно снижен во 2-ой группе и в большей степени в 3-ей группе пациентов (с низкой ФВ ЛЖ). После хирургической коррекции порока МЦК по ЛП в 1-ой группе не менялся. Во 2-ой и особенно в 3-ей группе МЦК в стенке ЛП исходно был сниженным, а после операции имел небольшую тенденцию к повышению. Снижение МЦК по ЛП во 2-ой и 3-ей группах как до, так и после коррекции АС является следствием повышенной нагрузки на данный отдел, развившейся на фоне дисфункции ЛЖ Следствием этого также явилось развитие гипертензии малого круга кровообращения – так, в 3-ей группе было отмечено наиболее высокое давление в легочной артерии, которое составляло в среднем 46,4 мм рт. ст.
Таким образом, в 1-ой группе пациентов с ФВ ЛЖ выше 70% после хирургической коррекции АС происходит снижение МЦК и равномерное распределение уровня объемной скорости микроциркуляции в стенках всех камер сердца, во 2-ой группе с ФВ ЛЖ от 70% до 45% отмечено сохранение градиента МЦК между предсердиями и желудочками с наиболее высоким уровнем микроциркуляции по ПЖ и ЛЖ. В 3-ей группе пациентов с ФВ ЛЖ ниже 45% наблюдался наиболее выраженный градиент МЦК по предсердиям и желудочкам с достоверно более низким уровнем микроциркуляции по ЛЖбп и ЛП. Следует подчеркнуть, что объемная скорость МЦК в области верхушки ЛЖ во всех группах оставалась на достаточно высоком уровне – от 75 до 77 мл/100г/мин, также как и по ПЖ, где уровень микроциркуляции не опускался ниже 70 мл/100г/мин.
После хирургической коррекции АС градиент систолического давления между полостью ЛЖ и аортой статистически значимо снижался по всем группам практически не отличаясь между собой и не зависел от ФВ ЛЖ. Следует также отметить, что выраженность гипертрофии ТЗСЛЖ и ТМЖП оставались постоянной как до, так и после операции во всех трех группах, так как для регрессии гипертрофии требуется продолжительный временной интервал.
При сравнительной оценке данных ЭхоКГ было выявлено, что в 3-ей группе пациентов с низкой ФВ ЛЖ до коррекции АС наряду с более низким МЦК в стенках всех камер сердца отмечены самые высокие абсолютные и индексированные показатели размеров и объемов ЛЖ: КДР, КСР, КДО, КСО, ИКДР, ИКСР, ИКДО, ИКСО, а также размеры предсердий. В ближайший послеоперационный период в данной группе происходило статистически значимое уменьшение абсолютных и индексированных показателей ЛЖ, но при этом они оставались достоверно выше, чем в 1-ой и во 2-ой группах.
Развившаяся гипертрофия миокарда ЛЖ на фоне АС вначале имеет положительное значение, так как позволяет сохранить функцию органа, несмотря на заболевание. Этот период называется стадией компенсации. По мере нарастания массы органа, возникает относительная недостаточность его кровоснабжения – хроническая ишемия. В дальнейшем, когда в органе возникают дистрофические изменения, происходит ослабление функции и, в конечном счете, когда адаптационные механизмы исчерпаны, наступает декомпенсация органа. Применительно к сердцу – развивается сердечная недостаточность (Allard M. F., Lopaschuk G. D. 1996.).
В нашем исследовании вышесказанные морфологические изменения в гипертрофированном сердце на фоне АС отражены в нарушении МЦК в стенках предсердий и ЛЖбп в 3-ей группе пациентов с низкой ФВ ЛЖ, что позволяет говорить о срыве компенсаторных механизмов функционального состояния микрососудистой системы.
Таким образом, на основании полученных нами результатов мы можем выделить 3 стадии изменений состояния МЦК в стенках камер сердца у пациентов с АС, соответствующим трем состояниям сократительной функции ЛЖ: 1–я стадия характеризуется наиболее высокой объемной скоростью МЦК в стенках предсердий и желудочков (выше 70 мл/100г/мин) на фоне нормальных величин размеров и объемов ЛЖ, что соответствует высокой ФВ ЛЖ (выше 70%), это можно назвать стадией компенсации системы микроциркуляции, 2-я стадия характеризуется исходным умеренным снижением уровня микроциркуляции в стенке ЛП (ниже 60 мл/100г/мин) при умеренной дилатации полости ЛЖ (до 25% выше нормы), что соответствует показателям ФВ ЛЖ от 70 до 45% – стадия субкомпенсации, 3-я стадия характеризуется снижением объемной скорости МЦК в стенке ЛЖ (ниже 70 мл/100г/мин), а также ПП (ниже 60 мл/100г/мин) и выраженным снижением МЦК в стенке ЛП (ниже 40 мл/100г/мин) при выраженной дилатации полости ЛЖ (до 80% выше нормы), что сопровождалось снижением сократительной функции ЛЖ – стадия декомпенсации.
Проведя сравнительную оценку по количеству осложнений в сердечно-сосудистой системе, возникшие в ранний послеоперационный период по всем трем группам было выявлено, что в 3- ей группе пациентов с низкой ФВ ЛЖ наряду со снижением объемной скорости МЦК в стенках предсердий и ЛЖбп и значительно увеличенных размеров и объемов камеры ЛЖ было отмечено наибольшее количество осложнений, что составило 46% случаев в виде нарушения ритма, а также возникновения острой сердечной недостаточности.
Таким образом, полученные результаты по исследованию уровня микроциркуляции в стенках различных камер сердца у пациентов с АС методом лазер-допплер-флоуметрии позволяют оценить функциональное состояние микроциркуляторного кровотока и определить стадию его изменения.
ВЫВОДЫ
1. Состояние микроциркуляции в стенках камер сердца у пациентов с аортальным стенозом характеризуется наиболее низкой объемной скоростью микроциркуляторного кровотока в стенке левого предсердия по сравнению с остальными камерами. Низкая объемная скорость микроциркуляторного кровотока в стенке левого предсердия сопряжена с высокой степенью гипертрофии левого желудочка.
2. Прогрессирование патологических изменений структурно-геометрических параметров левого желудочка при аортальном стенозе характеризуется стадийным изменением состояния микроциркуляторного кровотока в стенках камер сердца:
1-ая стадия характеризуется наиболее высокой объемной скоростью кровотока в стенках предсердий и желудочков (выше 70 мл/100г/мин) на фоне нормальных величин наружных размеров и объемов левого желудочка (стадия компенсации),
2-ая стадия выражается снижением объемной скорости кровотока в стенке левого предсердия (ниже 60 мл/100г/мин), при умеренной дилатации полости левого желудочка (до 25 % выше нормы) (стадия субкомпенсации),
3-я стадия характеризуется снижением объемной скорости микроциркуляторного кровотока в стенке левого желудочка (ниже 70 мл/100г/мин), а также правого предсердия (ниже 60 мл/100г/мин) и наибольшим снижением уровня микроциркуляции в стенке левого предсердия (ниже 40 мл/100г/мин) при выраженной дилатации полости левого желудочка (до 80 % выше нормы) (стадия декомпенсации).
3. Состояние микроциркуляции в стенках предсердий и желудочков взаимосвязано с фракцией выброса левого желудочка, и проявляется снижением объемной скорости микроциркуляторного кровотока при низкой сократительной способности левого желудочка.
4. Изменение состояния микроциркуляторного кровотока в стенках предсердий и желудочков у пациентов с аортальным стенозом после оперативного вмешательства имеет обратную корреляционную зависимость с исходным уровнем микроциркуляции: при исходно высокой объемной скорости микроциркуляторного кровотока регистрировали ее снижение, при исходно низком уровне микроциркуляции происходило увеличение объемной скорости микроциркуляторного кровотока, что характеризует оптимизацию уровня микроциркуляции после коррекции порока.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. С целью интраоперационной оценки состояния микроциркуляции в стенках различных камер сердца у кардиохирургических больных рекомендуется использовать лазер-допплер-флоуметрию, как быстродействующий, прямой, количественный метод определения величины перфузии крови в ткани в реальном масштабе времени в мл на 100 г ткани в мин. до и после хирургической коррекции порока. Для этого необходимо произвести два измерения на работающем сердце. Первое измерение - до подключения аппарата искусственного кровообращения на субъэпикарде каждой камеры сердца. Повторное – на тех же участках стенок камер сердца сразу же после хирургической коррекции порока и отключения аппарата искусственного кровообращения до ушивания грудной клетки. При этом одновременно с измерением микроциркуляции необходимо регистрировать артериальное давление и ЧСС в режиме «on line».
2. Для прогнозирования характера раннего послеоперационного периода следует ориентироваться на стадию изменения состояния микроциркуляции в стенках камер сердца. Снижение объемной скорости микроциркуляторного кровотока ниже 40 мл/100г/мин характеризует декомпенсированное состояние микроциркуляции и повышает риск возникновения осложнений в сердечно-сосудистой системе.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1. Исследование функциональной работоспособности миокарда и микроциркуляции в разных отделах сердца у больных с аортальным стенозом и аортальной недостаточностью при хирургической коррекции / , , , // Бюллетень НЦССХ им. РАМН «Сердечно-сосудистые заболевания»: Тезисы докладов одиннадцатого всероссийского съезда сердечно-сосудистых хирургов. – 2005. – №5. – С.48.
2. Микроциркуляция миокарда у больных с аортальным пороком при эксцентрической и концентрической гипертрофии левого желудочка / , , , , // Бюллетень НЦССХ им. РАМН «Сердечно-сосудистые заболевания»: Тезисы докладов десятой ежегодной сессии научного центра сердечно-сосудистой хирургии им. Бакулева РАМН с всероссийской конференцией молодых ученых. – 2006. – №3. – С.36.
3. Интраоперационная оценка эффективности коррекции аортального порока по данным лазер-допплеровской флоуметрии / , , , , . // Пятые научные чтения, посвященные памяти акад. РАМН , с международным участием. Юбилейная конференция и Первый съезд кардиохирургов Сибирского федерального округа. Тезисы докладов. – Новосибирск, 2006. – С. 42.
4. Миокардиальный кровоток левого желудочка и гемодинамика у пациентов с аортальным пороком до и после хирургической коррекции / , , , , // Бюллетень НЦССХ им. РАМН «Сердечно-сосудистые заболевания»: Тезисы докладов двенадцатого всероссийского съезда сердечно-сосудистых хирургов. – 2006. – №5. – С.34.
5. Исследование микроциркуляции у больных с аортальным пороком до и после коррекции / , , , , // Патология кровообращения и кардиохирургия. – 2006. – №2. – С. 27–34.
6. Микроциркуляторный кровоток различных камер сердца у больных с аортальным пороком при кристаллоидной и кустодиоловой кардиоплегии / , , , // Бюллетень НЦССХ им. РАМН «Сердечно-сосудистые заболевания» (приложение): Тезисы докладов одиннадцатой ежегодной сессии научного центра сердечно-сосудистой хирургии им. РАМН с всероссийской конференцией молодых ученых. – 2007. – №3. – С. 121
7. Предварительные данные по сравнительной характеристике микроциркуляции в эпикарде и миокарде левого желудочка сердца у пациентов с аортальным и митральным пороком до и после хирургического лечения / , , , // Бюллетень НЦССХ им. РАМН «Сердечно-сосудистые заболевания»: Тезисы докладов тринадцатого всероссийского съезда сердечно-сосудистых хирургов. – 2007. – №6. – С. 38.
8. Интраоперационные исследования субэпикарлиального и миокардиального кровотока по левому и правому желудочкам у больных с аортальным пороком до и после операции / // Бюллетень НЦССХ им. РАМН «Сердечно-сосудистые заболевания»: Тезисы докладов тринадцатого всероссийского съезда сердечно-сосудистых хирургов. – 2007. – №6. – С. 343.
9. Оценка микроциркуляторного кровотока различных камер сердца у пациентов с аортальным стенозом до и после коррекции порока в зависимости от фракции выброса левого желудочка / , , , , -Прокофьев, .// Патология кровообращения и кардиохирургия. – 2008. – №3. – С. 16-22. (Журнал из списка ВАК)
10. Перестройка микроциркуляторного кровотока различных камер сердца после хирургической коррекции аортального стеноза / , , , , -Прокофьев, // Патология кровообращения и кардиохирургия. – 2008. – №4. – С. 18-23. (Журнал из списка ВАК)
11. Интраоперационное исследование микроциркуляторного кровотока у больных с аортальным стенозом и низкой фракцией выброса левого желудочка до и после хирургической коррекции порока / , , , , -Прокофьев, , // Бюллетень НЦССХ им. РАМН «Сердечно-сосудистые заболевания» (приложение): Тезисы докладов четырнадцатого всероссийского съезда сердечно-сосудистых хирургов. – 2008. – №6. – С. 53.
12. Микроциркуляторный кровоток миокарда и субэпикарада у пациентов с аортальным пороком до и после хирургической коррекции порока / , , , // Патология кровообращения и кардиохирургия. – 2009. – №3. – С. 25-29. (Журнал из списка ВАК)
13. Интраоперационное исследование микроциркуляторного кровотока камер сердца у пациентов с аортальным стенозом в зависимости от систолической функции левого желудочка / , , , , // Кардиология и сердечно-сосудистая хирургия. – 2010. – №2. – С. 58-62. (Журнал из списка ВАК)
14. Интраоперационное исследование микроциркуляции различных отделов сердца после коррекции аортального стеноза и оценка ранних послеоперационных осложнений / , , // Бюллетень НЦССХ им. РАМН «Сердечно-сосудистые заболевания» (приложение): Тезисы докладов четырнадцатой ежегодной сессии научного центра сердечно-сосудистой хирургии им. РАМН с всероссийской конференцией молодых ученых. – 2010. – №3. – С. 26.
СПИСОК СОКРАЩЕНИЙ:
АП – аортальный порок
АС – аортальный стеноз
ЛДФ – лазер-допплер-флоуметрия
МЦК – микроциркуляторный кровоток
∆ МЦК – разность МЦК (МЦК после операции – МЦК до операции)
ЭхоКГ – эхокардиография
ФВ – фракция выброса
ЛЖ – левый желудочек
ЛЖбп – боковая поверхность левого желудочка
ЛЖв –верхушка левого желудочка
ПЖ – правый желудочек
ЛП – левое предсердие
ПП – правое предсердие
ГЛЖ – гипертрофия левого желудочка
АДС – систолическое артериальное давление
АДД – диастолическое артериальное давление
ЧСС – частота сердечных сокращений
КДО – конечный диастолический объем
ИКДО – индекс конечного диастолического объема
КДР – конечный диастолический размер
ИКДР – индекс конечного диастолического размера
КСО – конечный систолический объем
ИКСО – индекс конечного систолического объема
КСР – конечный систолический размер
ИКСР – индекс конечного систолического размера
ММ ЛЖ – масса миокарда левого желудочка
ИММ ЛЖ – индекс массы миокарда левого желудочка
ТЗСЛЖ – толщина задней стенки левого желудочка
ТМЖП – толщина межжелудочковой перегородки
Соискатель


