Задания для школьного тура Всероссийской олимпиады по химии
Дата проведения: 9.10.2009 г
Время выполнения по всем параллелям 60 минут.
8-I. Имеется смесь порошков поваренной соли, песка, серы и железа. Предложите способ разделения этой смеси, который позволит выделить каждое вещество в индивидуальном виде.
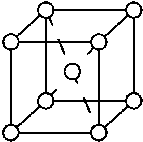
8-II. Металлическое железо образует объемноцентрированную кубическую решетку, одна ячейка которой изображена на рисунке (один атом в центре куба и восемь атомов в вершинах куба). Расстояние между центром и вершиной куба 0,247 нм (1 нм = 10-9 м). Масса атома железа 9,03 · 10-23 г. Рассчитайте плотность металлического железа.
8-III. Каждая приведенная ниже фраза имеет только одно правильное окончание. Укажите его.
1. Дальтонизм, это:
а) научная школа; б) точка зрения; в) болезнь; г) философское учение.
2. Первым философский камень получил:
а) Демокрит; б) Аристотель; в) Карл Маркс; г) никто.
3. Масса покоя атома - величина
а) относительная; б) абсолютная; в) периодическая; г) мнимая.
4. писал: <Периодическому закону будущее не грозит:
а) разрушением; б) покушением; в) предвкушением; г) развитием>.
5. Ломоносов открыл закон:
а) Кулона; б) исключенного третьего; в) сохранения массы; г) о всеобщей воинской
обязанности.
6. Больше всего в воздухе содержится:
а) азота; б) кислорода; в) озона; г) углекислого газа.
7. Отношение массы части к массе целого есть:
а) массовая доля; б) целая доля; в) тяжелая доля; г) тяжелая женская доля.
9-I. Красящий пигмент оранжевой краски – свинцового сурика – имеет состав Pb3O4.
1. Какова возможная степень окисления свинца в этом соединении?
2. К какому классу химических соединений можно отнести это вещество?
3. При взаимодействии свинцового сурика с углем можно получить металлический свинец. Напишите уравнение реакции.
4. Сколько г свинца можно получить из 6,85 г сурика, если выход реакции от теоретически возможного составляет 97%?
9-II. Поставьте приведенные формулы химических веществ в соответствие с областями их применения, указанными ниже. (Решение можно записать в виде "число-буква").
AgBr / абразивный материал А BN / боевое отравляющее вещество Б C12H25SO3Na / действующее вещество в изолирующих противогазах В CaSO4 · 0,5H2O / детская присыпка Г CCl2F2 / компонент моющих средств Д ClCN / компонент порохов Е KAl(SO4)2 · 12H2O / наполнитель электроламп Ж Kr / основа искусственных драгоценных камней З Na2O2 / пигмент масляных красок И Na2S2O3 · 5H2O / протрава при крашении тканей К Pb3O4 / светочувствительное вещество (фотография) Л S / строительный материал М ZnO / фиксаж (фотография) Н ZrO2 / хладагент О9-III. Заполните пропуски (вещества вместо... и коэффициенты вместо _) в уравнениях химических реакций.
1... + 5... = 3... + 4+ 11O2 = 2... + 8SO2 3Cl2 + 6... = ... + 5KCl + _H2O ... + 6H2O = _Mg(OH)2 + 2NH3 ... + 3... = 3HCl + H3PO4 _FeSO4 + _KMnO4 + _H2SO4 = _MnSO4 + _... + _K2SO4 + _ H2O1. Даны правые части уравнений химических реакций. Каждое из них описывает взаимодействие двух веществ. Запишите эти уравнения полностью.
= NaOH + NH3
= I2 + 2 FeCl2 + 2 KCl
= CO2 + 2HCl
= 2 FeSO4 + 2H2 + 9CO
= Fe(NO3)3 + 2NO + CO2
= 2NaHSO4 + SO2 + S + 2H2O
= 2K2CO3 + O2
= 2 Cu(NO3)2 + 2NO2 + 3H2O
= 4 Al(OH)3 + 3CH4
= LiCl + AlCl3 + 4H2
2. Рассчитайте объем (в литрах при н. у.) оксида углерода (IV), образующегося при взаимодействии 6 л (н. у.) ацетилена и 18 л (н. у.) кислорода.
3. Составьте все возможные изомеры состава вещества С5Н10 и назвать их в соответствии с номенклатурой.
1. Образец сплава цинка с алюминием массой 10,0 г растворили в избытке соляной кислоты. При этом выделилось 7,03 л газа (приведено к н. у.).
Определите массовые доли металлов в сплаве. Какое количество газа выделится при растворении того же сплава в горячем растворе концентрированной щелочи?
2. Расшифруйте вещества Х1,Х2 и Х3 в схеме превращений
СН3СООС2Н5 → Х1 → Х2 →Х3 → С4Н10 .
Приведите уравнения соответствующих реакций.
3.Смесь двух солей - иодида и хлорида натрия массой 208,34 г – растворили в воде и через полученный раствор пропустили избыток хлора. Затем раствор выпарили и остаток прокалили до постоянной массы, которая составила 116,88 г. определите массовые проценты солей исходной смеси.
Решение
8 класс.
8-I. Каждый ответ оценивается в 2 балл. Итого 6 баллов.
Имеется смесь порошков поваренной соли, песка, серы и железа. Предложите способ разделения этой смеси, который позволит выделить каждое вещество в индивидуальном виде. |
| Для начала смесь нужно поместить в воду. При этом соль растворится, а все остальное — нет. Сера всплывет, ее нужно аккуратно собрать, промыть водой и высушить. Раствор отфильтровать. Фильтрат выпарить досуха, и полученную при этом соль высушить. На фильтре останется смесь железа и песка. В принципе, если смесь высушить и высыпать на бумажку, железо можно отделить магнитом. |
8-II. Итоговый балл – 8 баллов.
Металлическое железо образует объемноцентрированную кубическую решетку, одна ячейка которой изображена на рисунке (один атом в центре куба и восемь атомов в вершинах куба). Расстояние между центром и вершиной куба 0,247 нм (1 нм = 10-9 м). Масса атома железа 9,03 · 10-23 г. Рассчитайте плотность металлического железа.
|
Плотность вещества — это отношение массы к объему. Таким образом, нужно найти объем ячейки и массу ячейки. Объем ячейки — это объем куба a3. Большая диагональ куба 2 · 0,247 · 10-9 м = 4,94 · 10-10 м. Сторона куба a = d/(3 - 1/2) (это легко найти по теореме Пифагора) = 2,85 · 10-10 м. Объем куба a3 = 2,315 · 10-29 м3 = 2,315 · 10-23 см3. Число атомов железа в ячейке = 1 (в центре) + 1/8 · 8 (в вершинах) = 2. Масса 2 · 9,03 · 10-23 г = 1,803 · 10-22 г. Плотность 1,803 · 10-22 г / 2,315 · 10-23 см3 = 7,79 г/см3. |
8-III. Каждый ответ оценивается в 1 балл. Итого 7 баллов.
1-в, 2-г, 3-б, 4-а, 5-в, 6-а, 7-а.
9 класс
9-I. Каждый пункт оценивается в 1 балл. Итого 4 балла.
1) Pb2PbO4 - степени окисления +2 и +4 или (не совсем верное, но оценивается) Pb(PbO2)2 Степени окисления свинца +2 и +3
2) Это свинцовая соль свинцовой (свинцовистой) кислоты
3) Pb3O4 + 2 C = 3 Pb + 2 CO2
4) 6,85 г составляет 0,01 моль сурика; из него получится 0,01 моль или 6,21 г свинца. С учетом выхода 6,21 г свинца х 0,97 = 6,02 г
9-II. Каждый правильный ответ оценивается в 1 балл. Итого 14 баллов.
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
9-III. Каждое правильное уравнение оценивается в 2 балла. Итого 12 баллов.
.Заполните пропуски (вещества вместо... и коэффициенты вместо _) в уравнениях химических реакций. 1... + 5... = 3... + 4+ 11O2 = 2... + 8SO2 3Cl2 + 6... = ... + 5KCl + _H2O ... + 6H2O = _Mg(OH)2 + 2NH3 ... + 3... = 3HCl + H3PO4 _FeSO4 + _KMnO4 + _H2SO4 = _MnSO4 + _... + _K2SO4 + _ H2O |
| C3H8 + 5O2 = 3CO2 + 4H2O 4FeS2 + 11O2 = 2Fe2O3 + 8SO2 3Cl2 + 6KOH = KClO3 + 5KCl + 3H2O Mg3N2 + 6H2O = 3Mg(OH)2 + 2NH3 POCl3 + 3H2O = 3HCl + H3PO4 10FeSO4 + 2KMnO4 + 8H2SO4 = 2MnSO4 + 5Fe2(SO4)3 + K2SO4 + 8H2O |
10 класс
1. Каждое уравнение оценивается в 1 балл. Итого 10 баллов.
NaNH2 + H2O = NaOH + NH3
2 FeCl3 + 2 KI = I2 + 2 FeCl2 + 2 KCl
COCl2 + H2O = CO2 + 2HCl
Fe2(CO)9 + 2 H2SO4 = 2 FeSO4 + 2H2 + 9CO
FeCO3 + NO2 = Fe(NO3)3 + 2NO + CO2
Na2S2O3 + 2 H2SO4 = 2 NaHSO4 + SO2 + S + H2O
2 K2O2 + 2 CO2 = 2K2CO3 + O2
Cu2O + 6 HNO3 = 2 Cu(NO3)2 + 2NO2 + 3H2O
Al4C3 + H2O = 4 Al(OH)3 + 3CH4
LiAlH4 + 4 HCl = LiCl + AlCl3 + 4H2
2. Оценивается в 3 балла.
Условию задания соответствует уравнение реакции
СН ≡ СН + 5/2 О2 → 2 СО2 + Н2О
Для полного сгорания ацетилена необходимо, чтобы выполнялось мольное (объемное) отношение ацетилена: кислород = 1: 2,5. В условии задания это отношение равно 6:18=1:3, т. е. кислород находится в избытке и ацетилен полностью сгорает. На 1 моль сгоревшего ацетилена образуется 2 моль СО2. при сгорании 6л ацетилена соответственно образуется 12 л оксида углерода (IV).
3. За каждый составленный изомер определяется 0,5 балла.
11 класс
1. Итоговый балл – 5.
w(Zn) = 60%
w(Al) = 40% (колебания в пределах 2% принимаются за правильный ответ)
При растворении в щелочи выделится 14,06 л (0,626 моль) газа.
2.Итоговый балл-4.
1.СН3СООС2Н5 + NaOH → CH3- COONa + C2H5OH
2.C2H5OH→ C2H4 + H2O
3.C2H4+HBr→ C2H5Br
4.C2H5Br
+ 2Na → C4H10
C2H5Br
Таким образом, зашифрованными веществами являются: Х1-этанол, Х2- этилен, Х3 –этилбромид.
3. Итоговый балл – 6.
Исходная смесь содержит 58,4 г NaCl и 149,94 г NaI, или в массовом отношении: NaCl – 28 мас. %, NaI – 72 мас.%.



