Студент:
Группа:
Дата сдачи работы:
Лабораторная работа № 1
ОПРЕДЕЛЕНИЕ МОЛЯРНОЙ МАССЫ ЭКВИВАЛЕНТА МЕТАЛЛА
Цель работы:
Установка для измерения молярной массы эквивалента металла (эвдиометр):
Основные понятия: химический эквивалент, молярная масса химического эквивалента.
Основные законы, используемые для определения молярной массы эквивалента металла:
Закон эквивалентов:
![]() ,
,
где mM – масса металла; ![]() – измеренный объем водорода;
– измеренный объем водорода; ![]() – молярный объем химического эквивалента водорода при условиях опыта.
– молярный объем химического эквивалента водорода при условиях опыта.
Объединенный газовый закон:
![]() ,
,
где ![]() – парциальное давление водорода в закрытой бюретке; Т – температура, при которой проводится эксперимент;
– парциальное давление водорода в закрытой бюретке; Т – температура, при которой проводится эксперимент; ![]() – молярный объем химического эквивалента водорода при нормальных условиях (Т0= 273,15 К; Р0= 101,3 кПа = 760 мм рт. ст.). Так как число эквивалентности водорода zэкв = 2, то
– молярный объем химического эквивалента водорода при нормальных условиях (Т0= 273,15 К; Р0= 101,3 кПа = 760 мм рт. ст.). Так как число эквивалентности водорода zэкв = 2, то ![]() =
= ![]() =
=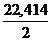 = 11,207 л/моль
= 11,207 л/моль
Закон Дальтона:
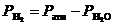 ,
,
где ![]() – давления насыщенного водяного пара при температуре опыта.
– давления насыщенного водяного пара при температуре опыта.
Расчетная формула молярной массы химического эквивалента металла:
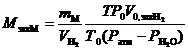 .
.
Относительная ошибка эксперимента:
h =½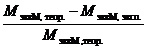 ½100%.
½100%.
Таблица. Условия проведения опыта, результаты измерений и расчетов
№ | Условия проведения опыта | Результаты измерений | ||||
опыта | Т, К | Ратм, мм рт. ст. |
мм рт. ст. | mM, г | hнач, мл | hкон, мл |
1 | ||||||
2 | ||||||
№ | Результаты | расчетов | ||||
опыта |
мм рт. ст. |
мл | МэквМ, эксп г/моль |
г/моль | МэквМ, теор г/моль | h |
1 | ||||||
2 |
Расчеты:
Уравнение реакции:
Выводы: (указывают металл, его молярную массу эквивалентна, определенную в ходе опыта, и относительную ошибку эксперимента)
Создатель документа



