ЛАБОРАТОРНАЯ РАБОТА № 9
Определение электродных потенциалов металлов и ЭДС гальванических элементов.
I. Разделы теоретического курса для повторения.
Возникновение скачка потенциала на границах раздела металл - вода, металл - раствор соли металла. Стандартный водородный электрод. Понятие о гальванических элементах и процессах, протекающих на электродах. Стандартные электродные потенциалы металлов. Ряд стандартных электродных потенциалов. Выводы из положения металла в ряду. Уравнение Нернста. Обратимые и необратимые электроды. Металлические электроды I и II рода, окислительно-восстановительные электроды, газовые электроды. Электроды сравнения. Химические и концентрационные гальванические элементы. Электродвижущая сила (ЭДС) гальванических элементов. Процессы, протекающие на электродах при работе гальванического элемента.
3. Вопросы и упражнения.
1. Чему равен потенциал серебряного электрода, погруженного в раствор соли серебра с концентрацией
См = 10-2 моль/л?
2. Как зависит величина потенциала водородного электрода от рН среды? Чему равен потенциал водородного электрода при рН = I; рН = 7, рН = 10?
3. Рассчитайте потенциал стандартного серебряного электрода по отношению к:
а) насыщенному каломельному электроду,
б) насыщенному медно - сульфатному электроду,
в) насыщенному хлорсеребряному электроду?
4. Составьте схемы гальванических элементов, в которых протекают реакции:
а) 2Ag+ + Cu 0 → Ag 0 + Cu+2
б) Cd 0 + CuSO4 → CdSO4 + Cu
5. Определите величину ЭДС и укажите процессы, протекающие на электродах в следующих гальванических элементах:
а) Zn /ZnSО4 // CdSО4 / Сd
б) Рb/ Рb(NOз)2) // AgNО3/ Ag
6. Рассчитайте ЭДС следующего концентрационного гальванического элемента:
а) Zn/ZnCI2 //ZnCI2 /Zn
0,01 моль/л 1,0 моль/л
Какой из электродов является анодом, а какой - катодом?
3. Экспериментальная часть
1. Определение величины стандартного электродного потенциала цинка.
Соберите цинковый электрод (Zn/ZnSO4), погрузив хорошо зачищенный наждачной бумагой цинковый стержень в раствор соли с концентрацией ионов цинка I моль/л.

Рис.I. Схема установки для определения величины электродного потенциала металла.
1 - исследуемый электрод (цинковый, медный и др.)
2 - хлорсеребряный электрод сравнения
3 - потенциометр.
4 - стаканчик насыщенным раствором хлорида калия
В соответствии с рис.1, соберите гальванический элемент из исследуемого цинкового электрода (Zn/ZnSO4) и насыщенного хлорсеребряного электрода сравнения (KCl/AgCl/Ag):
Условная запись этого гальванического элемента:
( - ) Zn/ZnSO4//KCl/AgCl/Ag ( + )
Для этого носики электродов погружают в стаканчик с раствором хлорида калия, а сами электроды с помощью соединительных проводов подключают к соответствующим клеммам потенциометра.
Потенциал насыщенного хлорсеребряного электрода сравнения по отношению к стандартному водородному электроду равен +0,201В.
Ехл. сер. нас.= +0,201В или 201мВ.
В соответствии с инструкцией о порядке измерений при использовании соответствующего потенциометра определите ЭДС составленного гальванического элемента и потенциал цинкового электрода по насыщенному хлорсеребряному электроду.
Зная величину потенциала электрода сравнения, рассчитайте величину потенциала цинкового электрода по отношению к стандартному водородному электроду. Сравните полученное значение с табличным значением:
E0 = - 0,76 B.
Запишите найденные значения:
- измеренное значение Э. Д.С. гальванического элемента, составленного из стандартного цинкового электрода и насыщенного хлорсеребряного электрода сравнения:
Э. Д.С. (Zn/ZnSO4//KCl/AgCl/Ag) =
- экспериментальное значение потенциала стандартного цинкового электрода по отношению к насыщенному хлорсеребряному электроду сравнения:
E ( ) по хлор - серебряному насыщ.. =
- экспериментальное значение потенциала стандартного цинкового электрода по отношению к стандартному водородному электроду сравнения:
E ( ) по стандартному водородному. =
Внимание! Учитывая высокую токсичность солей тяжелых металлов, все отработанные растворы не сливаются в раковину, а сдаются лаборанту для последующей утилизации.
2. Определение величины стандартного электродного потенциала меди.
Аналогично п. I, соберите медный электрод, погрузив зачищенный медный стержень в I M раствор сульфата меди.
Составьте гальванический элемент из исследуемого медного электрода и насыщенного хлорсеребяного электрода сравнения.
Определите ЭДС гальванического элемента. Приведите условную запись для данного гальванического элемента.
Чему равен потенциал медного электрода по насыщенному хлорсеребряному электроду?
Рассчитайте потенциал медного электрода по отношению к стандартному водородному электроду и сравните его с табличным значением стандартного электродного потенциала меди:
E0 = 0,34 B
Запишите найденные значения:
Э. Д.С. (Сu/CuSO4//KCl/AgCl/Ag) =
E (![]() ) по хлор - серебряному насыщ.. =
) по хлор - серебряному насыщ.. =
E (![]() ) по стандартному водородному электроду =
) по стандартному водородному электроду =
3. Определение ЭДС химического гальванического элемента. (Медно – цинковый гальванический элемент).
Соберите гальванический элемент, составленный из стандартного цинкового и стандартного медного электродов (рис.2).
В соответствии с инструкцией о порядке измерений с использованием соответствующего потенциометра, определите ЭДС данного гальванического элемента.
Э. Д.С.(Сu/CuSO4// Zn/ZnSO4)эксп. =………..
Сравните полученное в эксперименте значение с расчетным (теоретическим) значением ЭДС для медно - цинкового гальванического элемента:
ЭДС теорет. = E катода –Е анода =
= E0(Cu+2/Cu0) - E0( Zn+2/Zn0) = 0,34 –(- 0,76) = 1,1B.

![]() Рис.2 Схема установки для определения ЭДС химического гальванического элемента:
Рис.2 Схема установки для определения ЭДС химического гальванического элемента:
1 – медный электрод, 2 – цинковый электрод
3 - электролитический ключ ( стаканчик с раствором хлорида калия),
4 - потенциометр
Напишите уравнения процессов, протекающих на катоде и аноде данного гальванического элемента при его работе.
4. Определение ЭДС концентрационного гальванического элемента.
Соберите гальванический элемент, составленный из стандартного цинкового электрода (цинковый электрод, погружен в раствор соли цинка с концентрацией 1 моль/л) и цинкового электрода, погруженного в раствор соли цинка с концентрацией См = 10-2 моль/л (рис.3).
Zn/ZnSO4 // Zn/ZnSO4
См = 10-2 моль/л См = 10-2 моль/л
![]()
|
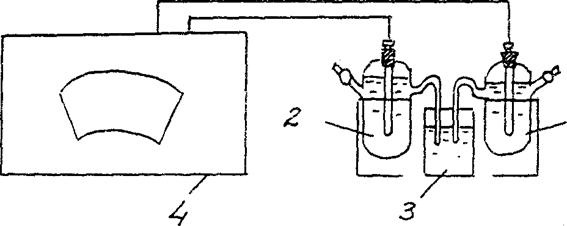
Рис.2 Схема установки для определения ЭДС концентрационного гальванического элемента:
1 – цинковый электрод в растворе соли с См = 10-2 моль/л ,
2 – цинковый электрод в растворе соли с См = 1 моль/л
3 - электролитический ключ (раствор хлорида калия),
4 - потенциометр
В соответствии с инструкцией о порядке измерений с использованием соответствующего потенциометра, определите ЭДС данного гальванического элемента.
Э. Д.С.(Сu/CuSO4// Zn/ZnSO4)эксп. =………..
Сравните полученное в эксперименте значение с расчетным (теоретическим) значением ЭДС для данного концентрационного гальванического элемента.



