На правах рукописи
Экспрессия генов, контролирующих
водно-солевой баланс в ткани почки гипертензивных крыс НИСАГ
03.02.07 – Генетика
Автореферат
диссертации на соискание ученой степени
кандидата биологических наук
Новосибирск 2013
Работа выполнена в лаборатории эволюционной генетики Федерального государственного бюджетного учреждения науки Института цитологии и генетики СО РАН г. Новосибирск.
Научный руководитель
Официальные оппоненты:
Ведущее Учреждение:
Доктор биологических наук, профессор
Доктор биологических наук, профессор
Зав. лабораторией регуляции экспрессии генов ФБГУН Институт цитологии и генетики СО РАН, г. Новосибирск
Доктор биологических наук, профессор
Зав. кафедрой естественных наук Специализированного учебно-научного центра Новосибирского государственного университета, г. Новосибирск
Федеральное государственное бюджетное учреждение «Научно-исследовательский институт молекулярной биологии и биофизики» Сибирского отделения Российской академии медицинских наук, г. Новосибирск
Защита диссертации состоится __________________ 2013 года на утреннем заседании диссертационного совета Д 003.011.01 по защите диссертаций на соискание ученой степени кандидата наук, по защите диссертаций на соискание ученой степени доктора наук в ИЦиГ СО РАН в конференц зале Института г. Новосибирск, проспект Лаврентьева 10, т\ф (383), Факс (3, e-mail: *****@
С диссертацией можно ознакомиться в библиотеке ИЦиГ СО РАН
Автореферат разослан «____»______________2013 г.
Учёный секретарь диссертационного совета,
Доктор биологических наук
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы.
Гипертоническая болезнь (ГБ) – широко распространенное, в подавляющем большинстве случаев полигенное заболевание человека, развитие которого связано с определенным вкладом большого числа генов, а также средовых факторов. Изучение природы гипертонии на всех уровнях, в том числе на молекулярно-генетическом, является актуальной научной задачей, имеющей большое практическое значение для клинической медицины. Одним из факторов развития ГБ является стресс (Gasperin et al. 2009). Однако, молекулярно-генетические механизмы, ответственные за развитие гипертонии при эмоциональном стрессе, изучены недостаточно.
Для исследования механизмов артериальной гипертонии широко используются модельные животные - инбредные линии крыс и мышей, которые воспроизводят разные формы и механизмы гипертензивных состояний. Для изучения стресса, как фактора, провоцирующего развитие гипертонии, в Институте цитологии и генетики СО РАН была создана путем селекции инбредная линия крыс с наследственной индуцированной стрессом артериальной гипертензией (линия НИСАГ - ISIAH) (Markel et al. 1992, 1999). В отличие от других гипертензивных линий, крысы НИСАГ наиболее полно реализуют свою генетическую предрасположенность к гипертонии именно в условиях эмоционального стресса. Так как гипертония человека может иметь стресс-зависимую природу, то линия НИСАГ рассматривается в качестве адекватной биологической модели артериальной гипертонии человека.
Известно, что при ГБ почки вовлекаются в патологический процесс одними из первых. Структурные нарушения в них нередко являются важным морфологическим критерием при определении стадии, степени тяжести и прогноза заболевания. Имеющиеся данные о морфологии и гистологии почек у крыс линии НИСАГ указывают на их важную роль при развитии стресс-индуцируемой формы артериальной гипертензии (Шмерлинг и соавт. 2001, Антонов и соавт. 2010, Федосеева и соавт. 2011).
Мы предположили, что возникновение и поддержание гипертензивного статуса у стресс-чувствительных крыс НИСАГ, вероятно, происходит на фоне нарушения функции почек, обеспечивающих водно-солевой баланс организма.
Цель работы: Выявление генетических особенностей почечной регуляции водно-солевого баланса и артериального давления в покое и при эмоциональном стрессе у гипертензивных крыс НИСАГ.
В связи с этим были поставлены следующие задачи:
1. Определение генов с дифференциальной экспрессией в корковом и мозговом веществе почек гипертензивных крыс НИСАГ и нормотензивных крыс WAG (контрольная линия) с помощью микроматриц. Проведение функциональной аннотации дифференциально экспрессирующихся генов и выявление изменений в метаболических путях в покое и после действия стресса.
2. Изучение межлинейных различий в экспрессии мРНК генов, регулирующих водно-солевой баланс, в почках крыс НИСАГ и WAG методом ПЦР в реальном времени.
3. Изучение влияния эмоционального стресса на экспрессию генов, обеспечивающих различия функционального состояния почек крыс НИСАГ и WAG, методом ПЦР в реальном времени.
Научная новизна работы. В данной работе впервые:
· Проведено сравнение транскрипционной активности генов в мозговом и корковом веществе почек у крыс НИСАГ и WAG с помощью микроматриц. При межлинейных сравнениях в покое найдено 126 и 65 дифференциально экспрессирующихся генов в корковом и в мозговом веществе почек, соответственно. Среди них 61.1% генов в корковом веществе и 78.5% генов в мозговом веществе почек имеют более низкий уровень экспрессии мРНК у крыс НИСАГ по сравнению с WAG. В корковом веществе почек найдена группа из 38 генов, описываемая термином «ответ на стимул» (согласно базе данных «Gene ontology»), включающая в себя гены, относящиеся к ответу на внешний стимул, ответу на гормональный стимул, регуляции ответа на стресс.
· Методом ПЦР в реальном времени исследована транскрипционная активность генов Mlr (минералокортикоидный рецептор), α-ENaC и β-ENaC (эпителиальный натриевый канал, α- и β-субъединицы), Egf (эпидермальный фактор роста), Egfr (рецептор эпидермального фактора роста), Ephx2 (эпоксидгидролаза 2), Comt (катехол-О-метилтрансфераза) в корковом и мозговом веществе почек крыс линий НИСАГ и WAG в покое и после действия эмоционального стресса.
· При межлинейных сравнениях в покое для крыс линии НИСАГ со стресс-чувствительной гипертонией в корковом веществе почек показано, что характерной особенностью является более высокий уровень экспрессии мРНК генов Egfr, Ephx2, и более низкий уровень экспрессии мРНК генов β-ENaC, Mlr, Соmt по сравнению с контрольными нормотензивными крысами. В мозговом веществе почек крыс линии НИСАГ показан более высокий уровень экспрессии мРНК генов Egfr, Mlr, Ephx2 и более низкий уровень экспрессии β-ENaC, Соmt.
· В условиях эмоционального стресса в корковом веществе почек у крыс линии НИСАГ отмечено повышение уровня транскрипции мРНК гена β-ENaC . В мозговом веществе почек действие эмоционального стресса вызывало повышение транскрипции мРНК генов α-ENaC, β-ENaC и Ephx2 у крыс НИСАГ.
· Показано, что возникновение и поддержание гипертензивного статуса у стресс-чувствительных крыс НИСАГ сопровождается изменением транскрипционной активности генов почки, что может приводить к таким последствиям как усиление симпатической стимуляции органа, увеличение местного сосудистого сопротивления, и к нарушению водно-солевого баланса.
Теоретическая и научно-практическая ценность работы.
Работа расширяет имеющиеся представления о механизмах участия почки в становлении стресс-чувствительного гипертензивного статуса. Данные по микроматрицам могут быть использованы для создания подробной картины нарушений функционирования почки при стресс-зависимой форме артериальной гипертонии. Данные о дифференциальной экспрессии генов у гипертензивных и нормотензивных крыс могут быть полезны для дальнейших исследований с целью разработки новых фармакологических препаратов с гипотензивным действием.
Положения, выносимые на защиту:
§ Большая часть дифференциально экспрессирующихся генов в почках крыс НИСАГ и WAG связана с ответом на стресс. Корковое и мозговое вещество почек различно реагирует на воздействие мягкого эмоционального стресса.
§ Развитие гипертензивного статуса у крыс НИСАГ связано с изменением активности генов в ткани почки, участвующих в регуляции функции симпатической нервной системы, водно-солевого баланса, а также сосудистого сопротивления.
Апробация результатов.
Материалы диссертации обсуждены на конференциях «Genomics Research. Asia» (г. Тэджен, 2012), «Постгеномные методы анализа в биологии, лабораторной и клинической медицине: геномика, протеомика, биоинформатика», (г. Новосибирск, 2011), «Fundamental Medicine: From Scalpel toward Genome, Proteome and Lipidome» (г. Казань, 2011), «Медико–биологические аспекты мультифакторных патологий» (г. Курск, 2011), «Фундаментальные аспекты компенсаторно-приспособительных процессов» (г. Новосибирск, 2011), «Студент и научно технический прогресс» (г. Новосибирск, 2011), «Студент и научно технический прогресс» (г. Новосибирск, 2010), «Bioinformatics of Genome Regulation and Structure» (BGRS'2010) (г. Новосибирск, 2010), отчетной сессии Института цитологии и генетики СО РАН (г. Новосибирск, 2010).
Публикации.
По материалам диссертации опубликовано 2 научных статьи в рецензируемых отечественных изданиях и 19 тезисов в сборниках трудов конференций.
Структура диссертации.
Диссертационная работа состоит из оглавления, списка сокращений, введения, обзора литературы, описания использованных материалов и методов, результатов, обсуждения, выводов, списка цитируемой литературы и приложений. Работа изложена на 150 страницах печатного текста, содержит 27 рисунков, 13 таблиц и 6 приложений. Библиографический указатель литературы включает 228 источников, из них 25 отечественных и 203 зарубежных.
Материалы и методы
Экспериментальные животные: В эксперименте использовали крыс - самцов двух инбредных линий: гипертензивных крыс линии НИСАГ и нормотензивных крыс линии WAG (Wistar Albino Glaxo) в возрасте 6 -7 месяцев.
Для измерения артериального давления применяли как прямой, так и непрямой метод (Bunag et al. 1973). Животных содержали в стандартных условиях вивария ИЦиГ СО РАН, воду и пищу давали без ограничения. Стресс вызывали помещением крысы в тесный проволочный домик на 2.5 часа. Для получения образцов тканей почки крыс декапитировали, почку быстро выделяли, делали поперечный срез. На срезе разделяли корковое и мозговое вещество. Для анализа транскрипционной активности генов на микроматрицах полученные образцы тканей (50 мг) сразу после выделения гомогенизировали в 1мл тризола (TRIzol reagent, Invitrogen, USA). Для анализа транскрипционной активности генов методом ПЦР в реальном времени остальную часть почки замораживали в жидком азоте и хранили при -70оС до выделения РНК. Изучение экспрессии методом ПЦР в реальном времени проводили у крыс в состоянии покоя и после эмоционального стресса отдельно в корковом и мозговом веществе почек (n=5 в каждой группе). Все эксперименты выполнены в соответствии с Международными правилами проведения работ с использованием экспериментальных животных.
Олигонуклеотиды синтезированы и (Новосибирск) с очисткой методом высокоэффективной жидкостной хроматографии.
Выделение суммарной РНК из тканей крыс и удаление хромосомной ДНК из препаратов РНК проводилось с помощью набора SV total RNA isolation system (Promega, USA) согласно инструкции производителя.
Электрофоретический анализ нуклеиновых кислот и амплифицированных ПЦР фрагментов проводили в агарозном либо полиакриламидном гелях с использованием стандартных методов (Маниатис и соавт. 1984). Спектрофотометрический анализ количества РНК проводили на спектрофотометре «Eppendorf BioPhotometer Plus (Eppendorf, Germany). Качество препаратов РНК оценивали, сравнивая поглощение при длинах волн 230, 260 и 280 нм.
Реакция обратной транскрипции РНК проводилась со специфическими праймерами в объёме 20 мкл. 2 мкг РНК, обработанной ДНКазой, денатурировали 5 мин при 70°С, далее проводили отжиг со смесью специфических праймеров (по 75 нг каждого) в течение 4 мин при 37°С. Реакцию проводили в буфере для ревертазы, содержащем 500 мкМ каждого из 4-х dNTP и 400 ед. акт. РНК-зависимой ДНК-полимеразы MoMLV в течение 10 мин при 37°С, 40 мин при 42°С. Реакцию останавливали инактивацией фермента в течение 5 мин при 70°С. Полученную кДНК хранили при -70°С.
Полимеразная цепная реакция в реальном времени (ПЦР-РВ) проводилась на амплификаторе ABI PRISM 7000 Sequence Detector System (Applied Biosystems, USA) с использованием набора реагентов для проведения ПЦР-РВ с Taq ДНК-полимеразой и ингибирующими активность фермента антителами в присутствии красителя SYBR GreenI и референсного красителя ROX (Синтол, Москва) согласно рекомендациям производителя. Анализ проводили на 96-луночных планшетах (Axygen 96M2-HS-C, США) в объеме 25 мкл с использованием 10х ПЦР буфера, 250 мкМ каждого из четырех dNTP, 200 нМ каждого праймера, с добавлением 0.1 мкл продукта обратной транскрипции и 1.2 ед. активности фермента Taq ДНК-полимеразы. Амплификацию проводили по стандартной схеме, при температуре отжига 62оС. Температуру детекции сигнала подбирали для каждого гена согласно кривой диссоциации. Для контроля специфичности реакции снимали кривые плавления. В качестве гена сравнения использовали ген циклофилина (Ppia) экспрессия которого, согласно данным микрочипов не различалась между линиями в покое и при стрессе, как в корковом, так и в мозговом веществе почек. В каждом эксперименте на один планшет помещали образцы кДНК с праймерами на целевой ген (по 4 повтора для каждого образца кДНК) и аналогичные образцы с праймерами на ген сравнения (также по 4 повтора). Каждый образец кДНК анализировали на двух планшетах. Относительный уровень экспрессии генов определяли методом ∆∆Сt. В качестве образца-калибратора использовали результаты измерения, полученные для крыс нормотензивной линии WAG в покое.
Сравнительный анализ экспрессии 22228 генов на микроматрицах (RatRef-12 Expression BeadChip, Illumina, Inc., California, USA) между линиями крыс НИСАГ и WAG был проведен в корковом и в мозговом веществе почки. Исследовали крыс самцов обеих линий в покое и после воздействия эмоционального стресса. Исследовали по 3 крысы в каждой группе индивидуально. Межлинейные различия определяли по соотношению НИСАГ в покое/WAG в покое и НИСАГ при стрессе/WAG при стрессе. Выделение РНК, гибридизация и компьютерная обработка полученных результатов в программе BeadStudio выполнялись в фирме (г. Москва, Россия).
Базы данных: Rat Genome Database (RGD) (http://rgd. mcw. edu/) использовался для поиска генов, относящихся к развитию гипертензии. Инструмент DAVID 2008 (http://david. abcc. ncifcrf. gov) - для функциональной аннотации дифференциально экспрессирующихся генов в терминах Gene Ontology (GO) и Kyoto Encyclopedia of Genes and Genomes (KEGG).
Статистический анализ результатов гибридизации и определение генов, дифференциально экспрессирующихся в почках крыс НИСАГ и WAG, проводили в программе BeadStudio с использованием gene expression module, rank invariant нормализацией и p < 0.01. Результаты ПЦР-РВ обрабатывали программой 7000 System SDS Software RQ Study Application (Applied BioSystems, USA) в автоматическом режиме. Достоверность различий в экспрессии мРНК генов оценивали с помощью непараметрического парного критерия Вилкоксона.
Результаты и обсуждение
Значения уровней артериального давления у крыс НИСАГ и WAG представлены в Табл. 1.
Результаты сравнительного анализа экспрессии 22228 генов в почках крыс НИСАГ и WAG с помощью микроматриц выявили 126 и 65 генов дифференциально экспрессирующихся в корковом и мозговом веществе почек, соответственно. Среди них 61.1% генов в корковом веществе и 78.5% генов мозговом веществе почек имеют более низкий уровень экспрессии мРНК у крыс НИСАГ по сравнению с WAG (Табл. 2). Найдены как сходство, так и различия в списках дифференциально экспрессирующихся генов коркового и мозгового вещества почек, что может говорить о различной функциональной роли данных отделов при стрессе (Рис.1). Эмоциональный стресс оказал различное влияние на уровень транскрипции генов в корковом и мозговом веществах почки у крыс гипертензивной и нормотензивной линий (Таблица 2).
Таблица 1. Средний уровень артериального давления у крыс НИСАГ и WAG в покое и после действия эмоционального стресса
АД в покое, мм. рт. ст. | АД при стрессе, мм. рт. ст. | |
НИСАГ (n=12) | 175±0.7*** | 208±3.6### |
WAG (n=12) | 124±3.1*** | 135±1.2### |
***p<0.001-межлинейные различия; ###p<0.001; - реакция на стресс;
Таблица 2. Число дифференциально экспрессирующихся генов в почках крыс НИСАГ и WAG в покое и при стрессе
Корковое вещество почки | ||||
Уровень транскрипции | Число генов | Уровень транскрипции | Число генов | Общее число генов |
Н покой < W покой | 77 | Н покой > W покой | 49 | 126 |
Н стресс < W стресс | 42 | Н стресс > W стресс | 22 | 64 |
Мозговое вещество почки | ||||
Н покой < W покой | 51 | Н покой > W покой | 14 | 65 |
Н стресс < W стресс | 124 | Н стресс > W стресс | 75 | 199 |
Н < W – уровень транскрипции у крыс НИСАГ ниже, чем у крыс WAG
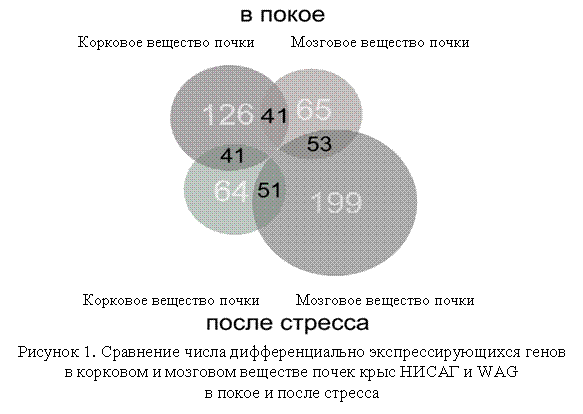 |
Н > W - уровень транскрипции у крыс НИСАГ выше, чем у крыс WAG
Функциональная аннотация дифференциально экспрессирующихся генов крыс НИСАГ и WAG в покое выявила в корковом веществе группу из 38 генов, описываемую термином «ответ на стимул», что составляет 30.2% от всех дифференциально экспрессирующихся генов коркового вещества (Табл. 3). Группа генов «ответ на стимул» включает в себя несколько групп, описываемых терминами «ответ на внешний стимул», «ответ на гормональный стимул», «регуляция ответа на стресс» и «ответ на стресс». Результаты позволяют предполагать, что различия в функциональном состоянии коркового вещества почек крыс НИСАГ и крыс WAG в покое связаны с различным уровнем транскрипционной активности генов, связанных с ответом на экзогенный и эндогенный (гормональный) стимул, либо с ответом на стресс.
Таблица 3. Результаты функциональной аннотации генов, дифференциально экспрессирующихся в почках крыс НИСАГ и WAG в покое и при стрессе
Категории Gene Ontology | Число генов | p value | Число генов | |
Н < W | Н > W | |||
Корковое вещество почки в покое | ||||
ответ на стимул | 38 | 3.4E-4 | 23 | 15 |
ответ на внешний стимул | 15 | 2,3E-4 | 8 | 7 |
ответ на гормональный стимул | 8 | 2,9E-2 | 4 | 4 |
регуляция ответа на стресс | 5 | 5,8E-2 | 2 | 3 |
ответ на стресс | 22 | 2.6E-5 | 16 | 6 |
ответ на оксидативный стресс | 6 | 4,3E-3 | 3 | 3 |
ответ на гипоксию | 6 | 5,1E-3 | 5 | 1 |
Мозговое вещество почки в покое | ||||
ответ на стресс | 9 | 5.6E-2 | 7 | 1 |
Корковое вещество почки при стрессе | ||||
регуляция артериального давления | 3 | 3,6E-2 | 2 | 1 |
Мозговое вещество почки при стрессе | ||||
ответ на стресс | 21 | 2.3E-2 | 17 | 4 |
ответ на гипоксию | 5 | 9.6E-2 | 5 | 0 |
регуляция артериального давления | 4 | 7.2E-2 | 3 | 1 |
Н < W – уровень транскрипции у крыс НИСАГ ниже, чем у крыс WAG
Н > W - уровень транскрипции у крыс НИСАГ выше, чем у крыс WAG
Обобщающие категории, напечатаны полужирным шрифтом.
Группа генов, описываемая термином «регуляция артериального давления», была выявлена при межлинейных сравнениях только после воздействия стресса (Табл. 3). В нее вошли: Adra1b (adrenergic, alpha-1B-, receptor), Ephx2 (epoxide hydrolase 2,), P2rx4 (purinergic receptor P2X, ligand-gated ion channel 4), Sod2 (superoxide dismutase 2),
Скрининг дифференциально экспрессирующихся генов в тканях почек у нормотензивной и гипертензивной линий крыс в покое и при стрессе, выявил ряд генов, которые зарегистрированы в базе данных RGD как гены гипертонической болезни (Табл. 4). Из таблицы видно, что только два гена являются дифференциально экспрессирующимися во всех вариантах опыта - это Comt и Ephx2.
Таблица 4. Пересечения дифференциально экспрессирующихся генов крыс НИСАГ и WAG со списком генов RGD, имеющих отношение к гипертензии
Ген | Acc.# | Название гена | Соотношение экспрессии мРНК гена |
НИСАГ покой/WAG покой | |||
Корковое вещество почки | |||
Becn1 | NM 053739.1 | beclin 1 (coiled-coil, myosin-like BCL2-interacting protein) | 2.21 |
Cat | NM 012520.1 | сatalase | 1.75 |
Cldn16 | NM 131905.1 | claudin 16 | 0.51 |
Clu | XM .1 | сlusterin | 0.23 |
Comt | NM 012531.1 | catechol-O-methyltransferase | 0.17 |
Cst3 | NM 012837.1 | cystatin C | 0.62 |
Ephx2 | NM 022936.1 | epoxide hydrolase 2, cytoplasmic | 16.7 |
Fads1 | NM 053445.1 | fatty acid desaturase 1 | 0.59 |
Sncg | NM 031688.1 | synuclein, gamma (breast cancerspecific protein) | 0.49 |
Tf | NM .1 | transferrin | 0.49 |
Мозговое вещество почки | |||
Comt | NM 012531.1 | catechol-O-methyltransferase | 0.22 |
Ephx2 | NM 022936.1 | epoxide hydrolase 2, cytoplasmic | 20.6 |
RT1-Ba | NM .1 | RT1 class II, locus Ba | 0.27 |
НИСАГ стресс/ WAG стресс | |||
Корковое вещество почки | |||
Adra1b | NM 016991.2 | adrenergic, alpha-1B-, receptor | 0.35 |
Clu | XM .1 | clusterin | 0.30 |
Comt | NM 012531.1 | catechol-O-methyltransferase | 0.17 |
Ephx2 | NM 022936.1 | epoxide hydrolase 2 | 14.62 |
Мозговое вещество почки | |||
Adra1b | NM 016991.2 | adrenergic, alpha-1B-, receptor | 0.41 |
Becn1 | NM 053739.1 | beclin 1) | 2.26 |
Clu | XM .1 | clusterin | 0.57 |
Comt | NM 012531.1 | catechol-O-methyltransferase | 0.18 |
Cxcl10 | NM 139089.1 | chemokine (C-X-C motif) ligand 10 | 0.49 |
Ephx2 | NM 022936.1 | epoxide hydrolase 2 | 14.4 |
RT1-Ba | NM .1 | RT1 class II, locus Ba | 0.26 |
Sod2 | NM 017051.2 | superoxide dismutase 2 | 0.64 |
Проведение анализа в базе данных KEGG позволило выявить метаболические пути с участием генов, дифференциально экспрессирующихся в почках крыс НИСАГ и WAG. В покое в корковом и в мозговом веществе почки различия были найдены для «молекул клеточной адгезии» и «метаболизма тирозина». После действия стресса в мозговом веществе почки сохранились различия, касающиеся «молекул клеточной адгезии». Кроме того, у крыс НИСАГ по сравнению с крысами WAG наблюдали различную транскрипционную активность у генов, относящихся к метаболизму ксенобиотиков, биосинтезу стероидных гормонов, а также к метаболизму глутатиона.
По результатам анализа микроматриц, данных литературы и данных RGD, было выбрано несколько генов, имеющих отношение к регуляции водно-солевого гомеостаза и АД, для изучения их экспрессии методом ПРЦ-РВ в корковом и мозговом веществе почек крыс линий НИСАГ и WAG в покое и после воздействия эмоционального стресса.
Уровень экспрессии мРНК гена Mlr
В корковом веществе почки найдено достоверное снижение экспрессии мРНК гена Mlr у гипертензивных крыс НИСАГ в покое, а также снижение экспрессии мРНК этого гена у нормотензивных крыс WAG до уровня крыс НИСАГ под действием эмоционального стресса (Рис. 2 а). В мозговом веществе почек уровень экспрессии мРНК гена Mlr был более высоким у крыс НИСАГ, а реакции на стресс обнаружено не было (Рис. 2 б). Наши результаты согласуются с результатами других авторов. Так, у крыс SHR уровень экспрессии мРНК гена Mlr в целой почке был повышен (Cavallari et al. 2008).
Минералокортикоидный рецептор (Mlr) активируется несколькими лигандами, основным из которых в почке является альдостерон (Nagase et al. 2007). У крыс НИСАГ содержание альдостерона в плазме крови при стрессе повышено (Антонов и соавт. 2010).
а. Mlr корковое вещество | б. Mlr мозговое вещество | ||||||||||
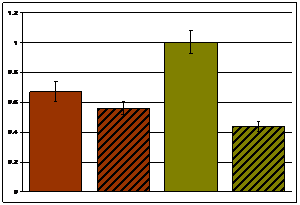
|
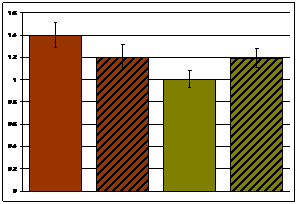
| ||||||||||
Рисунок 2. Экспрессия мРНК гена Mlr в корковом и мозговом веществе почки крыс НИСАГ и WAG в покое и после действия эмоционального стресса; ## p<0.01 - межлинейные различия; ** p<0.01 реакция на стресс |
Уровень экспрессии мРНК генов канала ENaC
Гены α-ENaC и β-ENaC кодируют α- и β-субъединицы эпителиального натриевого канала ENaC, основного регулятора реабсорбции натрия в почках. Известно, что α-субъединица ENaC является основной структурной единицей канала, но с гипертонией чаще связывают β-субъединицу (Gao et al. 2012).
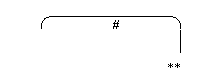
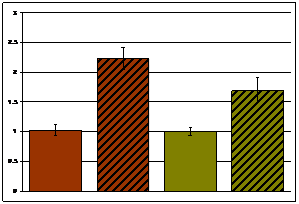
В покое межлинейных различий в уровне экспрессии мРНК гена α-ENaC не найдено (Рис.3а, б). После действия эмоционального стресса уровень экспрессии мРНК гена α-ENaC в корковом веществе почки не изменялся у обеих линий крыс (Рис.3а), а в мозговом веществе почки достоверно увеличивался у крыс обеих линий (Рис.3б). Также показаны межлинейные различия реакции на стресс в мозговом веществе почки. Она была выше у крыс НИСАГ.
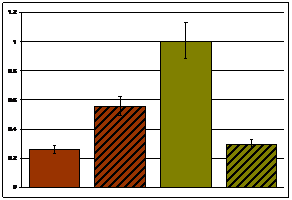
Известно, что синтез α-ENaC контролируется не только альдостероном, но и другими гормонами, ответственными за водно-солевой гомеостаз – вазопрессином и глюкокортикоидами. Ранее было показано, что глюкокортикоидная реакция крыс НИСАГ на рестрикционный стресс и другие виды стресса превышает таковую у крыс линии WAG (Markel et al. 2007). Увеличение экспрессии натриевого канала ENaC и связанная с этим активация реабсорбции натрия при эмоциональном стрессе, наряду с характерной для крыс НИСАГ усиленной симпатоадреналовой, минералокортикоидной и глюкокортикоидной реакциями, очевидно, способствуют развитию артериальной гипертензии. Для мРНК гена β-ENaC в покое достоверная межлинейная разница в экспрессии найдена как в корковом (Рис. 4а), так и в мозговом (Рис. 4б) веществе почек. Под действием эмоционального стресса уровень мРНК гена β-ENaC достоверно изменялся и в корковом, и в мозговом веществе почек крыс обеих линий. У крыс НИСАГ показано повышение экспрессии мРНК гена β-ENaC при стрессе, а у крыс WAG корковое и мозговое вещество почки реагирует разнонаправлено.
а. α-ENaC корковое вещество | б. α-ENaC мозговое вещество | ||||||||||||||||
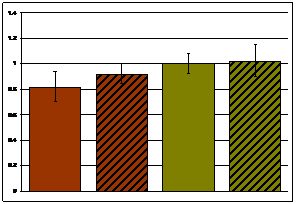
|
| ||||||||||||||||
Рисунок 3. Экспрессия мРНК гена α-ENaC в корковом и мозговом веществе почки крыс НИСАГ и WAG в покое и после действия эмоционального стресса ##p<0.01- межлинейные различия; **p<0.01 реакция на стресс | |||||||||||||||||
а. β-ENaC корковое вещество | б. β-ENaC мозговое вещество | ||||||||||||||||
|
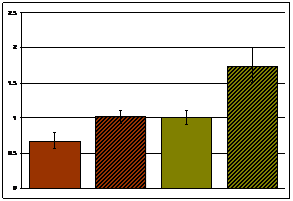
| ||||||||||||||||
Рисунок 4. Экспрессия мРНК гена β-ENaC в корковом и мозговом веществе почки крыс НИСАГ и WAG в покое и после действия эмоционального стресса; ##p<0.01- межлинейные различия; *p<0.05; **p<0.01 реакция на стресс |
Уровень экспрессии мРНК генов Egfr и Egf
Egf (эпидермальный фактор роста) связываясь с Egfr (рецептор эпидермального фактора роста) может выступать как вазоконстриктор, изменяя сосудистый тонус, и участвовать в ремоделировании почечных сосудов (Ying et al. 2005).
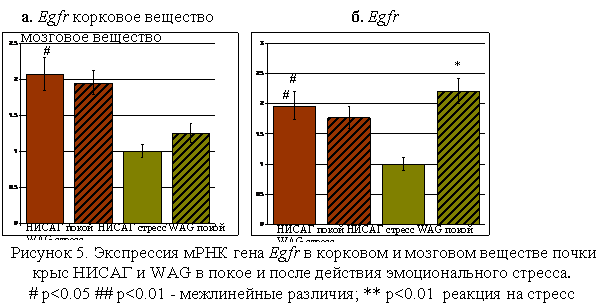
В почках крыс НИСАГ уровень экспрессии мРНК гена Egfr был значительно выше, чем у крыс WAG. При действии эмоционального стресса уровни экспрессии мРНК гена Egfr у крыс НИСАГ и WAG не изменялись (Рис. 5а) в корковом веществе почек, а в мозговом веществе почки у крыс WAG экспрессия резко возрастала (более чем в 2 раза), становясь практически такой же, как у крыс НИСАГ (Рис. 5б).
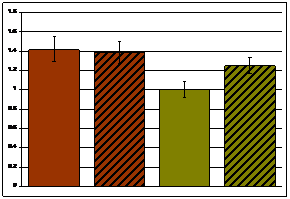
В корковом (Рис. 6а) и в мозговом (Рис. 6б) веществе почки достоверных межлинейных различий в уровне экспрессии мРНК гена Egf найдено не было.
а. Egf корковое вещество | б. Egf мозговое вещество | ||||
|
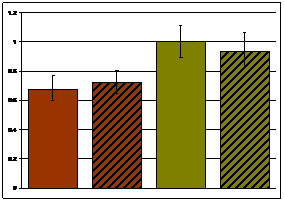
| ||||
Рисунок 6. Экспрессия мРНК гена Egf в корковом и мозговом веществе почки крыс НИСАГ и WAG в покое и после действия эмоционального стресса |
При воздействии эмоционального стресса экспрессия мРНК гена Egf у крыс НИСАГ и WAG не изменялась.
Повышенный уровень экспрессии мРНК гена Egfr ранее был показан в почках гипертензивных крыс DS с соль-зависимой гипертонией и у крыс LH со спонтанно развивающейся гипертонией (Swaminathan et al. 1996), что рассматривалось как основа процесса ремоделирования почечных сосудов (Wei-Zhong et al. 2005).
Уровень экспрессии мРНК гена Ephx2
Ген Ephx2 кодирует фермент - растворимую эпоксидгидролазу (sEH). sEH катализует деградацию эпоксиэйкозатриеновых кислот (EETs) до их неактивных производных – дигидроэпоксиэйкозатриеновых кислот (DHETs). EETs являются вазодилататорами, и их гидролиз с помощью sEH регулирует сосудистый тонус.
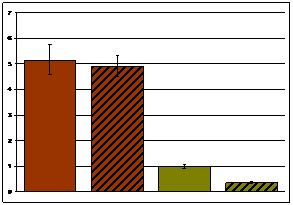
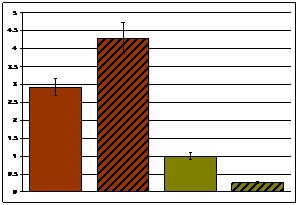
В корковом и в мозговом веществе почек найдена межлинейная разница в экспрессии мРНК гена Ephx2 как в покое, так и после действия эмоционального стресса (Рис.7а, б). У крыс WAG после действия стресса экспрессия уменьшалась в корковом и мозговом веществе почки. Снижение уровня мРНК гена Ephx2 у крыс WAG, позволяет предполагать увеличение количества EETs. Это может быть частью компенсаторной реакции организма, направленной на снижение уровня артериального давления в условиях стресса. У крыс НИСАГ реакция на эмоциональный стресс была найдена только в мозговом веществе почки, при этом уровень экспрессии мРНК у крыс НИСАГ значительно повышался. Стабильно высокий уровень экспрессии мРНК гена Ephx2 указывает на участие данного гена в процессе развития и поддержания гипертензивного статуса у крыс НИСАГ.
а. Ephx2 корковое вещество | б. Ephx2 мозговое вещество | ||||||||||||||||||
|
| ||||||||||||||||||
Рисунок 7. Экспрессия мРНК гена Ephx2 в корковом и мозговом веществе почки крыс НИСАГ и WAG в покое и после действия эмоционального стресса; ## p<0.01 - межлинейные различия; ** p<0.01 реакция на стресс |
Уровень экспрессии мРНК гена Соmt
Comt (катехол-О-метилтрансфераза) – участвует в инактивации катехоламинов и влияет на активность симпатической стимуляции.
В корковом и в мозговом веществе почек в покое экспрессия мРНК гена Соmt была ниже у крыс НИСАГ по сравнению с крысами WAG (Рис.8а, б). В условиях мягкого эмоционального стресса в корковом веществе почек экспрессия мРНК гена Соmt не изменялась у крыс НИСАГ и снижалась у крыс линии WAG до уровня экспрессии крыс НИСАГ. В мозговом веществе почек у крыс обеих линий реакция на стресс не была показана, достоверные межлинейные отличия сохранялись после действия стресса (Рис.8б).
Ранее у крыс гипертензивных линий SHR и DS также было показано снижение уровня экспрессии мРНК Соmt и инактивации катехоламинов в почках (Mannisto et al 1999, Kajimoto et al 2007, Tsunoda et al 2008).
Найденное нами снижение уровня экспрессии гена Соmt может повышать уровень симпатической стимуляции почек и оказывать влияние на формирование гипертензивного статуса у крыс линии НИСАГ.
![]()
![]()
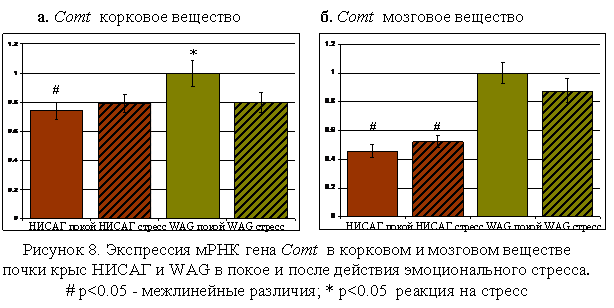
Эмоциональный стресс может приводить к развитию оксидативного стресса (Ueyama et al 1999), что сопровождается изменением уровня транскрипции многих генов. Известно, что повреждающие эффекты острого оксидативного стресса реализуются главным образом в мозговом веществе почки (Tyther et al 2007). Наша работа выявила имеющиеся сходство и различия в функциональном состоянии коркового и мозгового вещества почек у изучаемых линий крыс, а также различную реакцию коркового и мозгового вещества в ответ на эмоциональный стресс.
На Рис. 9 представлена обобщающая схема возможного взаимодействия генов с измененной экспресией у крыс НИСАГ, рассмотренных в нашей работе. Как видно из рисунка, «пусковым механизмом», вероятно, является снижение экспрессии мРНК гена Comt. Это понижает уровень инактивации катехоламинов в почке, которые, в свою очередь, вызывают сокращение почечных сосудов, а также стимулируют высвобождение ренина. Активация ренин-ангиотензин-альдостероновой системы (РААС) повышает уровень ангиотензина II (АТII) и альдостерона. АТII может, в свою очередь, активировать экспрессию мРНК генов Ephx2 и Egfr (Fortuno et al. 2005). Повышение уровня Ephx2 оказывает влияние на концентрацию потенциальных вазодилятаторов EETs, переводя их в неактивные производные, что также увеличивает сосудистое сопротивление. АТII повышает экспрессию рецептора Egfr (Touyz et al. 2003). Известно, что взаимодействие этого рецептора с его лигандами запускает процесс ремоделирования сосудов и их сужение (Ying et al. 2005). Также активация синтеза белка Egfr может регулироваться EETs (Zhang et al. 2011). Egfr оказывает влияние на работу канала ENaC, который является ключевым механизмом регуляции баланса натрия. Активация канала может осуществляться в результате взаимодействия альдостерона с его рецептором Mlr, что усиливает экспрессию α-субъединицы ENaC.
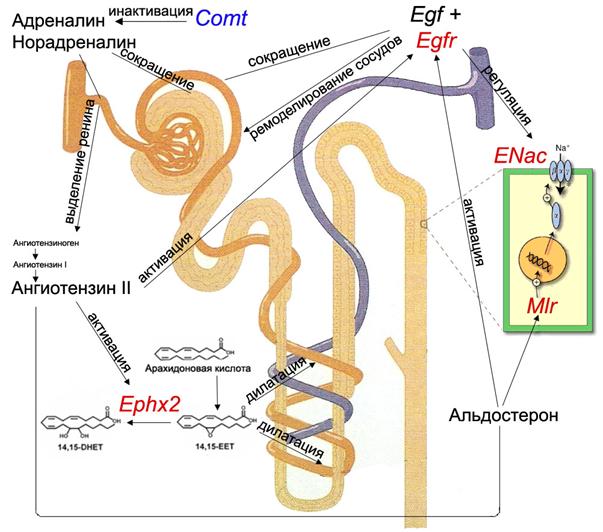

В настоящее время считается, что развитие гипертонической болезни имеет две фазы (Esler et al. 2000). На первом этапе повышение АД имеет транзиторный характер и связано с эпизодами гиперактивации симпатической нервной системы и РААС и с их взаимодействием. Во второй фазе формируется стойкое повышение АД и это обусловлено в значительной мере нарушением почечных функций, особенно способности экскретировать натрий. Переход первой фазы во вторую связывают с тем, что повторяющиеся вследствие симпатических разрядов повышения АД повреждают преимущественно почечные структуры (юкстамедуллярные и медуллярные районы), которые не имеют достаточной ауторегуляции при скачкообразных перепадах АД. Это представление о двухэтапном развитии гипертонической болезни, по сути, объединяет имеющиеся в настоящее время многочисленные гипотезы о патогенезе гипертонической болезни (Guyton et al. 1984, Sealey et al. 1988, , Julius et al.1996, Cowley et al. 1995, Kurokawa et al. 1996, Shulutko et al.1997, Brenner et al. 1997). Полученные нами данные, отраженные на схеме (Рис. 9), хорошо согласуются с этими представлениями.
Ряд исследований позволяет предполагать, что результаты изучения генетического контроля заболеваний и физиологических признаков, полученные на моделях животных, могут иметь прямое отношение к заболеваниям человека (Korstanje et al. 2004). Сходство генетического контроля заболеваний человека и модельных животных подтверждается и сходством списков генов, аннотированных в базе данных RGD в качестве генов, ответственных за развитие ряда заболеваний, в том числе и гипертонии. Наша работа дает новый материал для выявления молекулярных механизмов регуляции повышенного артериального давления, и поиска полиморфизмов, потенциально связанных с процессами нарушения функции почек и развития гипертензивного статуса. Кроме того, данные о дифференциальной экспрессии генов у гипертензивных и нормотензивных крыс могут быть полезны для дальнейших исследований с целью разработки новых фармакологических препаратов с гипотензивным действием.
ВЫВОДЫ
1. Анализ транскрипционной активности генов в почках крыс НИСАГ и WAG с помощью микроматриц показал, что большая часть дифференциально экспрессирующихся генов в корковом и мозговом веществе почек описывается термином «ответ на стресс». Это позволяет предположить, что крысы гипертензивной линии НИСАГ, находясь в состоянии «покоя», тем не менее, находятся в перманентно стрессированном состоянии по сравнению с нормотензивными крысами WAG.
2. Мягкий эмоциональный стресс может вызывать различные изменения в уровне экспрессии генов в корковом и мозговом веществе почек, что говорит о различной функциональной роли данных отделов почки при стрессе.
3. Экспрессия мРНК гена Comt в корковом и мозговом веществе почек у крыс НИСАГ снижена, что ассоциируется с усилением симпатической стимуляции почек.
4. На существование различий в регуляции системы водно-солевого обмена у гипертензивных крыс НИСАГ и нормотензивных крыс WAG значительное влияние оказывает повышенный уровень экспрессии мРНК генов Mlr в покое и α-ENaC в условиях эмоционального стресса в мозговом веществе почек крыс НИСАГ.
5. Экспрессия мРНК генов Egfr, Ephx2 повышена у крыс НИСАГ в мозговом и корковом веществе почек, что содействует увеличению сопротивления сосудистого русла почек у крыс со стресс-зависимой гипертензией.
6. Развитие гипертензивного статуса у крыс НИСАГ со стресс-зависимой гипертензией связано с изменением в ткани почки активности генов, участвующих в регуляции функции симпатической нервной системы, водно-солевого баланса, а также сосудистого сопротивления.
СПИСОК ПУБЛИКАЦИЙ ПО ТЕМЕ ДИССЕРТАЦИИ
1. О. (), , Иванова эмоционального стресса на экспрессию мРНК гена α-ENaC в почке гипертензивных крыс линии НИСАГ. Доклады академии наук. 2011, том 439, № 4, с. 563-565. (Список ВАК)
2. О. (), , Маркель экспрессии генов Egf и Egfr в ткани почки гипертензивных крыс линии НИСАГ (ISIAH). Российский физиологический журнал им. . 2012, Том 98, № 3, с. 69-76. (Список ВАК)
3. , , Маркель уровень экспрессии мРНК гена Ephx2 в почках гипертензивных крыс линии НИСАГ (ISIAH). Молекулярная биология. 2013, Том, № , с. (Список ВАК)
4. Abramova T. Kidney genes expression in hypertensive ISIAH rats.«1st International conference Genomics Research Asia».Теджен. Южная Корея.13-14 ноября 2012.
5. , , (), , Маркель контроль артериального давления у крыс НИСАГ с наследуемой индуцируемой стрессом артериальной гипертензией. Сборник трудов I-ой Международной Интернет-Конференции "Медицина в XXI веке: тенденции и перспективы", Казань, 12-15 марта 2012 г. Стр. 213-214.
6. , , (), , Маркель контроль физиологических признаков у крыс гипертензивной линии НИСАГ. Тез. конференции «Постгеномные методы анализа в биологии, лабораторной и клинической медицине: геномика, протеомика, биоинформатика», Новосибирск, 2011,ноября. Стр.65.
7. , , (), , , , Маркель анализ дифференциально экспрессирующихся генов у крыс гипертензивной линии НИСАГ. Тез. докладов конференции «Постгеномные методы анализа в биологии, лабораторной и клинической медицине: геномика, протеомика, биоинформатика», Новосибирск, 2011,ноября. Стр. 179.
8. Pylnik T. O. (Аbramova Т.О.), Pletneva L. S., Redina O. E., Markel A. L., Smolenskaya S. E., Ivanova L. N. Characterization of renal regulation of ion exchange in rats with stress-dependent hypertension. First international conference «Fundamental Medicine: From Scalpel toward Genome, Proteome and Lipidome» Kazan 25-28 April 2011. p.105.
9. , , О. (), Маркель –индуцируемая гипертензия: генетический контроль и механизмы формирования. Тез. докладов конференции «Медико – биологические аспекты мультифакторных патологий» Курск 17-19 мая 2011г. с. 92.
10. (), , Маркель эмоционального стресса в изменении экспрессии мРНК гена ENaC в почке гипертензивных крыс линии НИСАГ. Тез. докладов конференции «Медико–биологические аспекты мультифакторных патологий» Курск 17-19 мая 2011г. с. 91.
11. , , (), Маркель контроль нейромедиаторной регуляции поведения крыс НИСАГ в тесте открытого поля. Тез. докладов конференции «Фундаментальные аспекты компенсаторно-приспособительных процессов». Новосибирск 12-14 апреля 2011г. с.209.
12. , , (), Маркель контроль центральных и периферических механизмов эндокринной регуляции артериального давления у крыс НИСАГ. Тез. докладов конференции «Фундаментальные аспекты компенсаторно-приспособительных процессов». Новосибирск 12-14 апреля 2011г. с.191.
13. О. (), , Маркель ионного обмена в почках крыс НИСАГ с наследуемой индуцируемой стрессом артериальной гипертензией. Тез. докладов конференции «Фундаментальные аспекты компенсаторно-приспособительных процессов». Новосибирск 12-14 апреля 2011г. с.186.
14. , , (), , Маркель генетического контроля физиологических признаков у крыс НИСАГ с наследуемой индуцируемой стрессом артериальной гипертензией. Тез. докладов XXI Съезда Физиологического общества им. ,сентября 2010, г. Калуга. С.515.
15. О. (), , Маркель дифференциально экспрессирующихся генов в почках крыс гипертензивной линии НИСАГ. Тез. докладов XXI Съезда Физиологического общества им. ,сентября 2010, г. Калуга. С.510.
16. О. (), Изменение экспрессии генов в почках крыс НИСАГ в покое и под воздействием эмоционального стресса. Тез. докладов конференции «Студент и научно технический прогресс». Новосибирск 16-20 апреля, 2011г. С. 199.
17. , Пыльник T. O. (), Изучение экспрессии генов эпителиального натриевого канала в почках крыс линии НИСАГ с наследуемой индуцируемой стрессом артериальной гипертензией. Тез. докладов конференции «Студент и научно технический прогресс». Новосибирск 11-15 апреля, 2010г. С. 219.
18. Пыльник T. O. (), Изучение экспрессии гена Comt в почках гипертензивных крыс НИСАГ и нормотензивных крыс WAG. Тез. докладов конференции «Студент и научно технический прогресс». Новосибирск 11-15 апреля, 2010г. С. 193.
19. Pylnik T.O. (Аbramova Т. О.), Smolenskaya S. E., Markel A. L., Ivanova L. N., Redina O. E.. Identification of candidate genes for hypertension phenotype manifestation in ISIAH rat. The Seventh International Conference on Bioinformatics of Genome Regulation and Structure (BGRS'2010) Novosibirsk, June 20-27, 2010. P. 239.
20. O. E. Redina, S. E. Smolenskaya, T. O. Pylnik (Аbramova Т.О.), A. L. Markel. The genetic control of physiological traits in hypertensive ISIAH rats. The Seventh International Conference on Bioinformatics of Genome Regulation and Structure (BGRS 2010), Novosibirsk, Russia June 20-27, 2010. P.241
21. к, (), , . Изучение генов с различной экспрессией у гипертензивных крыс НИСАГ и нормотензивных крыс WAG. Тез. докладов Пятый съезд Вавиловского общества генетиков и селекционеровиюня 2009 года, Москва. С. 97.
22. , , (),. Функциональный анализ генома крыс НИСАГ с наследуемой индуцируемой стрессом артериальной гипертензией. Тез. докладов Пятый съезд Вавиловского общества генетиков и селекционеровиюня 2009 года, Москва. С. 98.
Подписано к печати 19.06.2013г.
Формат бумаги 60 х 90 1\16 Печ. л.1. Уч. изд. л.0,7
Тираж 110 экз. Заказ № 41
Отпечатано на полиграфической базе ИЦиГ СО РАН
Новосибирск, пр. акад. Лаврентьева, 10



