1 - ознакомительный (узнавание ранее изученных объектов, свойств);
2 - репродуктивный (выполнение деятельности по образцу, инструкции или под руководством);
3 – продуктивный (планирование и самостоятельное выполнение деятельности, решение проблемных задач).
2.3. условия реализации УЧЕБНОЙ дисциплины
2.3.1. Требования к минимальному материально-техническому обеспечению
Реализация учебной дисциплины требует наличия учебного кабинета химических дисциплин; лаборатории общей или органической химии.
Оборудование учебного кабинета: посадочные места по количеству обучающихся, рабочее место преподавателя, Периодическая таблица , таблицы строения неорганических веществ, механизма растворения веществ в воде, прибор для опытов с электрическим током, справочник физико-химических величин
Технические средства обучения: мультимедиа-проектор, ноутбук, колонки, набор цифровых образовательных ресурсов по дисциплине (презентации к лекциям, видеоопыты, анимационные схемы и модели химических процессов)
Оборудование лаборатории и рабочих мест лаборатории:
доска для сушки лабораторной посуды, вытяжной шкаф, столы лабораторные, штативы для пробирок, набор вспомогательных принадлежностей для хозяйственной деятельности и техники безопасности. Приборы: весы технические электронные, плитка электрическая с закрытой спиралью, шкаф сушильный, рефрактометр. Комплекты: химической посуды и реактивов для выполнения лабораторных опытов.
2.3.2. Информационное обеспечение обучения
Перечень рекомендуемых учебных изданий, Интернет-ресурсов, дополнительной литературы
Основные источники:
1. , , Трощенко химия. СПб.;2008.
2. Гранберг химия. М.; 2007.
3. Ким химия. Новосибирск; 2009.
Дополнительные источники:
1. , , Гаверова задач и упражнений по
органической химии. Academia.; 2007.
2. , , Г Органическая химия. Academia.; 2010.
Интернет-ресурсы:
1. Портал фундаментального химического образования
http://www. *****
2. Каталог образовательных Интернет-ресурсов http://www. *****
3. Мир химии http://chem. *****
4. лектронная библиотека по химии и технике http://*****
2.4. Контроль и оценка результатов освоения УЧЕБНОЙ Дисциплины
Контроль и оценка результатов освоения учебной дисциплины осуществляется преподавателем в процессе проведения практических занятий и лабораторных работ, тестирования, а также выполнения обучающимися индивидуальных заданий, проектов, исследований.
Результаты обучения (освоенные умения, усвоенные знания) | Формы и методы контроля и оценки результатов обучения |
умение: · составлять и изображать структурные полные и сокращенные формулы органических веществ и соединений; · определять свойства органических соединений для выбора методов синтеза углеводородов при разработке технологических процессов; · описывать механизм химических реакций получения органических соединений; · составлять качественные химические реакции, характерные для определения различных углеводородных соединений; · прогнозировать свойства органических соединений в зависимости от строения молекул; · решать задачи и упражнения по генетической связи между различными классами органических соединений; · определять качественными реакциями органические вещества, проводить количественные расчеты состава веществ; · применять безопасные приемы при работе с органическими реактивами и химическими приборами; · проводить реакции с органическими веществами в лабораторных условиях; · проводить химический анализ органических веществ и оценивать его результаты. знание: · влияния строения молекул на химические свойства органических веществ; · влияния функциональных групп на свойства органических веществ; · изомерии как источник многообразия органических соединений; · методов получения высокомолекулярных соединений; · особенностей строения органических веществ, их молекулярного строение, валентного состояние атома углерода; · особенностей строения и свойств органических веществ, содержащих в составе молекул атомы серы, азота, галогенов, металлов; · особенностей строения и свойств органических соединений с большой молекулярной массой; · природных источников, способов получения и областей применения органических соединений; · теоретических основ строения органических веществ, номенклатуры и классификации органических соединений; · типов связей в молекулах органических веществ. | Письменная проверочная работа Письменная самостоятельная работа Письменная проверочная работа Письменная самостоятельная работа Устный опрос Письменная проверочная работа Письменная проверочная работа Выполнение химического эксперимента на лабораторных работах Выполнение химического эксперимента на лабораторных работах Выполнение химического эксперимента на лабораторных работах Стандартизированный контроль Письменная проверочная работа Устный опрос Письменная проверочная работа Стандартизированный контроль Письменная проверочная работа Стандартизированный контроль Письменная проверочная работа Письменная проверочная работа Стандартизированный контроль |
3. Методические указания по изучению учебного материала
по теме Введение
При изучении данной темы необходимо обратить внимание на особенности состава органических соединений, экологические проблемы химических и нефтехимических производств.
Вопросы для самоконтроля
1. Что такое органическая химия?
2. Какие основные природные источники сырья для промышленности
органического синтеза Вы знаете?
3. Каковы особенности органических соединений?
4. Что такое явление изомерии?
Литература [ 1 ], с.12-16
Методические указания по теме 1.1. Общие вопросы теории химического строения органических веществ.
При изучении данной темы необходимо обратить внимание на значение теории строения органических веществ , явление изомерии, на составление структурных формул – изомеров углеводородов.
Для вывода формул изомеров, различающихся последовательностью связей углеродных атомов в молекуле (изомерия углеродного скелета) необходимо:
а) составить структурную формулу углеродного скелета нормального строения с заданным числом углеродных атомов;
б) постепенно укорачивать цепь (каждый раз на один атом углерода) и производить все возможные перестановки одного или нескольких атомов углерода и таким образом вывести формулы всех возможных изомеров.
ПРИМЕР: Составить структурные формулы всех изомерных углеводородов состава С5Н12.
Решение:
1. Составим формулу углеродного скелета с нормальной цепью из 5 углеродных атомов.
С – С – С – С – С.
2. Укоротим цепь на один атом углерода и осуществим все возможные перестановки.
С – С – С – С
½
С
3. Укоротим цепь еще на один атом углерода и осуществим возможные перестановки.
С
½
С – С – С
½
С
4. Расставим необходимое количество атомов водорода.
1. СН3 – СН2 – СН2 – СН2 – СН3
2. СН3 – СН – СН2 – СН3
½
СН3
3. СН3
½
Н3С – С – СН3
½
СН3
Вопросы для самоконтроля
1. Что такое электронные орбитали? Какого типа они бывают?
2. Какими квантовыми числами характеризуется состояние электронов в атоме?
3. Какие валентные углы характерны для атомов углерода в состояниях sp3-, sp2-,
sp - гибридизации?
4. Какое состояние углеродного атома называется:
sp3 - гибридизацией,
sp2 - гибридизацией,
sp – гибридизацией?
5. Напишите электронные схемы строения молекул: Н2, СН4, СН3ОН, СН3Сl.
6. В чём различие между понятиями «полярность» и «поляризуемость»?
7. Какой тип разрыва ковалентной связи характерен для обозначенных
парой электронов связей в соединениях:
7.1. H3C : CH3 ; 7.2. H3 C : Cl ; 7.3. H3C : K?
Литература [ 1 ], с.22-38
Методические указания по теме 1.2. Элементный анализ органических соединений
При изучении данной темы необходимо обратить внимание на установление формул веществ по результатам качественного анализа.
Установить формулу вещества – значит, найти количество атомов каждого элемента в молекуле вещества
Установление формул веществ по их плотности и количественному составу
ПРИМЕР 1. Установить формулу вещества, содержащего 80% углерода и 20% водорода, если масса 1л его при нормальных условиях равна 1,34г.
Решение:
1. Вычисляем массу газа количеством вещества 1моль
1,34г - 1л
Хг - 22,4л Х = 1,34г•22,4л / 1л = 30г
2.Вычисляем массу углерода в молекуле:
m (C) где: w (C) – массовая доля углерода (в%) ;
w (C) = ¾¾¾¾¾ ·100% m (C) – масса углерода;
M (CxHy) M (CxHy) – молярная масса углерода.
m(С) = M (CxHy) • w (C)/100% = 30г • 0,8 = 24г
3. Вычисляем количество вещества атомов углерода
n = m/M n(C) = 24г/12г/моль = 2моль
4. Вычисляем массу водорода
m(H) = 30г• 0,2 = 6г
5. Вычисляем количество вещества атомов водорода
n(H) = 6г / 1г/моль = 6моль
Формула С2Н6
ПРИМЕР 2. Массовая доля углерода в углеводороде составляет 83,33%. Относительная плотность паров этого вещества по водороду составляет 36. Определить формулу углеводорода.
Решение:
1.Вычисляем молярную массу вещества:
М(СхНу) = 2г/моль • 36 =72г/моль
2.Берём образец количеством вещества 1моль и определяем его массу:
m = n •M m(СхНу) = 1моль • 72 г/моль = 72г
3. Вычисляем массу углерода в молекуле:
m(С) = 72г • 0,8333 =60г
4. Вычисляем количество вещества атомов углерода:
n = m/M n(C) = 60г/12г/моль = 5моль
5. Вычисляем массу водорода:
m(H) = 72г – 60г = 12г
6. Вычисляем количество вещества атомов водорода:
n(H) = 12г / 1г/моль = 12моль Формула С5Н12
Установление молекулярных формул веществ по продуктам сгорания
ПРИМЕР 3. При сгорании 1,3г вещества было получено 4,4г диоксида углерода и 0,9г воды. Плотность паров вещества по водороду 39. Определите молекулярную формулу вещества.
Решение:
1.Вычисляем молярную массу вещества:
М(СхНу) = 2г/моль • 39 =78г/моль
2. Берём образец количеством вещества 1моль и определяем его массу:
m = n •M m(СхНу) = 1моль • 78 г/моль = 78г
3. Определяем массу диоксида углерода полученную при сгорании вещества количеством 1моль:
1,3г (СхНу) - 4,4г(СО2)
78г(СхНу) - Хг(СО2) Х = 78 • 4,4 /1,3 = 264г
4. Вычисляем массу углерода в молекуле:
44г (СО2) – 12г
264г(СО2) - Хг m(С) = Х = 264 • 12 /44 =72г
5. Вычисляем количество вещества атомов углерода:
n = m/M n(C) = 72г/12г/моль = 6моль
6. Определяем массу воды, полученной при сгорании вещества количеством 1моль:
1,3г (СхНу) - 0,9г (Н2О)
78г (СхНу) - Хг (Н2О) Х = 78 • 0,9 / 1,3 = 54г
7. Вычисляем массу водорода:
18г (Н2О) - 2г (Н)
54г (Н2О) - Хг (Н) m(H) = Х = 54•2 /18 = 6
8. Вычисляем количество вещества атомов водорода:
n(H) = 6г / 1г/моль = 6моль
9. Вычисляем массу углеводородной части в веществе:
m(С) + m (Н) = 72 + 6 = 78г
Следовательно, кислорода в веществе нет
Формула С6Н6
Установление молекулярных формул веществ по их общим формулам
Каждому классу органических соединений присуща общая формула, выражающая химический состав и отношение атомов элементов в молекуле вещества.
общая формула алканов СnН2n+2
общая формула алкенов СnН2n
общая формула алкинов СnН2n-2
ПРИМЕР 4. 1л газообразного алкана при нормальных условиях имеет массу 1,964г. Определите молекулярную формулу алкана.
Решение:
1. Вычисляем массу алкана количеством вещества 1моль
m = 1,964•22,4 /1 = 44г
2. Определяем число атомов углерода в молекуле по общей формуле
СnН2n+2 =44
12n +2n + 2 = 44
14 n = 44 – 2 = 42 n = 42 : 14 = 3
Следовательно, в искомой формуле 3 атома углерода,
а водорода 2n + 2, т. е. 2 • 3 + 2 = 8.
Формула С3Н8
Вопросы для самоконтроля
1. Какими химическими реакциями можно отличить органическое вещество от
неорганического?
2. Какие экспериментальные данные необходимы для установления эмпирической
формулы, молекулярной формулы?
3. Какие химические реакции лежат в основе определения содержания углерода и
водорода в органическом веществе?
4. Что такое явление гомологии?
5. Вывести формулу предельного углеводорода, имеющего элемен тарный состав:
C – 82,76 % и Н – 17,24 %
Литература [ 1 ], с.17 – 22
Методические указания по теме 2.1. Алканы
При изучении данной темы необходимо обратить внимание на составление названий органических соединений.
В последние годы в научной, а также в учебной химической литературе в качестве систематической используется преимущественно номенклатура органических соединений, разработанная Международным союзом теоретической и прикладной химии, номенклатура ИРАС (ИЮПАК), обычно именно её называют “международной систематической номенклатурой”. В учебной литературе ещё используется и рациональная номенклатура.
1. Приступая к выполнению упражнений по номенклатуре, необходимо прежде всего изучить этот вопрос по учебнику, где детально рассмотрены рекомендации для названия данного класса органических веществ и номенклатурные системы. Здесь же даны лишь краткие характеристики рекомендуемых номенклатур и приведены примеры.
2. Необходимо обращать внимание на правильное написание названий. Например, в названиях по международной номенклатуре цифры должны отделяться от слов чёрточками, а цифры от цифр – запятой: 1,4-дибром-2,3-диметил-бутан.
Хотя составные части названий принято писать слитно, по дидактическим соображениям сложные названия можно разделять чёрточками.
Например: название метилэтилпропилизобутилметан может быть написано и рекомендуется писать так:
метил-этил-пропил-изобутил-метан.
В расчлененном на составные части названии нагляднее представляется строение соединения и его формула
Вопросы для самоконтроля
1. Какие углеводороды называются алканами?
2. Что такое сигма – связь?
3. Напишите структурные формулы изомеров состава С5 Н12 и назовите их по
рациональной и современной международной номенклатуре.
4. Напишите структурные формулы радикалов состава С4Н9 и назовите их.
5. Какие способы получения алканов Вам известны? Проиллюстрируйте их на примере синтеза пропана.
Литература [ 1 ], с.41 – 57
Методические указания по теме 2.2. Циклоалканы
При изучении данной темы необходимо обратить внимание на особенности химических свойств циклоалканов в зависимости от строения молекул; на способы получения циклоалканов в промышленности и лаборатории.
Вопросы для самоконтроля
1. Какие углеводороды называются циклоалканами?
2. Напишите структурные формулы изомерных циклоалканов состава С4Н8 и назовите их.
3. Какие вещества образуются при действии на циклогексан брома, бромоводорода?
4. Напишите уравнения реакций окисления циклобутана и циклогексана.
Литература [ 1 ], с.59 – 65
Методические указания по теме 2.3. Алкены
При изучении данной темы необходимо обратить внимание на составление структурных формул – изомеров алкенов.
Имеется несколько видов структурной изомерии в алкенах:
- изомерия углеродного скелета;
- изомерия положения кратных связей;
- пространственная изомерия.
Для вывода структурных формул всех изомеров, обусловленных различным положением кратных связей, поступают следующим образом:
выводят все структурные изомеры, связанные с изомерией углеродного скелета;
перемещают графически кратную связь в те положения, в которые это возможно с точки зрения четырёхвалентности углерода.
ПРИМЕР: Написать структурные формулы всех пентенов состава С5Н10.
Решение:
1. Составим формулы всех изомеров, различающихся строением углеродного скелета:
а) С – С – С – С – С б) С – С – С – С в) С
½ ½
С С – С – С
½ 2.Переместим кратную связь для случаев а) и б) С
 → С = С– С – С – С СН2 = СН – СН2 – СН2 – СН3
→ С = С– С – С – С СН2 = СН – СН2 – СН2 – СН3
а) С – С – С – С – С –
→ С – С = С – С – С СН3 – СН = СН – СН2 – СН3
 → С = С – С – С СН2 = С – СН2 – СН3
→ С = С – С – С СН2 = С – СН2 – СН3
½ ½
С СН3
б) С – С – С – С ¾ → С – С – С – С СН3 – С = СН – СН3
½ ½ ½
С С СН3
→ С – С – С ═ С СН3 – СН – С = СН2
½ ½
С СН3
Таким образом для С5Н10 возможно пять изомеров алкенов.
Вопросы для самоконтроля
1. Какие углеводороды называются алкенами?
2. Как образуется p - связь?
3. Напишите структурные формулы всех изомерных алкенов состава С5Н10 и
назовите их по рациональной и современной международной номенклатурам.
4. Напишите структурные формулы :
4.1. изопропилэтилена;
4.2. a, b - диметилэтилена.
Назовите их по современной международной номенклатуре.
5. Какие вещества можно получить при каталитическом дегидрировании пропана и бутана?
6. Какие вещества образуются при присоединении бромоводорода к алкенам состава С4Н8?
7. Напишите уравнения реакций окисления пропилена в различных условиях:
7.1. горение на воздухе;
7.2. действие щелочного раствора КмnO4 на холоде;
7.3. действие раствора КмnО4 в присутствии кислоты при нагревании.
Литература [ 1 ], с.66 –80
Методические указания по теме 2.4. Алкины
При изучении данной темы необходимо обратить внимание на определение количества орбиталей в молекулах углеводородов.
Пример 1. Указать типы электронных орбиталей и объяснить, сколько орбиталей типа s, p, sp, sp2, sp3 образуют молекулу органического вещества.
Для определения типа гибридизации и подсчета количества орбиталей типа s, p, sp, sp2, sp3 необходимо знать: что гибридизация – это смешение орбиталей и их выравнивание по форме и энергии.
Для атома углерода возможны три валентных состояния с различными типами гибридизации, именно, sp3, sp2, sp – гибридизация.
sp3 – гибридизация состоит в том, что в момент образования связей возбужденный атом углерода пересматривает одну s – и три р – орбитали таким образом, что получаются четыре эквивалентные гибридные орбитали, каждая из которых представляет собой продукт смешения (25% s - и 75%
р - орбиталей). Число гибридных орбиталей всегда равно числу исходных.
| | | | здесь указаны только валентные злектроны атома углерода, |
2s 2px 2py 2pz подвергающиеся гибридизации.
4 (sp3) Такой тип гибридизации характерен для алканов.
В результате перекрывания гибридных sp3 – орбиталей атома углерода и s – орбиталей четырех атомов водорода образуется молекула метана с прочными
s - связями, т. е. молекула метана имеет: sp3 – орбитали – 4, s – орбитали – 4, так как s – орбитали имеются только у атомов водорода.
В молекуле этана СН3-СН3 образованной из двух углеродных тетраэдров количество орбиталей равно:
sp3 – орбитали – 4 х 2 = 8
s – орбитали – 3 х 2 = 6
sp2 – гибридизация – смешение одной s – орбитали и двух p – орбиталей: образуются три гибридизованные орбитали.
| | | | После гибридизации остается негибридизованная 2pz орбиталь. |
2s 2px 2py 2pz
3 (sp2) Такой тип гибридизации характерен для алкенов.
Рассмотрим задачу.
Написать структурную формулу пропилена, над атомами углерода указать типы гибридизации электронных орбиталей, указать сколько орбиталей типа s, p, sp, sp2, sp3 образуют молекулу пропилена.
Решение:
Обозначим у каждого атома углерода его валентное состояние – тип гибридизации электронных орбиталей.
sp2 sp2 sp3
СН2 = СН – СН3
1 2 3
Орбитали типа sp2 образует первый и второй углеродный атом, т. е. их 3х2=6. Первый и второй атом углерода содержит ещё по одной р – орбитали, которые образуют p – связь, их всего 2. Третий углеродный атом находится в состоянии sp3 – гибридизации. Следовательно, орбиталей sp3 всего - 4. Так, количество орбиталей в молекуле пропилена:
sp3 – орбитали – 4
sp2 – орбитали – 6
р – орбитали – 2
s – орбитали – 6
sp – гибридизация – смешение одной s – орбитали и одной p – орбитали: образуются две гибридные орбитали.
| | | | После гибридизации остается негибридизованы две р орбитали. |
2s 2px 2py 2pz
2 (sp) Такой тип гибридизации характерен для алкинов.
В молекуле ацетилена оба атома углерода находятся в состоянии sp – гибридизации.
sp sp
CH º CH
Каждый атом углерода имеет по две гибридные орбитали и по две негибридизованные р – орбитали, т. е. в молекуле ацетилена находится:
sp – орбиталей – 2 х 2 = 4
р – орбиталей – 2 х 2 = 4
s – орбиталей – 1 х 2 = 2
Вопросы для самоконтроля
1. Какова общая формула алкинов?
2. Какова особенность в строении молекул алкинов?
3. Напишите структурные формулы изомеров алкинов состава С5Н8
и назовите их по рациональной и современной международной номенклатуре.
4. Напишите структурные формулы нескольких гомологов ацетилена.
5. Какие общие свойства у алкенов и алкинов? Чем они обусловлены? На
пишите соответствующие уравнения реакций.
6. При каких условиях, и каким способом можно из метана получить
ацетилен?
Литература [ 1 ], с.83 – 9 6
Методические указания по теме 2.5. Диеновые углеводороды
При изучении данной темы необходимо обратить внимание на:
- природу сопряжённой связи в молекулах диеновых углеводородов;
- особенности химических свойств сопряжённых алкадиенов;
- зависимость свойств природного и синтетического каучука от строения молекул.
Вопросы для самоконтроля
1. Какие углеводороды называются алкадиенами?
2. Какова общая формула диеновых углеводородов?
3. Какова особенность в строении молекул диеновых углеводородов?
4. Напишите структурные формулы сопряжённых диенов состава С5Н8 и
назовите их.
Литература [ 1 ], с.83 – 9 6
Методические указания по теме 2.6. Ароматические углеводороды
При изучении данной темы необходимо обратить внимание на составление структурных формул изомеров ароматических углеводородов.
ПРИМЕР: Составить структурные формулы всех ароматических углеводородов состава С8Н10.
РЕШЕНИЕ:
В случае ароматических соединений возможна изомерия скелета в боковой цепи и изомерия положения заместителей в ароматическом кольце.
1. Составим структурную формулу с нормальной боковой цепью:
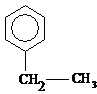
2. Укоротим боковую цепь на один атом углерода и произведем все возможные перестановки СН3 в бензольном кольце.
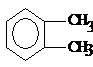
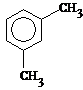
![]()
Имеется 4 изомера состава С8Н10
Вопросы для самоконтроля
1. Каково современное представление о строении молекул бензола?
2. Чем определяется изомерия гомологов бензола?
3. Напишите формулы изомеров аренов состава С8Н10 и назовите их.
4. Напишите структурные формулы соединений:
4.1. n.– ксилола;
4.2. м. – метилизопропилбензола;
4.3. о. – диэтилбензола.
5. Объясните в чём сходство бензола с алканами и алкенами?
6. Напишите уравнения реакций получения из бензола орто - и пара-
хлортолуола. Объясните последовательность реакций на основе
правил ориентации.
Литература [ 1 ], с.100 –134
Методические указания по теме 2.7. Нефть и продукты её переработки
При изучении данной темы необходимо обратить внимание на особенности физических свойств нефти, на физические и химические методы переработки нефти.
Вопросы для самоконтроля
1. Почему нефть не имеет постоянной температуры кипения?
2. В чём сущность процесса перегонки нефти?
3. Какие наиболее важные фракции образуются при перегонке нефти?
4. Какие химические методы переработки нефти Вы знаете?
5. В чём сущность пиролиза нефти?
6. Каково значение нефти и нефтепродуктов в народном хозяйстве?
Литература [ 1 ], с.100 –134
Методические указания по теме 3.1. Галогенопроизводные
При изучении данной темы необходимо обратить внимание на правильность в написании формул, уравнений и схем реакций, характеризующих химические свойства монофункциональных соединений.
Рекомендации к написанию формул, уравнений и схем реакций
1. При выполнении упражнений необходимо обращать особое внимание на правильность написания структурных формул органических соединений. Удобнее всего использовать полуразвернутые (упрощенные) структурные формулы, в которых черточками указываются все связи между атомами, за исключением связей с атомами водорода. Формулы с горизонтально написанной углеродной цепью выгодно по возможности писать так, чтобы функциональные группы, находящиеся на конце цепей, располагались справа, а заместители у неконцевых атомов углерода – под или над углеродной цепью:
CH3
½
CH3 – CH – CH2 – Br CH3 – CH2 – CH – CH3
½
Br
CH3
½
CH3 – CH – CH3 – Br CH3 – CH2 – CH2 – CH2 – Br
½
Br
2. В начальных упражнениях с формулами ароматических соединений
в бензольных ядрах лучше писать все С – и Н – атомы. При упрощенном изображении бензольных колец замещающие атомы и группы необходимо отчетливо соединять с атомами бензольного ядра валентными черточками.
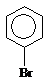
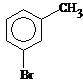
3. Органические реакции могут быть выражены уравнениями, в которых набирают коэффициенты и уравнивают количество атомов в правой и левой частях. Однако часто пишут не уравнения, а схемы реакций. Так поступают в тех случаях, когда процесс протекает одновременно в нескольких направлениях или через ряд последовательных стадий, например:
 CH3 – CH2 – CH2 – CI + HCI
CH3 – CH2 – CH2 – CI + HCI
CI2
 CH3 – CH2 – CH3
CH3 – CH2 – CH3
свет
СH3 – CH – CH3 + HCI
½
CI
или
NаOH, t°C CuО, t°C
CH3 – CH2 – CI –––––––® CH3 – CH2 – OH –––––® CH3 – CH = O
Как показано в приведенных примерах, схемах действующий реагент изображают над стрелкой. Для простоты коэффициенты в правой и левой частях схемы не уравнивают, а некоторые вещества, такие, как, например Cu, H2O, NaCI и т. д. образующиеся при реакциях, в схемах или совсем не показывают, или указывают под стрелкой со знаком минус. Направление превращений веществ в реакциях указывается стрелкой. Над стрелкой указывают реагенты и условия реакций, катализатор и т. п.
Вопросы для самоконтроля
1. Напишите электронные формулы следующих молекул:
СН3 - Вr, СН2 = СНВr, СН3 - СН – Вr
ê
СН3
2. Напишите структурные формулы изомеров состава С4Н9Сl и назовите их по
рациональной номенклатуре.
3. При помощи каких реакций можно осуществить следующие превращения:
3.1. ацетилен ® 1,1 – дихлорэтан
3.2. метилацетилен ® 2,2 – дихлорпропан
4. При каких условиях осуществляется хлорирование толуола в ядро и бо
ковую цепь? Назовите образующиеся соединения.
5. Напишите уравнения реакций получения из хлористого этила: этилового
спирта, этилена пропионитрила.
6. Напишите схему механизма щелочного гидролиза хлористого этила и укажите факторы, влияющие на его скорость.
7. Укажите способы получения фторэтана, тетрафторэтилена.
Литература [ 1 ], с.139 – 150
Методические указания по теме 3.2. Гидроксильные соединения и их
производные
При изучении данной темы необходимо обратить внимание на особенности физических свойств и токсичность гидроксильных соединений и их производных.
Вопросы для самоконтроля
1. Что называется спиртами?
2. Напишите структурные формулы изомеров одноатомных спиртов состава
С4Н9ОН и назовите их по рациональной и современной международной
номенклатурам.
3. Напишите структурные формулы спиртов и назовите их по современной
международной номенклатуре:
3.1. метил-этил-карбинол;
3.2. вторичный бутиловый спирт;
3.3. метил-винил-карбинол.
4. Какие спирты можно получить при гидратации в кислой среде:
4.1. 2-метилпропена;
4.2. триметилэтилена.
5. Какие способы используются для промышленного получения метилового спирта?
6. Какими способами получают этиловый спирт в промышленности? Напишите
уравнения соответствующих реакций.
Литература [ 1 ], с.152 – 184
Методические указания по теме 3.3 Альдегиды и кетоны
При изучении данной темы необходимо обратить внимание на качественные реакции на альдегиды и кетоны, токсичность действия альдегидов и кетонов на живые организмы.
Вопросы для самоконтроля
1. Какие органические соединения относятся к альдегидам и кетонам?
2. Напишите структурные формулы всех возможных альдегидов состава С4Н8О и
назовите их по рациональной и международной номенклатурам.
3. Напишите структурные формулы карбонильных соединений:
3.1. 2-метилбутаналь;
3.2. 2,3-диметилпентаналь;
3.3. 2-метилбутанон-2
и назовите их по рациональной номенклатуре
4. Напишите уравнения реакций получения пропионового альдегида путём:
4.1. окисления пропилового спирта;
4.2. оксосинтеза соответствующего алкена;
4.3. из ацетиленового углеводорода по реакции Кучерова.
5. Напишите схемы получения ацетона из следующих исходных веществ:
5.1. этилового спирта;
5.2. пропилена;
5.3. ацетилена.
Литература [ 1 ], с.187-214
Методические указания по теме 3.4. Карбоновые кислоты и их производные. Липиды
При изучении данной темы необходимо обратить внимание на особенности физических и химических свойств карбоновых кислот и их производных, их получении и применении в промышленности.
Вопросы для самоконтроля
1. Какие вещества называются карбоновыми кислотами?
2. Как они классифицируются?
3. Какова общая формула предельных одноосновных карбоновых кислот?
4. Напишите структурные формулы изомеров карбоновых кислот состава С5Н10О2 и
назовите их по рациональной и международной номенклатурам.
5. Почему карбоновые кислоты имеют аномально высокие температуры кипения и
плавления?
6. Какие кислоты получаются при окислении: пропилена, пропаналя, метилкетона,
этилбензола?
7. Напишите уравнения реакций взаимодействия уксусной кислоты с гидроксидом
натрия, бромом, пятихлористым фосфором, кетеном, этиловым спиртом. Назовите
полученные соединения.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |




