4.2. Примеры решения задач
Пример 1. Определить для серной кислоты: 1) относительную молекулярную массу Мr ,
2) молярную массу М.
Дано.
![]()
Мr, М = ?
Решение. Относительная молекулярная масса вещества равна сумме относительных атомных масс всех элементов, атомы которых входят в состав молекулы данного вещества, и определяется по формуле
Mr =
где ni - число атомов i-гo химического элемента, входящих в состав молекулы данного вещества; Ar,i - относительная атомная масса этого элемента. Относительные атомные массы приводятся в таблице . Химическая формула серной кислоты имеет вид H2SO4. Так как в состав молекулы серной кислоты входят атомы трех элементов, то стоящая в правой части равенства сумма будет состоять из трех слагаемых и эта формула примет вид
Mr=n1A1 +n2A2 + n3A3 =2*1+1*32 + 2*16 =98.
Значения относительных атомных масс водорода, серы, кислорода взяты в таблице . Зная относительную молекулярную массу Мr, найдем молярную массу серной кислоты по формуле
M=0,001Mr кг/моль =0,098 кг/моль.
Ответ.
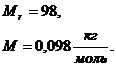
Пример 2. В баллоне объемом V=10 л находится гелий под давлением р1=1 МПа и при температуре Т1=300 К. После того как из баллона было взято m =10 г гелия, температура в баллоне понизилась до T2 =290 К. Определить давление p2 гелия, оставшегося в баллоне.
Дано.
He,
V=10 л,
р1=1 МПа,
Т1=300 К,
m =10 г,
T2 =290 К,
p2 =?
Решение. Для решения задачи воспользуемся равнением Менделеева-Клапейрона, применив его конечному состоянию газа
где m2 - масса гелия в баллоне в конечном состоянии, M - молярная масса гелия, R - молярная газовая постоянная. Из уравнения выразим искомое давление:
Массу m2 гелия выразим через массу m1, соответствующую начальному состоянию, и массу m гелия, взятого баллона:
m2=m1 - m.
Массу m1 гелия найдем также из уравнения Менделеева - Клапейрона, применив его к начальному состоянию:
Подставив выражение для массы m1 и m2, найдем
Ответ.
4.3. Задачи для контрольной работы по теме
«2. Молекулярная физика. Термодинамика»
201. Определить количество вещества и число молекул кислорода массой 0,5 кг.
202. Сколько атомов содержится в ртути: 1) количеством вещества 0,2 моль; 2) массой 1 г?
203. Вода при температуре 4°С занимает объем 1 см3. Определить количество вещества и число молекул воды.
204. Найти молярную массу и массу одной молекулы поваренной соли(N aC l ).
205. Определить массу одной молекулы углекислого газа(CO2).
206. Определить концентрацию молекул кислорода, находящегося в сосуде вместимостью 2 л. Количество вещества v кислорода равно 0,2 моль.
207. Определить количество вещества водорода, заполняющего сосуд объемом 3 л, если концентрация молекул газа в сосуде 2*1018 м -3.
208. В баллоне вместимостью 3л содержится кислород массой 10г. Определить концентрацию молекул газа.
209. Определить относительную молекулярную массу: 1) воды(H2O); 2) углекислого газа(CO2);
3) поваренной соли (N aC l ).
210. Определить количество вещества и число молекул азота массой 0,2 кг.
211. В цилиндр длиной 1,6 м, заполненный воздухом при нормальном атмосферном давлении, начали медленно вдвигать поршень площадью основания 200 см2. Определить силу, действующую на поршень, если его остановить на расстоянии 10 см от дна цилиндра.
212. В баллоне находится газ при температуре 400 К. До какой температуры надо нагреть газ, чтобы его давление увеличилось в 1,5 раза?
213. Баллон вместимостью 20 л заполнен азотом при температуре 400 К. Когда часть газа израсходовали, давление в баллоне понизилось на 200 кПа. Определить массу израсходованного газа. Процесс считать изотермическим.
214. В баллоне вместимостью 15л находится аргон под давлением 600 кПа и при температуре 300 К. Когда из баллона было взято некоторое количество газа, давление в баллоне понизилось до 400 кПа, а температура установилась 260 К. Определить массу аргона, взятого из баллона.
215. Два сосуда одинакового объема содержат кислород. В одном сосуде давление 2 МПа и температура 800 К, в другом 2,5 МПа, 200 К. Сосуды соединили трубкой и охладили находящийся в них кислород до температуры 200 К. Определить установившееся в сосудах давление.
216. Вычислить плотность азота, находящегося в баллоне под давлением 2 МПа и имеющего температуру 400 К.
217. Определить молярную массу газа, если при температуре 154 К и давлении 2,8 МПа он имеет плотность 6,1 кг/м3.
218. Найти плотность азота при температуре 400 К и давлении 2 МПа.
219. В сосуде вместимостью 40 л находится кислород при температуре 300 К. Когда часть газа израсходовали, давление в баллоне понизилось на 100 кПа. Определить массу израсходованного кислорода. Процесс считать изотермическим.
220. Определить плотность водяного пара, находящегося под давлением 2,5 кПа и имеющего температуру 250 К.
221. Определить внутреннюю энергию водорода, а также среднюю кинетическую энергию молекулы этого газа при температуре 300 К, если количество вещества этого газа равно 0,5моль.
222. Определить суммарную кинетическую энергию поступательного движения всех молекул газа, находящегося в сосуде вместимостью 3 л под давлением 540 кПа.
223. Количество вещества гелия 1,5 моль, температура 120 К. Определить суммарную кинетическую энергию поступательного движения всех молекул этого газа.
224. Внутренняя энергия одного моля некоторого двухатомного газа равна 6,02 кДж. Определить среднюю кинетическую энергию вращательного движения одной молекулы этого газа. Газ считать идеальным.
225. Определить среднюю кинетическую энергию одной молекулы водяного пара при температуре 500 К.
226. Определить среднюю квадратичную скорость молекулы газа, заключенного в сосуд вместимостью 2 л под давлением 200 кПа. Масса газа 0,3 г.
227. Водород находится при температуре 300 К. Найти среднюю кинетическую энергию вращательного движения одной молекулы, а также суммарную кинетическую энергию всех молекул этого газа; количество вещества водорода равно 0,5 моль.
228. При какой температуре средняя кинетическая энергия поступательного движения молекулы газа равна 4,14*10-21 Дж.
229. В азоте взвешены мельчайшие пылинки, которые движутся так, как если бы они были очень крупными молекулами. Масса каждой пылинки равна 6*10-10 г. Газ находится при температуре 400 К. Определить средние квадратичные скорости, а также средние кинетические энергии поступательного движения молекулы азота и пылинки.
230. Определить среднюю кинетическую энергию поступательного движения и вращательного движения молекулы азота при температуре 1000 К.
231. Определить молярную массу двухатомного газа и его удельные теплоемкости, если известно, что разность (cр - cv) удельных теплоемкостей этого газа равна 260 Дж/(кг*К).
232. Найти удельные ср и сv, теплоемкости углекислого газа.
233. Определить показатель адиабаты у идеального газа, который при температуре 350 К и давлении 0,4 МПа занимает объем 300 л и имеет теплоемкость Cv=857 Дж/К.
234. В сосуде вместимостью 6 л находится при нормальных условиях двухатомный газ. Определить теплоемкость Сv этого газа при постоянном объеме.
235. Определить относительную молекулярную массу и молярную массу газа, если разность его удельных теплоемкостей (ср - cv )=2,08 кДж/(кг*К).
236. Определить молярные теплоемкости газа, если его удельные теплоемкости сv=10,4кДж/(кг*К) и сp=14,6 кДж/(кг*К).
237. Найти удельные сv и ср теплоемкости азота.
238. Вычислить удельные теплоемкости газа, зная, что его молярная масса 4*10 -3 кг/моль и отношение теплоемкостей Ср/Сv=1,67.
239. Трехатомный газ под давлением 240 кПа и температуре 20°С занимает объем 10 л. Определить теплоемкость Ср этого газа при постоянном давлении.
240. Одноатомный газ при нормальных условиях занимает объем 5 л. Вычислить теплоемкость Сv этого газа при постоянном объеме.
241. Найти среднее число столкновений за время 1 с и среднюю длину свободного пробега молекулы гелия, если газ находится под давлением 2 кПа при температуре 200 К.
242. Определить среднюю длину свободного пробега молекулы азота в сосуде вместимостью 5л. Масса газа 0,5 г.
243. Водород находится под давлением 20 мкПа и имеет температуру 300 К. Определить среднюю длину свободного пробега молекулы такого газа.
244. При нормальных условиях длина свободного пробега молекулы водорода равна 0,160мкм. Определить диаметр молекулы водорода.
245. Какова средняя арифметическая скорость молекул кислорода при нормальных условиях, если известно, что средняя длина свободного пробега молекулы кислорода при этих условиях равна 100 нм?
246. Кислород находится под давлением 133 нПа при температуре 200 К. Вычислить среднее число столкновений молекулы кислорода при этих условиях за время 1 с.
247. При каком давлении средняя длина свободного пробега молекул азота равна 1 м, если температура газа 10°С?
248. В сосуде вместимостью 5л находится водород массой 0,5 г. Определить среднюю длину свободного пробега молекулы водорода в этом сосуде.
249. Средняя длина свободного пробега молекулы водорода при некоторых условиях равна 2мм. Найти плотность водорода при этих условиях.
250. В сферической колбе вместимостью 3л, содержащей азот, создан вакуум с давлением 80 мкПа. Температура газа 250 К. Можно ли считать вакуум в колбе высоким?
Примечание. Вакуум считается высоким, если длина свободного пробега молекул в нем много больше линейных размеров сосуда.
251. Определить количество теплоты, которое надо сообщить кислороду объемом 50 л при его изохорном нагревании, чтобы давление газа повысилось на 0,5 МПа.
252. При изотермическом расширении азота при температуре 280 К объем его увеличился в два раза. Определить: 1) совершенную при расширении газа работу; 2) изменение внутренней энергии; 3) количество теплоты, полученное газом. Масса азота 0,2 кг.
253. При адиабатном сжатии давление воздуха было увеличено от 50 кПа до 0,5 МПа. Затем при неизменном объеме температура воздуха была понижена до первоначальной. Определить давление газа в конце процесса.
254. Кислород массой 200 г занимает объем 100 л и находится под давлением 200 кПа. При нагревании газ расширился при постоянном давлении до объема 300 л, а затем его давление возросло до 500 кПа при неизменном объеме. Найти изменение внутренней энергии газа, совершенную газом работу и теплоту, переданную газу.
255. Объем водорода при изотермическом расширении при температуре З00 К увеличился в 3 раза. Определить работу, совершенную газом, и теплоту, полученную при этом. Масса водорода равна 200 г.
256. Азот массой 0,1 кг был изобарно нагрет от температуры 200 К до температуры 400 К. Определить работу, совершенную газом, полученную им теплоту и изменение внутренней энергии азота.
257. Во сколько раз увеличится объем водорода, содержащий количество вещества 0,4 моль при изотермическом расширении, если при этом газ получит количество теплоты 800 Дж? Температура водорода 300 К.
258. Какая работа совершается при изотермическом расширении водорода массой 5 г, взятого при температуре 290 К, если объем газа увеличивается в три раза?
259. Какая доля количества теплоты, подводимого к идеальному двухатомному газу при изобарном процессе, расходуется на увеличение внутренней энергии газа и какая доля - на работу расширения? Газ - многоатомный.
260. Определить работу, которую совершит азот, если ему при постоянном давлении сообщить количество теплоты 21 кДж. Найти также изменение внутренней энергии газа.
261. Идеальный газ совершает цикл Карно при температурах нагреваК и холодильника 400 К. Во сколько раз увеличится коэффициент полезного действия цикла, если температура нагревателя возрастет до 600 К?
262. Идеальный газ совершает цикл Карно. Температура нагревателя в четыре раза больше температуры холодильника. Какую долю количества теплоты, полученного за один цикл от нагревателя, газ отдаст холодильнику?
263. Определить работу изотермического сжатия газа, совершающего цикл Карно, КПД которого 40%, если работа изотермического расширения равна 8 Дж.
264. Газ, совершающий цикл Карно, отдал холодильнику теплоту 14 кДж. Определить температуру нагревателя, если при температуре холодильника 280 К работа цикла 6 кДж.
265. Газ, являясь рабочим веществом в цикле Карно, получил от нагревателя теплоту 4,38кДж и совершил работу 2,4 кДж. Определить температуру нагревателя, если температура холодильника 273 К.
266. Газ, совершающий цикл Карно, отдал холодильнику 67% теплоты, полученной от нагревателя. Определить температуру холодильника, если температура нагреваК.
267. Во сколько раз увеличится коэффициент полезного действия цикла Карно при повышении температуры нагревателя от 380 К до 560 К? Температура холодильника 280К.
268. Идеальная тепловая машина работает по циклу Карно. Температура нагреваК, температура холодильника 250 К. Определить термически КПД цикла, а также работу рабочего вещества при изотермическом расширении, если при изотермическом сжатии совершена работа 70 Дж.
269. Газ, совершающий цикл Карно, получает теплоту 84 кДж. Определить работу газа, если температура нагревателя в три раза выше температуры холодильника.
270. В цикле Карно газ получил от нагревателя теплоту 500 Дж и совершил работу 100 Дж. Температура нагреваК. Определить температуру холодильника.
271. Найти массу воды, вошедшей в стеклянную трубку с диаметром канала 0,8 мм, опущенную в воду на малую глубину. Считать смачивание полным.
272. Какую работу надо совершить при выдувании мыльного пузыря, чтобы увеличить его объем от 8 см3 до 16 см3? Считать процесс изотермическим.
273. Какая энергия выделится при слиянии двух капель ртути диаметром 0,8 мм и 1,2 мм в одну каплю?
274. Определить давление внутри воздушного пузырька диаметром 4 мм, находящегося в воде у самой ее поверхности. Считать атмосферное давление нормальным.
275. Пространство между двумя стеклянными параллельными пластинками с площадью поверхности 100 см2 каждая, расположенными на расстоянии 20 мкм друг от друга, заполнено водой. Определить силу, прижимающую пластинки друг к другу. Считать мениск вогнутым с диаметром, равным расстоянию между пластинками.
276. Глицерин поднялся в капиллярной трубке диаметром канала 1 мм на высоту 20 мм. Определить поверхностное натяжение глицерина. Считать смачивание полным.
277. В воду опущена на очень малую глубину стеклянная трубка с диаметром канала 1 мм. Определить массу воды, вошедшей в трубку.
278. На сколько давление воздуха внутри мыльного пузыря больше нормального атмосферного давления, если диаметр пузыря 5 мм?
279. Воздушный пузырек диаметром 2,2 мкм находится в воде у самой ее поверхности. Определить плотность воздуха в пузырьке, если воздух над поверхностью воды находится при нормальных условиях.
280. Две капли ртути радиусом 1,2 мм каждая слились в одну большую каплю. Определить энергию, которая выделится при этом слиянии. Считать процесс изотермическим.
5. Справочные данные
5.1. Единицы СИ, имеющие специальные наименования
Наименование | Обозначение | Краткое обозначение |
Длина | метр | м |
Масса | килограмм | кг |
Время | секунда | с |
Сила электрического тока | ампер | А |
Термодинамическая температура | кельвин | К |
Количество вещества | моль | моль |
Сила света | кандела | кд |
Плоский угол | радиан | рад |
Телесный угол | стерадиан | ср |
Частота | герц | Гц |
Наименование | Обозначение | Краткое обозначение |
Сила | ньютон | Н |
Энергия, работа, теплота | джоуль | Дж |
Мощность | ватт | Вт |
Электрический заряд | кулон | Кл |
Потенциал | вольт | В |
Электрическая емкость | фарад | Ф |
Электрическое сопротивление | ом | Ом |
Магнитный поток | вебер | Вб |
Магнитная индукция | тесла | Тл |
Индуктивность | генри | Гн |
Освещенность | люкс | лк |
5.2. Множители и приставки для образования десятичных кратных и дольных единиц
и их наименования
Приставка | Обозначение | Множитель |
экса | Э | 1018 |
пэта | П | 1015 |
тера | Т | 1012 |
гига | Г | 109 |
мега | М | 106 |
кило | к | 103 |
гекто | г | 102 |
дека | да | 101 |
деци | д | 10-1 |
санти | с | 10-2 |
милли | м | 10-3 |
микро | мк | 10-6 |
нано | н | 10-9 |
пико | пк | 10-12 |
фемто | ф | 10-15 |
атто | а | 10-18 |
5.3. Основные физические постоянные

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |




