
Автор-составитель:
, д. т.н, профессор
Учебно-методический комплекс по дисциплине Химия составлен в соответствии с требованиями Государственного образовательного стандарта высшего профессионального образования и на основании примерной учебной программы данной дисциплины в соответствии с государственными требованиями к минимуму содержания и уровню подготовки инженера по специальности 190701.65 Организация перевозок и управление на транспорте. Дисциплина входит в федеральный компонент цикла общих математических и естественнонаучных дисциплин специальности и является обязательной для изучения. Данный учебно-методический комплекс рассмотрен и одобрен на заседании Учебно-методической комиссии РОАТ. Протокол №4 от 01.01.2001.
Содержание
Рабочая учебная программа по дисциплине …………………………………… | 4 |
Конспект лекций по дисциплине ……………………………………………….. | 16 |
Методические указания студентам ……………………………………………. | 38 |
Методические указания преподавателям ……………………………………… | 39 |
Экзаменационные вопросы по дисциплине …………………………………… | 40 |
Экзаменационные билеты по дисциплине …………………………………….. | 43 |

1.1 ЦЕЛИ И ЗАДАЧИ ДИСЦИПЛИНЫ
Дисциплина «Химия» относится к блоку естественнонаучных дисциплин Государственного образовательного стандарта высшего профессионального образования и предназначена для студентов инженерно-технических специальностей. Изучение дисциплины способствует развитию познавательных интересов, интеллектуальных и творческих способностей, самостоятельности в приобретении новых знаний. Данная рабочая программа посвящена химическим основам понимания природных и техногенных явлений, с учетом специализации выпускников транспортного вуза.
В курсе «Химия» изучаются фундаментальные законы химии, как основа современной технологии. Без глубокого изучения химических законов невозможно понимание современных технологических процессов, использующихся в промышленности, на транспорте, в строительстве, природных явлениях и в защите окружающей среды.
Цель изучения дисциплины - ознакомить студентов с процессами превращения веществ, сопровождающихся изменением химических и физических свойств, создание теоретической базы для успешного усвоения ими специальных дисциплин и, в частности, – формирование научного и инженерного мышления. Фундаментальная подготовка студентов соответствует целям и задачам ГОС ВПО по примерным программам инженерно-технических специальностей.
В современной жизни, особенно в производственной деятельности человека, химия имеет исключительно важное значение. На различных предприятиях железнодорожного транспорта многие производственные процессы связаны с химическими процессами: в гальванических цехах, на шпалопропиточных заводах, в котельных, при сварочных и газорезных работах на предприятиях по ремонту подвижного состава, при нанесении лакокрасочных покрытий, во время химической чистке тканевых изделий для железнодорожного транспорта, в цехах по переработке отходов, на очистных сооружениях и т. д..
Коррозия металлов и железобетона, также является целью изучения химии. Железнодорожный транспорт (транспортные сооружения, оборудование, подвижной состав) работает в сложных природных условиях, перевозит грузы различной химической агрессивности, подвергается электрокоррозии (утечка блуждающих токов). В результате, наблюдается интенсивное разрушение металлических и железобетонных конструкций (трубопроводов, рельсов, опор, кабелей, мостов и др. объектов). Повышенные коррозионные процессы происходят также на других объектах железнодорожного транспорта: локомотивных и вагонных депо, гальванических цехах и многих других предприятиях, использующих агрессивные соединения (щелочи, кислоты, хлориды, сульфаты, ПАВ и др.).
Таким образом, изучение методов защиты металлов от коррозии также является целью изучения химии.
Задачей изучения дисциплины являются: 1) профессиональная подготовка специалистов и получения будущими специалистами необходимых знаний о средствах и мерах защиты металлов от коррозии, применении легированных сталей на железнодорожном транспорте и умении выбора химической и электрохимической защиты, применении прогрессивных технологий таких, как электролиз и гальванические элементы различных типов на предприятиях железнодорожного транспорта и на подвижном составе; 2) получение дипломированными специалистами теоретических представлений и практических навыков применения прогрессивных технических знаний, обеспечивающих высокий университетский уровень инженера.
Данная программа построена в соответствии с требованиями Государственного образовательного стандарта и Примерной программы дисциплины «Химия» Министерства образования Российской Федерации, принятой 08.12.2000 г.
Представляемый курс включает входящие в программу «Химия» разделы: Строение вещества, Общие закономерности химических процессов, Растворы, Электрохимические процессы.
1.2 ТРЕБОВАНИЯ К УРОВНЮ ОСВОЕНИЯ СОДЕРЖАНИЯДИСЦИПЛИНЫ
В ходе изучения дисциплины «Химия» должны быть сформированы знания и умения использовать: фундаментальные понятия, законы, модели классической и современной химии.
Изучив дисциплину «Химия», согласно Государственному образовательному стандарту высшего профессионального образования и государственные требования к минимуму содержания и уровню подготовки выпускника предполагают, что в результате изучения дисциплины студент должен:
- иметь представление: о предмете, цели, задачах дисциплины и об ее значении для будущей профессиональной деятельности;
о превращениях веществ, составе и строении веществ, зависимости свойств растворов от их состава и внешних условий, оценивать энергетические затраты при превращении одних веществ в другие, а также о законах и закономерностях протекания во времени сложных и взаимосвязанных явлений, физико-химических методах анализа, производственного контроля.
- знать:
· основные законы и закономерности химии,
· строение вещества на современном уровне,
· расчеты концентрации растворов, произведения растворимости для возможности грамотно пользоваться справочной литературой,
· рассчитывать электродвижущую силу гальванических элементов и количеств веществ, образующихся при электролизе и для оценки скорости коррозионных процессов,
· механизмы и условия протекания химических реакций,
· предвидеть их результаты,
· определять возможность управлять химическим процессом на основании энергетических оценок,
· проводить реакции быстрее и в нужном направлении и в условиях наиболее приемлемых для производственных масштабов;
· разбираться в методах качественной аналитики.
- уметь:
· работать с химическими реактивами,
· применять физико-химические методы для решения задач в области взаимосвязанных явлений, для решения задач производственного контроля.
- приобрести навыки:
· использования учебной и технической литературы,
· информационных материалов из Интернета,
· работы с приборами,
· проведения измерений и расчётов, решения химических задач,
· осмысления, анализа и защиты полученных результатов.
Знания и навыки, полученные при изучении дисциплины «Химия» дают возможность студентам изучать все последующие дисциплины учебного плана на качественно более высоком уровне.
1.3 ОБЪЕМ ДИСЦИПЛИНЫ И ВИДЫ УЧЕБНОЙ РАБОТЫ
Форма обучения – ОЧНАЯ
Вид занятий | часы |
Аудиторные занятия: | 90 |
Лекции | 54 |
Лабораторные работы | 18 |
Практические занятия | 18 |
Индивидуальные занятия | 4 |
Самостоятельная работа | 6 |
ВСЕГО ЧАСОВ НА ДИСЦИПЛИНУ | 100 |
Экзамен (количество) | 2 |
1.4 СОДЕРЖАНИЕ КУРСА
1. Раздел «Строение вещества»
1.1. Введение.
Основные цели и задачи курса.
Химия как предмет естествознания. Предмет химии и ее связь с другими науками. Значение химии в формировании научного мировоззрения в изучении природы и развитии техники. Химизация производства и сельского хозяйства. Химия и охрана окружающей среды.
1.2.Строение атома и систематика химических элементов
1.2.2.Квантово - механическая модель атома. Квантовые числа. Атомные орбитали. Принцип Паули. Правила и порядок заполнения атомных орбиталей. Строение многоэлектронных атомов.
Периодическая система элементов . Изменение свойств химических элементов и их соединений. Окислительно - восстановительные свойства элементов. Значение периодического закона .[5, 4-19; 2, 17-31; 6, модели II-III, семы 1,2]
1.3. Химическая связь
Основные типы и характеристики химической связи. Ковалентная и ионная связь. Метод валентных связей, понятие о методе молекулярных орбиталей. Строение и свойства простейших молекул.[5, 20-35; 2, 35-48; 4, 96-120]
1.4. Типы взаимодействия молекул. Комплексные соединения
Основные виды взаимодействия молекул. Силы межмолекулярного взаимодействия. Водородная связь. Донорно - акцепторное взаимодействие молекул. Комплексные соединения. Комплексы, комплексообразователи, лиганды, заряд и координационное число комплексов. Типы комплексных соединений. Понятие о теориях комплексных соединений.[5, 19-20; 4, 98-113; 6, модель IV, схема 3]
1.5. Химия вещества в конденсированном состоянии
Агрегатное состояние вещества. Химическое строение твердого тела. Аморфное и кристаллическое состояние вещества. Кристаллы. Кристаллические решетки. Химическая связь в твердых телах. Металлическая связь и металлы, химическая связь в полупроводниках и диэлектриках. Реальные кристаллы.[4, 114,185-188; 2, 82-110; 6, модель IX, схема 9]
2.Раздел «Общие закономерности химических процессов»
2.1. Энергетика химических процессов. Химическое равновесие.
Энергетические эффекты химических реакций. Внутренняя энергия и энтальпия. Термохимия. Законы Гесса. Энтальпия образования химических соединений. Энтропия и ее изменение при химических процессах. Энергия Гиббса и энергия Гельмгольца и ее изменение при химических процессах. Условия самопроизвольного равновесия. Константа равновесия и ее связь с термодинамическими функциями. принцип Ле - Шателье.[5, 37-42; 3, 121-129; 4, 121-127; 6, модель VI, схема 4]
2.2. Равновесие в гетерогенных системах
Химическое равновесие в гетерогенных системах. Фазовое равновесие и правило фаз. Физико - химический анализ двухкомпонентных систем. Распределение третьего компонента между двумя несмешивающимися жидкостями. Экстракция. Сорбция. Поверхностные вещества. Адсорбция. Адсорбционное равновесие.
Гетерогенные дисперсные системы. Коллоидные системы и их получение. Строение коллоидных частиц. Агрегативная и кинетическая устойчивость систем. Коагуляция. Эмульсии. Суспензии.[5, 74-87; 2, 231-242; 6, модель VI, схема 6]
2.3. Химическая кинетика
Скорость химической реакции и ее зависимость от концентрации и температуры. Константа скорости реакции. Гомогенный катализ. Цепные реакции. Физические методы ускорения химических реакций. Скорость гетерогенных химических реакций. Гетерогенный катализ.
3.Раздел «Растворы»
Типы растворов, способы выражения концентрации растворов. Законы идеальных растворов. Растворы неэлектролитов и электролитов. Водные растворы электролитов. Сильные и слабые электролиты. Свойства растворов электролитов.
Активность. Электролитическая диссоциация воды. Водородный показатель среды. Ионные реакции в растворах. Произведение растворимости. Буферные растворы.
Гидролиз солей. Диссоциация комплексных соединений. Теория кислот и оснований.
4.Раздел «Электрохимические процессы»
4.1. Электрохимические процессы
Окислительно - восстановительные процессы: определение, термодинамика, составление уравнений реакций. Определение, классификация электрохимических процессов. Закон Фарадея. Термодинамика электродных процессов. Понятие об электродных потенциалах. Гальванические элементы. ЭДС и ее измерение. Стандартный водородный электрод и водородная шкала потенциалов. Уравнение Нернста. Потенциалы металлических, газовых и окислительно - восстановительных электродов. Кинетика электродных процессов. Электрохимическая и концентрационная поляризация. Электролиз. Последовательность электродных процессов. Выход по току. Электролиз с нерастворимыми и растворимыми анодами. Практическое применение электролиза. .[5, 88-100; 2, 259-270; 6, модель X, схема 11]
4.2. Коррозия и защита металлов и сплавов
Основные виды коррозии. Химическая коррозия. Электрохимическая коррозия. Коррозия под действием блуждающих токов. Метод защиты от коррозии: легирование, электрохимическая защита, защитные покрытия. Изменение свойств коррозионной среды. Ингибиторы коррозии.![]()
1.5 Лабораторные работы (лабораторный практикум)
Лабораторные занятия по дисциплине «Химия» проводятся в специально оборудованных лабораториях с применением необходимых средств обучения: лабораторного оборудования, образцов для исследований, методических пособий.
Поскольку в химической лаборатории находятся электроприборы, газ, вода, ядовитые и огнеопасные вещества, студенты должны строго соблюдать правила внутреннего распорядка и техники безопасности. Группа студентов должна быть перед лабораторными занятиями проинструктирована преподавателем, каждый студент заполняет журнал по лабораторной безопасности и расписывается.
Перед каждым лабораторным занятием студент должен изучить соответствующий раздел учебника, конспект лекций и описание лабораторной работы.
При оформлении отчета по проделанной работе в лабораторной тетради записывают дату, номер, название работы и опыта; конспект теоретического материала; краткое описание хода опыта и результаты, полученные при его выполнении. При выполнении лабораторной работы студент ведет рабочие записи результатов наблюдений и измерений (испытаний), оформляет расчеты. Окончательные результаты оформляются в форме выводов к работе.
№№ и названия разделов и тем | Цель и содержание лабораторной работы | Результаты лабораторной работы |
Лабораторная работа № 1 Химическая кинетика и химическое равновесие | ||
Раздел 2. Общие закономерности химичеких процессов Тема: 2.1 Энергетика химических процессов. Химическое равновесие. 2.3 Химическая кинетика. | Рассмотреть влияние различных факторов на скорость химической реакции и на смещение химического равновесия в обратимом процессе. | Наблюдение закона действующих масс (влияние концентрации на скорость химической реакции). Практическое овладение универсальным принципом Ле - Шателье. Умение управлять с его помощью обратимым процессом. |
Лабораторная работа № 2 Гидролиз солей | ||
Раздел 3. Растворы | Определить рН водных растворов солей. Проанализировать соли с точки зрения электролитической диссоциации. Овладение методикой составления уравнений гидролиза солей. | Овладение навыками составления уравнения гидролиза. Значения рН по теории и практическому измерению. Оценка точности измерения рН |
Лабораторная работа № 3 Электролиз растворов солей | ||
Раздел 4. Электрохимические процессы. Тема: 4.1. Электрохимические процессы | Ознакомление с основными положениями электрохимии и закономерностями протекания электролиза | Составление уравнений электродных реакций. Определение процесса, протекающего на катоде и аноде. Оценка количества выхода продуктов электролиза. |
Лабораторная работа № 4 Коррозия металлов | ||
Раздел 4. Электрохимические процессы Тема: 4.2. Коррозия и защита металлов и сплавов | Ознакомиться с теорией коррозионных процессов, принципами защиты от коррозии и выполнить ряд экспериментов, подтверждающих основные положения теории. | Составление уравнений реакций электрохимической коррозии металлов в зависимости от вида металлического покрытия. Оценка его устойчивости в агрессивной (кислой) среде. Доказательство наличия выхода окисленного металла из - под покрытия методом качественной реакции. |
1.6 Самостоятельная работа
Разделы и темы для самостоятельного изучения | Виды и содержание самостоятельной работы |
1. Раздел «Строение вещества» 5.2. Химия металлов Зависимость свойств металлов от их положения в периодической системе . Интерметаллические соединения и твердые растворы металлов. Основные методы получения металлов. Физико - химические процессы при сварке и пайке металлов, d - элементы IV - VII групп. Химия элементов семейства железа, их химические соединения. Химия платиновых металлов. Химия металлов подгрупп меди и цинка.[2, 341-370; 3, 275-302] 5.3. Химия неметаллических элементов Неметаллы и полуметаллы. Зависимость свойств неметаллов от их положения в периодической системе . Бор и его соединения. Элементы VI и VII групп и их соединения.[2, 382-410; 3, 325-341] 5.4. Неорганическая химия элементов IV группы. Химия полупроводников Углерод и его аллотропные формы. Монооксид и диоксид углерода. Карбонаты. Силикаты. Стекла. Ситаллы. Фарфор, техническая и строительная керамика. Сверхпроводящие материалы. Элементные полупроводники. Полупроводниковые соединения. Физико - химические способы обработки полупроводников.[4, 254-272] 5.10. Ядерная химия. Радиохимия Состав атомных ядер. Изотопы. Радиоактивность. Радиоактивные ряды. Химическое воздействие ионизирующих излучений на вещества. Использование радиоактивных изотопов. Искусственная радиоактивность. Ядерные реакции. Ядерная энергетика. Химия тория, урана, плутония и других радиоактивных элементов и материалов.[4,501-511; 2, 516-530] | Проработка учебного материала по учебной и научной литературе, работа с вопросами для самопроверки. Обсуждение проблемных вопросов с преподавателями в рамках индивидуальных консультаций. Выполнение тестов и заданий, размещенных в системе КОСМОС для самопроверки. |
2. Раздел «Растворы» 5.1.Свойства растворов. растворимость, буферные растворы [ 1,; 2, ].Равновесие в гетерогенных системах. Фазовое равновесие и понятие фаз. Экстракция. Сорбция. Поверхностные вещества. Адсорбция. Адсорбционное равновесие [ 1,; 2, ].Гетерогенные дисперсные системы. Коллоидные системы и их получение. Строение коллоидных частиц. Агрегативная и кинетическая устойчивость систем. Коагуляция. Эмульсии. Суспензии [ 1,; 2, ]. 5.7. Химия воды Строение молекул и свойства воды. Диаграмма состояния воды. Диаграмма плавкости систем типа вода - соль. Кристаллизация воды и водных растворов в различных условиях. Химические свойства воды. Взаимодействие воды с простыми веществами и химическими соединениями. Природные воды и их состав. Жесткость воды. Коллоидные вещества природных вод и их удаление. умягчение и обессоливание воды. Методы осаждения, ионного обмена и мембранные методы.[1, 267-273; 2, 490-495; 6, схема 8] | Проработка учебного материала по учебной и научной литературе, работа с вопросами для самопроверки. Обсуждение проблемных вопросов с преподавателями в рамках индивидуальных консультаций. Выполнение тестов и заданий, размещенных в системе КОСМОС для самопроверки. |
3. Раздел «Полимеры» 5.5. Химия вяжущих веществ Определение и классификация вяжущих веществ и их свойства. Воздушные и гидравлические вяжущие вещества. Известковые и гипсовые вяжущие вещества. Портландцемент. Процессы схватывания и твердения. Бетон. Коррозия бетонов и методы борьбы с ней.[3, 65-90] 5.6. Элементы органической химии. Органические полимеры материалы Строение, классификация и свойства органических соединений. Углеводороды и их производные. Кремнийорганические соединения.[1, 179-194; 2, 419-430] Состав и свойства органического топлива. Термохимия топлива. Твердое топливо и его переработка. Жидкое и газообразное топливо. Понятие о физико - химических процесса горения топлива. Химия смазочно - охлаждающих средств, применяемых при обработке металлов и сплавов. Физико - химические свойства и механизм воздействия рабочих сред гидравлических систем. Химия полимеров. Метод получения полимеров. Зависимость свойств полимеров от состава и структуры. Химия полимерных конструкционных материалов. Химия композиционных материалов. Полимерные покрытия и клеи. Химия полимерных диэлектриков. Химия полимерных проводников.[1, 195-211; 2, 450-461; 6, модель IX, схема 10] | Проработка учебного материала по учебной и научной литературе, работа с вопросами для самопроверки. Обсуждение проблемных вопросов с преподавателями в рамках индивидуальных консультаций. Выполнение тестов и заданий, размещенных в системе КОСМОС для самопроверки. |
4. Раздел «Электрохимические процессы» 5.8. Электрохимические процессы в энергетике и машиностроении Химические источники тока. Электрохимические генераторы. Электрохимические преобразователи (хемотроны). Электрохимическкя обработка металлов и сплавов. Получение и свойства гальванопокрытий.[1, 106-213; 2, 290-298] | Проработка учебного материала по учебной и научной литературе, работа с вопросами для самопроверки. Обсуждение проблемных вопросов с преподавателями в рамках индивидуальных консультаций. Выполнение тестов и заданий, размещенных в системе КОСМОС для самопроверки. |
5. Раздел «Химия и охрана окружающей среды» 5.9. Химия и охрана окружающей среды Технический прогресс и экологические проблемы. Роль химии в решении экологических проблем. Продукты горения топлива и защита воздушного бассейна от загрязнения. Метод малоотходной технологии. Водородная энергетика. Получение и использование водорода.[1, 241-251; 2, 284-290] Охрана водного бассейна. Характеристика сточных вод. Методы очистки сточных вод. Методы замкнутого водоворота.[1, 265-278] | Проработка учебного материала по учебной и научной литературе, работа с вопросами для самопроверки. Обсуждение проблемных вопросов с преподавателями в рамках индивидуальных консультаций. Выполнение тестов и заданий, размещенных в системе КОСМОС для самопроверки. |
Результаты самостоятельной работы контролируются при аттестации студента при защите контрольной работы.
1.8 Учебно-методическое обеспечение дисциплины
Основная литература
1. Глинка, химия: Учебник/ . -17-е изд. - М.: Издательство Юрайт, 2010.
2. Коровин, химия: Учебник/ . -11-е изд. - М.: Высшая школа, 2009.
3. Ахметов, и неорганическая химия: Учебник/ . - 4-е изд.-М.: Высшая школа, 2001.
4. Угай, и неорганическая химия: Учебник/ . -2-е изд. - М.: Высшая школа, 2000.
5. Зубрев, химия на железнодорожном транспорте: Учебное пособие/ . -2-е изд. - М.: Желдориздат, 2002.
6. Заглядимова, в моделях, схемах и таблицах: Учебное пособие/ . – М.: МИИТ, 2011.
Дополнительная литература
1. Ахметов, и семинарские занятия по общей и неорганической химии: Учебное пособие/ , , . -4-е изд.-М.: Высшая школа, 2002.
2. Физическая химия. В 2 кн. Кн. 1. Строение вещества. Термодинамика: Учебник для вузов/ , , и др.; Под ред. . -3-е изд. - М.: Высшая школа, 2001.
3. Физическая химия. В 2 кн. Кн.2. Электрохимия. Химическая кинетика и катализ: Учебник для вузов/ , , и др.; Под ред. . -3-е изд. - М.: Высшая школа, 2001.
4. Задачи и упражнения по общей химии: Учебное пособие/ Под ред. . -4-е изд. - М.: Высшая школа, 2008.
5. Пузаков, задач и упражнений по общей химии: Учебное пособие/ , , . - М.: Высшая школа, 2004.
1. 9 Материально-техническое и информационное обеспечение дисциплины
В учебном процессе для освоения дисциплины используются следующие технические средства:
· химическая лаборатория, химические реактивы;
· компьютерное и мультимедийное оборудование (на лекциях, для самоконтроля знаний студентов, для обеспечения студентов методическими рекомендациями в электронной форме);
· приборы и оборудование учебного назначения (при выполнении лабораторных работ);
· пакет прикладных обучающих программ (для самоподготовки и самотестирования);
· электронная библиотека курса (в системе КОСМОС - электронные лекции, тесты для самопроверки, тесты для сдачи зачёта).
КОНСПЕКТ ЛЕКЦИЙ ПО ДИСЦИПЛИНЕ «ХИМИЯ»
ВВЕДЕНИЕ
Основной целью изучения курса Химии в инженерном вузе является умение увидеть в конкретной производственной ситуации химическую проблему и квалифицированно разрешить ее. Выполнение такой задачи требует многостороннего, т. е. системного изучения вещества – его природы и свойств, взаимодействия с другими веществами, практического использования. Именно поэтому общая структура курса Химии представлена следующими тремя взаимосвязанными блоками:
1. Строение веществ.
2. Поведение веществ.
3. Инженерная химия (использование веществ).
Учитывая дефицит времени как аудиторных лекционных часов (4 часа), так и недостаток времени у студентов, обучающихся без отрыва от производства, Вам предлагается способ интенсивного изучения предмета с использованием пособия модульного типа «Химия в моделях, схемах, таблицах», где курс в целом и его отдельные блоки представлены в виде графических моделей и конспект-схем.
Если на конспект-схемах представлен конкретный материал темы, то структурированные модели дают его обобщение, т. е. связи между основными теоретическими понятиями курса, разделов.
Рассмотрим последовательно модели и конспект-схемы.
Графических моделей всего 10, из них: одна представляет курс Химии в целом; три – модели блоков; шесть – модели подблоков (две модели на каждый блок).
Каждая модель начинается с четкой постановки цели изучения конкретного блока или подблока. А сама структура модели показывает путь достижения этой цели. Общий вид модели показан на рис. 1.1. Как видите, модель блока состоит из двух ромбов – верхнего (предмет изучения) и нижнего (результат), которые соединены между собой внутренним, а иногда и внешним циклами.
Следует отметить, что все модели между собой взаимосвязаны. Например, первые два блока характеризуют теоретическое содержание курса, третий - его практическое приложение; одновременно третий блок, например, отражает в своих подблоках два различных аспекта прикладной химии - использование вещества (конструкционные и др. материалы) и энергии (электрохимические процессы).
Общий вид графической модели
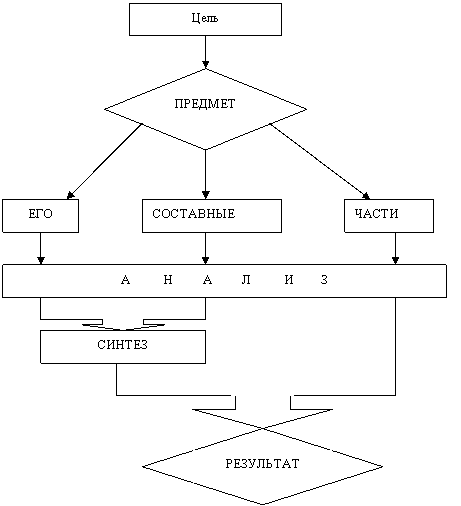
Рис. 1.1
Чтобы увидеть эту диалектичность в моделях, необходимо научиться использовать определенные мыслительные приемы, такие как:
- анализ (деление на элементы),
- сравнение (сходство и различие),
- классификация (выделение основных признаков),
- следствие (логический вывод) и др.
Так как графические модели содержат не конкретный материал, а его обобщение, ориентировку в нём, то одной модели может соответствовать несколько конспект-схем (например, модель VI содержит материал 3-х схем). Конкретный материал всего курса Общей химии представлен концентрированно на 12 конспект-схемах (им соответствуют 6 моделей подблоков), что позволяет успешно и достаточно быстро его усвоить. Каждая схема начинается с постановки вопроса, отражающего суть проблемы данной темы. Изучив этот материал с помощью конспект-схемы (и соответствующей модели), студенты должны уметь четко ответить на поставленный вопрос и тем самым разрешить выдвинутую учебную или инженерную проблему.
Предметом изучения курса химии является вещество в реакции, прогнозирование его свойств. Для достижения этой цели необходимо знание количественных характеристик этих свойств и практического применения веществ, обладающих данными свойствами. При этом следует иметь в виду, что количественные показатели в целом должны отражать три аспекта изучения вещества: структурный, термодинамический, кинетический. Табл. 1 в III части пособия наглядно демонстрирует это, указывая для каждого из аспектов:
- основные количественные показатели и законы;
- свойства вещества в реакции;
- применение вещества и энергии.
Итак, предлагаемый структурный способ компактного изображения учебного материала делает его наглядным и доступным для изучения каждым студентом. Однако использование данного пособия не исключает индивидуальной работы с литературой, а лишь направляет её, облегчая поиски наиболее важной информации в учебниках.
СТРУКТУРА КУРСА ОБЩЕЙ ХИМИИ
Структура курса Общей химии представлена в виде системы трех основных блоков (рис. 1.2):
I. Строение веществ
II. Поведение веществ
III. Инженерная химия
В структурном представлении учебного материала очень важным является понятие системы как множества взаимосвязанных между собой элементов. С этой точки зрения мы и предлагаем подходить к изучению курса Химии.
Первый блок рассматривает вещество (свойства атома, свойства веществ) как систему в статичном, дореакционном состоянии на основе его внутренней структуры (строение атома, периодичность, химическая связь).
Но поведение вещества в каждой конкретной ситуации зависит не только от его собственных свойств, но и от реагирующих с ним веществ той же химической системы. Иными словами, вещество познается во взаимодействии, т. е. его внутренняя структура (I блок) проявляется в химических реакциях (II блок). В этом смысл II блока, который рассматривает основные закономерности протекания химических реакций (термодинамические и кинетические) и влияние реакционной среды (растворы), т. е. поведение веществ в процессе.
Наиболее важные инженерные проблемы курса Химии составляют содержание III блока. Материал этого блока (конструкционные и др. материалы, электрохимические процессы) следует изучать на основе первых двух, т е. опираясь на внутреннее строение вещества и используя общие закономерности протекания химических процессов.
Такое системное изучение курса является наиболее целесообразным, показывая как предмет в целом, так и место каждого, раздела в нем.
На модели I курс «Общая химия» представлен через структурные элементы учебой деятельности: цель - предмет - средства реализации (анализ, синтез) - результат (рис. 1.3).
СТРУКТУРА КУРСА ОБЩЕЙ ХИМИИ
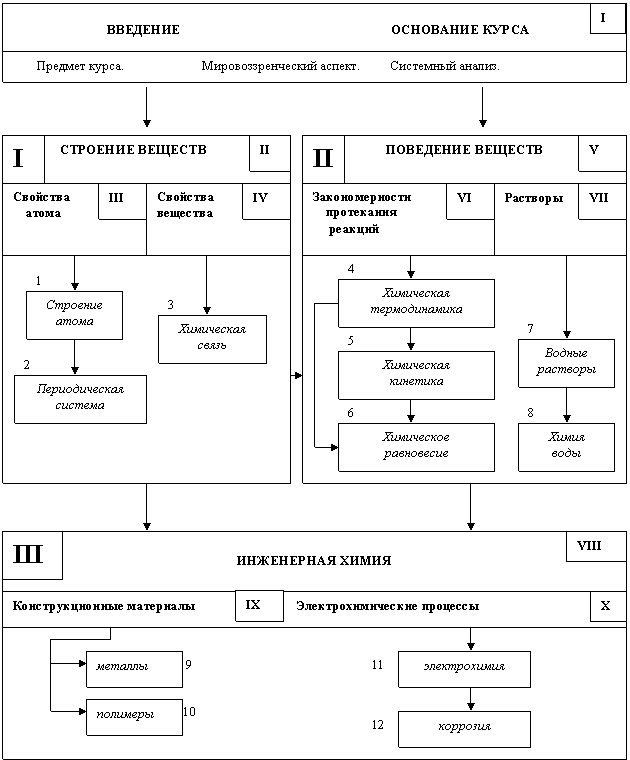
ВВЕДЕНИЕ В КУРС ОБЩЕЙ ХИМИИ (модель I)
Рис. 1.2
Рис. 1.2
Основной предмет изучения курса Химии - вещество в реакции - рассматривается с точки зрения его строения, поведения и применения.
Строение веществ определяется их положением в периодической системе и энергией химических связей Есв.
Поведение же веществ в реакции - это, прежде всего возможность протекания данной реакции, т. е. направление процесса (![]() G) и его скорость (V), характеризуемая энергией активации (Еа).
G) и его скорость (V), характеризуемая энергией активации (Еа).
В сочетании со строением поведение веществ дает основные закономерности химических реакций – структурные, термодинамические, кинетические.
Применяя выделенные закономерности к изучению свойств различных материалов, энергетике (химические источники тока) и коррозии металлов, получаем общий курс химии в целом.
Модель I
ОБЩАЯ ХИМИЯ
Цель: Прогнозирование поведения вещества в реакции с целью практического использования
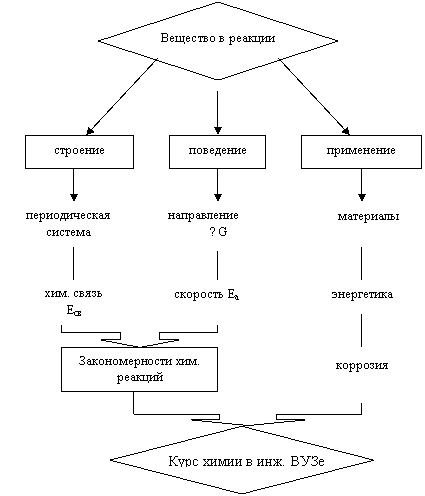
Рис. 1.3

СТРОЕНИЕ ВЕЩЕСТВ
ВВЕДЕНИЕ В БЛОК «СТРОЕНИЕ ВЕЩЕСТВ»
(модель II)
Предметом изучения блока «Строение веществ» является вещество, точнее свойства вещества как отражение его строения на разных уровнях: электронном (Э), атомном (А), молекулярном (М) и кристаллическом (К) (рис. 1.4).
СТРОЕНИЕ ВЕЩЕСТВ
I блок Модель II
Цель: Прогнозирование свойств веществ на основе структуры
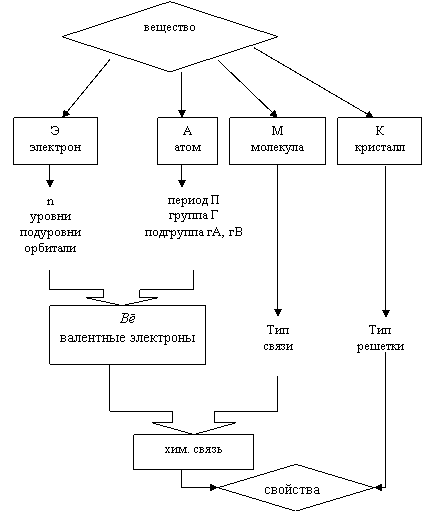 |
Рис. 1.4
Хотя свойства вещества в целом определяются тремя уровнями: А, М и К, тем не менее основное внимание уделим электронному строению атома как ответственному за химизм (в процессе химического превращении ядро неизменно).
Главным носителем химических свойств веществ являются наиболее подвижные валентные электроны (Вē), структура которых определяется положением элемента в периодической системе (периоде, группе, подгруппе), отражающей сложную электронную структуру атома - уровни, подуровни, орбитали.
На основе знания структуры Вē, типа связи и типа решетки можно прогнозировать физико-химические свойства веществ (реакционная способность, металличностъ, неметалличность, растворимость, электрические, механические и др. свойства).

I блок включает два подблока – «Свойства атома» (модель III) и «Свойства вещества» (модель IV).
СВОЙСТВА АТОМА (модель III)
Свойства атома, как известно, определяются местонахождением его в периодической системе, которая и является предметом изучения данного подблока (рис. 1.5). Место же каждого атома в периоде, группе, подгруппе, в свою очередь, определяется его внутренним строением (ядро, электроны, их взаимосвязь - радиус). Так как электрон - «волна» (не только частица), атом обладает сложной структурой, состоящей из уровней, подуровней, орбиталей. Поэтому понятие орбитали (s, p, d, f) является основным (исходным) для понимания энергетической структуры и свойств атома.
Внутренний цикл модели раскрывает структуру валентных электронов Вē, ответственных за химические свойства.
Номер периода показывает количество электронных уровней и подуровней, а также номер внешнего уровня (n). Номер группы дает общее (суммарное) число валентных электронов (∑Вē). В группе А - валентными электронами заполняется только внешний n уровень (s-и p-электроны),а в группе В - внешний nS и предвнешний (n-1)d, иногда (n-2)f. В связи с этим группу А составляют s и р электронные семейства, а группу В - соответственно d и f. Так определяется структура Вē.
Пользуясь правилом Хунда, можно определить валентность (по числу неспаренных электронов). Эти знания дают возможность прогнозирования химических свойств атомов - металличности (Ме) и неметалличности (нМе).
Однако для количественной оценки этих свойств (внешний цикл) необходимо использовать такие характеристики атомов как энергия ионизации (J) и электроотрицательность (ЭО) зависящие от порядкового номера (Z) и радиуса атома (r). При этом не забывайте периодический закон, согласно которому химические свойства являются функцией структуры внешних электронов (n слоя) и, в конечном счете, заряда ядра атома Z.
СВОЙСТВА АТОМА
I подблок Модель III
Цель: Прогнозирование свойств атома по положению в Периодической системе
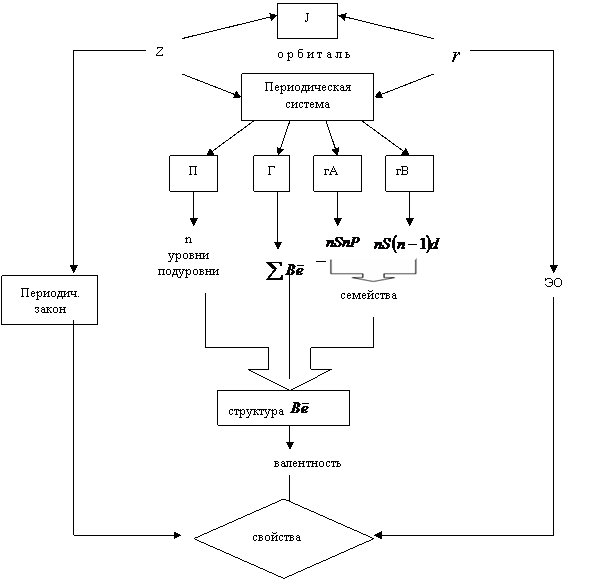 |
Рис. 1.5
 Вывод Свойства веществ на атомном уровне прогнозируются на основе структуры Вē с учетом периодического закона, а количественно измеряются величинами J (Ме) и ЭО (нМе), а также Z и r.
Вывод Свойства веществ на атомном уровне прогнозируются на основе структуры Вē с учетом периодического закона, а количественно измеряются величинами J (Ме) и ЭО (нМе), а также Z и r.
СВОЙСТВА ВЕЩЕСТВА (модель IV)
Так как возможность протекания реакции, зависит от перераспределения связей между атомами в молекуле, химическую связь можно считать ответственной за реакционную способность веществ и все его физико-химические свойства. Поэтому тип связи, определяемый свойствами соединяющихся атомов (∆ЭО), является основным предметом изучения данной темы (рис. 1.6). Различают ковалентную (нМе-нМе), ионную (Ме-нМе) и металлическую (Ме-Ме) химические связи.
В основе наиболее прочной ковалентной связи (К), реализуемой через общие электронные пары, лежит ее жесткая пространственная направленность – геометрическая форма (следствие формы перекрывающихся орбиталей).
Взаимодействие ионов в случае ионной связи (И) происходит за счет электростатического притяжения разноименных зарядов, в результате чего образуется кристалл.
Металлическая же связь (Ме) осуществляется делокализованными электронами (ē), что приводит к появлению особых специфических свойств металла (электропроводимость, теплопроводность, пластичность и др.).
Кроме основных химических сил в конденсированном состоянии вещества возможны дополнительные межмолекулярные связи – силы Ван-дер-Ваальса и водородные связи, изменяющие свойства веществ (tкип, tпл, теплоемкость и др.).
По типу связи можно прогнозировать и агрегатное состояние веществ. Если ионные и металлические связи дают только кристаллические вещества, то ковалентные – и газы, и кристаллы. А межмолекулярные связи дают не только жидкость, но и молекулярные кристаллы. Отметим, что любой кристалл характеризуется определенным значением координационного числа (К. Ч.), от которого зависят многие его свойства, особенно механические. Таким образом, все рассмотренное выше составляет внутренний цикл модели.
Внешний же цикл характеризует количественно свойства связи, которые, в конечном счете, определяют свойства вещества. Самой главной характеристикой связи является ее энергия (Есв), зависящая от длины (rсв) и числа связей.
Важнейшей характеристикой связи (кроме Есв, rсв) является и величина электроотрицательности ЭО. Разность ЭО взаимодействующих атомов определяет тип связи и ее ионность (в ковалентных молекулах – полярность). С ионностью связаны, прежде всего, электрические свойства веществ, их растворимость и, конечно, реакционная способность.
СВОЙСТВА ВЕЩЕСТВА
1,2 подблок Модель IV
Цель: Прогнозирование свойств вещества на основе типа связи
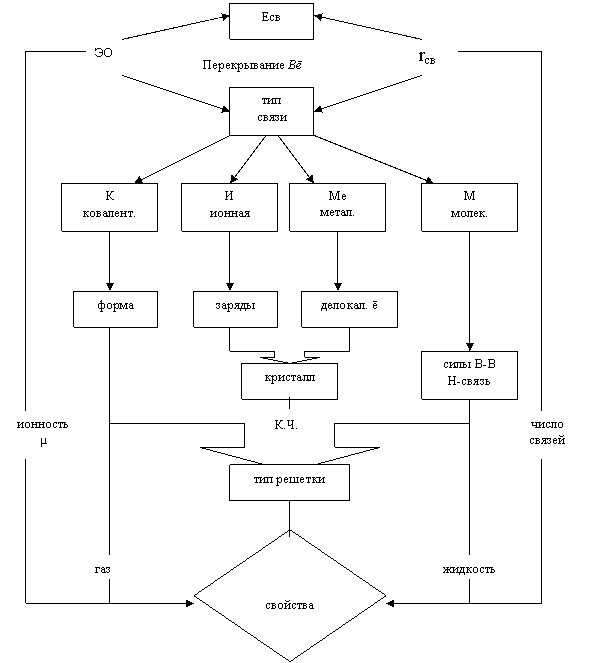 |
Рис. 1.6

Вывод Физико-химические свойства веществ (реакционная способность, растворимость, механические, электрические) прогнозируются на основе типа химической связи (Есв, rсв, ЭО), типа кристаллической решетки (К. Ч.) и агрегатного состояния веществ.
ПОВЕДЕНИЕ ВЕЩЕСТВ
ВВЕДЕНИЕ В БЛОК «ПОВЕДЕНИЕ ВЕЩЕСТВ»
(модель V)
Основным предметом изучения II блока является химическая реакция, к общим свойствам которой относятся: направление процесса, его скорость, выход продукта и определенная среда протекания (рис.2.1).
ПОВЕДЕНИЕ ВЕЩЕСТВ
II блок Модель V
Цель: Реализация химического процесса на основе его общих свойств
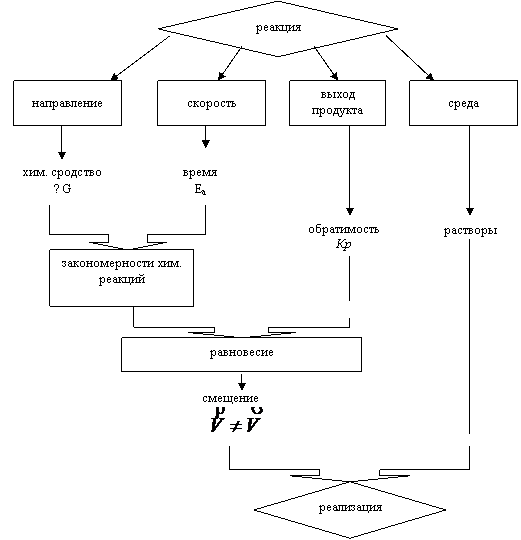 |
Рис. 2.1
Химическое сродство взаимодействующих веществ друг к другу, определяемое величиной энергии Гиббса (∆G), и протекание реакции во времени, связанное с энергией активации (Еа), составляют соответственно термодинамические и кинетические закономерности протекании реакций.
Химически обратимые реакции (Кр), подчиняющиеся общим законам термодинамики и кинетики, характеризуются состоянием химического равновесия. В результате смещения в ту или иную сторону (V1≠V2) под действием внешних условий (С, Т, Р и др.) в определенной среде взаимодействия (растворы) получаем реальный процесс (практическая реализация реакции).
 Вывод Для реализации химического процесса необходимо знание внутренней движущей силы процесса – его химического сродства (∆G), внешних условий его протекания (С, Т, Р, К) и направления смещения равновесия (Кр) с учетом среды реакции (раствора).
Вывод Для реализации химического процесса необходимо знание внутренней движущей силы процесса – его химического сродства (∆G), внешних условий его протекания (С, Т, Р, К) и направления смещения равновесия (Кр) с учетом среды реакции (раствора).
Данный блок состоит из двух подблоков – «Закономерности протекания реакций» (модель VI) и «Растворы» (модель VII).
ЗАКОНОМЕРНОСТИ ПРОТЕКАНИЯ РЕАКЦИЙ (модель VI)
Для управления процессом необходимо, прежде всего, вскрыть термодинамические и кинетические законы протекания реакции. Эти законы и составляют основной предмет изучения данного раздела (рис. 2.2).
Поскольку термодинамические величины характеризуют реакцию при заданных условиях (Р, Т=const), являясь функцией состояния системы, не зависящей от промежуточных стадий, а кинетика, напротив, изучает сам механизм (стадии) реакции в реальных изменяющихся условиях, то термодинамический подход определяет теоретическую возможность процесса (по ΔG0), а кинетический – практическую осуществимость его (на основе Еа).
Сравнивая эти два подхода, следует иметь в виду, что универсальный критерий осуществимости процесса ΔG0 зависит преимущественно от внутренних факторов – энтальпийного (ΔН0) и энтропийного (ΔS0), а реальное протекание его – от внешних условий (С, Т, Р, Кат). Но на скорость химического процесса влияет и природа реагирующих веществ, так как реакция идет только между активными молекулами.
Чтобы целенаправленно управлять процессом, необходимо уметь подбирать оптимальные условия смещения его равновесия с помощью принципа Ле-Шателье и величины константы равновесия Кр. Таким образом, мы проанализировали внутренний цикл – использование общих законов протекания реакций для управления ими. Обратите внимание на изменение скорости химических реакций и смещении химического равновесия основаны методы управления технологическими процессами.
ЗАКОНОМЕРНОСТИ ПРОТЕКАНИЯ РЕАКЦИЙ
II. 1 подблок Модель VI
Цель: Управление процессом на основе общих закономерностей его протекания
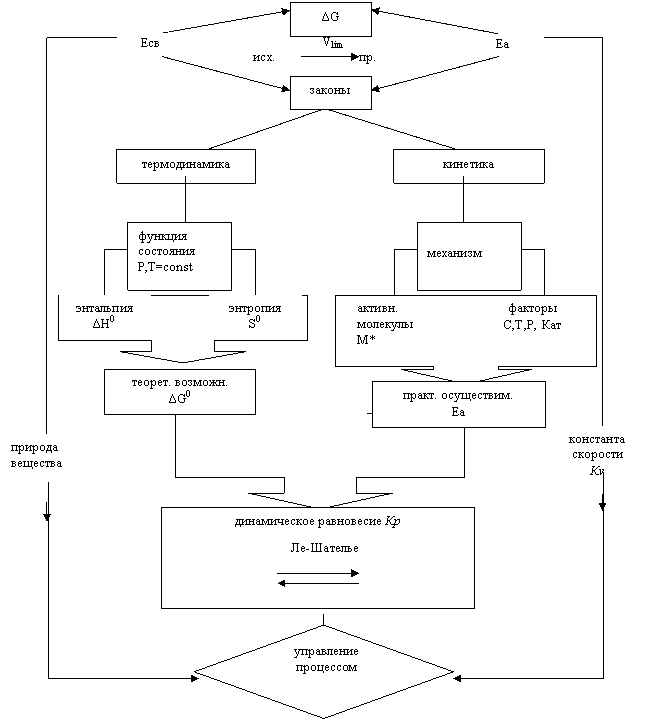 |
Рис. 2.2
Обращаясь к количественной стороне превращения исходных веществ в продукты (исх.®пр.), следует выделить в качестве главной величины энергию Гиббса (ΔG), затем ее химическую часть – энергию активации (Еа), ответственную за скорость (Кv), и наконец, энергию связи (Есв) как исходную характеристику, отражающую природу реагирующих веществ.

Вывод Управление процессом следует осуществлять на основе знаний законов термодинамики (закон Гесса, ΔG0=ΔН0-ТΔS0), кинетики (закон действия масс, закон Аррениуса, правило Вант-Гоффа), принципа Ле-Шателье (Кр) с учетом структурного подхода (Есв).
РАСТВОРЫ (модель VII )
Истинные растворы, которые Вам предстоит изучить, принадлежат к высокодисперсным системам. Кроме них существуют низкодисперсные системы типа суспензий и эмульсий и коллоидные системы (золи), занимающие промежуточное положение между ними по степени дисперсности.
Благодаря своим особым свойствам и характеристикам (адсорбция, поверхностное натяжение, коагуляция и др) дисперсные системы1 представляют большой практический интерес.
Обращение к изучению истинных растворов связано прежде всего с тем, что физико-химические свойства веществ зависят не только от их структуры, термодинамических и кинетических условий, но и характера среды реакции - неэлектролитов и электролитов. Тип раствора и является предмет изучения данной темы (рис. 2.3)
Физико-химическая природа процесса растворения (ключевое понятие) включает в себя как диффузию (физическая часть), так и сольватацию (химическая часть), последняя преобладает в электролитах.
Диффузия лежит в основе фазового перехода, характеризуемого величинами ∆Hф. п. и ∆Sф. п. (в случае электролита добавляется еще ∆Hсольв. и ∆Sсольв.). Именно от их сочетания (∆G=∆H-T∆S) зависит растворимость веществ. Законы же Рауля объясняют такие физические свойства веществ в растворах, как повышение температуры кипения (∆tкип) и понижение температуры замерзания (∆tзам) по сравнению с чистыми веществами.
____________________________
1Дисперсными системами называются такие, в которых одно вещество раздроблено (диспергировано) в другом. Раздробленное вещество называют дисперсной фазой, а среду в которой она распределена – дисперсионной средой (в случае истинных растворов имеем соответственно растворенное вещество и растворитель).
II. 2 подблок Модель VII
РАСТВОРЫ
Цель: Прогнозирование изменений физико-химических свойств веществ в растворах
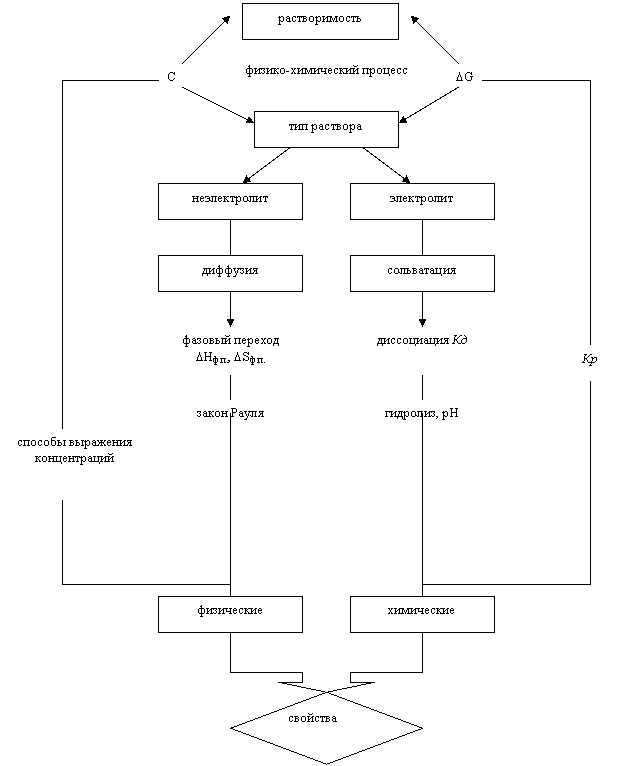 |
Рис. 2.3
В свою очередь сольватация (гидратация) является причиной процесса электролитической диссоциации веществ, характеризуемого величиной константы диссоциации (Кд). Применительно к диссоциации воды Кд превращается в ионное произведение воды (![]() ) и затем в pH (водородный показатель).
) и затем в pH (водородный показатель).
Таким образом, в растворе вода может быть или просто реакционной средой, или реагентом. В первом случае она изменяет в основном физические свойства веществ (агрегатное состояние, растворимость, tкип, tзам). Во втором - физико-химические свойства (реакционная способность, кислотные, основные, окислительно-восстановительные, электрические).
Известные Вам величины ∆G и Кр лежат соответственно в основе теоретического прогноза растворимости веществ и всех равновесных процессов, происходящих в растворах.
Обратите внимание, что за счет управления растворимостью повышается эффективность многих технологических процессов.

Вывод Прогнозирование изменений физико-химических свойств веществ в растворах осуществляется на основе знаний типа раствора (по типу связи) и таких его характеристик, как ∆G, Кр, С.
При изучении данной темы не забывайте и другие дисперсные системы (коллоиды, эмульсии, суспензии, пены), их основные свойства и области применения.
ИНЖЕНЕРНАЯ ХИМИЯ
ВВЕДЕНИЕ
Модельно-структурное наглядное представление учебного материала, лежащее в основе первых двух частей, находит свое продолжение в заключительной части пособия.
Как вы помните, было выделено всего 3 обобщенных блока курса химии:
1. Строение веществ;
2. Поведение веществ;
3. Инженерная химия.
Все блоки объединены общей идеей изучения вещества с точки зрения его природы (внутренней структуры), поведения в процессах, практического использования в профессиональной деятельности инженера.
Два первых общетеоретических блока «Строение веществ» и «Поведение веществ» составляли содержание соответственно первой и второй частей данного пособия. Материал третьего блока «Инженерная химия», который необходимо изучать на основе первых двух, изложен в данной практической части методического пособия. Здесь рассмотрены основные химические проблемы инженерной практики. Особое внимание следует уделить учебно-профессиональным задачам, решение которых дает возможность использовать теоретические знания курса Химии в конкретных инженерных ситуациях.
Кроме традиционного приложения справочных таблиц инженерного характера данное пособие содержит две обобщенные таблицы с описаниями. Одна из них рассматривает фундаментальные понятия курса в развитии, а вторая является как бы синтезом моделей и схем. Последняя тем самым концентрированно представляет курс Химии в целом и одновременно дает способ работы с ним.
ВВЕДЕНИЕ В БЛОК «ИНЖЕНЕРНАЯ ХИМИЯ»
(модель VIII)
Во внутреннем цикле модели VIII рассмотрены элементы основного предмета изучения данного блока - вещество и реакция. В качестве вещества изучаются конструкционные материалы - металлы и полимеры с их основными свойствами - металличностью и эластичностью (рис. 3.1).
В качестве реакции рассматриваются преимущественно окислительно-восстановительные процессы, лежащие в основе химических источников тока (ХИТ), используемых в энергетике, а также коррозии и электролиза, знание теории которых дает возможность химически грамотно защитить металлические конструкции от коррозии.
Практическое применение конструкционных материалов и энергетики базируется на фундаментальных знаниях строения и поведения веществ, что и отражено во внешнем цикле.
 Вывод Практическое использование веществ и процессов возможно только на основе системного изучения двух теоретических блоков – «Строение веществ» и «Поведение веществ».
Вывод Практическое использование веществ и процессов возможно только на основе системного изучения двух теоретических блоков – «Строение веществ» и «Поведение веществ».
Данный блок включает два подблока: «Конструкционные материалы» (модель IX) и «Электрохимические процессы» (модель Х).
III блок Модель VIII
ИНЖЕНЕРНАЯ ХИМИЯ
Цель: Практическое использование веществ и процессов на основе теоретического знания о них
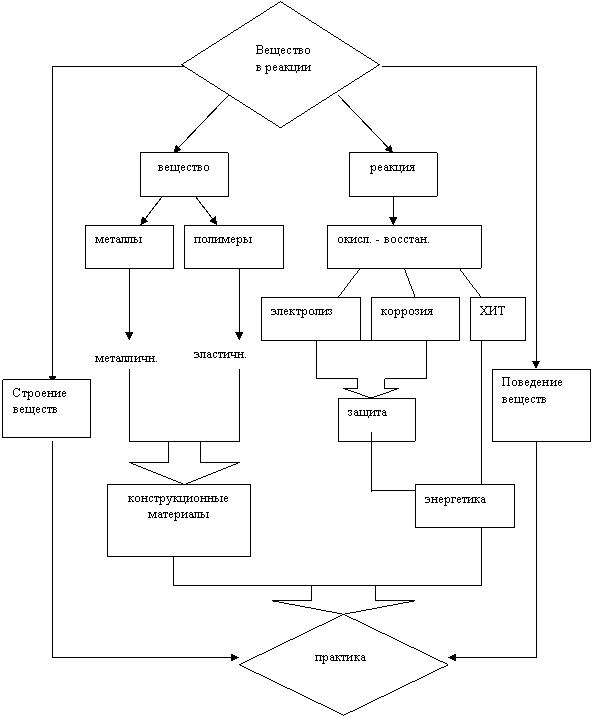 |
Рис. 3.1
КОНСТРУКЦИОННЫЕ МАТЕРИАЛЫ (модель IХ)
Сфера практического применения конструкционного материала определяется прежде всего его характером. Поэтому вид материала и является основным предметом изучения данной темы (рис. 3.2).
КОНСТРУКЦИОННЫЕ МАТЕРИАЛЫ
III. I подблок МодельIX
Цель: Практическое применение металлических и полимерных материалов на основе прогнозирования их свойств
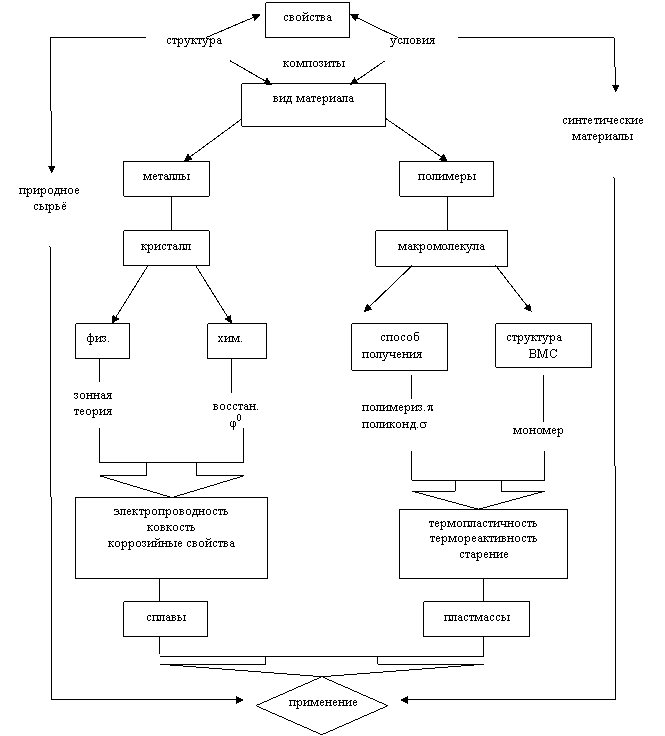 |
Рис. 3.2
Потребность в таких свойствах как высокая электропроводность, ковкость, износостойкость, термическая устойчивость, удовлетворяется металлами, основой которых является кристалл. В случае же необходимости иметь материалы, обладающие эластичностью, термопластичностью, коррозионной стойкостью, диэлектрическими свойствами и т. д., используют полимерные материалы, у которых макромолекулярное строение.
Физические свойства металлов (электропроводимость, пластичность, твердость, тугоплавкость, коррозионные свойства) диагностируются на основе знания металлической связи (ее специфики в конкретном металле) и зонной теории твердого тела. Химические же свойства (восстановительная способность) - величиной стандартного электродного потенциала φ0 (функция ∆G0).
Свойства полимеров зависят от очень многих факторов. Во-первых, от способа получения - полимеризации (разрыв π-связи) и поликонденсации (наличие функциональных групп при σ-связи). Во-вторых, от структуры, определяемой внутренней природой мономеров и связями между ними.
На практике чаще используются композиты (ключевое понятие), а не «чистые» металлы и полимеры. Это связано с тем, что как сплавы (смесь, твердый раствор), так и пластмассы (полимер, наполнитель) резко меняют свойства отдельных компонентов, что дает возможность получения материалов с нужными свойствами.
Во внешнем цикле показано, что свойства как металлических (природное сырье), так и полимерных (синтетических) материалов определяются, прежде всего, их структурой и конечно же условиями получения.
 |
ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ (модель X)
Различают электрохимические процессы двух типов: одни идут самопроизвольно (∆G < 0) за счет превращения химической энергии в электрическую X®Э, другие - только под действием электрического тока Э®Х (∆G > 0). Этим и определяется их практическое использование. Следовательно, тип процесса является основным предметом изучения данной темы (рис. 3.3).
Химизм любого электрохимического процесса отражает следующее ключевое уравнение обратимой реакции
|
направление которой и определяет тот или иной тип процесса. Первый тип процессов включает химические источники тока и коррозию и характеризуется величиной ЭДС (исходя из
DG0 = - nFE0). В основе электрохимической коррозии лежит механизм образования локальных микрогальванических элементов (пар), на подавлении работы которых и основана защита металлов от коррозии.
ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
III.2 подблок Модель X
Цель: Использование электрохимических процессов в зависимости от их типа
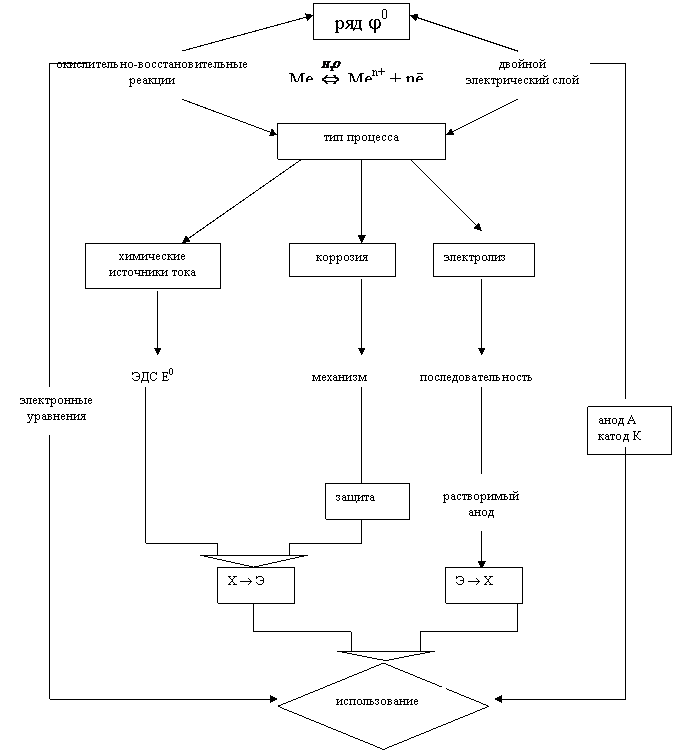
Второй тип процессов представляет электролиз, который используется для получения веществ (металлов, кислот, щелочей и др.), а в инженерной практике с помощью растворимого анода производятся металлические покрытия, очистка металлов, электрохимическая обработка их. Конкретное протекание электролиза определяется последовательностью выделения веществ на электродах (катод, анод), характеризуемой значениями электродных потенциалов.
Именно ряд φ есть самая важная количественная характеристика в электрохимии. Стандартный электродный потенциал (φ°) возникает вследствие образования двойного электрического слоя на границе фаз (Ме - раствор). Двойной электрический слой, в свою очередь, - результат гетерогенной окислительно-восстановительной реакции, в которой процессы окисления и восстановления пространственно разделены. Поэтому анодный А (окисление) и катодный К (восстановление) процессы, составляющие химическую сущность электрохимии, есть не что иное, как электронные уравнения.

Методические указания студентам
Зачеты, установленные утвержденным учебным планом, служат формой проверки усвоения студентом знаний по изучаемым дисциплинам (теоретические зачеты), контроля выполнения лабораторных и расчетно-графических работ, курсовых проектов (работ), а также учебной, производственной и преддипломной практик. Теоретические зачеты оцениваются отметкой "зачет", "незачет". По некоторым дисциплинам, а также курсовым проектам (работам), и всем видам практик предусмотрены зачеты с оценками "отлично", "хорошо", "удовлетворительно", "неудовлетворительно" (так называемые дифференцированные зачеты). Теоретический зачет проводится по окончании чтения семестрового курса лекций до начала экзаменационной сессии путем опроса или в иной форме, устанавливаемой кафедрой; принимается преподавателем, читающим лекционный курс, и при положительных результатах оценивается отметкой "зачет", проставляемой в зачетную книжку студента и зачетную ведомость, а при отрицательных результатах - отметкой "незачет", проставляемой только в зачетную ведомость. Преподавателю предоставляется право поставить зачет без опроса тем студентам, которые в процессе занятий и по результатам промежуточного контроля и текущей аттестации показали успешное овладение учебным материалом. Неявка студента на зачет проставляется преподавателем в зачетной ведомости отметкой "неявка". Студент имеет право до окончания экзаменационной сессии на пересдачу каждого зачета (курсового проекта, работы и т. д.) не более двух раз. Дата, время и аудитория проведения теоретического зачета и проведения двух его пересдач назначаются преподавателем и согласовываются с учебным отделом института (деканатом). Студенты, не выполнившие без уважительных причин до начала экзаменационной сессии всех установленных учебным планом лабораторных, расчетно-графических работ, домашних заданий, курсовых проектов (работ) не допускаются к экзамену по данной дисциплине. К экзаменам по другим дисциплинам они могут быть допущены по разрешению директора (заместителя директора мо учебной работе) института. При наличии уважительных причин (болезнь, семейные обстоятельства и др.) невыполнения в полном объеме учебного плана семестра студенту по его заявлению на имя директора института (декана факультета) может быть предоставлена возможность сдачи зачетно - экзаменационной сессии по индивидуальному графику.
Методические указания преподавателям
Экзамены, установленные утвержденным учебным планом по дисциплине или ее части, преследуют цель оценить полученные студентом теоретические знания, их уровень, развитие творческого мышления, степень приобретения навыков самостоятельной работы, умение синтезировать полученные знания и применять их к решению практических задач. Экзамены сдаются по расписанию в периоды экзаменационных сессий, предусмотренных учебными планами. Расписание экзаменов для всех форм обучения составляется учебным управлением, подписывается директором филиала и доводится до сведения преподавателей и студентов не позднее, чем за 15 дней до начала экзаменов. Директор филиала могжет разрешить хорошо успевающим студентам досрочную сдачу экзаменов при согласии преподавателя (лектора). Пересдача экзамена в период экзаменационной сессии с неудовлетворительной оценки или сдача экзамена при неявке допускается с разрешения директора. Повторная сдача экзамена или дифференцированного зачета (защиты курсовой работы, проекта) с целью повышения положительной оценки разрешается в исключительных случаях директором филиала. Экзамены проводятся на основе утвержденных на филиале билетов в устной или письменной формах. Экзаменатору предоставляется право задавать вопросы сверх вопросов билета, а также помимо теоретических вопросов, давать задачи и примеры по программе данного курса. Экзамены принимаются преподавателями, читающими курс лекций в данном потоке. Когда отдельные разделы лекционного курса, по которым установлен один экзамен, читаются несколькими преподавателями, - экзамен может проводиться с их участием, но с простановкой одной оценки. Во время экзамена студенты могут пользоваться учебными программами, а также с разрешения экзаменатора справочной литературой и другими подсобными материалами. При использовании студентами других, неразрешенных материалов и технических средств, преподаватель вправе прекратить экзаменационное испытание. Успеваемость студентов оценивается следующими отметками: "отлично", "хорошо", "удовлетворительно", "неудовлетворительно". Положительные оценки проставляются в экзаменационную ведомость и зачетную книжку студента, неудовлетворительная оценка проставляется только в экзаменационную ведомость. Экзаменатору предоставляется право оценить успеваемость и поставить, по согласованию со студентами, оценку без опроса тем студентам, которые в процессе обучения показали успешное овладение учебным материалом по результатам текущей аттестации или промежуточного контроля, позволяющим оценить знания студента по сдаваемому предмету. При несогласии студента с выставляемой оценкой экзамена (дифференцированного зачёта) ему предоставляется право его сдачи в установленном порядке. Неявка студента на экзамен проставляется экзаменатором в экзаменационную ведомость отметкой "неявка".
Экзаменационные вопросы
1. Основные цели и задачи курса химии. Место химии в ряду естественно - научных дисциплин и её связь с другими науками. Значение химии в формировании научного мировоззрения. Структурный, термодинамический и кинетический подходы, их сущность и отличие.
2. Квантово-механическая модель атома. Квантовые числа. Атомные орбитали. Принцип Паули. Электронные формулы элементов.
3. Правило и порядок заполнения атомных орбиталей. Строение многоэлектронных атомов.
4. Принцип наименьшей энергии. Правило Гунда. Распределение электронов по энергетическим уровням и подуровням.
5. Ионизационный потенциал, сродство к электрону. Электроотрицательность. Окислительно-восстановительные свойства элементов.
6. Периодическая система элементов . Её структура (период-группа-подгруппа). Какие важнейшие химические свойства веществ можно прогнозировать по периодической системе?
7. Периодическая система элементов - важнейший инструмент понимания природы вещества. Периодический закон.
8. Основные типы и характеристики химической связи.
9. Образование ковалентной связи. Свойства ковалентной связи. Энергия связи.
10. Полярность молекул, дипольный момент.
11. Ионная связь. Способ образования ионной связи. Отличие ионной связи от ковалентной.
12. Силы межмолекулярного взаимодействия. Водородная связь.
13. Аморфные и кристаллические состояния веществ. Кристаллы. Кристаллические решетки.
14. Кристаллическое и аморфное состояние вещества. Типы кристаллических решеток. Зависимость свойств веществ от характера связей между частицами в кристаллах.
15. Укажите тип кристаллической решетки в твердых кристаллах: H2O, SiC, C (алмаз), Ti, Na2CO3. Предскажите их применение.
16. Атомный и молекулярный уровни строения вещества; их количественные характеристики.
17. Дайте сравнительную характеристику (структура-свойства) веществ на разных уровнях их организации: атомном-молекулярном-кристаллическом. Какими количественными характеристиками они измеряются?
18. Химическая реакция как система. Её составные элементы. Структурный, термодинамический и кинетический подходы для описания поведения веществ в реакции и их свойств (основные понятия, количественные характеристики, практическое использование).
19. Первый и второй законы термодинамики. Термодинамический потенциал.
20. Общие закономерности протекания реакций. Химическая термодинамика. Термохимия. Тепловой эффект реакции. Энтальпия. Закон Гесса.
21. Законы Гесса. Термохимические расчеты.
22. Энтальпия образования химических соединений. Теплота химического процесса.
23. Энтропия и её зависимость от температуры, практическая значимость понятия.
24. Энтропия. Расчет энтропии химической реакции.
25. Свободная энергия Гиббса (∆G) - универсальный критерий теоретической возможности процесса. Её расчет в стандартных и нестандартных условиях.
26. Энергия Гиббса, ее связь с направлением химической реакции.
27. Функция состояния системы как общее свойство всех термодинамических величин (∆H, S, ∆G), их расчет.
28. Оценка реакционной способности и устойчивости веществ по значениям их термодинамических функций.
29. Практическое значение термодинамических величин (∆H, S, ∆G) для решения проблем техники безопасности.
30. Химическая кинетика. Закон действующих масс для гомогенной и гетерогенной реакции. Температурный коэффициент. Энергия активации и ее расчет.
31. Скорость химических реакций. Влияние различных факторов на скорость реакции (концентрации, температуры, площади поверхности и др.).
32. Химическое равновесие. Принцип Ле-Шателье. Влияние на химическое равновесие химических реакций давления, концентрации и температуры. Константа равновесия.
33. Принцип Ле-Шателье. Его универсальность. Примеры обратимых процессов (растворимость, электрохимические процессы) и условия их смещения. Константа равновесия. Её физический смысл.
34. Растворы. Типы растворов. Сольватация, гидратация. Растворы неэлектролитов. Температура кипения и замерзания растворов. Закон Рауля.
35. Закон Рауля. Его суть и практическое значение.
36. Свойства растворов. Растворимость. Произведение растворимости. Концентрация растворов. Различные способы выражения концентраций.
37. Сильные и слабые электролиты. Коэффициент активности электролита и неэлектролита. Константа и степень диссоциации слабых электролитов. Сильные электролиты. Активность.
38. Диссоциация воды. Водородный показатель. Ионное произведение воды.
39. Электролитическая диссоциация. Степень диссоциации. Константа диссоциации.
40. Диссоциация воды. Водородный показатель pH и его влияние на ход процессов. Кислотные дожди.
41. Состав природных вод. Жесткость воды (временная и постоянная). Способы снижения жесткости воды.
42. Гидролиз. Константа и степень гидролиза.
43. Вещество в растворе. Вода как среда и как сореагент. Электролиты. Условия необратимости ионообменных реакций.
44. Окислительно-восстановительные реакции. Эквиваленты. Степень окисления элемента в химических соединениях.
45. Инженерная химия. Охарактеризуйте важнейшие темы этого блока. Какие темы наиболее применимы в вашей профессии?
46. Металлы. Физико-химические свойства металлов. Их обоснование.
47. Важнейшие конструкционные материалы (металлы, сплавы, полимеры). Как улучшить свойства сплава и пластмассы (твердость, жаростойкость, коррозионную устойчивость).
48. Электрохимические процессы. Окислительно-восстановительные реакции как источник энергии. ЭДС гальванического элемента и природа металла.
49. Два типа электрохимических процессов – переход химической энергии в электрическую и наоборот. Важнейшая количественная характеристика процесса. Её физический смысл и практическое применение.
50. Электрохимические процессы, их особенности. Рассмотрите их с трёх точек зрения - структурной, термодинамической, кинетической.
51. Электрохимические процессы. Термодинамика электрохимических процессов. Основные условия протекания электрохимических процессов.
52. Теория гальванических элементов. Физический смысл электродного потенциала. Его связь с изобарным потенциалом.
53. Механизм возникновения электрического тока в гальваническом элементе. Электродные потенциалы. Таблица стандартных потенциалов.
54. Устройство гальванического элемента. Расчет электродвижущей силы гальванического элемента. Уравнение Нернста. Типы аккумуляторов.
55. Двойной электрический слой. Условия его образования. Основное электрохимическое уравнение превращения энергии.
56. Электролиз. Законы Фарадея. Перенапряжение. Выход по току.
57. Коррозия металлов. Классификация коррозионных процессов. Поляризация. Способ защиты от коррозии. Коррозия с кислородной, водородной деполяризацией.
58. Электрохимическая коррозия, её структурное, термодинамическое и кинетическое описание. Защита металлов от коррозии. Деполяризация.
59. Использование электрохимических процессов в инженерной практике: ХИТ, защита металлов от коррозии, электролиз с растворимым анодом.
60. Гетерогенные окислительно-восстановительные реакции в растворах. Их механизм и практическое использование (ХИТ, электролиз, защита от коррозии).















