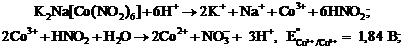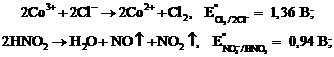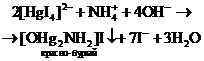ПРИМЕР ОФОРМЛЕНИЯ ЛАБОРАТОРНЫХ РАБОТ ПО КУРСУ «АНАЛИТИЧЕСКАЯ ХИМИЯ»
ГРУППА КАТИОНОВ ЩЕЛОЧНЫХ МЕТАЛЛОВ И АММОНИЯ (NH4+, K+, Na+)
Ион | Реакция; регент | Уравнение реакции, признаки реакции | Чувствительность реагента, условия проведения | Мешающие ионы |
K+ Na+
| Окрашивание бесцветного пламени | K+ – окрашивают пламя в бледно-фиолетовый цвет; Na+ – в монохроматический желтый цвет;
| Чрезвычайно высокая чувствительность, особенно для натрия. Ушко платиновой или нихромовой проволочки, впаянной в стеклянную трубочку предварительно тщательно очищают. Для этого проволочку опускают в раствор соляной кислоты, а затем вносят в пламя грелки. Эту операцию повторяют до тех пор, пока пламя горелки не перестанет окрашиваться. Затем в ушко проволочки помещают небольшой кристаллик анализируемого вещества и вносят в пламя горелки. Фиолетовое окрашивание от калия маскируется желтым цветом натрия. В этом случае прибегают к специальным приспособлениям – синему стеклу или, что лучше, “индиговой призме” (полой внутри стеклянной призме, заполненной раствором индиго). | все катионы ─ все катионы |
K+ | винная кислота H2C4H4O6 или гидротартрат натрия NaHC4H4O6 | K+ + HC4H4O6– ® KHC4H4O6¯ – образование белого кристаллического осадка, плохо растворимого в воде и органических кислотах | m = 0,25 мкг K+. Wlim = 4000. В микропробирке к 4-5 к. раствора соли калия прибавить 4-5 к. раствора гидротартрата натрия. 1). концентрация ионов калия должна быть довольно высока; 2). реакция ведется на холоду, т. к. гидротартрат калия обладает довольно высокой растворимостью в воде, которая увеличивается с повышением температуры ( 3). рН = 4
4). потирание стеклянной палочкой. Если для реакции берется винная кислота или раствор имеет рН, отличающееся от оптимальных значений, в раствор вводится кристаллический ацетат натрия. |
|
K+ | Гексанитрокобальтат(III) натрия Na3[Co(NO2)6] | 2K+ + Na+ +[Co(NO2)6]3– – образование желтого осадка преимущественного состава K2Na[Co(NO2)6], нерастворимого в уксусной кислоте. | Wlim = 13000. На капельной пластине к 1 к. раствора соли калия прибавить 1-2 к. раствора реагента, дать постоять. Реакция должна проводится при значении рН 4 1). при рН < 4 осадок растворяется с образованием слабой азотистой кислоты, которая легко разлагается, а Co(III) восстанавливается до Co(II):
Одновременно могут протекать реакции:
2). при рН > 5 реагент разлагается и выпадает темно-бурый осадок гидроксида Co(III):
Если раствор имеет рН, отличающееся от оптимальных значений, в раствор вводится кристаллический ацетат натрия. Раствор реагента необходимо использовать свежеприготовленным (имеет бурую окраску). Раствор реагента, имеющий розовую окраску, непригоден для определения ионов калия. |
|
| Едкие щелочи NaOH, KOH |
– выделяется газ с резким специфическим запахом. | Сlim = 1:500000. В газовой камере. Простейшие газовые камеры можно сделать из двух чашек Петри, двух часовых стекол или часового стекла и воронки, закрытой кусочком ваты. На верхнее стекло помещают индикаторную бумагу (фенолфталеиновую, универсальную индикаторную), которая через некоторое время изменяет свой цвет, т. к. газообразный аммиак растворяется в воде:
Для ускорения выделения газообразного аммиака газовую камеру слегка можно нагреть (40 0C) на водяной бане. Вместо pH-индикаторной бумаги можно воспользоваться фильтровальной бумагой, пропитанной Hg2(NO3)2, которая чернеет под действием NH3:
| Ионы Na+ при предельном соотношении Неограниченно специфическая. |
| Реактив Несслера K2[HgI4] + KOH |
| Сlim = 1:500000. В газовой камере. На верхнее часовое стекло помещают фильтровальную бумагу, смоченную реактивом Несслера. На нижнее часовое стекло наносят по капле исследуемого раствора и раствора щелочи. Нагревают слегка на водяной бане (40 0С). В присутствии ионов аммония появляется красно-оранжевое пятно. На капельной пластинке. К капле разбавленного раствора соли аммония на капельной пластинке прибавляют 1-2 капли реактива Несслера. Выпадает красно-бурый осадок. В присутствии следов ионов | Металлическая ртуть, ионы Ca2+, Mg2+, SO42–, S2– и амины органических соединений. Присутствие солей металлов, образующих малорастворимые гидроксиды. |
Отделение ионов аммония связыванием в гексаметилентетраамин (уротропин) | 4 | К 2-3 каплям исследуемого раствора прибавляют равный объем 40%-ного раствора формальдегида и каплю фенолфталеина. Затем добавляют по каплям раствор Na2CO3 до появления устойчивой розовой окраски (pH>10). Раствор нагревают 1-2 мин, осадок карбонатов и гидроксидов отделяют. Фильтрат подкисляют 2 н. раствором CH3COOH до исчезновения розовой окраски и проводят обнаружение K+. | ||
Удаление ионов | В фарфоровой чашке к исследуемому раствору добавляют для подкисления концентрированную кислоту, выпаривают досуха и прокаливают на слабом огне до полного удаления ионов |