Санкт-Петербургская Академия
постдипломного педагогического образования
Кафедра естественнонаучного образования
Методическая разработка урока химии на тему
«Кислоты в свете электролитической диссоциации, их классификация и свойства»
Работу выполнил слушатель курсов по программе
«Современные образовательные технологии»
учитель химии
Иваньшина
Санкт-Петербург
2007
План урока
на тему «Кислоты в свете электролитической диссоциации, их классификация и свойства»
Цель урока
обобщить и углубить знания учащихся о свойствах кислот, используя прием «кластеры», развивать умение наблюдать, сравнивать, делать выводы.
Задачи
Учащиеся должны:
- уметь классифицировать кислоты по разным признакам,
- уметь уверенно составлять молекулярные и ионные уравнения,
- уметь проводить химические эксперименты, характеризующие химические свойства кислот,
- изучить новый материал, используя прием «Кластеры».
Оборудование и реактивы
На демонстрационном столе:
- прибор для титрования щелочи,
- индикаторы,
-набор кислот,
- растворы оснований,
- оксид магния,
- оксид меди(II),
- цинк,
- железная и медная проволоки.
На ученических столах:
- растворы соляной и серной кислот,
- набор индикаторов,
- раствор гидроксида натрия,
- цинк,
- медная проволока.
- штативы с пробирками,
- таблица растворимости кислот, оснований и солей в воде.
Тип урока – комбинированный.
Планируемый результат: составление кластеров, облегчающих усвоение нового материала и его закрепление на основе проведения химического эксперимента.
Текст к уроку
В качестве текста к уроку используется материал параграфа 38 (с. 156-159) учебника Габриелян . 8 класс. –М.: Дрофа,2001.
Приемы
Стадия вызова: прием «Кластеры».
Стадия осмысления: прием «Кластеры», лабораторный эксперимент.
Стадия рефлексии: самостоятельная работа.
Ход урока
Стадия вызова
Беседа по материалу параграфа 20, сопровождаемая демонстрационным и лабораторным экспериментом, составление кластеров.
Вопросы классу.
1) Какие вещества относятся к классу кислот?
2) Как определить основность кислоты и как в связи с этим подразделяют кислоты?
3) Как классифицируют кислоты по наличию или отсутствию кислорода в кислотном остатке? Привести примеры кислот.
4) Как можно разделить кислоты по отношению к воде?
5) Каковы физические свойства кислот?
6) Чем объяснить общие химические свойства кислот при различии качественного и количественного состава?
7) Как растворы кислот изменяют окраску индикаторов?
(Выполняется лабораторный опыт «Испытания растворов кислот с помощью индикаторов»).
В ходе беседы учащиеся вначале с помощью учителя, а затем самостоятельно составляют кластеры. Пример составленного кластера приведен на рис.1. На рисунке синим цветом отображены сведения, известные учащимся (по теме «Основания»), а красным – полученные в ходе урока (параграф 38).
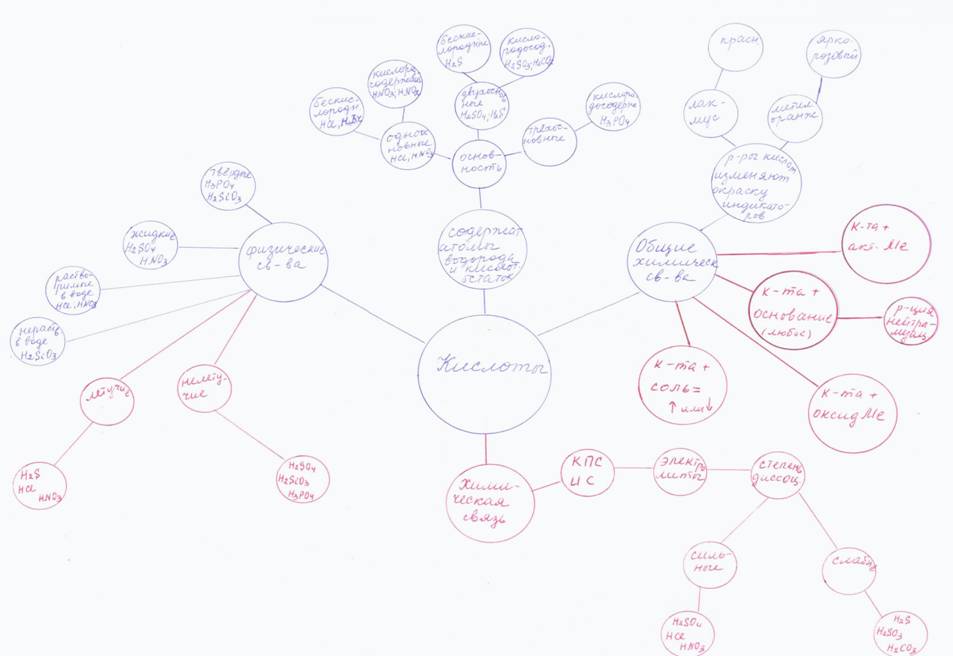
Рис.1. Кластер
Стадия осмысления.
Учащиеся знакомятся с материалом параграфа 38 «Кислоты, их классификация и свойства» и продолжают последовательно составлять кластеры.
Продолжение беседы. Ответы учащихся на вопросы учителя с использованием составленных кластеров.
1) Какие виды химической связи в молекулах кислот?
2) Дать определение кислот с точки зрения электролитической диссоциации.
3) Как различают кислоты по степени диссоциации?
4) Какие кислоты относятся к сисльным электролитам, а какие к слабым?
5) Назовите летучие кислоты.
6) Назовите нелетучие кислоты.
7) Какие кислоты относятся к стабильным, а какие к нестабильным?
8) Какие химические свойства характерны для кислот?
(Выполнение лабораторных опытов «Взаимодействие цинка с раствором соляной кислоты», «Взаимодействие серной кислоты с гидроксидом меди (II)». Демонстрационный опыт «Взаимодействие раствора серной кислоты с раствором гидроксида натрия с использованием прибора для титрования»).
Стадия рефлексии.
Задание классу.
Дать характеристику серной кислоты, используя различные признаки классификации.
Самостоятельная работа.
1 вариант
С какими из перечисленных веществ будет реагировать раствор серной кислоты: CO2 , H2 S, MgO, KOH. Написать полные и сокращенные ионные уравнения ионных реакций.
2 вариант
С какими из перечисленных веществ будет реагировать раствор соляной кислоты:.SO2 , Al, Cu, NaOH. Написать полные и сокращенные ионные уравнения возможных реакций.
Домашнее задание.
Параграф 38, упражнения 3 и 4 (с.159) – письменно.
Литература
1. Габриелян . 8 класс.- М.: Дрофа,2001.
2. Левкин и неорганическая химия: материалы к экзаменам. СПб.: «Паритет»,2003.
3. , Обухов химии.-М.: Просвещение, 1985.
4. Общая методика обучения химии.- М.: Просвещение,1982.
5. , Жуков эксперимент с малыми количествами реактивов.-М.: Просвещение,1989.




