Лабораторная работа 2.1
Определение показателя адиабаты
для воздуха методом Клемана-Дезорма
Библиографический список
1. . Курс физики. – М.: Высшая школа, 1985.
2. . Курс общей физики. – М.: Наука, 1988. Т. 1.
Цель работы – изучение газовых законов.
Приборы и принадлежности: прибор Клемана-Дезорма
Описание метода измерений
и экспериментальной установки
Величину показателя адиабаты ![]() ,
,
где:
Сp — теплоемкость газа при постоянном давлении,
 |
СV – теплоемкость газа при постоянном объеме,
можно определить с помощью прибора Клемана-Дезорма
(см. рисунок), состоящего из баллона 1 с воздухом, насоса 4 и спиртового манометра 5.
В баллон при закрытом кране 2 накачивается воздух. При накачивании воздух, сжимаемый под поршнем насоса, нагревается, следовательно, необходимо выждать 2 – 3 минуты, пока благодаря теплообмену температура в баллоне не станет равной комнатной. После этого измеряют манометром избыточное давление воздуха p1 (в миллиметрах столба жидкости, налитой в манометр). Давление в баллоне станет равным
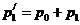
где p0 – атмосферное давление; p1 – избыток давления в баллоне над атмосферным давлением p0, измеряемый манометром.
Открывают на короткое время кран 2, чтобы давление в баллоне сравнялось с атмосферным (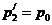 ), после чего закрывают кран.
), после чего закрывают кран.
Пусть масса воздуха после накачивания насосом в сосуде объемом V равна m. При открывании крана часть воздуха выходит. Обозначим массу вышедшего воздуха ![]() , тогда как масса оставшегося воздуха
, тогда как масса оставшегося воздуха ![]() .
.
Масса воздуха ![]() , которая заключается в объеме V, занимала перед открытием крана меньший объем V1. Так как процесс кратковременный и заметного теплообмена между газом и стенками нет, то его можно считать адиабатическим. Согласно уравнению Пуассона (для массы газа, равной
, которая заключается в объеме V, занимала перед открытием крана меньший объем V1. Так как процесс кратковременный и заметного теплообмена между газом и стенками нет, то его можно считать адиабатическим. Согласно уравнению Пуассона (для массы газа, равной ![]() ) получим
) получим
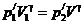 (1)
(1)
Вследствие адиабатического расширения газа температура его понизилась, а затем в результате теплообмена температура газа через небольшой промежуток времени станет равной комнатной. При этом давление газа поднимается до величины
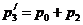 .
.
Начальное и конечное состояние газа наблюдается при одинаковой температуре. Поэтому на основании закона Бойля – Мариотта получим
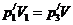 (2)
(2)
Решая уравнения (1) и (2) относительно g, определяем
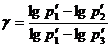 (3)
(3)
Разложим ![]() и
и ![]() в ряд Тейлора, ограничившись в этом случае двумя первыми членами:
в ряд Тейлора, ограничившись в этом случае двумя первыми членами:
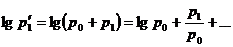
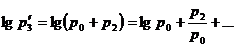
Подставляя эти значения в формулу (3), находим окончательно
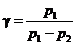 (4)
(4)
Порядок выполнения лабораторной работы
1. Накачивают насосом немного воздуха. При накачивании воздух, сжимаемый под поршнем насоса, нагревается, следовательно, необходимо выждать 2 – 3 минуты, пока благодаря теплообмену температура в баллоне не станет равной комнатной. После этого измеряют манометром и записывают в таблицу избыточное давление воздуха р1 (в миллиметрах столба жидкости, налитой в манометре).
2. Открывают кран 2 и в тот момент, когда уровни жидкости в обоих коленах манометра 5 сравняются, быстро закрывают кран. Выждав 2 – 3 минуты, пока газ, охлаждаемый при адиабатическом расширении, нагревается до комнатной температуры, измеряют и записывают в таблицу избыточное давление р2. Следует помнить, что р1 и р2 отсчитываются как разность высот жидкости в обоих коленах U-образного манометра.
3. По формуле (4) вычисляют значение g.
4. Опыт повторяют не менее 5 раз.
5. Подсчитывают абсолютную и относительную погрешность g.
Таблица
№ п/п | p1, мм | p2, мм | g |
| Dg | (Δg)2 |
1 | ||||||
2 | ||||||
3 | ||||||
4 | ||||||
5 | ||||||
6 |
Контрольные вопросы
1. Почему теплоёмкости газов зависят от способов и условий нагревания?
2. Почему Сp больше, чем СV?
3. Какой процесс называется адиабатическим?
4. Что происходит с внутренней энергией газа при адиабатическом процессе?
5. Как теоретически рассчитать показатель адиабаты для воздуха?



