УЧЕБНЫЙ ПЛАН ПО ДИСЦИПЛИНЕ «ХИМИЯ» для студентов Института гражданской защиты направления подготовки 280100 «Природообустройство и водоотведение» профиль подготовки 280110 «Природоохранное обустройство территории» |
Рекомендуемая литература.
1. Основная литература.
1.1. . Общая химия. М.: Высш. шк., 1985.
1.2. Общая химия. Биофизическая химия. Химия биогенных элементов. М.: Высш. шк., 20с.
1.3. . Аналитическая химия. Аналитика. Ч. 1. Общие теоретические вопросы. Качественный анализ. – М.: Высщ. шк., 2005.
1.4. . Курс качественного химического полумикроанализа. – М.: Химия, 1973.
1.5. . Количественный анализ. – М.: Химия, 1972.
1.6. . Аналитическая химия. Т. 1, 2. – М.: Высш. шк., 2002.
1.7. , , . Аналитическая химия. Лабораторный практикум. – М.: Дрофа, 2004.
2. Дополнительная литература.
2.1. , . Общая химия. С.-Пб.: Химия, 1995.
2.2. , , . Общая химия. МГУ, 1999.
2.3. , . Неорганическая химия. М.: Высш. шк., 1004.
2.4. , . Неорганическая химия. М.: Высш. шк., 19с.
2.5. . Общая и неорганическая химия. М.: Высш. шк., 1998.
2.6. , , . Аналитическая химия. – М.: Просвещение, 1979.
2.7. и др. Аналитическая химия. Т. 1, 2, 3. – М.: Высш. шк., 1983.
2.8. . Аналитическая химия. – М.: Высш. шк., 1993.
2.9. Основы аналитической химии. / Под ред. . Т. 1, 2. – М.: Высш. шк., 2001.
2.10. , . Практикум по аналитической химии. – Воронеж: Воронеж. гос. технол. акад., 2002.
3. Сборники задач и методических материалов.
3.1. . Задачи и упражнения по общей химии. М.: "Интеграл-пресс", не ранее 1985 г.
3.2. и др. Сборник задач и упражнений по качественному анализу. – М.: Просвещение, 1976.
3.3. и др. Сборник задач и вопросов по аналитической химии. – М.: Высш. шк., 1985.
ТЕМЫ ЛЕКЦИЙ И ИХ АННОТАЦИИ
I семестр
Тема 1. Основные понятия и законы химии. Классификация и номенклатура неорганических веществ. (2 часа)
Атомно-молекулярное учение.
Основные законы стехиометрии: закон сохранения массы; общий закон сохранения массы и энергии; закон эквивалентов (понятие эквивалента, фактора эквивалентности, молярной массы эквивалента, количества эквивалента вещества).
Классификация и номенклатура неорганических веществ.
Тема 2. Строение вещества (4 часа)
Строение атома.
Представления о сложном строении атома. Квантовая модель строения атома. Квантовые числа электронов. Распределение электронов в атомах: принцип Паули, правило Хунда, принцип наименьшей энергии.
Периодический закон и периодическая система . Современная формулировка периодического закона. Периодические свойства атомов элементов и их изменение в периодах и группах (атомный радиус, ионный радиус, потенциал ионизации, энергия сродства к электрону).
Химическая связь. Электроотрицательность как свойство атомов в молекуле.
Интерпретация химической связи с точки зрения теории валентной связи. Ковалентная связь (полярная и неполярная), механизмы образования ковалентной связи. Полярность молекул. Свойства ковалентной связи (энергия и длина связи, направленность и насыщаемость связи). Понятие валентности и степени окисления.
Основные виды химической связи и их характеристика. Ионная связь. Металлическая связь. Координационная связь. Водородная связь. Ван-дер-Ваальсовая связь.
Тема 3. Основы химической термодинамики. Кинетика химических процессов.
Катализ (4 часа)
Химическая кинетика. Скорость химических реакций, ее зависимость от различных факторов. Катализ. Химическое равновесие, принцип Ле Шателье.
Энергетика и направление химических реакций. Первое начало термодинамики. Закон Гесса. Второе начало термодинамики. Понятия о самопроизвольном, обратимом и необратимом процессах. Энтропия. Свободная энергия Гиббса.
Тема 4. Основы химии растворов (6 часов)
Растворы. Основные понятия. Классификация растворов. Способы выражения концентрации растворов. Теории растворов. Гидраты и кристаллогидраты. Тепловые эффекты процесса растворения.
Растворимость, влияние на растворимость природы компонентов раствора, растворимость твердых и жидких веществ в жидкостях, растворимость газов в жидкостях. Закон Генри.
Коллигативные свойства разбавленных растворов. Осмос, осматическое давление. Отклонение свойств разбавленных растворов солей, кислот и оснований от законов Рауля и Вант-Гоффа.
Теория электролитической диссоциации. Степень диссоциации (ионизации). Теория растворов слабых электролитов. Константа диссоциации. Закон разведения Освальда. Теория растворов сильных электролитов. Обменные реакции в растворах.
Диссоциация воды. Водородный показатель (рH). Роль электролитов в процессах жизнедеятельности.
Равновесия в гетерогенных системах. Произведение растворимости. Растворимость малорастворимых соединений.
Индикаторы. Определение рН среды. Гидролиз солей.
Тема 5. Окислительно-восстановительные реакции. Электрохимические аспекты процессов окисления–восстановления. Понятие о гальваническом элементе.
Электролиз ( 4 часа)
Электрохимические свойства растворов. Окислительно-восстановительные реакции. Степень окисления. Окислители и восстановители. Составление уравнений окислительно-восстановительных реакций. Подбор стехиометрических коэффициентов в уравнениях ОВР методами электронного баланса и полуреакций.
Стандартный электродный потенциал, его зависимость от различных факторов, уравнение Нернста. Электрохимический ряд напряжения металлов. Определение направления протекания ОВР, электродвижущая сила окислительно-восстановительного процесса.
Гальванические элементы: устройство, принцип действия, ЭДС гальванического элемента.
Тема 6. Химия комплексных соединений (2 часа)
Общие сведения о комплексных соединениях. Вернера. Основные типы и номенклатура комплексных соединений, изомерия комплексных соединений. Диссоциация комплексных соединений в растворе. Константы устойчивости комплексных соединений. Природа химической связи в комплексных соединениях с точек зрения ТВС.
Тема 7. Дисперсные системы (4 часа)
Дисперсные системы, их характеристика и классификация. Способы получения, свойства и применение дисперсных систем. Устойчивость дисперсных систем.
Тема 8. Биологическая роль химических элементов и их соединений (2 часа)
Распространенность (кларки) химических элементов в природе. Макро - и микроэлементы в среде и организме человека. Топография важнейших биогенных элементов в организме человека. Биологическая роль химических элементов в организме человека.
Тема 9 Химические свойства элементов-неметаллов и их соединений (5 часов)
Общая характеристика элементов, способы получения простых веществ: промышленные, лабораторные. Физические свойства. Химические свойства элементов-неметаллов: взаимодействие с простыми веществами (реакции с кислородом, водородом и др. неметаллами, реакции с металлами), со сложными веществами (реакции с водой, кислотами, щелочами и пр.).
Тема 10. Химические свойства s-, p-металлов и их соединений (3 часа)
Общая характеристика элементов, промышленные способы получения простых веществ. Физические свойства металлов. Химические свойства: взаимодействие с простыми веществами (реакции с кислородом, водородом и др. неметаллами), со сложными веществами (реакции с водой, кислотами, щелочами и пр.).
II семестр
Тема 11. Химические свойства d-металлов и их соединений (4 часа)
Общая характеристика элементов, промышленные способы получения простых веществ. Физические свойства металлов. Химические свойства: взаимодействие с простыми веществами (реакции с кислородом, водородом и др. неметаллами), со сложными веществами (реакции с водой, кислотами, щелочами и пр.). Гидратно-гидролитические равновесия в растворах ионов d-металлов. Комплексообразующие свойства ионов d-металлов.
Тема 12. Основные понятия аналитической химии. Общая характеристика аналитических реакций в растворе (5 часа)
Введение в аналитическую химию. Классификация методов аналитической химии. Характеристика аналитических реагентов.
Равновесные химические процессы в аналитической химии: понятия степени и константы диссоциации, реальные и идеальные системы, активность, коэффициент активности, ионная сила раствора.
Расчет pH в водных растворах кислот и оснований. Влияние растворителя на кислотно-основные свойства вещества. Значение рН в химическом анализе
Буферные растворы. рН буферных растворов, буферная емкость. Значение буферных растворов в химическом анализе.
Гетерогенные химические равновесия в аналитической химии. Условия образования осадка. Применение реакций осаждения в химическом анализе
Гидролиз в химическом анализе. Количественные характеристики процесса гидролиза: расчет pH в водных растворах гидролизующихся солей, константа и степень гидролиза. Значение гидролиза в химическом анализе.
Реакции комплексообразования в химическом анализе. Равновесие в растворах комплексных соединений. Использование комплексных соединений для обнаружения, маскирования, разделения, концентрирования. Константы устойчивости (нестойкости) комплексных соединений.
Окислительно-восстановительные реакции в химическом анализе. Влияние различных факторов на величину ОВ потенциала: соотношение концентраций окисленной и восстановленной форм, pH, температура.
Тема 13. Качественный химический анализ. Классификация ионов. Систематический и дробный методы анализа (3 часа)
Качественный анализ. Аналитические классификации ионов: сероводородная, кислотно-основная, аммиачно-фосфатная. Чувствительность аналитических реакций. Способы повышения чувствительности аналитических реакций. Дробный и систематический методы анализа, основные принципы. Составление схем проведения дробного и систематического анализа на примере различных групп ионов.
Тема 14. Количественный химический анализ (6 часов)
Сущность титриметрического (объемного) анализа. Классификация титриметрических методов анализа: по типу реакции, лежащей в основе определения, по способу фиксирования конечной точки титрования, по способу титрования. Растворы в титриметрическом анализе, их стандартизация. Требования, предъявляемые к реакциям в титриметрии. Расчеты в титриметрии.
Кислотно-основное титрование (протолитометрии). Теоретические и практические возможности метода. Рабочие растворы в кислотно-основном титровании. Индикаторы в методе кислотно-основного титрования, интервал перехода окраски индикаторов, выбор индикатора.
Комплексометрия. Теоретические и практические возможности метода. Комплексонометрия (хелатометрия). Комплексоны. Этилендиаминтетрауксусная кислота и ее производные как лиганды. Способы фиксирования конечной точки титрования, индикаторы хелатометрического титрования. Практическое применение хелатометрии.
Окислительно-восстановительное титрование (редоксметрия). Возможности метода. Классификация методов окислительно-восстановительного титрования. Способы фиксирования конечной точки титрования в редоксметрии. Перманганатометрия: рабочие растворы, индикаторы в перманганатометрии. Практическое применение метода. Бихроматометрия: рабочие растворы, индикаторы в бихроматометрии, практическое применение метода. Йодометрия: рабочие растворы (растворы йода и тиосульфата натрия), практическое применение йодометрии.
Седиметрия. Возможности метода. Классификация методов. Рабочие растворы в седиметрии. Способы установления конечной точки титрования в седиметрии.
Гравиметрия. Сущность гравиметрического (весового) анализа. Практическое применение метода.
ПЛАНЫ ЛАБОРАТОРНОГО ПРАКТИКУМА
I семестр
Лабораторные работы проводятся в специализированных лабораториях неорганической и аналитической химии с соблюдением правил техники безопасности, предусмотренных инструкцией (инструктаж по технике безопасности проводится на первом занятии в химической лаборатории с обсуждением основных особенностей работы с потенциально опасными веществами перед соответствующей лабораторной работой).
Тема 1. Основные понятия и законы химии (2 часа)
Решение задач[1] по теме "Основные понятия и законы химии". Вычисления по химическим формулам. Определение химической формулы вещества. Вычисление с применением понятий "количество вещества", "молярная масса", "молярный объем". Законы газового состояния. Закон эквивалентов.
№ 1, 5, 9, 17, 36, 66, 73, 86, 91, 99, 104, 121
Тема 2. Строение вещества (4 часа)
Решение задач по теме "Строение атома. ПСХЭ и Периодический закон": № 000, 183, 185, 188, 193, 209, 211
Решение задач по теме "Химическая связь. Строение вещества": № 000, 232, 235, 238, 260, 263, 279
Тема 3. Основы химической термодинамики. Кинетика химических процессов. Катализ (4 часа)
Лабораторная работа № 1. Химическая кинетика. Влияние различных факторов на скорость химической реакции
Опыт № 1. Зависимость скорости химических реакций от концентрации взаимодействующих веществ.
Опыт № 2. Зависимость скорости химических реакций от температуры.
Опыт № 3. Влияние величины поверхности раздела реагирующих веществ на скорость реакции в гетерогенной системе.
Решение задач по теме "Химическая кинетика": № 000, 328, 330, 331, 333, 336, 341-343
Лабораторная работа № 2. Катализ и катализаторы
Опыт № 1. Изучение гомогенного катализа на примере разложения пероксида водорода.
Опыт № 2. Изучение гетерогенного катализа на примере разложения пероксида водорода.
Лабораторная работа № 3. Химическое равновесие. Смещение химического равновесия.
Опыт № 1. Влияние концентрации веществ на состояние химического равновесия.
Опыт № 2. Влияние температуры на состояние химического равновесия.
Решение задач по теме "Химическое равновесие": № 000, 359, 364, 366
Решение задач по теме "Энергетика и направление химических реакций": № 000, 285, 289, 292, 296, 300, 303, 308
Тема 4. Основы химии растворов (6 часов)
Решение задач по теме "Способы выражения концентрации растворов": № 000, 394, 399, 410, 414, 429, 439, 448, 451
Решение задач по теме "Коллигативные свойства разбавленных растворов": № 000, 465, 470, 477, 481, 485, 489,
Решение задач по теме "Электролитическая диссоциация": № 000, 505, 511, 514, 518-520, 530, 533, 540, 545
Лабораторная работа № 4. Электролитическая диссоциация.
Опыт № 1. Электропроводность растворов некоторых веществ.
Опыт № 2. Влияние концентрации раствора слабого электролита на степень его диссоциации.
Опыт № 3. Смещение равновесия диссоциации слабых электролитов.
а) Влияние соли слабой кислоты на диссоциацию кислоты;
б) Влияние соли слабого основания на диссоциацию основания.
Решение задач по теме "Гетерогенные равновесия": № 000-562, 567-570
Решение задач по теме "Гидролиз": № 000-587
Лабораторная работа № 5 Индикаторы. Определение рН среды. Гидролиз солей.
Опыт № 1. Кислотно-основные индикаторы. Визуально-колориметрический метод определения рН раствора.
а) Окраска некоторых индикаторов в различных средах;
б) Определение рН раствора при помощи универсальной индикаторной бумаги.
Опыт № 2. Определение рН растворов некоторых солей.
Опыт № 3. Случаи полного (необратимого) гидролиза.
Опыт № 4. Факторы, влияющие на степень гидролиза солей.
а) Влияние температуры на степень гидролиза солей;
б) Влияние разбавление раствора на степень гидролиза солей.
в) Влияние изменения концентрации ионов водорода на гидролиз солей.
Тема 5. Окислительно-восстановительные реакции. Электрохимические аспекты процессов окисления–восстановления. Понятие о гальваническом элементе.
Электролиз (4 часа)
Решение задач по теме "Составление уравнений ОВР. Электродный потенциал, гальванические элементы, электролиз": № 000, 626, 633, 639, 641, 651, 654, 658, 673, 685, 687, 688, 698, 702, 706,708
Лабораторная работа № 6. Окислительно-восстановительные реакции
Опыт № 1. Восстановительные свойства металлов:
а) Взаимодействие магния с водой;
б) Взаимодействие железа с водными растворами сульфатов меди и цинка.
Опыт № 2. Влияние кислотности среды на протекание ОВР.
а) Окислительные свойства бихромат-иона в кислой среде;
б) Влияние кислотности среды на характер восстановления перманганат-иона.
Опыт № 3. Окислительно-восстановительные свойства соединений неметаллов.
а). Восстановительные свойства галогенид-ионов.
б). Окислительно-восстановительная двойственность перекиси водорода.
Тема 6. Химия комплексных соединений (2 часа)
Решение задач по теме "Комплексные соединения": № 000-722, 723-726
Лабораторная работа № 7. Реакции комплексообразования.
Опыт № 1. Образование и диссоциация соединений с комплексным катионом: получение и исследование сульфата тетраамминмеди(II).
Опыт № 2. Образование и диссоциация соединений с комплексным анионом: получение и исследование тетрайодовисмутата(III) калия.
Опыт № 3. Различие между простыми и комплексными ионами.
а) Определение катиона Fe(III) роданид-ионами в виде простого иона и в виде гексацианоферрат(III)-иона;
б) Взаимодействие ионов Fe(III) и гексацианоферрат(III)-ионов с сульфатоми железа(II) и меди(II).
Тема 7. Дисперсные системы, их классификация. Получение и свойства дисперсных систем (4 часа)
Решение задач по теме "Дисперсные системы" (методические разработки кафедры)
Тема 8. Биологическая роль химических элементов и их соединений (2 часа)
Решение задач по теме "Биологическая роль химических элементов и их соединений" (методические разработки кафедры)
Тема 9. Химические свойства р-элементов и их соединений (4 часа)
Решение задач по теме "Химические свойства элементов-неметаллов VIA, VIIA групп и их соединений" № 000, 771, 773, 775; № 000, 795, 811, 828, 831(а, в, е, и); № 000, 841, 856.
Лабораторная работа № 8. Химия элементов-неметалов.
Опыт № 1. Получение неметаллов в виде простых и сложных веществ:
а) получение хлора и соляной кислоты;
б) получение диоксида серы и сернистой кислоты;
в) получение аммиака и растворение его в воде.
Опыт № 2. Окислительно-восстановительные свойства соединений неметаллов:
а) хлорная вода и ее свойства;
б) окислительные и восстановительные свойства сульфит-иона;
в) окислительные свойства разбавленной и концентрированной серной кислоты;
г) окислительные свойства азотной кислоты.
Тема 10. Химические свойства s-, p-металов и их соединений (2 часа)
Решение задач по теме "Химические свойства элементов-металлов I-IIIA групп и их соединений": № 000, 970, 978, 1008, 1029, 1052, 1053, 1055.
Лабораторная работа № 9. Химия s- и p-металлов.
Опыт № 1. Взаимодействие металлов с разбавленными и концентрированными растворами кислот и щелочей.
Опыт № 2. Получение гидроксидов металлов и их свойства (растворение в кислотах, щелочах, солях аммония).
II семестр
Тема 11. Химические свойства d-металлов и их соединений (4 часа)
Решение задач по теме "Химические свойства d-металлов": № 000, 1086, 1092, 1094, ; № 000, 986, 996, , 1028(а, б).
Лабораторная работа № 10. Химия d-металлов.
Опыт № 1. Взаимодействие металлов с разбавленными и концентрированными растворами кислот и щелочей.
Опыт № 2. Получение гидроксидов металлов и их свойства (растворение в кислотах, щелочах, солях аммония).
Опыт № 4. Комплексные соединения d-металлов.
Тема 12. Основные понятия аналитической химии. Общая характеристика аналитических реакций в растворе (8 часов)
Решение задач по теме "Чувствительность аналитических реакций"
1. Открываемый минимум ионов натрия дигидроантимонатом калия равен 0,3 мкг, минимальный объем исследуемого раствора – 9,9×10–4 см3. Вычислите предельное разбавление раствора для этой реакции.
2. Открываемый минимум ионов Ag+ хроматом калия равен 0,15 мкг. Предельное разбавление раствора 6500 мл/г. Вычислить минимальный объем исследуемого раствора.
3. Микрокристаллоскопическая реакция открытия ионов Ва2+ с раствором серной кислоты удается с раствором объемом 0,001 см3. Предельное разбавление равно 20000 см3/г. Вычислить открываемый минимум.
Решение задач по теме "Сильные и слабые электролиты":
4. Определить и сопоставить концентрации ионов водорода в растворах 0,1 М HCl и 0,1 М уксусной кислоты.
5. Вычислить рН и рОН 0,001 М раствора соляной кислоты без учета ионной силы.
Решение задач по теме "Буферные растворы"
6. Вычислите рН буферной смеси, содержащей 0,01 моль уксусной кислоты и 0,5 моль ацетата натрия.
7. Вычислите рОН и рН буферной смеси, содержащей 0,1 моль гидроксида и 0,01 моль хлорида аммония.
8. При приготовлении формиатной буферной смеси 100 см3 23 н. раствора муравьиной кислоты смешали с 30 см3 15 н. раствора формиата калия. Вычислите рН полученной смеси.
Решение задач по теме "Гетерогенные равновесия"
9. Рассчитать произведение растворимости, если в 100 мл воды растворимость составляет:
а) 0,058 г Hg2SO4; б) 2,33×10–4 г BaSO4;
в) 3,2×10–3 г Ag2СO3; г) 6,8×10–16 г Ag2S.
10. Вычислить растворимость Hg2Cl2 в воде по значению его произведения растворимости.
11. Вычислить растворимость Ca3(PO4)2 в воде по ПР.
12. Какая из двух сравниваемых солей более растворима в воде: BaSO4 или СaSO4.
Решение задач по теме "Гидролиз. Количественные характеристики гидролиза"
13. Привести по одному примеру солей, растворы которых имеют: а) кислую; б) щелочную, в) нейтральную среду. Ответ подтвердить расчетами.
14. Рассчитайте константу гидролиза, степень гидролиза и рН в 0,1 М растворе ацетата натрия.
15. Рассчитайте константу гидролиза, степень гидролиза и рН в 0,1 М растворе хлорида аммония.
Решение задач по теме "Комплексные соединения"
16. Вычислить концентрацию каждого продукта диссоциации в 0,1 М растворе [Zn(NH3)4]Cl2.
17. Вычислите концентрацию ионов Co2+ в 0,01 М растворе хлорида кобальта(II), содержащем 1 М H3N×H2O.
Решение задач по теме "Окислительно-восстановительные процессы"
18. Определить молярную массу эквивалента окислителя и восстановителя в реакциях:
а). ![]() ; б).
; б). 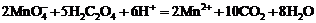 .
.
в). ![]() ; г).
; г). ![]() .
.
д). ![]() ; е).
; е). ![]() .
.
ж). ![]() ; з).
; з). ![]() .
.
19. Рассчитать окислительно-восстановительный потенциал в растворе, содержащем:
а). [MnO4–]= 1 моль/дм3, [Mn2+] = 0,1 моль/дм3, [H+] = 1·10–3 моль/дм3;
б). [MnO4–]= 0,2 моль/дм3, [Mn2+] = 0,1 моль/дм3, рH = 5.
в). [Cr2O72–]= 1 моль/дм3, [Cr3+] = 0,1 моль/дм3, pH = 2;
г). 0,1 моль/дм3 КMnO4, 0,01 моль/дм3 NaOH и MnO2(тв).
Тема 13. Качественный химический анализ. Классификация ионов. Систематический и дробный методы анализа (10 часов)
Лабораторная работа № 11. Техника выполнения аналитических реакций.
Лабораторная работа № 12. Реакции комплексообразования в качественном химическом анализе.
Лабораторная работа № 13. Реакции осаждения в качественном химическом анализе.
Лабораторная работа № 14. Окислительно-восстановительные реакции в качественном химическом анализе.
Лабораторная работа № 15. Анализ сухого вещества.
Тема 14. Количественный химический анализ Общая характеристика аналитических реакций в растворе (12 часов)
Решение задач по теме "Способы выражения концентрации растворов. Вычисления по результатам прямого титрования".
20. В 500 см3 раствора содержится 2,6578 г Na2CO3. Вычислите Т(Na2CO3) и молярную концентрацию эквивалента карбоната натрия при нейтрализации этого раствора до СО2.
21. Вычислить молярную концентрацию раствора гидроксида натрия, Т(NaOH), если на титровании 20,00 см3 его израсходовали 19,20 см3 0,1000 М раствора соляной кислоты, приготовленной из фиксанала.
22. Какую массу щавелевой кислоты Н2С2О4×2Н2О нужно взять для приготовления раствора, на титровании которого расходуется 20,00 см3 0,1 М раствора гидроксида натрия?
Лабораторная работа № 16. Стандартизация раствора гидроксида натрия по соляной кислоте.
Решение задач по теме "Комплексообразование и применение реакций комплексообразования в количественном химическом анализе. Расчеты по результатам комплексонометрического титрования".
23. Какая масса ЭДТА (Na2H2C10H12O8N2×2H2O) потребуется для приготовления 500 см3 0,01 М раствора?
24. Какую массу бромида натрия, содержащего 10% индифферентных примесей, следует взять для анализа, чтобы на титрование ее потребовалось 15,00 см3 0,1 н. раствора нитрата ртути(II) (fэкв. = 1/2)?
25. На титрование 20,00 см3 раствора хлорида никеля(II) израсходовали 21,22 см3 0,02065 М раствора ЭДТА. Определить концентрацию (г/дм3) раствора соли никеля.
Лабораторная работа № 17. Определение общей жесткости воды.
Решение задач по теме "Окислительно-восстановительные реакции в количественном химическом анализе. Расчеты по результатам окислительно-восстановительного титрования".
26. Какую массу КMnO4 надо взять для приготовления 500,0 см3 0,05 н. раствора, используемого для титрования в кислой среде.
27. Рассчитать массу H2C2O4·2H2O, которую надо взять для приготовления раствора объемом 500,0 см3, чтобы на титрование 25,00 см3 полученного раствора израсходовалось 20,25 см3 раствора КMnO4 с концентрацией 3,2800г/дм3.
28. Вычислить массовую долю (%) H2C2O4·2H2O в техническом препарате щавелевой кислоты, если 0,2003 г ее оттитровали 29,30 см3 раствора КMnO4 с концентрацией 0,1076 н.
Лабораторная работа № 18. Определение перманганатной окисляемости природной воды
Лабораторная работа № 19. Определение химического потребления кислорода природных вод.
Решение задач по теме "Реакции осаждения в количественном химическом анализе. Расчеты по результатам осадительного титрования".
29. Какая масса кристаллогидрата 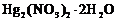 потребуется для приготовления 500 см3 0,05000н. раствора.
потребуется для приготовления 500 см3 0,05000н. раствора.
30. Какое вещество (NaBr или KBr) было взято для анализа, если на титрование 0,2332 г его по методу Мора было израсходовано 18,77 см3 0,1044 М раствора нитрата серебра?
31. Какой объем рассола, содержащего 60 г/дм3 хлорида натрия, следует взять для приготовления 200,0 см3 раствора, чтобы на титрование 25,00 см3 его расходовалось 20,00 см3 0,05000 н. раствора нитрата ртути(I)?
[1] . Задачи и упражнения по общей химии. М.: "Интеграл-пресс", не ранее 1985 г.




