ВАРИАНТЫ КОНТРОЛЬНОЙ РАБОТЫ
ДЛЯ СТУДЕНТОВ I КУРСА ЗАОЧНОГО ОБУЧЕНИЯ
Вариант 1
1. Строение ядра атома. Внутриядерные силы. Взаимопревращения протонов и нейтронов.
2. Общая характеристика коллоидных растворов. Строение мицеллы. Факторы, определяющие устойчивость коллоидных растворов.
3. Описать различия в строении и химических свойствах предельных и непредельных углеводородов.
4. Написать формулы изомеров гептана и назвать их по международной номенклатуре.
5. Найти рН и молярную концентрацию 4% раствора NaOH (a=1).
Вариант 2
1. Общая характеристика периодического закона . Как и почему изменяются свойства элементов в пределах периода?
2. Общая характеристика буферных систем. Механизм буферного действия (на примере бикарбонатного буфера). Буферная ёмкость.
3. Общая характеристика спиртов. Классификация спиртов. Изомерия. Химические свойства спиртов.
4. Написать формулы соединений:
а) 2,3-диметил-3-этилгексан; б) 1.1-дихлорэтан; в) 2-метилбутанол-2.
5. В 100 мл раствора содержится 4,9 г серной кислоты. Найти рН, молярную и процентную концентрацию (a=1).
Вариант 3
1. Строение молекулы. Типы химических связей в молекуле. Привести примеры.
2. Обязательные условия протекания химических реакций. Энергия активации. Зависимость между величиной энергии активации и скоростью реакции. Уравнение Аррениуса.
3. Общая характеристика ароматических соединений. Физико-химические свойства и химические свойства бензола.
4. Написать формулы изомеров гексена и назвать их по международной номенклатуре.
5. В 250 мл раствора содержится 35,5 г сернокислого натрия. Найти молярную и процентную концентрацию.
Вариант 4
1. Характеристика электрона с использованием квантовых чисел. Найти квантовые числа для электронов внешнего слоя атома алюминия.
2. Обратимые химические реакции. Характеристика состояния равновесия. Принцип Ле-Шателье.
3. Общая характеристика органических соединений и их классификация.
4. Дать название по международной номенклатуре соединению:
СН2 = СН - СН - СН2 - СН - CH - CH3
CН 3 NН2 Cl
5. Найти рН и процентную концентрацию 0,05 М раствора серной кислоты (a=1)..
Вариант 5
1. Неполярная и полярная ковалентная связь. Привести примеры.
2. Концентрация ионов водорода и гидроксила в нейтральной, кислой и щелочной среде. Водородный показатель.
3. Строение и химические свойства фенолов.
4. Написать формулы соединений:
а) 2,3,3-триметил-4-этилгептан;
б) пропанол-2; в) гексадиен-1,4.
5. При добавлении к 200 мл буферного раствора 0,4 г NaOH значение рН изменилось с 6,8 до 8,8. Найти буферную ёмкость.
Вариант 6
1. Описать химические связи в молекулах:
N2, NH3, CH3 Cl, Al2 O3
2. Общая характеристика буферных систем. Механизм буферного действия (на примере фосфатного буфера). Буферная ёмкость.
3. Строение, физико-химические и химические свойства непредельных углеводородов.
4. Написать формулы изомеров пентена и назвать их по международной номенклатуре.
5. Раствор соляной кислоты с рН = 0 разбавили водой в 100 раз. Найти рН, молярную и процентную концентрацию полученного раствора.
Вариант 7
1. Строение ядра атома Соотношение между протонами и нейтронами у атомов одного и разных химических элементов. Изотопы.
2. Характеристика процесса растворения.
3. Строение, физико-химические и химические свойства предельных углеводородов.
4. Написать формулы соединений:
а) 1,4-диметилбензол; б) бутин-2; в) 2,2-диметилпентен-3-ол-5.
5. К 200 мл раствора, содержащего 23,8 г бромида калия, прибавили 300 мл раствора, содержащего 51 г нитрата серебра. Осадок отфильтровали. Какие соли и в какой молярной концентрации находятся в фильтрате?
Вариант 8
1. Характеристика периодического закона на основании современных представлений об электронном строении атомов.
2. Общая характеристика катализа. Гомогенный и гетерогенный катализ.
3. Общая характеристика органических соединений. Электронная формула углерода. Функциональные группы органических соединений.
4. Написать формулу соединения: 2,2-диметилгептен-3-ол-7.
5. Найти рН, молярную и процентную концентрацию раствора, содержащего в 200 мл 0,02 моля азотной кислоты.
Вариант 9
1. Естественная радиоактивность. Виды радиоактивного излучения.
2. Способы количественной оценки концентрации растворов.
3. Общая характеристика и классификация карбоновых кислот. Физико-химические и химические свойства карбоновых кислот.
4. Написать формулы соединений: а) 2-хлор-3-метилгексанол-5; б) пентандиаль.
5. При повышении температуры на 20°С скорость реакции увеличилась с 20 ммоль/л ·мин до 80 ммоль/л ·мин. Какова величина температурного коэффициента?
Вариант 10
1. Катодные лучи и их роль в открытии электрона. Характеристика электронов с использованием квантовых чисел. Найти квантовые числа для электронов внешнего слоя атома азота.
2. Первый и второй законы термодинамики.
3. Общая характеристика гетероциклических соединений.
4. Найти концентрацию ионов водорода и гидроксила в растворе с рН = 15.
5. В 500 мл раствора содержится 24,5 г серной кислоты. Найти молярную и процентную концентрацию.
Вариант 11
1. Составить электронные формулы атомов следующих химических элементов: натрия, аргона, скандия, стронция.
2. Зависимость скорости химической реакции от концентрации реагирующих веществ. Закон действующих масс.
3. Общая характеристика и классификация альдегидов. Физико-химические и химические свойства альдегидов.
4. Написать изомеры пентанола и назвать их по международной номенклатуре.
5. На сколько градусов следует увеличить температуру для того, чтобы скорость реакции возросла в 27 раз? Температурный коэффициент данной реакции равен 3.
Вариант 12
1. Описать химические связи в молекулах: CH3Br, CaO, J2, NH4Cl.
2. Обратимые химические реакции. Характеристика состояния равновесия. Константа равновесия. Принцип Ле-Шателье.
3. Общая характеристика полициклических ароматичесих соединений.
4. Дать названия по международной номенклатуре соединениям:

![]() а) СН3 - СН - СН - СН2 - СН3
а) СН3 - СН - СН - СН2 - СН3
СН3 С2Н5
б) ССl4 в) CH2 = CН - CH2 - CH3
5. Найти концентрацию ионов водорода и гидроксила в растворе с рН = 10.
Вариант 13
1. Образование ионной связи. Привести примеры.
2. Общая характеристика окислительно-восстановительных реакций.
3. Общая характеристика и классификация спиртов. Физико-химические и химические свойства спиртов.
4. Дать названия по международной номенклатуре соединениям:
![]()
![]() а) CH2 = CH - CH - CH2 - CH - CH3
а) CH2 = CH - CH - CH2 - CH - CH3
CH3 OH
б) CH3 - CH - CH - CH3
 | |
CH3 Cl
5. Определить скорость химической реакции, в ходе которой в 250 мл раствора за 5 минут содержание одного из реагирующих веществ снизилось с 0,4 моля до 0,3 моля.
Вариант 14
1. Общая характеристика периодической системы элементов . Как и почему изменяются металлические свойства химических элементов в периодах и главных подгруппах?
2. Скорость химической реакции. Константа скорости. Зависимость скорости реакции от температуры. Температурный коэффициент Вант-Гоффа.
3. Общая характеристика альдегидов и кетонов. Физико-химические и химические свойства альдегидов.
4. Написать формулы соединений:
а) 2-метил-3-хлоргексанол-4;
б) 2- хлор –3 - пропил - 4- этилгептан.
5. Найти процентную концентрацию и рН 0,1 М раствора соляной кислоты (a=1).
Вариант 15
1. Строение электронной оболочки атомов. Написать электронные формулы следующих атомов: углерода, неона, кальция и криптона.
2. Общая характеристика водных растворов. Механизм растворения.
3. Описать различия в строении и химических свойствах предельных и непредельных углеводородов.
4. Написать формулы изомеров пентена и назвать их по международной номенклатуре.
5. К 1 л воды прибавили 0,63 г азотной кислоты и 0,8 г едкого натра. Каков рН полученного раствора?
Вариант 16
1. Общая характеристика строения молекулы. Типы химических связей в молекуле. Привести примеры.
2. Основные различия между коллоидными и истинными растворами.
3. Общая характеристика ароматических соединений. Химические свойства бензола.
4. Написать формулы соединений:
а) 2-метил-3-пропилгексен-1-ол-6; б) бутаналь.
5. Сколько потребуется хлорида калия для приготовления 300 мл раствора с концентрацией 0,15 М?
Вариант 17
1. В каком из перечисленных соединений имеется наиболее полярная ковалентная связь? HF, HCl, HBr, HJ. Дать необходимое обоснование.
2. Общая характеристика электрохимических систем. Электрохимический (гальванический элемент).
3. Общая характеристика органических соединений. Изомерия органических соединений. Привести примеры изомеров бутилового спирта..
4. Дать название по международной номенклатуре соединений:
а) СH3 – CH - CH2 – C = CH2 б) CH3 - CH - CH = CH2
CH3 C2H5 CH3
![]()
![]() O
O
в) CH3 - CH2 - C
![]() H
H
5. Найти концентрацию ионов водорода и гидроксила в растворе с рН = 0.
Вариант 18
1. Написать электронные формулы химических элементов с порядковыми номерами: 6,9.14,20, 35.
2. Общая характеристика коллоидных растворов. Строение мицеллы. Факторы, определяющие устойчивость коллоидных растворов.
3. Общая характеристика углеводородов. Физико-химические и химические свойства предельных углеводородов.
4. Написать формулы соединений:
а) 2-метил-3-этилгексин -4-аль-6; б) пропанон.
5. 1,12 г КОН растворили в воде и довели объем раствора до 200 мл. Найти рН, молярную и процентную концентрацию полученного раствора (a=1).
Вариант 19
1. Искусственная радиоактивность. Заурановые элементы.
2. Скорость химической реакции. Константа скорости. Зависимость скорости реакции от концентрации реагирующих веществ. Закон действующих масс.
3. Общая характеристика альдегидов и кетонов. Физико-химические и химические свойства альдегидов.
4. Написать изомеры гексанола и назвать их по Женевской номенклатуре.
5. Скорость химической реакции с температурным коэффициентом, равным 3, при 0°С составляет 1 моль/л-мин. Вычислить скорость этой реакции при 30о С.
Вариант 20
1. Характеристика периодического закона на основании современных представлений об электронном строении атома.
2. Общая характеристика электрохимических систем. Электролиз.
3. Общая характеристика спиртов. Физико-химические и химические свойства спиртов.
4. Дать названия по международной номенклатуре соединениям:
![]()
![]() О
О
а) СН3 - СН2 - СH - СH3 б) CH3 - CH2 - CH2 - CH2 - C

![]() Н
Н
CH3
![]()
![]()
![]()
![]() в) O O
в) O O
![]()
![]() C - CH2 - CH2 - C
C - CH2 - CH2 - C
H H
г) CH3 - C - CH2 - CH3
O
5. Сколько потребуется хлорида калия для изготовления 400 мл 0,15 М раствора? Какова процентная концентрация полученного раствора?
Вариант 21
1. Строение электронной оболочки атомов. Написать электронные формулы атомов: кислорода, неона, кальция, брома.
2. Строение молекулы воды. Водородная связь в воде. Водородный показатель. Индикаторный метод определение рН.
3. Органические полимеры. Способы получения. Биополимеры. Привести примеры.
4. Написать формулы изомеров гептана и назвать их по международной номенклатуре.
5. Химическая реакция с температурным коэффициентом, равным 2, при 20о С протекает за 2 мин. За какое время завершится эта реакция при 50о С?.
Вариант 22
1. Описать химические связи в молекулах:
N2, O2, H2O, H2S, CH3Cl, AlCl3, MgO.
2. Обязательные условия протекания химических реакций. Зависимость скорости реакции от энергии активации. Уравнение Аррениуса.
3. Общая характеристика ароматических соединений. Физико-химические и химические свойства бензола.
4. Написать формулы соединений:
а) 2-хлор-3-метилгептен-4-ол-7; б) 2,3,4-триметилгексадиол-5.6
5. На титрование 5 мл раствора NaOH пошло 10 мл 0,05 М раствора HCl. Найти рН, молярную и процентную концентрацию раствора NaOH.
Вариант 23
1. Агрегатное состояние вещества. Строение твердого вещества. Типы кристаллических решеток.
2. Общая характеристика растворов. Основные различия между истинными и коллоидными растворами.
3. Общая характеристика углеводородов. Физико-химические и химические свойства непредельных углеводородов.
4. Написать формулы соединений:
а) 2-метилбутаналь-4; б) 2,2-диметил-3-этилгексен-5.
5. Как и почему изменится равновесие при уменьшении давления в следующих реакциях:
![]()
![]()
![]()
![]() а) N2O4 2NO2; б) 2NO + O2 2NO2.
а) N2O4 2NO2; б) 2NO + O2 2NO2.
Вариант 24
1. Естественная радиоактивность. Виды радиоактивного излучения.
2. Общая характеристика коллоидных растворов. Основные различия между коллоидными и истинными растворами.
3. Общая характеристика органических соединений. Электронная формула атома углерода. Функциональные группы органических соединений.
4. Описать с помощью химических реакций следующие превращения:
 ОН
ОН

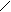 O
O
![]()
![]() C2H4 CH3 - C CH3 - CH - O - CH2 - CH3
C2H4 CH3 - C CH3 - CH - O - CH2 - CH3
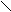 Н
Н
Дать названия реагирующим веществам и продукту превращения.
5. Как необходимо изменить температуру и давление для смещения равновесия в сторону продуктов разложения в реакции:

![]() CаCO3 CaO + CO2 (Q = - 178 кДж/моль).
CаCO3 CaO + CO2 (Q = - 178 кДж/моль).



