Лабораторная работа № 9
ПОСТРОЕНИЕ ДИАГРАММЫ СОСТОЯНИЯ ДВУХКОМПОНЕНТНОГО СПЛАВА
ЦЕЛЬ РАБОТЫ: по температурам ликвидуса и солидуса и концентрации сплава построить диаграмму состояния двухкомпонентного сплава, для специально выбранных сплавов построить кривые охлаждения.
Приборы и принадлежности: линейка, карандаш, ручка, калькулятор, миллиметровая бумага, справочные данные.
Теоретическое введение
Процессы, заключающиеся в превращении одной фазы вещества в другую фазу того же вещества, протекающие без химических реакций, называются фазовыми превращениями. Примеры: плавление, кристаллизация, полиморфные превращения, парообразование и т. д.
Системы, в которых происходят фазовые превращения, делятся на гомогенные и гетерогенные. Гомогенной называется однородная система, каждой точке которой в условиях равновесия соответствуют одинаковые значения давления, температуры и концентрации. Примеры: чистые вещества в твердом и жидком состояниях, расплавы и т. д. Гетерогенными называются сложные системы, состоящие из ряда однородных или гомогенных систем. Примеры: вещества при температурах плавления или кристаллизации и т. д.
Таким образом, фаза вещества – однородная часть гетерогенной системы, которая имеет границу раздела и может быть отделена от общей системы механическим путем. Компонентами называются химические элементы и соединения, из которых может быть образована любая фаза системы. В расплавленном состоянии обычно все компоненты находятся в атомарном состоянии, образуя жидкий неограниченный однородный раствор, в любой точке которого химический состав статистически одинаков. При затвердевании расплава атомы компонентов укладываются в кристаллическую решетку, образуя твердое тело – сплав.
Сплавами называют твердые вещества, полученные путем диффузии элементов в твердом, жидком или газообразном состоянии. Обычно сплавы получают путем расплавления двух или нескольких компонентов и последующей кристаллизации.
Построение диаграмм состояния.
В бинарных системах термодинамическое состояние характеризуется температурой, давлением и концентрацией компонентов. Исходя из этого, следует пользоваться трехмерной системой координат. В обычных условиях изменения давления малы и давление, как фактор, влияющий на систему, можно исключить. Следовательно, можно сказать, что диаграмма стояния представляет собой зависимость температур фазовых превращений от их состава. Диаграмма состояния строится по набору кривых охлаждения (термограмм), которые получают методом баллистического термического анализа. Берутся сплавы разных концентраций и на координатную плоскость наносятся температуры ликвидуса (начала кристаллизации) и солидуса (конца кристаллизации).
По характеру взаимодействия компонентов различают такие сплавы как твердые растворы, механические смеси и химические соединения.
1. Системы с эвтектикой, т. е. с образованием механической смеси
 Одним из основных типов диаграмм состояния двухкомпонентных конденсированных систем является диаграмма состояния с эвтектикой, приведенная на рис.1,а. Такую диаграмму состояния дают компоненты А и В, которые в твёрдом виде не образуют между собой химического соединения или твёрдого раствора. Диаграмма состояния рассматривается для расплава. Всё сказанное о ней справедливо также для раствора.
Одним из основных типов диаграмм состояния двухкомпонентных конденсированных систем является диаграмма состояния с эвтектикой, приведенная на рис.1,а. Такую диаграмму состояния дают компоненты А и В, которые в твёрдом виде не образуют между собой химического соединения или твёрдого раствора. Диаграмма состояния рассматривается для расплава. Всё сказанное о ней справедливо также для раствора.
Рис.1. Диаграмма состояния системы с эвтектикой и нерастворимостью компонентов в твердом состоянии
Температуры плавления чистых компонентов А и В отмечены точками ![]() и
и ![]() . Кривая
. Кривая ![]() Е соответствует составу расплава; каждая точка на ней характеризует равновесие расплава с кристаллами вещества А, т. е. показывает растворимость вещества А в расплаве при данной температуре. Кривая
Е соответствует составу расплава; каждая точка на ней характеризует равновесие расплава с кристаллами вещества А, т. е. показывает растворимость вещества А в расплаве при данной температуре. Кривая ![]() Е указывает состав расплава, который при соответствующей температуре находится в равновесии с кристаллами вещества В; каждая точка на кривой
Е указывает состав расплава, который при соответствующей температуре находится в равновесии с кристаллами вещества В; каждая точка на кривой ![]() Е отражает растворимость вещества В в расплаве. Кривые
Е отражает растворимость вещества В в расплаве. Кривые ![]() Е и
Е и ![]() Е называются линиями ликвидуса.
Е называются линиями ликвидуса.
Точка Е пересечения кривых ![]() Е и
Е и ![]() Е показывает температуру и состав расплава, который одновременно находится в равновесии с кристаллами вещества А и В. Точка Е называется эвтектической точкой. Расплав, соответствующий точке Е, называется эвтектическим расплавом, а температура
Е показывает температуру и состав расплава, который одновременно находится в равновесии с кристаллами вещества А и В. Точка Е называется эвтектической точкой. Расплав, соответствующий точке Е, называется эвтектическим расплавом, а температура ![]() называется эвтектической температурой. Смесь кристаллов веществ А и В, которая одновременно выпадает при температуре
называется эвтектической температурой. Смесь кристаллов веществ А и В, которая одновременно выпадает при температуре ![]() , называется твёрдой эвтектикой. Твёрдая эвтектика состоит из двух твёрдых фаз (кристаллов А и В).
, называется твёрдой эвтектикой. Твёрдая эвтектика состоит из двух твёрдых фаз (кристаллов А и В).
Каждая точка на прямой FG показывает состав системы, состоящей из расплава (точка Е), и двух твёрдых фаз: кристаллов А и В. Линия FG называется эвтектической прямой или линией солидуса. Ниже этой прямой жидкая фаза отсутствует.
Линиями ликвидуса ![]() Е и Е
Е и Е![]() и солидуса FG диаграмма делится на четыре площади (рис.1.а). Площадь выше линии ликвидуса
и солидуса FG диаграмма делится на четыре площади (рис.1.а). Площадь выше линии ликвидуса ![]() Е
Е![]() -одна фаза (расплав). Остальные три площади:
-одна фаза (расплав). Остальные три площади: ![]() FЕ- расплав + кристаллы А;
FЕ- расплав + кристаллы А; ![]() GЕ- расплав + кристаллы В; AFGB- смесь кристаллов А и В.
GЕ- расплав + кристаллы В; AFGB- смесь кристаллов А и В.
Рассмотрим процесс охлаждения расплава, заданного фигуративной точкой М на диаграмме (см. рис.1,а). Фигуративной точкой называется любая точка на диаграмме, характеризующая температуру и состав системы в целом.
В точке М имеем двухвариантную систему Ф=1 и i=3-1=2, т. е. можно менять произвольно температуру и состав расплава (в определённых пределах), не меняя число фаз.
При понижении температуры до точки ![]() (точнее до температуры немного ниже точки
(точнее до температуры немного ниже точки ![]() ) начинается выпадение первых кристаллов вещества А. При этом Ф=2 и i=3-2=1, т. е. имеем одновариантную систему. Это значит, что можно менять произвольно только температуру. А состав расплава при каждой температуре определяется кривой
) начинается выпадение первых кристаллов вещества А. При этом Ф=2 и i=3-2=1, т. е. имеем одновариантную систему. Это значит, что можно менять произвольно только температуру. А состав расплава при каждой температуре определяется кривой ![]() Е.
Е.
При дальнейшем охлаждении системы продолжается понижение температуры и выпадение кристаллов А из расплава. В результате расплав обогащается компонентом В. В фигуративной точке ![]() система продолжает оставаться двухфазной одновариантной. Для определения состава расплава проводим через точку
система продолжает оставаться двухфазной одновариантной. Для определения состава расплава проводим через точку ![]() горизонтальную линию
горизонтальную линию ![]() , которая называется коннодой. По точкам
, которая называется коннодой. По точкам ![]() и
и ![]() определяют температуру и состав равновесных (сопряженных) фаз: точка
определяют температуру и состав равновесных (сопряженных) фаз: точка ![]() - состав твёрдой фазы (кристаллы А), точка
- состав твёрдой фазы (кристаллы А), точка ![]() - состав расплава.
- состав расплава.
Кривая охлаждения на рис.1,б в интервале температур между точками a и d опускается более полого, чем на участке Ma. Это объясняется тем, что при кристаллизации вещества А из расплат выделяется теплота, которая замедляет падение температуры (см. рис.1,а) и система достигает фигуративной точки ![]() . При этом состав расплава в точке Е становится эвтектическим и начинается выпадение твёрдой эвтектики, т. е. смеси кристаллов А и В.
. При этом состав расплава в точке Е становится эвтектическим и начинается выпадение твёрдой эвтектики, т. е. смеси кристаллов А и В.
В точке ![]() (после выпадения первых кристаллов В) находятся в равновесии три фазы: одна жидкая и две твёрдые (Ф=3) и число степеней свободы равно i=3-3=0, т. е. в точке
(после выпадения первых кристаллов В) находятся в равновесии три фазы: одна жидкая и две твёрдые (Ф=3) и число степеней свободы равно i=3-3=0, т. е. в точке ![]() имеется безвариантная трёхфазная двухкомпонентная система. Значение i=0 показывает, что три данные фазы могут находиться в равновесии только при вполне определённых условиях, когда температура равна тактической температуре
имеется безвариантная трёхфазная двухкомпонентная система. Значение i=0 показывает, что три данные фазы могут находиться в равновесии только при вполне определённых условиях, когда температура равна тактической температуре ![]() раствор имеет эвтектический состав (точка Е). Ни температуру, ни состав расплава нельзя менять произвольно, не меняя числа фаз. Согласно закону фазового равновесия Гиббса кристаллизация эвтектики из раствора должна происходить при постоянной температуре. Кроме того, соотношение масс кристаллов А и В в выпадающей эвтектике должно быть таким же, как и весовое содержание веществ А и В в расплаве эвтектического состава. На кривой охлаждения (см. рис. 1, б) выпадение твердой эвтектики представлено прямой dd'. И в связи с тем, что кристаллы А и В при кристаллизации твердой эвтектики выпадают одновременно и у них нет условий для роста, твердая эвтектика имеет мелкокристаллическое строение. Застывший расплав состава е0 (при температуре ниже
раствор имеет эвтектический состав (точка Е). Ни температуру, ни состав расплава нельзя менять произвольно, не меняя числа фаз. Согласно закону фазового равновесия Гиббса кристаллизация эвтектики из раствора должна происходить при постоянной температуре. Кроме того, соотношение масс кристаллов А и В в выпадающей эвтектике должно быть таким же, как и весовое содержание веществ А и В в расплаве эвтектического состава. На кривой охлаждения (см. рис. 1, б) выпадение твердой эвтектики представлено прямой dd'. И в связи с тем, что кристаллы А и В при кристаллизации твердой эвтектики выпадают одновременно и у них нет условий для роста, твердая эвтектика имеет мелкокристаллическое строение. Застывший расплав состава е0 (при температуре ниже ![]() ) состоит из сравнительно крупных кристаллов А, которые выпадали в интервале температур между точками
) состоит из сравнительно крупных кристаллов А, которые выпадали в интервале температур между точками ![]() и
и ![]() , и мелкокристаллической смеси кристаллов А и В в твердой эвтектической смеси.
, и мелкокристаллической смеси кристаллов А и В в твердой эвтектической смеси.
Процесс кристаллизации в фигуративной точке ![]() при температуре
при температуре ![]() заканчивается полным застыванием жидкого расплава. После исчезновения в системе жидкой фазы остаются две твердые фазы (кристаллы А и В; Ф= 2), число степеней свободы становится равным i = 3 - 2 = 1. Это означает, что температура может меняться произвольно, так как состав фаз перестал быть переменным (имеются две твердые фазы из чистых веществ А и В). В точке е0, продолжается охлаждение двух твердых фаз (i=1).
заканчивается полным застыванием жидкого расплава. После исчезновения в системе жидкой фазы остаются две твердые фазы (кристаллы А и В; Ф= 2), число степеней свободы становится равным i = 3 - 2 = 1. Это означает, что температура может меняться произвольно, так как состав фаз перестал быть переменным (имеются две твердые фазы из чистых веществ А и В). В точке е0, продолжается охлаждение двух твердых фаз (i=1).
Линия, показывающая изменение состава жидкой фазы от начала процесса охлаждения расплава до ее исчезновения, называется путем кристаллизации. На рис. 1, а путь кристаллизации при охлаждении расплава М изображается кривой М![]()
![]() Е.
Е.
2. Системы с конгруэнтно и инконгруэнтно плавящимися химическими соединениями. Правило рычага.
Если компоненты А и В могут образовать твердое химическое соединение АВ, плавящееся без разложения, т. е. конгруэнтно на диаграмме состояния, приведенной на рис.2, кривая ликвидуса образует максимум в точке С, когда состав кристаллической фазы совпадает с составом жидкой фазы. По обе стороны от нее находятся эвтектики Е и Е1. Если состав системы находится между, чистым компонентом А и химическим соединением АВ, то при эвтектической температуре ![]() расплав состава
расплав состава ![]() , сосуществует с кристаллами А и АВ. Если состав системы лежит между химическим соединением АВ и компонентом В, то при температуре, соответствующей эвтектической точке Е1 расплав состава
, сосуществует с кристаллами А и АВ. Если состав системы лежит между химическим соединением АВ и компонентом В, то при температуре, соответствующей эвтектической точке Е1 расплав состава ![]() сосуществует с кристаллами АВ и В. Таким образом, рассматриваемая диаграмма состояния представляет собой сочетание двух диаграмм состояния с эвтектикой А - АВ и АВ - В.
сосуществует с кристаллами АВ и В. Таким образом, рассматриваемая диаграмма состояния представляет собой сочетание двух диаграмм состояния с эвтектикой А - АВ и АВ - В.
Рассмотрим процесс охлаждения расплава, заданного фигуративной точкой М и отвечающего составу конгруэнтно плавящегося химического соединения АВ. При этом составе число независимых компонентов равно единице, так как система может быть образована из одного химического соединения АВ. При температуре tс из расплава выпадают кристаллы АВ (Ф=2) и число степеней свободы i=1+2-1=0, т. е. система безвариантна и кристаллизуется при постоянной температуре.
Твердое химическое соединение постоянного состава - это одна фаза, одна кристаллическая решетка, в которой частицы компонентов правильно чередуются, причем соотношение между компонентами в кристаллической решетке повсюду одно и тоже.

Рис.2. Диаграмма состояния системы с химическим соединением, плавящимся конгруэнтно.

Рис. 3. Диаграмма состояния системы медь - магний.
Диаграмма состояния позволяет не только определить число равновесных фаз и их состав, но и соотношение между массами различных фаз при помощи так называемого правила рычага. Фигуративной точке![]() соответствует система, содержащая х0 вес. % компонента В. Эта система состоит из двух фаз: кристаллов АВ и расплава, в которых содержание компонента В составляет соответственно
соответствует система, содержащая х0 вес. % компонента В. Эта система состоит из двух фаз: кристаллов АВ и расплава, в которых содержание компонента В составляет соответственно ![]() и х2 вес. %. Общий материальный баланс можно представить в виде уравнения
и х2 вес. %. Общий материальный баланс можно представить в виде уравнения
, (1)
где ![]() - масса всей системы; Р1 и - массы кристаллов АВ и расплава соответственно.
- масса всей системы; Р1 и - массы кристаллов АВ и расплава соответственно.
Материальный баланс компонента В можно описать уравнением
![]() . (2)
. (2)
Исключая Р0 из уравнений (1) и (2), получаем соотношение
![]() , (3)
, (3)
называемое правилом рычага.
Решая совместно уравнения (3) и (1), можно найти две неизвестные величины Р1 и P2, если заданы Р0, х1 и х2.
3. Системы с твердыми растворами, компоненты которых взаимно неограниченно и ограниченно растворимы
Твердыми растворами называются однородные системы переменного состава, состоящие из двух и более компонентов. Различают твердые растворы двух типов: внедрения и замещения. В твердых растворах внедрения частицы (атомы, молекулы или ионы) одного компонента размещаются между узлами кристаллической решетки другого компонента. Растворы внедрения получаются, например, при растворении в металлах неметаллов - бора, углерода, водорода, азота. В твердых растворах замещения частицы (атомы или ионы одного компонента замещают в узлах кристаллической решетки частицы другого компонента (изоморфизм*).

Рис.4. Диаграмма состояния системы с неограниченной растворимостью компонентов
в твёрдом состоянии: а- без экстремальных точек; б – кривая охлаждения.
В твердых растворах замещения тип решетки и число атомов сохраняются, но изменяются ее объем и плотность. Для образования твердых растворов замещения необходимо выполнение ряда условий. Например, для соединений с ионными кристаллическими решетками требуется аналогия химического строения компонентов, равенство знаков зарядов ионов, возможная близость радиусов ионов, сходство симметрии и размер кристаллических ячеек. Частицы двух изоморфных компонентов замещают друг друга в узлах кристаллической решетки совершенно хаотично.
Твердые растворы могут получаться как из химических соединений (например, K2SO4 и Rb2SO4, КмпО4 и КСlO4), так из простых веществ (например, Си и Аи; Ag и Pi). К твердым растворам относятся бертоллиды, кристаллическая структура которых отличается от кристаллических структур исходных компонентов.
Диаграмма состояния с неограниченной растворимостью компонентов А и В в жидком и твердом состояниях представлена на рис. 4. Ниже линии солидуса ![]() находится область существования твердых растворов; выше линии ликвидуса
находится область существования твердых растворов; выше линии ликвидуса ![]() расположена область жидких растворов; между линиями солидуса и ликвидуса находится область равновесного сосуществования жидких и твердых растворов. Рассмотрим охлаждение расплава, обозначенного фигуративной точкой М. При температуре ta в точке До начинается кристаллизация твердого раствора и образуется двухфазная система, состоящая из расплава состава х0, находящегося в равновесии с твердым раствором состава x3 В интервале температур от ta до tc число степеней свободы равно единице (С=3 - 2=1) и каждой температуре соответствуют определенные составы жидкого и твердого раствора. Например, система состава х0 в фигуративной точке b0 состоит из двух фаз: жидкого раствора состава x1 (точка b1) и твердого раствора состава x2 (точка b2).
расположена область жидких растворов; между линиями солидуса и ликвидуса находится область равновесного сосуществования жидких и твердых растворов. Рассмотрим охлаждение расплава, обозначенного фигуративной точкой М. При температуре ta в точке До начинается кристаллизация твердого раствора и образуется двухфазная система, состоящая из расплава состава х0, находящегося в равновесии с твердым раствором состава x3 В интервале температур от ta до tc число степеней свободы равно единице (С=3 - 2=1) и каждой температуре соответствуют определенные составы жидкого и твердого раствора. Например, система состава х0 в фигуративной точке b0 состоит из двух фаз: жидкого раствора состава x1 (точка b1) и твердого раствора состава x2 (точка b2).

![]()

 Рис. 5. Диаграмма состояния системы с неограниченной
Рис. 5. Диаграмма состояния системы с неограниченной
растворимостью в твердом виде с экстремальными точками
с максимумом (а) и минимумом (б)
Согласно правилу рычага для фигуративной точки b0 (рис. 4)
![]() , (4)
, (4)
P1+P2=P0, (5)
где P0 - масса сплава; P1 и P2 - массы расплава и твердого раствора. Полное затвердение расплава произойдет при температуре tc; при этом состав х0 твердого раствора (точка с0) соответствует составу х0 исходного расплава а0. Так как на диаграмме состояния нет точек, в которых в равновесии находились бы три фазы и число степеней свободы было бы равно нулю, то на кривой охлаждения (рис. 4, б) нет горизонтальных участков. Путь кристаллизации изображается кривой 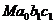 .
.
На рис.5,а и б представлен другой тип диаграммы состояния с неограниченной растворимостью в твердом состоянии. В экстремальной точке составы жидкого и твердого растворов совпадают.
Существуют также диаграммы состояния с ограниченной растворимостью компонентов в твердом состоянии (рис. 6). Кривые tАE, и tВE (линий ликвидуса) изображают состав расплавов, которые находятся в равновесии с твердыми растворами. Кривые tАD и tВC (линии солидуса) указывают состав твердых растворов, которые находятся в равновесии с соответствующими расплавами. Площадь tАDF соответствует твердому раствору a и площадь tВCG - твердому раствору b. Кривые DF и CG указывают составы двух равновесных твердых растворов.
Рассмотрим процесс охлаждения расплава, характеризуемого фигуративной точкой М на рис. 6. В интервале температур ta до tЕ имеем двухфазные одновариантные системы (i=3-2=1). Например, в фигуративной точке b0 в равновесии находится расплав состава х1 (точка b1) и твердый раствор b состава х2 (точка b2). При температуре tЕ в фигуративной точке b0 начинается и продолжается кристаллизация из расплава состава хЕ (точка Е) эвтектической смеси из двух твердых растворов a и b состава хD и хС (точки D и С).
Число степеней свободы в фигуративной точке равно нулю (i=3-3= 0) и поэтому все условия (температура и состав трех фаз) остаются постоянными, пока в равновесии находятся три фазы. После застывания расплава остаются два равновесных твердых раствора (a и b) и температура понижается (i =3-2 = 1). При температуре tе фигуративной точке е0 соответствует равновесие твердого раствора a (точка е1) и твердого раствора b (точка e2). Путь кристаллизации изображается кривой ![]() .
.
Рис.6. Диаграмма состояния системы с ограниченной растворимостью
 в твёрдом состоянии
в твёрдом состоянии

Рис.7. Диаграмма состояния системы олово – свинец.
Порядок выполнения работы
1. Выписать справочные данные для своего варианта (смотри таблицу 1 с заданиями).
2. По данным температурам ликвидуса, солидуса и концентрациям построить диаграмму состояния бинарного сплава.
3. Охарактеризовать диаграмму состояния для своего варианта.
4. Для 5 произвольно выбранных сплавов данной диаграммы состояния (смотри примечание) построить кривые охлаждения.
Примечание 1) для непрерывного ряда твердых растворов нарисовать 3 кривые охлаждения для произвольных сплавов и 2 кривые охлаждения для сплавов с концентрациями 100% компонента А и 100% компонента В;
2) для механических смесей нарисовать 2 кривые охлаждения для сплавов с концентрациями 100% компонента А и 100% компонента В, 1 кривую охлаждения для эвтектического сплава, 1 кривую охлаждения для сплава в доэвтектической области, 1 кривую охлаждения для сплава в заэвтектической области;
3) для диаграмм состояния с образованием устойчивого промежуточного химического соединения нарисовать 2 кривые охлаждения для сплавов с концентрациями 100% компонента А и 100% компонента В, 1 кривую охлаждения для сплава в дистектике, 1 кривую охлаждения для эвтектического сплава, 1 кривую охлаждения для сплава в доэвтектической области.
Таблица 1.
Варианты заданий
№ п/п | Системы | Молярное содержание компонента В, % | Температура ликвидуса, К | Температура солидуса, К |
1 | Al-Si | 100 | 1693 | |
80 | 1593 | |||
60 | 1219 | |||
20 | 950 | |||
10 | 845 | |||
0 | 932 | |||
2 | Si-As | 100 | 1363 | |
80 | 1217 | |||
60 | 1343 | |||
48 | 1356 | |||
43 | 1340 | |||
38 | 1346 | |||
30 | 1450 | |||
15 | 1600 | |||
0 | 1693 | |||
3 | Bi-Sb | 100 | 903,5 | |
80 | 835 | 683 | ||
50 | 755 | 583 | ||
20 | 624 | 553 | ||
0 | 544 | |||
4 | Bi2Te3 – Sb2Te3 | 100 | 891 | |
80 | 883 | 877 | ||
60 | 875 | 868 | ||
40 | 869 | 866 | ||
20 | 867 | 862 | ||
0 | 859 | |||
5 | Si-SiO2 | 80 | 2073 | |
60 | 1723 | |||
50 | 1880 | |||
40 | 1823 | |||
20 | 1523 | |||
0 | 1693 | |||
6 | Cu-Ni | 100 | 1726 | |
80 | 1673 | 1620 | ||
60 | 1623 | 1523 | ||
30 | 1473 | 1420 | ||
0 | 1083 | |||
| KCl-SnCl2 | 100 | 512 | |
90 | 496 | |||
75 | 481 | |||
65 | 473 | |||
60 | 460 | |||
47,5 | 583 | |||
30 | 853 | |||
0 | 1050 | |||
8 | KCl-PbCl2 | 100 | 769 | |
75 | 701 | |||
66,5 | 713 | |||
55 | 693 | |||
35 | 811 | |||
0 | 1048 | |||
9 | Cd-Bi | 100 | 544 | |
80 | 513 | |||
60 | 443 | |||
45 | 417 | |||
20 | 575 | |||
0 | 594 | |||
10 | Be-Si | 100 | 1693 | |
80 | 1603 | |||
60 | 1543 | |||
35 | 1363 | |||
15 | 1473 | |||
0 | 1560 | |||
11 | KCl-CdI2 | 100 | 658 | |
90 | 643 | |||
70 | 696 | |||
51 | 468 | |||
40 | 575 | |||
20 | 833 | |||
0 | 951 | |||
12 | KCl-CaCl2 | 100 | 1043 | |
90 | 978 | |||
81,5 | 911 | |||
65 | 1022 | |||
60 | 1027 | |||
33 | 873 | |||
10 | 1021 | |||
0 | 1050 | |||
13 | CuCl-CsCl | 100 | 912 | |
80 | 814 | |||
55 | 571 | |||
40 | 533 | |||
33,3 | 547 | |||
25 | 521 | |||
10 | 623 | |||
0 | 695 | |||
14 | InCl3-NaCl | 100 | 1073 | |
80 | 1030 | |||
62,4 | 975 | |||
53 | 999 | |||
49,4 | 1003 | |||
47 | 983 | |||
33 | 680 | |||
20 | 622 | |||
15 | 697 | |||
0 | 859 | |||
15 | Ag-Si | 100 | 1693 | |
80 | 1613 | |||
60 | 1563 | |||
40 | 1473 | |||
16 | 1103 | |||
0 | 1223 | |||
16 | Ba-Eu | 100 | 1099 | |
75 | 1093 | 1073 | ||
50 | 1073 | 1023 | ||
25 | 1023 | 983 | ||
0 | 983 | |||
17 | Ge-Si | 100 | 1685 | |
75 | 1643 | 1543 | ||
50 | 1543 | 1423 | ||
25 | 1398 | 1313 | ||
0 | 1213 | |||
18 | InAs-InP | 100 | 1323 | |
75 | 1303 | 1283 | ||
50 | 1273 | 1253 | ||
25 | 1223 | 1243 | ||
0 | 1209 | |||
19 | Au-Pb | 100 | 2050 | |
75 | 1925 | 1688 | ||
60 | 1600 | 1850 | ||
40 | 1500 | 1720 | ||
20 | 1567 | 1405 | ||
0 | 1337 | |||
20 | Sb-Pb | 100 | 600 | |
88 | 519 | |||
75 | 593 | |||
50 | 703 | |||
25 | 823 | |||
0 | 903,5 | |||
21 | Ag-Au | 100 | 1336 | |
75 | 1318 | 1298 | ||
50 | 1298 | 1268 | ||
25 | 1268 | 1253 | ||
0 | 1233 | |||
22 | MgCl2-TlCl | 100 | 708 | |
85 | 682 | |||
72 | 635 | |||
50 | 767 | |||
33,3 | 796 | |||
25 | 658 | |||
10 | 950 | |||
0 | 991 | |||
23 | RbCl-MgCl2 | 100 | 991 | |
76,3 | 764 | |||
31 | 732 | |||
67 | 749 | |||
50 | 823 | |||
35 | 783 | |||
21,3 | 898 | |||
100 | 990 | |||
24 | MnCl2-RbCl | 0 | 990 | |
15 | 870 | |||
35 | 713 | |||
45 | 793 | |||
55 | 797 | |||
32 | 733 | |||
20 | 803 | |||
0 | 923 | |||
25 | NaCl-ZnCl2 | 100 | 595 | |
85 | 573 | |||
73 | 535 | |||
65 | 623 | |||
48 | 769 | |||
32 | 882 | |||
0 | 1073 |
Контрольный тест
Задание | Ответы |
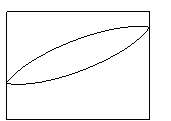
Установите соответствие между диаграммой состояния бинарных сплавов и наименованием сплава, к которому она относится: a)
c)
d)
| a) Для идеальных механических смесей. b) Для механических смесей с двусторонней растворимостью. c) Для непрерывного ряда твердых растворов. d) Для идеальных механических смесей с промежуточным химическим соединением. e) Для механических смесей с односторонней растворимостью. f) Для сплавов с промежуточным химическим соединением с частичной растворимостью компонентов. |
Литература.
1. Мозберг RK. Материаловедение. Таллин.: ВАЛГУС. 19с.
2. Епифанов твердого тела. М.: Высшая школа. 19с.
3. , Хромов твердого тела. М.: Высшая школа. 19с.
4. Гуляев . М: Мет. 19с.
5. Технология металлов и конструкционные материалы. Под ред. М.:Машиностроение. 19с.
6. и др. Материаловедение М: Машиностроение. 19с.



 7
7
 b)
b)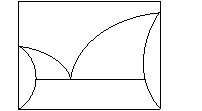

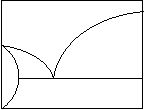 e)
e)