Ответы к заданиям школьного этапа Всероссийской олимпиады школьников по химии
На выполнение работы отводится 90 минут.
Общее количество баллов – 15 баллов
№ 1. Напишите уравнения реакций, необходимых для осуществления превращений:
Be -> Be (NO3)2 -> Be (OH)2 -> Na2BeО2 ->
->ВеО ->Ве (ОН)2 -> ВеС12
Стрелка между формулами не всегда иллюстрирует одностадийное превращение.
Решение:
1. 3Be + 8HNO3 = 3Be(NO3)2 + 2NO + 4H2O или 2Be + O2 = 2BeO; BeO + HNO3 = Be(NO3)2
2. Be (NO3)2 + 2 KOH = Be (OH) 2 + 2KNO3
3. Be (OH) 2 +2 KOH =сплав K2BeO2 + H2O
4. 2Be + O2 = 2BeO;
5. BeO + 2HCl = BeCl2 + H2O;
BeCl2 + 2 KOH= Be (OH) 2 + 2 KCl
6. Be (OH) 2 + 2HCl = BeCl2 + 2H2O
Максимальное количество баллов – 5 баллов
№2. При нагревании 23г неизвестного вещества А выделилось 4,48л аммиака (н. у.) и образовалось некоторое количество вещества Б. При полном обезвоживании вещества Б получилось 14,2г оксида фосфора (V). Установите формулу и дайте название вещества А.
Решение:
![]()
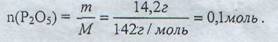
Оксид фосфора (V) может получиться при обезвоживании ортофосфорной кислоты по схеме:
2Н3РО4 -> Р2О5 => n(Н3РО4) = 0,2 моль,
m (Н3РО4 Н3РО4)= 0,2моль×98г/моль = 19,6 г.
mпродуктов = 3,4 + 19,6 = 23 г, следовательно, других продуктов нет.
n (NН3):n(НзРО4)=0,2:0,2=1:1.
Формула вещества NH4H2PO4 - дигидрофосфат аммония.
Максимальное количество баллов – 5 баллов
№3. 7,4г оксида 2-х валентного металла восстановили водородом. Пары продуктов реакции пропустили через трубку с оксидом фосфора (V), масса которой увеличилась на 1.8г. Определите, оксид какого металла взят.
Решение:
Уравнение реакции: MeO+H2+Me+H2O
Из продуктов реакции поглощаться оксидом фосфора будут пары воды: P2O5 + 3 H2O = 2H3PO4
n (H2O) = m/M = 1,8 г/18г/моль=0,1 моль
n (H2O) = n (MeO) = 0,1 моль
M (Me) = m/M =7,4 г/0,1 моль = 74 г/моль
M (Me) = M (MeO) – M(O) = 74 – 16 = 58 г/моль
Me – Ni.
Максимальное количество баллов – 5 баллов
Ответы к заданиям школьного этапа Всероссийской олимпиады школьников по химии
10 класс.
На выполнение работы отводится 90 минут.
Общее количество баллов – 22 балла
№1 . Смесь меди и хрома обработали концентрированной азотной кислотой. При этом выделилось 4,48л газа. При обработке того же количества смеси соляной кислотой в отсутствии кислорода выделилось также 4,48л газа (условия нормальные в обоих условиях). Определите массовые доли металлов в смеси.
Решение:
Напишем уравнения реакций:
Си + 4 HNO3 = Cu(NO3)2 + 2 NO2 + 2H2O (1)
Сг + HNO3 ![]() пассивируется (2)
пассивируется (2)
Сu + НСl ![]() (3)
(3)
Cr + 2HCI = CrCI2 + H2 ![]() (4)
(4)
По реакции (1) выделилось 4,48 л NO2 или 0,2 моль NO2 .
Следовательно, в смеси было 0,1 моль или 6,35 г меди.
По реакции (4) выделилось 4,48 л или 0,2 моль Н2.
Следовательно, в смеси металлов 0,2 моль или 10,4 г хрома.
Масса смеси 6,35 + 10,4= 16,75 г.

Максимальное количество баллов – 3 балла
№2. При полном сгорании углеводорода в кислороде образовалась 1,76г СО2 и 0,72г Н2О.
D (N2) =1. Найдите молекулярную формулу углеводорода.
Решение:
CxHy + O2->CO2 + H2O
1) n(CO2) = m(CO2) : M(CO2)
n= 1,76 : 44 = 0,44 моль (CO2)
2) n(H2O) = 0,72 : 0,04 моль (H2O)
3) Следовательно, С - 0,04 моль
H – 0,08 моль
x : y = n(C) : n(H)
4) x : y = 0,04 : 0,08
x : y = 1 : 2
5) Мч = CH2 = 14
6) Мч (CxHy) = 1×28 = 28
7) 28 : 14 = 2
8) Ответ: C2H4
Максимальное количество баллов – 4 балла
№3. Элементы А, Б, В образуют соединения друг с другом. Простое вещество А горит в простом веществе Б, образуя газ Г с резким запахом. Дополнительное взаимодействие вещества Г с простым веществом Б дает бесцветную жидкость Д, которая ниже 170С переходит в прозрачную кристаллическую модификацию. Раствор вещества Е, состоящего из элементов А и В, в веществе Ж, образованном из элементов Б и В, имеет слабо кислую реакцию среды. Вещества Е и Ж однотипны по составу, но существенно отличаются по свойствам. При взаимодействии Е с простым веществом Б получаются вещества Г и Ж. При соединении вещества Д с Ж образуется сильный окислитель 3, который с веществом А дает вещества Г и Ж Определите элементы А, Б, В и вещества Г, Д,Е, Ж,3 и напишите уравнения описанных реакций.
Решение:
![]()
S + О2 = SO2
2SO2 + О2 = 2SO3
H2S + Н2О  HS- + НзО
HS- + НзО
2H2S + 3О2 = SO2 + Н2О
SO3 + Н2О = H2SO4
2H2SO4 + S = 3SO2 +2H2O
Максимальное количество баллов – 15 баллов.
Задания для школьного этапа Всероссийской олимпиады школьников по химии
На выполнение заданий отводится 90 минут.
Общее количество баллов – 15,5 баллов.
№1. При электролизе раствора нитрата хрома (III) на катоде выделилось 20,8г хрома. Что и в каком количестве выделилось на аноде? Выделившийся хром растворили в соляной кислоте, после чего раствор оставили на воздухе, а затем к нему постепенном прилили раствор щелочи. Выпавший вначале осадок при этом полностью растворился. Напишите уравнения реакций и вычислите сколько миллилитров 40%-ного раствора NaOH (р =1,4г/мл) потребовалось для полного растворения осадка?
Решение:
1. Схема электролиза раствора Сг(NO3)3
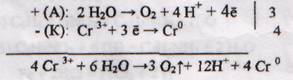
или 4 Сr (NО3)3 + 6 Н2О -> 3 О2![]() + 4 Сr + 12 HNO3
+ 4 Сr + 12 HNO3
2. На катоде выделилось 20,8 г хрома или
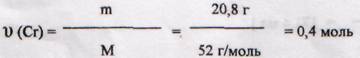
3. На аноде согласно уравнению реакции выделилось:

или 22,4 × 0,3 = 6,72 л О2
4. При растворении хрома в соляной кислоте Сr + 2НСl = СгС12+Н2![]() (1)
(1)
образуется СrСl2, который постепенно окисляется кислородом воздуха
4 СrСl2 + О2 + 4 НСl = 4 CrСl3 + 2Н2О (2)
![]() 5. При действии на СrСl3 раствором NaOH сначала образуется осадок Сr (ОН)3, который растворяется в избытке щелочи:
5. При действии на СrСl3 раствором NaOH сначала образуется осадок Сr (ОН)3, который растворяется в избытке щелочи:
СrСl3 + 3NaOH = Сr(OН)3 + 3NaCl (3)
Сr(ОН)3 + NaOH = Na[Cr (OH)4] (4) или (Cr(OH)3 + 3NaOH = Na3[Cr(0H)6]) (5)
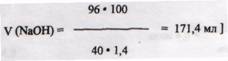
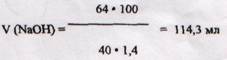 6. В реакцию (1) вступает 0,4 моль хрома и образуется 0,4 моль СrСl2, окисление которого дает 0,4 моль СrСl3. При действии на него щелочи по реакции (4) образуется 0,4 моль Na[Cr(OH)4] и затрачивается 1,6 моль NaOH или 1,6 × 40 = 64 г. Пересчитываем это количество NaOH на 40%-ный раствор:
6. В реакцию (1) вступает 0,4 моль хрома и образуется 0,4 моль СrСl2, окисление которого дает 0,4 моль СrСl3. При действии на него щелочи по реакции (4) образуется 0,4 моль Na[Cr(OH)4] и затрачивается 1,6 моль NaOH или 1,6 × 40 = 64 г. Пересчитываем это количество NaOH на 40%-ный раствор:
или
[ по уравнению (5) 2,4 моль NaOH или 2,4 моль × 40 = 96 г NaOH
Максимальное количество баллов – 6,5 баллов.
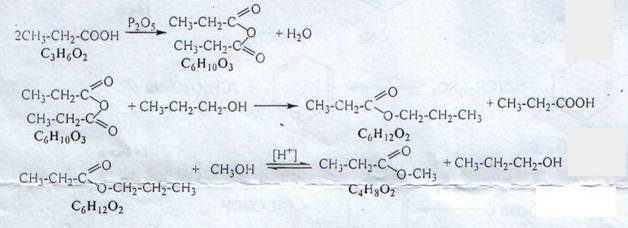
№2. Напишите уравнения реакций, соответствующего следующей схеме превращений:
С6H10 -> С3Н6О2 -> С6Н10О3 ->С6Н12О2 ->С4Н8О2
Укажите структурные формулы веществ и условия протекания реакций.
![]() Решение:
Решение:
![]() 5CH3CH2CH = CHCH2CH2CH3 + 8KMnO4 + 12H2SO4
5CH3CH2CH = CHCH2CH2CH3 + 8KMnO4 + 12H2SO4
![]() 5CH3 - CH2 – COOH + 5CH3 - CH2 – CH2 COOH + 4K2SO4 + 8MnSO4 + 12H2O
5CH3 - CH2 – COOH + 5CH3 - CH2 – CH2 COOH + 4K2SO4 + 8MnSO4 + 12H2O
![]()
Максимальное количество баллов – 4 балла.
№ 3. «История пластикового стаканчика».
Небольшой кусочек пластикового одноразового стаканчика нагрели без доступа воздуха
до 400°С. В результате нагревания был получен углеводород X (содержание углерода 92,26% по массе, плотность его паров по кислороду 3,25). Известно, что при окислении углеводорода X раствором перманганата калия в кислой среде в качестве единственного органического продукта образуется бензойная кислота.
1. Рассчитайте молекулярную формулу X.
2.Приведите структурную формулу, и название углеводорода X. Как называется исходный полимер?
3.Напишите уравнение реакции (со всеми продуктами и стехиометрическими коэффициентами) окисления углерода Х раствором перманганата калия, подкисленного серной кислотой.
Решение:
Содержание верного ответа и указания по оцениванию | Баллы |
1.Мr(Х) = 3,25 × 32 = 104 а. е.м. Найдем молекулярную формулу углеводорода X: С : Н = 0,9226/12б01 : 0,0774/1.008 = 1 : 1, с учетом молекулярной массы получаем C8H8. | 1 |
2. Поскольку при окислении углеводорода X раствором перманганата калия в кислой среде в качестве единственного органического продукта образуется бензойная кислота (C6H5COOH), то его молекула содержит в своем составе бензольное кольцо с одним заместителем. Вычитая из брутто-формулы С8Н8 фрагмент СбН5, получаем заместитель С2Н3. Единственно возможный вариант заместителя - винил, а углеводород X - стирол (винилбензол). Следовательно, полимер, из которого был изготовлен одноразовый стаканчик - полистирол. | 1 |
1 | |
3. Уравнение реакции окисления стирола раствором КМnО4, подкисленного H2SO4:
| 2 |
Максимальное количество баллов – 5 баллов.




