ДЕПАРТАМЕНТ ОБРАЗОВАНИЯ АДМИНИСТРАЦИИМУНИЦИПАЛЬНОГО ОБРАЗОВАНИЯГОРОД КРАСНОДАРМБОУ ДОД ЦДОД «Малая академия» г. Краснодар ул. Чапаева, 85/1 тел. / | Школьный этап всероссийской олимпиады школьников по химии учебный год задания подготовлены муниципальной предметно – методической комиссией; председатель ПМК: |
Задача 8-1. Смесь содержит равное число молекул хлорида калия и сульфата меди. Рассчитайте массовые доли (в процентах) веществ в такой смеси.
Решение задачи 8-1. Массовая доля вещества в смеси рассчитывается по формуле:
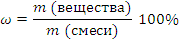
В моле любого вещества содержится одинаковое число структурных единиц – атомов или молекул. Значит, если мы возьмём порцию смеси, содержащей по одному молю каждого вещества, то она будет соответствовать условию задачи.
М (KCl) = 74,5 г/моль, M (CuSO4) = 160 г/моль. m=ν.М
m (KCl) = 74,5 г, m(CuSO4) = 160 г, m(смеси) = 74,5 +160 = 234,5 г
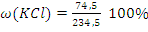 = 31,77%
= 31,77% 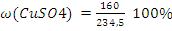 =68.23%
=68.23%
Ответ: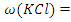 31,77%
31,77%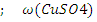 =68.23%.
=68.23%.
Критерии оценки: За определение порции смеси, содержащей равное число молекул компонентов смеси – 2 балла, расчёт молярных масс по 0,5 баллов, расчёт массовой доли каждого компонента по 1 баллу. Всего – 5 баллов.
Задача 8-2. В заливе Кара-Богаз-Гол в воде содержится 30 % глауберовой соли Na2SO4•10H2O. При температуре +5 °С она выпадает в виде белого осадка, как снег, а с наступлением теплого времени снова растворяется. Поскольку в этом заливе глауберова соль то появляется, то исчезает, она была названа мирабилитом, что означает «удивительная соль». Рассчитайте массу раствора, содержащего 1 моль этой соли.
Решение задачи 8-2. Массовая доля вещества в растворе рассчитывается по формуле:
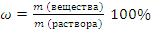 ; откуда следует, что
; откуда следует, что 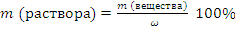
М (Na2SO4•10H2O) = 2.23+32+4.16+ 10.18 = 322 г/моль.
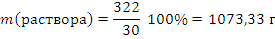
Ответ: 1073,33 граствора.
Критерии оценки: За расчёт молярной массы глауберовой соли – 2 балла, знание формулы для расчёта массовой доли вещества в растворе – 2 балла, расчёт массы раствора по массовой доле - 1балл. Всего – 5 баллов.
Задача 8-3. Созданию периодической системы элементов предшествовало множество попыток классификации известных к тому времени химических элементов. Так были выделены естественные группы химических элементов, обладающие сходными признаками, например: щелочные металлы, щёлочноземельные металлы, галогены, халькогены. Приведите в качестве примера состав группы элементов, общее название которых «халькогены». Что означает это название? Какие минералы, содержащие в своем составе халькогены, вы знаете, где они применяются?
Решение задачи 8-3. Кислород, сера, селен, теллур – это элементы, составляющие главную подгруппу VI группы периодической системы. Они имеют общее название – халькогены, что в переводе с греческого (chalcos – медь, genos – рожденный) означает «рождающий медные руды» и обусловлено тем, что в природе они чаще встречаются в форме соединений с медью (сульфидов, оксидов, селенидов и др.). К минералам, содержащим серу, относятся: ковеллин CuS, халькозин Cu2S, халькопирит CuFeS2. Эти минералы являются основным сырьем в металлургии для производства меди. Широко известный минерал пирит или серный колчедан FeS2 используют в производстве серной кислоты.
Критерии оценки: За определение группы элементов, имеющих общее название «халькогены»- 1 балл, трактовку названия - 2 балла, за примеры минералов (не менее трёх) – 3 балла. Всего – 6 баллов.
Задача 8-4. В ювелирном деле традиционно используют драгоценные камни, например, рубин, сапфир, аметист. Эти камни отличаются большой прочностью, прозрачностью и яркостью окраски. Рубин – драгоценный камень красного, аметист – фиолетового, сапфир – синего цвета. Однако не все знают, что цвет этих камней зависит только от примесей, а основной химический состав у них одинаков. Определите основное вещество этих драгоценных камней, если оно содержит 52,94% алюминия и 47,06% кислорода, а относительная молекулярная масса вещества больше относительной молекулярной массы водорода в 51 раз.
Решение задачи 8-4.
Из условия задачи следует, что Mr(в-ва) = M(H2).51 = 2 · 51 = 102 г
Массовая доля элемента в соединении определяется по формуле: ω =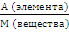 ;
;
N (Al) = ω(Al)· Mr(в-ва)/Ar(Al) = 0,5294·102/27 = 2
N (O) = ω(O)· Mr(в-ва)/Ar(O) = 0,4706·102/16 = 3
Формула вещества Al2O3
Критерии оценки: За расчёт относительной молекулярной массы вещества – 1 балл, формулы для определения массовой доли элемента в соединении – 2 балла, расчёт числа атомов в молекуле и установление формулы – 2 балла. Всего - 5 баллов.
Задача 8-5. Как получить почти чистый азот в пол-литровой банке, используя помимо банки только миску с водой, лёгкую негорючую пластинку, красный фосфор. Сколько молекул азота (при н. у.) будет находиться в банке?
Решение задачи 8-5.На негорючую пластинку необходимо поместить фосфор и поджечь. Пластинку с горящим фосфором поместить на поверхность воды в миску и накрыть пустой банкой. Горение прекратится, когда весь кислород под банкой будет израсходован. В банке останется почти чистый азот.
Расчёт числа молекул азота. В 0,5 литровой банке изначально находился воздух, объёмная доля азота в котором 78%.
V(N2) = 0,78 .0,5 л = 0,39 л. n(N2) = 0,39л : 22,4 л/моль = 0,0174 моль
N (N2) = 0,0174моль·6,02 ·1023 1/моль = 1,048 ·1022
Критерии оценки: За описание способа получения чистого азота – 2 балла, определение объёма азота в составе воздуха – 1 балл, расчёт количества вещества азота – 1 балл, расчёт числа молекул азота – 1балл. Всего – 5 баллов.
Общее количество баллов – 26.
ДЕПАРТАМЕНТ ОБРАЗОВАНИЯ АДМИНИСТРАЦИИМУНИЦИПАЛЬНОГО ОБРАЗОВАНИЯГОРОД КРАСНОДАРМБОУ ДОД ЦДОД «Малая академия» г. Краснодар ул. Чапаева, 85/1 тел. / | Школьный этап всероссийской олимпиады школьников по химии учебный год задания подготовлены муниципальной предметно – методической комиссией; председатель ПМК: |
Задача 9-1. Продукт взаимодействия 5 г водорода и 14,2 г хлора поглощен водой объемом 128 мл. Рассчитайте массовую долю (в %) вещества в образовавшемся растворе. Как называется этот раствор?
Решение задачи 9-1.При взаимодействии водорода и хлора образуется хлороводород по уравнению:
H2 + Cl2 = 2HCl
М=2г/моль М =71 г/моль М= 36,5 г/моль
ν = 1 моль ν = 1 моль ν = 2 моль
m= 2 г m= 71 г m==73 г
Рассчитаем количества вещества исходных реагентов:
ν =![]() ν(H2)=5/2=2.5 моль ν(Cl2)=14.2/71=0,2 моль
ν(H2)=5/2=2.5 моль ν(Cl2)=14.2/71=0,2 моль
Делаем вывод, что водород в избытке, следовательно, расчёт ведём по недостатку. Из 1 моль хлора образуется 2 моль хлороводорода,
а из 0,2 моль хлора получим 0,4 моль хлороводорода
m (HCl) = 0,2. 36.5=7,3 гm (H2О) = V.ρ = 128 мл. 1г/ мл = 128 г
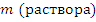 = 128 + 7.3 =135, 3 г соляной кислоты.
= 128 + 7.3 =135, 3 г соляной кислоты.
![]()
Ответ: 5,4 % раствор соляной кислоты.
Критерии оценки: Уравнение реакции – 1 балл, расчёт количества вещества каждого реагента – 2 балла, определение «избытка - недостатка» - 1 балл, расчёт количества вещества хлороводорода – 1 балл, определение массы получившегося раствора – 2 балла, расчёт массовой доли растворённого вещества – 1 балл.
Всего – 8 баллов.
Задача 9-2.Какую массу 10%-ного раствора гидрокарбоната натрия необходимо добавить к 150 г 8%-ного раствора соляной кислоты, чтобы уменьшить ее массовую долю в 2 раза?
Решение задачи 9-2. По условию задачи идёт реакция в соответствии с уравнением:
NaHCO3 + HCl = NaCl + CO2 + H2O
Пусть х – масса раствора гидрокарбоната натрия. n(NaHCO3) = m :M= 0,1x : 84.
По уравнению реакции количество прореагировавшей кислоты:
n(HCl) = n(NaHCO3) = 0,1x : 84; m(HCl) = n ⋅M = 0,043x.
Количество выделившегося газа: n(CO2) = n(NaHCO3); m(CO2) = 0,052x.
Масса получившегося раствора:
m1 (p-pa) = m(p-pa HCl) + m(р-раNaHCO3) - m(CO2) = 150 + x – 0,052x.
Масса соляной кислоты в исходном растворе:m(HСl) = w(HCl) ⋅m(p-pa) = 0,08⋅150 = 12 г.
Масса кислоты, оставшейся после реакции:m1(HCl) = 12 – 0,043x.
Составим и решим уравнение: w1(HCl) = m1 (HCl) :m1 (p-pa) , откуда х = 74,1 г.
Критерии оценки: Уравнение реакции – 2 балла, определение количества выделившегося газа – 1 балл, расчёт массы получившегося раствора– 2 балла, расчёт количества прореагировавшей кислоты - 2 балла, массы соляной кислоты в исходном растворе– 1 балл, определение массы кислоты, оставшейся после реакции - 1 балл, составление алгебраического выражения для расчёта массы раствора гидрокарбоната натрия– 1 балл. Всего – 10 баллов.
Задача 9-3. Какой объем займет 1 кг воздуха при 17оС и давлении 101,33 кПа?
Решение задачи 9-3. Молярная масса воздуха 29 г/моль. Определим количества вещества в 1кг воздуха: ν![]() ; ν
; ν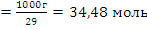
По уравнению Менделеева-Клапейрона найдём объём воздуха:
pV = νRT V= 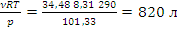
Ответ: 820 л
Критерии оценки: Расчёт количества вещества в 1 кг воздуха – 1 балл, знание уравнения Менделеева-Клапейрона - 2 балла, расчёт объёма воздуха - 1 балл.
Всего – 4 балла.
Задача 9-4. Для окисления 2,17 г сульфита щелочноземельного металла добавили хлорную воду, содержащую 1,42 г хлора. K полученной смеси добавили избыток бромида калия, при этом выделилось 1,6 г брома. Определите состав осадка, содержащегося в смеси, и рассчитайте его массу.
Решение задачи 9-4.Уравнение реакции: MeSO3 +Cl2 + H2O = 2HCl + MeSO4 (1)
Далее с избытком KBr из полученной смеси (HCl, MSO4, избыток Cl2 или избыток MSO3) с выделением Br2 может реагировать только Cl2:
2KBr + Cl2 = 2KCl + Br2, (2)
![]() (Br2) = m(Br2)/M(Br2) = 1,6/160 = 0,01 моль.
(Br2) = m(Br2)/M(Br2) = 1,6/160 = 0,01 моль.
По уравнению реакции (2): ![]() (Cl2) =
(Cl2) = ![]() (Br2) = 0,01 моль.
(Br2) = 0,01 моль.
Суммарно в двух реакциях израсходовано хлора:
![]() (Cl2) = m(Cl2)/M(Cl2) = 1,42/71 = 0,02 моль.
(Cl2) = m(Cl2)/M(Cl2) = 1,42/71 = 0,02 моль.
Следовательно, в реакции (1) прореагировало: 0,02 – 0,01 = 0,01 моль Cl2.
По уравнению реакции (1): ![]() (MeSO3) = n(Cl2) = 0,01 моль;
(MeSO3) = n(Cl2) = 0,01 моль;
M(MeSO3) = m(MeSO3)/![]() (MeSO3) = 2,17/0,01 = 217 г/моль.
(MeSO3) = 2,17/0,01 = 217 г/моль.
Таким образом, соль, участвующая в реакции, – сульфит бария BaSO3.
Уравнение реакции (1):
BaSO3 + Cl2 + H2O = 2HCl + BaSO4![]() .
.
![]() (BaSO4) =
(BaSO4) = ![]() (BaSO3) = 0,01моль,
(BaSO3) = 0,01моль,
m(BaSO4) = ![]() (BaSO4)•M(BaSO4) = 0,01•233 = 2,33 г.
(BaSO4)•M(BaSO4) = 0,01•233 = 2,33 г.
Ответ 2,33 г BaSO4.
Критерии оценки: Уравнения протекающих реакций – 2 балла, расчёт количества вещества брома и хлора по 1 баллу, расчёт количества вещества и молярной массы сульфита – по 1 баллу, расчёт количества вещества и массы сульфата бария – 2 балла.
Всего 8 баллов.
Задача 9-5.50 г смеси фосфата кальция и карбонатов кальция и аммония прокалили, в результате получили 25,2 г твердого остатка, к которому добавили воду, а затем пропустили избыток углекислого газа. Масса нерастворившегося остатка составила 14 г. Определите массу карбоната аммония в исходной смеси.
Решение задачи 9-5. При прокаливании смеси идут следующие процессы:
(1) СаСО3 = СаО + СО2
(2) (NH4)2CO3 ![]() 2NH3
2NH3![]() + СO2
+ СO2![]() + H2O
+ H2O![]() .
.
В твердом остатке после прокаливания – Са3(PO4)2 и CaO.
После добавления воды протекает реакция образования гидроксида кальция:
(3) СаО + H2O = Ca(OH)2.
После пропускания избытка углекислого газа образуется гидрокарбонат кальция, растворимый в воде:
(4) Са(ОН)2 + H2O + CO2 = Ca(HСО3)2.
Нерастворившийся остаток – Ca3(PO4)2, следовательно, m(Ca3(PO4)2) = 14 г.
Находим массу CaO: m(CaO) = 25,2 – 14 = 11,2 г.![]() (CaO) = 11,2/56 = 0,2 моль,
(CaO) = 11,2/56 = 0,2 моль,
![]() (CaCO3) =
(CaCO3) = ![]() (CaO) = 0,2 моль, тогда m(CaCO3) = 0,2•100 = 20 г.
(CaO) = 0,2 моль, тогда m(CaCO3) = 0,2•100 = 20 г.
m(NH4)2CO3 = m(смеси) – m(Ca3(PO4)2) – m(CaCO3) = 50 – 14 – 20 = 16 г.
Ответ. m(NH4)2CO3 = 16 г.
Критерии оценки: За составление уравнений реакций, протекающих при прокаливании смеси - по 1 баллу, определение состава твёрдого остатка после прокаливания– 1 балл, за уравнение реакций взаимодействия оксида кальция с водой и взаимодействия гидроксида кальция с углекислым газом – по 1 баллу, за установление масс фосфата, оксида кальция, карбоната кальция и карбоната аммония – по 1 баллу. Всего – 9 баллов.
ДЕПАРТАМЕНТ ОБРАЗОВАНИЯ АДМИНИСТРАЦИИМУНИЦИПАЛЬНОГО ОБРАЗОВАНИЯГОРОД КРАСНОДАРМБОУ ДОД ЦДОД «Малая академия» г. Краснодар ул. Чапаева, 85/1 тел. / | Школьный этап всероссийской олимпиады школьников по химии учебный год задания подготовлены муниципальной предметно – методической комиссией; председатель ПМК: |
Задача 10-1. При действии избытка воды на 20 г смеси, состоящей из карбида кальция и карбида алюминия, получили 7,84 л газов (н. у.). Найдите массовую долю карбида алюминия в исходной смеси.
Решение задачи 10-1.Пусть в исходной смеси х моль CаC2 и y моль Al4C3, тогда в ходе реакции образуется х моль C2Н2 и 3 y моль CН4:
х моль х моль
CаC2+ 2 Н2О = C2Н2 ↑ + Ca(OH)2
1 моль 1 моль
64 г22,4 л
y моль 3 y моль
Al4C3+ 12 Н2О = 3CН4↑ + 4Al(OH)3↓
1 моль 3 моль
144 г67,2 л
1. m = ν ·M, M (CаC2) = 64 г/моль, M (Al4C3) = 144 г/моль, m (CаC2) = 64x г, m (Al4C3) = 144y г m (смеси) = (64х + 144y) г V = ν·Vm, V(C2Н2) = 22,4 x л, V(CН4) = 67,2 у л.
2. ![]() Составим систему уравнений:
Составим систему уравнений:
64х + 144у = 20
22,4х + 67,2у = 7,84
Получим: у = 0,05 – количество вещества Al4C3 в исходной смеси
m = n ·M, m (Al4C3) = 0,05 моль ·144 г/моль = 7,2 г
ω(Al4C3) = m(Al4C3) : m (смеси);
ω (Al4C3) = 7,2 г :20 г = 0,36 (36%)
Критерии оценки: За уравнения реакций взаимодействия карбидов металлов с водой – по 1 баллу, выражения масскарбидов кальция и алюминия – по 1 баллу, расчёт объёма выделившихся в реакции газов – по 1 баллу, составление и решение системы уравнений – 2 балла, расчёт массы и массовой доли карбида алюминия в смеси – 2 балла. Всего – 10 баллов.
Задача 10-2. Смесь ацетилена и водорода массой 27 г сожгли в кислороде. После охлаждения продуктов сгорания до комнатной температуры сконденсировалось 27 мл воды. Определите состав газовой смеси.
Решение задачи 10-2. При горении газовой смеси протекают следующие реакции:
С2H2 + 2,5O2 ![]() 2CO2
2CO2![]() + H2O, (1)
+ H2O, (1)
2H2 + O2 ![]() 2H2O.(2)
2H2O.(2)
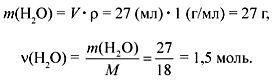
Пусть в уравнении (1): ![]() (C2H2) = х моль, тогда
(C2H2) = х моль, тогда ![]() (H2O) = х моль;
(H2O) = х моль;
в уравнении (2): ![]() (H2) = y моль, тогда
(H2) = y моль, тогда ![]() (H2O) = y моль.
(H2O) = y моль.
Составим систему уравнений:
![]()
Откуда: x = 1, y = 0,5.
m(С2H2) = ![]() (С2H2)•M(С2H2) = 1•26 = 26 г,
(С2H2)•M(С2H2) = 1•26 = 26 г,
m(H2) = ![]() (H2)•M(H2) = 0,5•2 = 1 г.
(H2)•M(H2) = 0,5•2 = 1 г.
![]() (С2H2) = 26/27 = 0,963, или 96,3%.
(С2H2) = 26/27 = 0,963, или 96,3%.
![]() (H2) = 1/27 = 0,037, или 3,7%.
(H2) = 1/27 = 0,037, или 3,7%.
Ответ. В смеси 96,3% C2H2 и 3,7% H2.
Критерии оценки: За уравнения реакций – 2 балла, расчёт массы и количества вещества воды - 1балл, расчёт количества вещества ацетилена и водорода - 2балла, расчёт массы ацетилена и водорода - 1 балл, расчёт массовых долей компонентов газовой смеси – 2 балла. Всего – 8баллов.
Задача 10-3. При сгорании в присутствии кислорода бесцветного газа А с резким характерным запахом образуется другой газ В, без цвета и запаха, реагирующий при комнатной температуре с литием с образованием твердого вещества С. Идентифицируйте вещества, напишите уравнения реакций.
Решение задачи 10-3.При комнатной температуре с литием способен взаимодействовать азот, который образуется при горении азотсодержащих соединений. Таким газообразным веществом с резким запахом является аммиак.
Вещество А – NH3, вещество В – N2, вещество С – Li3N.
4NH3 + 3O2 ![]() 2N2 + 6H2O,
2N2 + 6H2O,
N2 + 6Li = 2Li3N.
Ответ. NH3, N2, Li3N.
Критерии оценки: За аргументацию при определении вещества А (аммиак) – 2 балла, установление веществ В и С – 1 балл, за уравнения реакций – 2 балла. Всего 5 баллов.
Задача 10-4. На чашках весов уравновешены химические стаканы с 0,1 г металлического алюминия в каждом. Как изменится равновесие весов, если в один стакан прилить 5%-ный
раствор соляной кислоты массой 10 г, в другой – 5%-ный раствор гидроксида натрия массой 10 г.
Решение задачи 10-4. Металлический алюминий реагирует с соляной кислотой и
гидроксидом натрия согласно уравнениям:
2Al + 6 HCl = 2 AlCl3 + 3 H2
2Al + 2 NaOH + 6 H2O = 2 Na[Al(OH)4] + 3 H2
При одной и той же массе прореагировавшего алюминия в обоих случаях выделяется одинаковое количество водорода. Следовательно, если алюминий растворится полностью, то равновесие весов не изменится. В случае неполного растворения алюминия, перевесит та чашка весов, где меньшая доля алюминия вступит в реакцию.
В 5%-ных растворах массой 10 г содержится по 0,5 г (10×0,05) соляной кислоты и гидроксида натрия.
M(Al)=27г/моль; M(HCl)= 36,5 г/моль; M(NaOH)= 40 г/моль
Найдем, сколько потребуется соляной кислоты и гидроксида натрия для растворения алюминия массой 0,1 г.
Al массой 27× 2 г вступает в реакцию с HСl массой (36,5× 6) г
Al массой 0,1 г вступает в реакцию с HCl массой х г
х=0,406 г HCl
Al массой 27× 2 г вступает в реакцию с NaOH массой (40× 2) г
Al массой 0,1 г вступает в реакцию с NaOH массой y г; y=0,148 г NaOH
Оба вещества HCl и NaOH взяты в избытке, поэтому в обоих стаканах
произойдёт полное растворение алюминия, выделится равное количество вещества водорода и равновесие весов не нарушится.
Критерии оценки: За уравнение реакций взаимодействия алюминияссоляной кислотой и раствором щёлочи – 2балла; за расчёт массы веществ в исходных растворах и количества вещества НСl и NaOH – 2 балла; за расчёт массы веществ HCl и NaOH, необходимых для растворения 0,1 г алюминия – 2 балла. Вывод о том, что равновесие весов не нарушится – 2 балла.
Задача 10-5. Основатель всесоюзных и всероссийских химических олимпиад школьников профессор Московского государственного университета Альфред Феликсович Платэ рассказывал, что в годы Великой Отечественной войны ему было поручено срочно исследовать содержимое двухлитровой тонкостенной металлической ампулы, находившейся в пилотской кабине сбитого вражеского истребителя. По результатам анализаэта жидкость содержала 22 % углерода, 4,6 % водорода и 73,4 % брома (по массе). Результаты анализа ввергли инженеров и военных специалистов в недоумение.
Установите химический состав неизвестного соединения и выскажите ваши соображения о том, с какой целью эта тонкостенная ампула с необычным содержимым была закреплена в пилотской кабине.
Решение задачи 10-5. Соотношение между числом атомов элементов в изученной жидкости:
С : H : Br = (22/12) : 4,6 : (73,4/80) = 1,83 : 4,6 : 0,92 = 2 : 5 : 1.
Формула исследуемой жидкости – C2H5Br. Естественно, что обнаружение значительного количества этого вещества и к тому же в необычной упаковке вызвало недоумение, пока одному из химиков-экспериментаторов не пришла в голову очень простая мысль: этилбромидкипит при температуре +38°С и помещен в пилотскую кабину в качестве
потенциального противопожарного средства! При пожаре ампула лопается, и пары этилбромида, которые почти в 4 раза тяжелее воздуха, на некоторое время изолируют очаг пожара, прекращая распространение огня.
Критерии оценки: За установление формулы соединения- 2 балла; вывод о том, что этилбромид может служить противопожарным средством -2 балла.
Всего – 4 балла.
ДЕПАРТАМЕНТ ОБРАЗОВАНИЯ АДМИНИСТРАЦИИМУНИЦИПАЛЬНОГО ОБРАЗОВАНИЯГОРОД КРАСНОДАРМБОУ ДОД ЦДОД «Малая академия» г. Краснодар ул. Чапаева, 85/1 тел. / | Школьный этап всероссийской олимпиады школьников по химии учебный год задания подготовлены муниципальной предметно – методической комиссией; председатель ПМК: |
Задача 11-1. Рассчитайте объем (в литрах) при н. у. и массу (в граммах) порции газа, имеющего молекулярную формулу С4Н10 , которая содержит 2,4 ∙ 1024 атомов углерода.
Решение задачи 11-1. Количество вещества можно определить по формуле
ν(С)= N(C)/NА ν(С)= 2,4 ∙ 1024 : 6,02 ∙ 1023= 3,99 моль; ν(C4H10)= ν(С)/4 = 0.997 моль; V(C4H10) = ν(C4H10)Vm = N(C4H10)Vm /NA = N(C) Vm / 4NA =
= 2,4∙1024∙22,4 /4∙6,02∙1023 = 22,3 л
m(C4H10) = ν(C4H10)∙M(C4H10) = N(C4H10) )∙M(C4H10)/NA = N(C) ∙M(C4H10)/ 4NA =
= 2,4∙1024∙58 / 6,02∙1023∙4 = 57,8 г
Критерии оценки: За пересчёт числа атомов углерода в количество вещества углерода, количества вещества бутана, использование формул для расчета объёма и массы бутана – по 1 баллу. Всего – 4 балла.
Задача 11-2.
Осуществите следующие превращения:
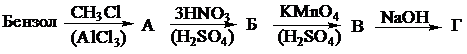
Решение задачи 11-2.
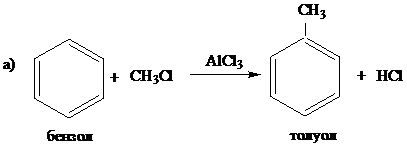
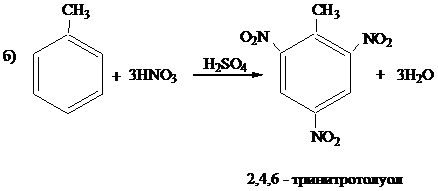

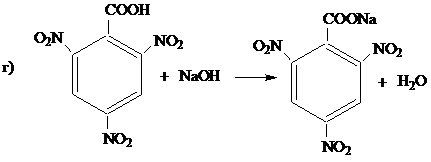
Критерии оценки: За написание уравнений реакций алкилирования бензола и окисления тринитротолуола – по 3 балла, за уравнения реакций нитрования толуола и реакции 2,4,6-тринитробензойной кислоты со щёлочью – по 2 балла. Всего 10 баллов.
Задача 11-3. Сожгли 5,1 г предельной одноосновной карбоновой кислоты. В результате было получено 7,69 л углекислого газа (объем измерен при 127 °С и 108 кПа). Определите молекулярную формулу кислоты и назовите ее.
Решение задачи 11-3. Общая формула гомологического ряда предельных одноосновных карбоновых кислот CnH2nO2, где n =1,2 и т. д.
Уравнение реакции горения кислоты может быть записано в следующем виде:
CnH2nO2 + (3n-2)/2 O2 = n CO2 + n H2O
По уравнению Менделеева-Клапейрона найдём количество вещества выделившегося оксида углерода (IV):
pV = νRT ν =pV/RT T = 273 + 127 =400 ν = 108.7,69/(8,31.400)= 0,25 моль
По уравнению реакции: ν CnH2nO2 =ν СО2/n = ![]() , в тоже время ν CnH2nO2 =
, в тоже время ν CnH2nO2 = ![]() =
= ![]()
Составим и решим алгебраическое выражение:![]() =
=![]() ; n = 5
; n = 5
Таким образом, формула кислоты C5H10O2 - пентановая (валериановая) кислота.
Критерии оценки: За написание уравнения реакции горения кислоты в общем виде – 2 балла, использование уравнения Менделеева-Клапейрона и расчёт количества вещества углекислого газа - 2 балла, установление формулы кислоты – 2 балла.
Всего - 6 баллов.
Задача 11-4. Навеску неизвестного минерала массой 4,42 г прокалили, при этом его масса уменьшилась на 28, 05 % и выделилось 0,448 л газа (н. у.) с плотностью по воздуху примерно 1,52. Такую же навеску минерала растворили в серной кислоте, при этом выделилось такое же количество газа. К образовавшемуся голубому раствору, содержащему только один вид катионов и анионов, прибавили избыток раствора сульфида натрия, образовавшийся осадок отфильтровали и прокалили без доступа воздуха. Его
масса составила 3,82 г. Определите состав минерала.
Решение задачи 11-4. Голубой цвет раствора указывает на то, что в нем содержатся катионы меди. Газ, выделяющийся при прокаливании минерала, имеет молярную массу:
М(газа) = D(возд) ×М(возд.) = 1,52× 29 = 44 г/моль.
Это соответствует молярной массе углекислого газа.
При растворении минерала в кислоте другие газы не выделяются, и образуется раствор, содержащий только один вид анионов, поэтому минерал представляет собой какое-то из карбонатных производных меди.
При смешении раствора, получающегося при взаимодействии минерала с серной кислотой, с сульфидом натрия, протекает реакция:
CuSO4 + Na2S = Na2SO4 + CuS
Рассчитаем химическое количество сульфида меди (II):
ν(CuS) = m/M =3,82 /95,5 = 0,04 моль
При прокаливании минерала образуется остаток массой 4,42 г×0,7195 =3,18 г, в состав которого входит медь.
Предположим, что количество вещества остатка равно количеству вещества меди.
Получаем М=79,5 г/моль, что соответствует молярной массе оксида меди. Еще 0,02 моль× 44 г/моль = 0,88 г приходится на долю выделившегося углекислого газа. В сумме это составляет 4,06 г. Оставшееся вещество массой0,36 г улетучивается при прокаливании минерала, но не представляющее собой газ, может быть только водой (0,02 моля).
Состав минерала равен:0,04 моль СuO, 0,02 моль CO2 , 0,02 моль H2O т. е.
2CuO×CO2 ×H2O илиCu2(OH)2CO3
Это малахит.
Критерии оценки: За установление молярной массы газа, выделившегося при прокаливании минерала и определение его природы – 2 балла; за установление в составе минерала меди по окраске его сернокислотного раствора – 1 балл; за уравнение реакции сульфата меди с сульфидом натрия – 1 балл; расчёт количества вещества сульфида меди – 1 балл; установление состава минерала – 3 балла. Всего 8 баллов.
Задача 11-5. При сжигании этановой кислоты в кислороде выделилось 235,9 кДж теплоты и осталось 10,0 л непрореагировавшего кислорода (измерено при давлении 104,1 кПа и температуре 400С). Рассчитайте массовые доли компонентов в исходной смеси, если известно, что теплоты образования оксида углерода (IV), паров воды и этановой кислоты составляют 393,5 кДж/моль, 241,8 кДж/моль и 484,2 кДж/моль соответственно.
Решение задачи 11-5. При горении этановой (уксусной) кислоты протекает следующая реакция:
CH3COOH(г) + 2O2(г) = 2 CO2(г) + 2 H2O(г) + Q кДж
1 моль 2 моль 2 моль 2 моль
По закону Гесса, тепловой эффект реакции равен сумме теплот образования конечных продуктов за вычетом суммы теплот образования исходных веществ, с учётом стехиометрических коэффициентов в уравнении реакции:
Q =,8 кДж/моль +,5 кДж/моль -484,2 кДж/моль = 786,4 кДж/моль, т. о. делаем вывод, что при горении 1 моль этановой кислоты должно выделиться 786,4 кДж тепла. Найдем количество вещества этановой кислоты, вступившей в реакцию:
ν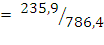 = 0,3 моль; М кислоты = 60 г/моль, mкислоты= ν.М = 0,3 моль.60 г/моль = 18 г
= 0,3 моль; М кислоты = 60 г/моль, mкислоты= ν.М = 0,3 моль.60 г/моль = 18 г
По уравнению реакции количества вещества кислорода в два раза больше количества вещества этановой кислоты: ν![]() 0,3.2= 0.6 моль в избытке остался кислород объёмом 10,0л, измеренным при давлении 104,1 кПа и температуре 400С. Рассчитаем количество вещества кислорода, не вступившего в реакцию по уравнению Клапейрона-Менделеева
0,3.2= 0.6 моль в избытке остался кислород объёмом 10,0л, измеренным при давлении 104,1 кПа и температуре 400С. Рассчитаем количество вещества кислорода, не вступившего в реакцию по уравнению Клапейрона-Менделеева
pV=νRT, ν= 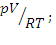 ν=104,1 кПа.10/8,31.313 = 0,4 моль
ν=104,1 кПа.10/8,31.313 = 0,4 моль
Общее количество вещества кислорода = 0,6+0,4 =1,0 моль mкислорода = 32 г
Масса смеси до реакции = 18 + 32 = 50 г
Массовая доля кислорода в смеси составит ω=![]() = 0%), массовая доля кислоты в смеси составит ω=
= 0%), массовая доля кислоты в смеси составит ω=![]() =0%).
=0%).
Критерии оценки:За составление термохимического уравнения реакции и расчёт теплового эффекта реакции -3 балла; расчёт количествавещества этановой кислоты, вступившей в реакцию – 2 балла, расчёт кислорода, вступившего в реакцию – 1 балл, расчет количества вещества кислорода, оставшегося в избытке с использованиемуравнения Клапейрона-Менделеева-2 балла, расчёт массовых долей компонентов исходной смеси – 2 балла. Всего 10 баллов.



