З А Н Я Т И Е N 5
ТЕМА:Химическая термодинамика.
Тепловые эффекты химических реакций.
Направление биохимических процессов
ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
Т Е Р М О Х И М И Я
Математические формулировки Частные случаи I-го закона
I-го закона
1. Для изолированных систем: 1. Процесс протекает при T, V =
Δ u = Q (1) const
где u – внутренняя энергия, кДж/моль – QV = Δu (4)
функция состояния 2. Процесс протекает при T, p =
const
2. Для закрытых систем: Qp = ΔH (5)
Δu = Q – pΔV – A´ (2) Н – энтальпия, кДж/моль –
Q – теплота, кДж/моль функция состояния
pΔV – работа расширения Физический смысл энтальпии:
А´ – полезная работа, кДж/моль а) внутренняя энергия расширен-
 ной системы
ной системы
функции процесса б) теплосодержание
3. Для открытых систем: в) ΔН – тепловой эффект изобар-
Δu = Q – pΔV – A´ + μΔn (3) но-изотермической реакции
m – химический потенциал
Δn – количество вещества, вводимого
в систему
Термохимия
ΔгН – теплота реакции aA + bB → cC + dD
ΔгНо298 – стандартная теплота ΔгН = (сΔfH(C) + dΔfH(D) –
ре акции – (aΔfH(A) + bΔfH(B)) (6)
ΔfHo298 – стандартная теплота образо-
вания химического соединения ΔгB = (aΔ~H(A) + bΔ~H(B)) –
Δ~Ho298 – стандартная теплота – (cΔ~H(C) + dΔ~H(D))
сгорания
ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ
ХИМИЧЕСКОЕ РАВНОВЕСИЕ
Математические формулировки Свободная энергия Гиббса
II закона
Неравенство Клаузиуса ΔгG – свободная энергия хими-
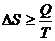 (1) ческой реакции
(1) ческой реакции
ΔfG – свободная энергия образо-
S – энтропия, Дж/моль. К вания химических веществ,
So298 – стандартная энтропия кДж/моль
2. Формула Больцмана S = klnW (2) ΔfGo298 – стандартная свободная
3. Расчет энтропийного фактора энергия образования, кДж/моль
химической реакции: Вычисления ΔгG химических реак-
аА + bB 6 cC + dD ций:
ΔгS = (cS(C) + dS(D)) – (aS(A) + bS(B)) 1) ΔгG = ΔгH – T ΔгS
2) Для условной реакции:
ΔгG = cΔfG(C) + dΔfG(D) – aΔfG(A) –
– bΔfG(B)
3) Для реакций в растворе:
![]()
Характеристики химического равновесия
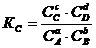
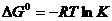
Частные случаи констант равновесия:
1) Константа диссоциации: СН3СООН ↔ Н+ + СН3СОО¯
![]()
2) Константа диссоциации: NH4ОН ↔ NH4+ + OH¯
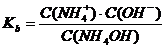
3) Константы гидролиза солей:
NH4CI + H2O ↔ NH4OH + HCI
NH4+ + H2O ↔ NH4OH + H+
![]()
CH3СООNa + H2О ↔ СН3СООН + NaOH
CH3СОО¯ + H2О ↔ СН3СООН + OH¯
![]()
МАТЕРИАЛЫ ДЛЯ САМОПОДГОТОВКИ СТУДЕНТОВ:
1. Вычислите тепловой эффект биохимического процесса брожения глюкозы: C6H12O6 → 2 C2H5OH + 2 CO2(г), если теплоты сгорания глюкозы и этилового спирта соответственно равны: –2816 кДж/моль и –1236 кДж/моль.
Решение: в соответствии со следствием из закона Гесса тепловой эффект реакции равен:
ΔrH = ΔкрH(C6H12O6) – 2ΔкрH(C2H5OH) = –2816 – 2(–1236) = –314 (кДж)
Данная реакция является экзотермической, т. е. протекает с выделением тепла.
2. Рассчитайте тепловой эффект реакции получения этилового эфира аминобензойной кислоты (полупродукта при получении анестезина) при стандартных условиях по уравнению реакции:
4 С2H5OCOC6H4NO2(ж) + 9 Fe + 4 H2O(ж) → 4 C2H5OCOC6H4NH2(ж) + 3 Fe3O4,
если известны стандартные теплоты образования участников реакции:
Вещество: ΔfHo298, кДж/моль
C9H9O4N(ж) –463,2
H2O(ж) –273,2
C9H11NO2(ж) –1759,0
Fe3O4 –1068,0
3. Теплота сгорания бензойной кислоты C6H5COOH равна –3227,5 кДж/моль. Теплоты образования воды и диоксида углерода при тех же условиях соответственно равны –285,8 и –393,5 кДж/моль. Вычислите теплоту образования C6H5COOH.
4. Дайте заключение о возможности самопроизвольного протекания химической реакции при Т = 298 К.
фермент

![]() Н3С – СH – COOH H3C–C–COOH + H2,
Н3С – СH – COOH H3C–C–COOH + H2,
![]()
![]() ║
║
ОН О
по следующим данным:
Вещество: ΔfHo298, кДж/моль So298, кДж/моль
H3C–CH–COOH
![]() –
–
OН
(молочная к-та)
![]() H3C – C – COOH
H3C – C – COOH
 ║ –
║ –
O
(пировиноградная к-та)
Н
Решение: 1) Рассчитаем ΔrHо298 по следствию из закона Гесса:

![]() ΔrHo298 = ΔfHo298 (H3C–C–COOH) – ΔfHo298 (H3C – CH – COOH) =
ΔrHo298 = ΔfHo298 (H3C–C–COOH) – ΔfHo298 (H3C – CH – COOH) =
 ║
║
O OH
= –586 – (–673) = 87 (кДж) (Реакция эндотермична)
2) Рассчитываем энтропийный фактор реакции (ΔrSo298)
ΔrSo298 = So298(H3C–C–COOH) + So298(H2) - So298 (H3C–CH–COOH) =

![]() ║
║
O OH
= 179 + 130 – 192 = 117 Дж/К = 0,117 кДж/К
3) Рассчитаем ΔrGo298 по уравнению: ΔG = ΔH – ТΔS
ΔrGo298 = 87 – 298 (0,117) = 52 кДж (ΔG > 0)
Данная реакция в стандартных условиях самопроизвольно не протекает.
5. Не производя вычислений, установите знак ΔS следующих процессов:
а) 2 NH3(г) → N2(г) + 3 H2(г)
б) CO2(тв) → CO2(г)
в) 2 NO(г) + O2(г) → 2 NO2(г)
г) 2 H2S(г) + 3 O2(г) → 2 H2O(ж) + 2 SO2(г)
д) 2 CH3OH(г) + 3 O2(г) → 4 H2O(г) + 2 CO2(г)
6. Недавними измерениями величин ΔH и ΔG для гидролиза АТФ было показано, что при 36оС и физиологических значениях рН они равны соответственно –4800 и –7000 ккал/моль. Вычислите величину ΔS для тех же условий. Каков смысл того, что ΔS имеет положительное значение?
7. Как повлияет повышение давления на равновесие в следующих обратимых реакциях, протекающих в газовой фазе:
1) N2O4 ↔ 2 NO2 4) 2 SO2 + O2 ↔ 2 SO3
2) 2 NO + O2 ↔ 2 NO2 5) N2 + 3 H2 ↔ 2 NH3
3) H2 + I2 ↔ 2 HI 6) CO + SO3 ↔ CO2 + SO2
МАТЕРИАЛЫ УИРС:
Расчет термодинамических характеристик (ΔrH, ΔrS, ΔrG) биохимических реакций.
ЛИТЕРАТУРА
ОСНОВНАЯ:
1. Конспект лекций.
2. Общая химия. Под ред. М., "Высшая школа" 1993 г., с. 10-42.
3. "Введение в бионеорганическую и биофизическую химию", М., 1989, с. 6-54.
ДОПОЛНИТЕЛЬНАЯ:
1. Практикум по общей химии. Под. ред. М., "Высшая школа", 1993 г., с. 17-31.
2. "Химия" СПб "Специальная литература", 1997 г., с. 107-126.
3. В. Уильямс, Х. Уильямс "Физическая химия для биологов", М., 1976, с. 58-123.



