1. [Co3+(NH3)6]; 9. [Co3+(NH3)2(NO2)4];
2. [Ni3+(H2O)4Cl2]; 10. [Pt4+Cl6];
3. [Zn2+ (OH) 4]; 11. [Fe2+ (CN) 6];
4. [Sb5+ (OH) 6]; 12. [Co3+F6];
5. [Co3+ (NH3)5Br]; 13. [Pt4+Br4];
6. [Fe3+F6]; 14. [Au3+Cl4];
7. [Co3+ (NH3)5SO4]; 15. [Co3+(NO2)6];
8. [Pt4+(NH3)4Cl];
3. Составьте молекулярные и ионные уравнения реакций, приводящие к образованию одного малорастворимого вещества:
1. FeCl3+K4 [Fe (CN) 6] →
2. [Pt (NH3)6] Cl4+AgNO3 →
3. K2SO4+Na3 [Co (NO2)6] →
4. [Pt (NH3)3Cl3] Cl+Pb (NO3)2 →
5. FeSO4+K3 [Fe (CN) 6] →
6. NaCl+K [Sb (OH) 6] →
7. [Co (NH3)5SO4] Cl+AgNO3 →
8. [Cu (NH3)4] SO4+BaCl2 →
9. [Co (NH3)5SO4] Br+AgNO3 →
10. [Co (NH3)5Br] SO4+BaCl2 →
11. CuSO4+K4 [Fe (CN) 6] →
12. Na3 [Co (CN) 6] +FeSO4 →
13. K3 [Fe (CN) 6] +AgNO3 →
14. K [Sb (OH) 6] +Na2SO4 →
15. Na3 [Co (CN) 6] +KCl →
4. Представьте указанные в вашем варианте вещества в виде комплексных соединений:
1. KCN∙AgCN; 9. 2KCN∙Ni(CN)2;
2. Co (NO3)3∙6NH3; 10. 2KCl∙PtCl4;
3. 2KCN∙Cu (CN) 2; 11. AgCl∙2NH3;
4. CoCl3∙6NH3; 12. 4KCN∙W (CN) 4;
5. 2KSCN∙Co (SCN) 2; 13. 2NH3∙PtCl4;
6. 4KCN∙Fe (CN) 2; 14. CoF3∙3NaF;
7. KCl∙AuCl3; 15. CrCl3∙6H2O;
8. CuCl2∙4NH3;
6. ТЕМА "Энергетика химических процессов"
Вопросы энергетики химических процессов являются предметом изучения отдельного раздела химии, называемого химической термодинамикой. Основными задачами этого раздела являются определение тепловых эффектов химических реакций, возможности самопроизвольного их течения в заданных условиях, а также выявление наиболее рациональных условий, обеспечивающих эффективный ход процесса.
При изучении данной темы студент должен:
- ознакомиться с основными термодинамическими понятиями и величинами;
- понять сущность и практическую значимость первого закона термодинамики, закона Гесса, второго закона термодинамики;
- разобраться в практических расчетах изобарного теплового эффекта при стандартных условиях ∆Н0298, изменения энтропии ∆S0298 и энергии Гиббса ∆G0298 для любой химической реакции;
- научиться на основе расчетов ∆Н, ∆S, ∆G судить о выделении или поглощении теплоты в процессе реакции, а также возможности ее самопроизвольного протекания.
Задание для самостоятельной расчетной работы
1. Используя справочные данные таблицы №5 , определите изобарный тепловой эффект ∆Н0298 химической реакции вашего варианта (таблица №4). Сделайте вывод о выделении или поглощении теплоты в процессе реакции.
2. Определите изменение энтропии ∆S0298 в ходе химической реакции, протекающей при стандартных условиях в идеальном газообразном состоянии. Объясните знак изменения ∆S0298 в результате данной реакции.
3. Определите изменение энергии Гиббса ∆G0298 в ходе химической реакции, используя справочные данные таблицы № 5. По знаку изменения энергии Гиббса ∆G0298 сделайте вывод о возможности самопроизвольного протекания.
Таблица №4
№ Варианта | Химические реакции |
1. | 4NH3(г)+5О2(г)↔6Н2О(г)+4NO(г) |
2. | CO(г)+3H2(г) ↔CH4(г)+H2O(г) |
3. | 4HCl(г)+О2(г) ↔2H2O(г)+Cl2(г) |
4. | 2CO(г)+3H2(г) ↔CH4(г)+CO2(г) |
5. | 2CH4(г)+О2(г) ↔2СO(г)+4H2(г) |
6. | CH4(г)+2H2O(г) ↔CO2(г)+4H2(г) |
7. | CH4(г)+H2O(г) ↔CO(г)+3H2(г) |
8. | 4NH3(г)+3О2(г) ↔6Н2О(г)+2N2(г) |
9. | C2H4(г)+3О2(г) ↔2СO2(г)+2H2O(ж) |
10. | 4NH3(г)+5О2(г) ↔6Н2О(ж)+4NO(г) |
11. | CH4(г)+О2(г) ↔2СO(г)+2H2O(г) |
12. | CO(г)+H2O(ж) ↔CO(г)+H2(г) |
13. | CH4(г)+СО2(г) ↔2СO(г)+2H2(г) |
14. | CH4(г) ↔C2H2(г)+3H2(г) |
15. | 2CO(г)+3H2(г) ↔C2H2(г)+3H2O(ж) |
Таблица №5
Вещество | Состояние | ∆Н0298, | ∆G0298, | S0298, |
С2Н2 | г | 226,750 | 209,200 | 200,820 |
NO | г | 90,370 | 86,690 | 210,200 |
С2Н4 | г | 52,280 | 68,173 | 219,450 |
NH3 | г | -45,190 | -16,647 | 192,500 |
CH4 | г | -74,850 | -50,830 | 186,190 |
СО | г | -110,520 | -137,270 | 197,910 |
СО2 | г | -393,510 | -394,380 | 213,650 |
H2O | г | -241,830 | -228,590 | 188,720 |
H2O | ж | -285,950 | -237,190 | 69,940 |
N2 | г | 0,000 | 0,000 | 200,000 |
H2 | г | 0,000 | 0,000 | 130,590 |
О2 | г | 0,000 | 0,000 | 205,030 |
Cl2 | г | 0,000 | 0,000 | 222,950 |
7. ТЕМА "Кинетика химических реакций. Химическое равновесие"
Учение о кинетике химических процессов является одним из важных разделов химии, посвященных изучению скоростей химических реакций в зависимости от различных факторов (концентрации реагентов, температуры, давления, катализаторов и др.). При рассмотрении обратимых химических реакций с одинаковыми скоростями прямого и обратного процессов (состояние химического равновесия), большое значение имеет принцип смещения химического равновесия Ле Шателье.
При изучении данного раздела необходимо:
- выучить закон действующих масс, правило Вант-Гоффа, принцип Ле Шателье;
- уметь составлять выражения скоростей прямой и обратной реакции для любого химического процесса;
- знать, как влияют различные факторы: температура, давление, концентрация, наличие катализатора на скорость химических реакций и особенности действия катализаторов;
- уметь составлять выражение константы химического равновесия, грамотно использовать принцип Ле Шателье при определении смещения химического равновесия.
Пример: N2 + 3H2![]() 2NH3 + Q
2NH3 + Q
Скорость прямой реакции: ![]() =
= ![]()
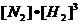 ;
;
Скорость обратной реакции: ![]() =
= ![]()
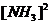 ;
;
Константа равновесия: Кс = ![]()
При увеличении концентрации Н2 равновесие сместится вправо, т. к. по правилу Ле Шателье преимущество получит та реакция, в ходе которой водород будет расходоваться, т. е. прямая.
При увеличении температуры равновесие сместится влево т. к. по правилу Ле Шателье преимущество получит та реакция, в ходе которой температура системы понижается, т. е. обратная реакции, идущая с поглощением теплоты.
При увеличении давления равновесие сместится вправо т. к. по правилу Ле Шателье преимущество получит та реакция, в ходе которой давление в системе понижается, т. е. прямая реакции, в ходе которой из 4 моль вещества образуется 2 моль вещества.
Задания для самостоятельной работы
Для каждой нижеприведенной реакции в соответствии с № варианта:
1) напишите кинетические уравнения скоростей прямой реакции, обратной реакции и выражение константы равновесия;
2) определите, в какую сторону сместится химическое равновесие при увеличении концентрации первого исходного вещества, повышении температуры и увеличении давления.
1) 2CO(Г)+O2(Г)↔2CO2(Г) ∆H= -556,0 кДж
2) Fe3O4(К)+CO(Г)↔3FeO(К)+CO2(Г) ∆H= 34,6 кДж
3) N2(Г)+O2(Г)↔2NO(Г) ∆H= 180,0 кДж
4) C(графит)+2N2O(Г)↔CO2(Г)+N2(Г) ∆H= -558,0 кДж
5) 4NH3(Г)+5O2(Г)↔4NO(Г)+6H2O(Ж) ∆H= -1122,6 кДж
6) 2H2(Г)+O2(Г)↔2H2O(Г) ∆H= -483,6 кДж
7) CaCO3 (K) ↔CaO (K) +CO2 (Г) ∆H= 179,0 кДж
8) CH4(Г)+2O2(Г)↔2H2O(Ж)+CO2(Г) ∆H= -890,3 кДж
9) 2SO2(Г)+O2(Г)↔2SO3(Г) ∆H= -198,0 кДж
10) 4NH3(Г)+3O2(Г)↔2N2(Г)+6H2O(Ж) ∆H= -1530,0 кДж
11) C2H5OH(Ж)+3O2(Г)↔2H2O(Ж)+2CO2(Г) ∆H= -1366,9 кДж
12) CO(Г)+H2O(Ж)↔CO2(Г)+H2(Г) ∆H= 2,9 кДж
13) 4HCl(Г)+O2(Г)↔2H2O(Г)+2Cl2(Г) ∆H= -114,4 кДж
14) PCl5(Г)↔PCl3(Г)+2Cl2(Г) ∆H= 92,6 кДж
15) 2HI(Г)↔H2(Г)+I2(Г) ∆H= 52,0 кДж
8. ТЕМА "Окислительно-восстановительные реакции"
Реакции окисления и восстановления играют важную роль при обмене веществ в живых организмах, в процессах горения жидкого и газообразного топлива, в электрохимических процессах гальванических элементов, аккумуляторах, в процессах электролиза, коррозии металлов, почвообразования, разрушения горных пород, в процессах самоочищения водоемов и т. д.
При изучении этой темы необходимо:
- приобрести навыки в определении степени окисления атомов элементов в простых и сложных веществах;
- усвоить понятия "окисление", "восстановление", "восстановитель", "окислитель";
-уметь отличать уравнения окислительно-восстановительных реакций от уравнений обменных реакций;
- получить навыки в составлении уравнений реакций окисления-восстановления, определять тип окислительно-восстановительных реакций.
Задания для самостоятельной работы
1. Укажите, какие из приведенных процессов представляют собой окисление, и какие – восстановление?
№ варианта
1. S→SO42─; MnO4─→Mn2+; Cl─→ClO3─; Cr3+→Cr0;
2. Ca→CaO; S2─→S0; ClO─→Cl2; CrO42─→Cr3+;
3. MnO42─→Mn0; P3─→P5+; NO2─→NO3─; Fe2O3→Fe0;
4. Al0→AlO2─; S2─→SO42─; MnO2→Mn0; Pb4+→Pb2+;
5. Mg2+→Mg0; PH3→H3PO4; AlO2─→Al0; Fe6+→Fe3+;
6. P2O5→PH3; MnO4─→Mn0; Fe2+→H2FeO4; Mn2+→MnO2;
7. NH3→NO; FeO→Fe2O3; SnO2→SnO; CrO42─→CrO;
8. ZnO22─→Zn0; PbO→PbO2; NO2─→NH3; CrO42─→Cr0;
9. BrO3─→Br2; Ni (OH) 3→Ni (OH) 2; MnO2→MnO4─; S0→SO42─;
10. NO2─→NO3─; Al0→AlO33─; Cl2O7→ClO─; Mn4+→MnO42─;
11. Mn2+→MnO42─; Cl7+→HCl; FeO2─→Fe0; SO32─→ SO42─;
12. I2→IO3─; MnO2→Mn0; NO→NH3; H2S→SO2;
13. PO43─→PH3; S2─→SO2; Al0→AlO2─; NO3─→NH3;
14. MnO2→MnO4─; SO42─→SO2; CeO42─→Cr2O3; N2O→ NO3─;
15. N2→NH3; H2S→SO2; MnO4─→MnO2; CrO42─→CrO;
2. Методом электронного баланса подберите коэффициенты, укажите окислитель и восстановитель для следующих окислительно-восстановительных реакций:
№ Варианта
1. Cu+HNO3→Cu (NO3)2+NO+H2O;
HBr+H2SO4→Br2+SO2+H2O;
KClO→KClO3+KCl;
2. Na2SO3→Na2S+Na2SO4;
KCl+KMnO4+H2SO4→Cl2+KCl+MnSO4+H2O;
Zn+HNO3→Zn (NO3)2+N2O+H2O;
3. KMnO4+KNO2+H2O→KNO3+MnO2+KOH;
Br2+KOH→KBr+KBrO3+H2O;
Mg+HNO3→Mg (NO3)2+N2+H2O;
4. Ca3 (PO4)3+C+SiO2→CaSiO3+P+CO;
Na+HNO3→NaNO3+NH4NO3+H2O;
PH3+O2→P2O5+H2O;
5. Ag+HNO3→AgNO3+NO+H2O;
KMnO4+H2S+ H2SO4→K2SO4+S+MnSO4 +H2O;
HIO3+HI→I2+H2O;
6. SiO2+HF→SiF4+O2;
NaI+NaIO3+H2SO4→I2+Na2SO4+H2O;
Mg+HNO3→Mg (NO3)2+NH4NO3+H2O;
7. HClO4+H2SO3→HCl+H2SO4;
NH3+O2→NO+H2O;
Cu+HNO3→Cu (NO3)2+NO+H2O;
8. Cl2+H2O→HClO4+HCl;
KI+KMnO4+H2SO4→I2+K2SO4+MnSO4+H2O;
Ni+HNO3→Ni (NO3)2+NO+H2O;
9. NaCl+MnO2+H2SO4→Cl2+Na2SO4+MnSO4+H2O;
KClO3→KCl+O2;
Mg+H2SO4→MgSO4+ H2S+H2O;
10. KMnO4+HCl→KCl+Cl2+MnCl2+H2O;
H2S+HIO3→S+I2+H2O;
Fe+HNO3→Fe (NO3)3+N2+H2O;
11. P+H2SO4→H3PO4+SO2+H2O;
Hg+HNO3→Hg (NO3)2+NO+H2O;
S+KOH→K2S+K2SO4+H2O;
12. Pb+HNO3→Pb (NO3)2+NO+H2O;
NH4NO2→N2+H2O;
K2Cr2O7+H2S+H2SO4→Cr2 (SO4)3+S+K2SO4+H2O;
13. Ca+HNO3→Ca (NO3)2+NH4NO3+H2O;
Br2+KOH→KBr+KBrO3+H2O;
AgNO3→Ag+NO2+O2;
14. CrCl3+H2O2+KOH→KCl+K2CrO4+H2O;
Al+HNO3→Al (NO3)3+NH4NO3+H2O;
V2O5+Ca→V+CaO;
15. As2S3+HNO3→H3AsO4+H2SO4+NO;
Fe (OH)2+O2+H2O→Fe(OH)3
K+H2SO4→K2SO4+H2S+H2O.
3. Какие свойства проявляют в окислительно-восстановительных реакциях данные вещества, учитывая степень окисления атома элемента, указанного в скобках вашего варианта? Дайте мотивированный ответ.
№ варианта
1. H2SO4 H2S SO3 (S);
2. Mn KMnO4 MnO2 (Mn);
3. K2Cr2O7 Cr Cr2O3 (Cr);
4. HNO2 NH3 NO (N);
5. Fe Fe2O3 H2FeO4 (Fe);
6. K2MnO4 Mn2O7 MnO (Mn);
7. SO2 S H2SO4 (S);
8. HCl Cl2 HClO4 (Cl);
9. MoO Mo MoO3 (Mo);
10. K2CrO4 Cr NaCrO2 (Cr);
11. HBr HBrO3 Br2 (Br);
12. HNO3 NaNO2 NH3 (N);
13. H2S H2SO4 H2SO3 (S);
14. H2 HCl BaH2 (H2);
15. V V2O5 V2O3 (V).
9. ТЕМА: "Концентрация растворов"
Концентрацией растворов называют содержание растворенного вещества в определенном массовом или объемном количестве раствора или растворителя.
Наиболее часто употребляемые в химии способы выражения концентрации растворов: массовые доли, молярная концентрация, молярная концентрация эквивалентов, моляльная концентрация. При выполнении индивидуальных заданий необходимо:
- усвоить основные способы выражения концентрации растворов;
- приобрести навыки в решении расчетных задач на концентрации растворов;
- получить представление о приготовлении аккумуляторных жидкостей, моющих растворов, растворов антифризов и др.
Задания для самостоятельной работы
Вариант №1
1. Вычислите массу BaCl2∙2H2O, необходимую для приготовления 500г раствора с массовой долей BaCl2 5%.
2. Вычислите объем раствора гидроксида натрия ρ=1,41г/см3 (38%), необходимый для приготовления 2кг моющего раствора с массовой долей NaOH 10%.
3. Вычислите массу K2CO3, необходимую для приготовления 100мл 0,1М раствора.
4. Для приговления антифриза к 5л воды прибавили 2л этилового спирта С2Н5ОН ρ=0,8г/см3. Вычислите температуру замерзания антифриза.
Вариант №2
1. Вычислите массу CuSO4∙5H2O, необходимую для приготовления 250мл 0,005н раствора.
2. Вычислите объем раствора серной кислоты ρ=1,59г/см3 (68%), необходимый для приготовления 5л аккумуляторной жидкости ρ=1,22г/см3 (30%).
3. Вычислите массу гидроксида калия, необходимую для приготовления 1л раствора ρ=1,08г/см3 с массовой долей КОН 10%.
4. Вычислите температуру замерзания раствора антифриза, полученного при растворении 1кг этиленгликоля С2Н4(ОН)2 в 2кг воды.
Вариант №3
1. Вычислите массу BaCl2∙2H2O, необходимую для приготовления 500мл 0,1н раствора.
2. Какой объем раствора гидроксида натрия ρ=1,41г/см3 (38%) и воды потребуется для приготовления 4кг моющего раствора с массовой долей NaOH 5%.
3. Вычислите массу MgSO4, необходимую для получения 0,5кг раствора с массовой долей MgSO4 10%.
4. При какой температуре будет замерзать раствор сахара с массовой долей С12Н22О11 50%.
Вариант №4
1. Вычислите массу гидроксида калия, необходимую для приготовления 500мл 0,05н раствора.
2. Какой объем воды необходимо добавить к 200мл раствора ρ=1,1г/см3 с массовой долей гидроксида натрия 50%, чтобы получить раствор с массовой долей гидроксида натрия 8%?
3. Какие массы медного купороса CuSO4∙5H2O и воды надо взять, чтобы приготовить 1кг раствора с массовой долей CuSO4 8%?
4. Для приготовления антифриза к 5л воды прибавили 1,6кг метилового спирта СН3ОН. Какова температура замерзания антифриза?
Вариант №5
1. Вычислите массу Na2CO3∙10H2O, необходимую для приготовления 250мл 0,01М раствора.
2. Какой объем раствора серной кислоты ρ=1,84г/см3 (98%) и воды потребуется для приготовления 3л аккумуляторной жидкости ρ=1,26г/см3 (35%)?
3. Вычислите массу гидроксида натрия, необходимую для приготовления 2кг моющего раствора с массовой долей NaOH 10%.
4. При какой температуре замерзает раствор антифриза, содержащий 1500г этиленгликоля С2Н4(ОН)2 и 2000г воды?
Вариант №6
1. Вычислите массу Na2CO3∙10H2O, необходимую для приготовления 3л 0,05н раствора.
2. Какой объем концентрированной хлороводородной кислоты ρ=1,19г/см3 (38%) нужно взять для приготовления 2л 0,25М раствора?
3. Вычислите массу КОН, необходимую для приготовления 3кг моющего раствора с массовой долей КОН 5%.
4. В каком отношении должны находиться масса воды и глицерина С3Н5(ОН)3, чтобы при их смешивании получился антифриз с температурой замерзания -400С?
Вариант №7
1. В 450г воды растворили 50г CuSO4∙5H2O. Определите массовую долю CuSO4 в этом растворе.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



