УДК 628.3:658.56
Интегрально-сорбционный метод контроля состава
сточных вод (экологический сторож)
,
Институт водных проблем РАН, г. Москва, Россия
Институт геохимии и аналитической химии им. РАН,
г. Москва, Россия
Скрытые залповые сбросы токсичных веществ в природные водоемы, к которым нередко прибегают промышленные предприятия, представляют серьезную экологическую опасность [4]. В связи с этим контроль качества сточных вод, отводимых в водоемы, имеет большое природоохранное значение. Хотя основное внимание уделяется разработке автоматизированных инструментальных систем мониторинга [3], проблема создания таких систем далека от решения вследствие их чрезвычайной дороговизны, отсутствия чувствительных сенсорных датчиков-анализаторов и надежных средств автоматизации анализа.
Предложенный интегрально-сорбционный способ определения состава сточных вод не является альтернативой системам оперативного контроля, однако в сочетании с соответствующим математическим обеспечением позволяет с достаточной для практики точностью восстанавливать качество сточной воды за определенный расчетный период работы сорбционной колонки.
При сорбции загрязняющего вещества его распределение по слою сорбента отражает изменение концентрации этого вещества в сточной воде по времени. Это распределение определяется разными способами: напрямую спектрофотометрически, изготовив колонку из стекла или сделав ее разборной, состоящей из нескольких секций, и затем осуществляя регенерацию в каждой секции отдельно, определяя содержание сорбированного компонента в регенерате. Выбор сорбента и форма его исходного состояния зависят от состава сточной воды. Сточная вода подается на вход колонки по байпасной схеме, а время сорбции выбирается экспериментально или на основе математической модели процесса.
Если известны физико-химические условия сорбции, то возникает сугубо математическая проблема: восстановить переменную входную концентрацию загрязняющих компонентов по известному итоговому распределению их концентраций по слою сорбента.
Скорость продвижения по колонне («фазовая» скорость) точек концентрационного профиля, соответствующих постоянным концентрациям некоторого i-го компонента в растворе или в сорбенте ![]() = Const или
= Const или ![]() , выражается соотношением [7]
, выражается соотношением [7]
![]() , (1)
, (1)
где ![]() – линейная скорость раствора, отнесенная к сечению колонны.
– линейная скорость раствора, отнесенная к сечению колонны.
Пусть некоторый раствор, например, часть потока сточной воды предприятия, постоянно со средней скоростью ![]() пропускается через сорбционное устройство. Если в результате какого-либо процесса, например, скрытого залпового сброса загрязняющего компонента i, в слое сорбента, равновесном с макросоставом сточной воды, например, находящегося преимущественно в форме иона
пропускается через сорбционное устройство. Если в результате какого-либо процесса, например, скрытого залпового сброса загрязняющего компонента i, в слое сорбента, равновесном с макросоставом сточной воды, например, находящегося преимущественно в форме иона ![]() , сформирована зона (пик) микрокомпонента i, то для определения фазовой скорости переноса этого пика можно воспользоваться соотношением
, сформирована зона (пик) микрокомпонента i, то для определения фазовой скорости переноса этого пика можно воспользоваться соотношением
![]()
![]() , (2)
, (2)
где ![]() - коэффициент Генри для линейной изотермы,
- коэффициент Генри для линейной изотермы, ![]() - коэффициент однократного разделения компонентов,
- коэффициент однократного разделения компонентов, ![]() – емкость ионита,
– емкость ионита, ![]() – суммарная концентрация всех компонентов в растворе. При известном значении фазовой скорости, определяемой по формулам (1) и (2), и с использованием экспериментальных данных о перемещении середины пика микрокомпонента в колонке
– суммарная концентрация всех компонентов в растворе. При известном значении фазовой скорости, определяемой по формулам (1) и (2), и с использованием экспериментальных данных о перемещении середины пика микрокомпонента в колонке ![]() , определяемом с помощью послойного анализа состава ионита, всегда можно рассчитать время
, определяемом с помощью послойного анализа состава ионита, всегда можно рассчитать время 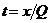 , то есть восстановить время залпового сброса. По данным о количестве вещества и ширине пика можно восстановить локальную концентрацию и протяженность скрытого сброса. Изложенная идея остается в силе для случая нескольких микрокомпонентов, а также для нескольких последовательных сбросов.
, то есть восстановить время залпового сброса. По данным о количестве вещества и ширине пика можно восстановить локальную концентрацию и протяженность скрытого сброса. Изложенная идея остается в силе для случая нескольких микрокомпонентов, а также для нескольких последовательных сбросов.
Возможность использования описанного метода в реальных условиях обусловлена разрешением двух самостоятельных проблем. Первая из них связана с обратной задачей динамики ионного обмена, относящейся к классу некорректных задач, решение которых требует привлечения современных методов решения некорректных задач математической физики [1].
Другой проблемой, с которой мы сталкиваемся при описании динамики ионного обмена из растворов с малыми концентрациями целевых компонентов (соизмеримых с ПДК в природных водах), является повышенная селективность сорбентов к этим компонентам, значительно превосходящая оценки, которые могут быть сделаны из известных литературных данных по равновесиям обмена на ионитах [8]. Такое нарушение линейности изотерм обмена при малых и сверхмалых концентрациях может быть связано со многими факторами, в том числе с неидеальностью (полифункциональностью) обычных ионитов. Отметим, что эффект инверсии селективности ионитов при обмене ионов одинакового заряда в литературе обсуждался [2,6 ].
Ранее был предложен и экспериментально апробирован подход к решению этой проблемы, обеспечивающий принципиальную возможность формирования и перемещения в слое ионита зоны целевого загрязняющего компонента с помощью специального ввода в состав исходного ионита микродобавок («зарядка сорбента») определяемых компонентов или близких к ним по свойствам «сильноудерживаемых» компонентов.
В работе использовали катионит КУ-2х8 и раствор, моделирующий катионный состав реки Москвы: Na+- 1,74; K+-0,179; Ca2+- 2,0; Mg2+- 0,494 мг-экв/л. В качестве примеров загрязняющих микрокомпонентов были взяты ионы Cu2+ и Ni2+ в концентрациях 5…10 мг/л, каждый в виде соответствующих сульфатных растворов. Согласно [5], использовали исходную Li-форму катионита, так как катионит КУ-2 менее селективен к иону Li+, чем к иону Na+ – наименее сорбируемому из макрокомпонентов исследуемого раствора. Это позволяет по скорости переноса по колонне переднего фронта обмена Na+–Li+ уточнять среднее значение линейной скорости пропускания раствора в случаях, когда последняя может неконтролируемым образом измениться. Образцы катионита Li-КУ-2 с микродобавками компонентов Cu2+ или Fe3+ на уровне 0,0046 мг-экв/г (~ 0,5% обменной емкости) готовили в статических условиях. Эксперименты проводили на ионообменной колонке L = 100 cм S = 0,65 см2 со съемным фильтрующим дном при длине слоя катионита l = 45…71 см. Объемная скорость пропускания раствора в пределах одного опыта оставалась постоянной и варьировалась от опыта к опыту в пределах 300…600 мл/ч. В заданные моменты времени прерывали подачу модельного раствора и в течение определенного времени через колонки пропускали раствор того же макросостава с добавкой Cu2+ (или смеси Cu2+ + Ni2+) в концентрации 5…10 мг/л. Этим имитировали «залповый выброс» контролируемого токсичного микрокомпонента с превышением ПДК в 5…10 раз. Отработанный катионит по специально разработанной методике равномерно выгружали порциями по 0,5…2 см слоя катионита в стеклянные бюксы, а затем с помощью различных известных аналитических методик определяли содержание элементов в пробах ионита. По полученным результатам строили кривые распределения концентраций компонентов по слою ионита.
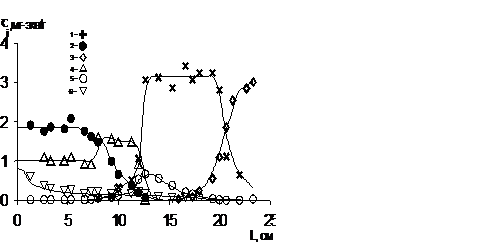
Распределение компонентов в слое катионита КУ-2 – Li+ после пропускания
модельного раствора в течение 36 ч v = 292 см/ч: 1 – Na+, 2 – Ca2+; 3 – Li+, 4 – Mg2+; 5 – K+; 6 – Cu2+ (СCuх50). В промежутке от t 1= 2ч до t2=4 ч раствор содержал
ион-ЗВ (5 мг/л Cu2+)
На рисунке представлены экспериментальные данные по распределению компонентов в слое катионита КУ-2 в Li+-форме после пропускания через него исследуемого модельного раствора в течение 36 ч. Ввод микрокомпонента-«загрязнителя» (Cu2+ в концентрации 6,5 мг/л) соответствует интервалу времени от t1=2 ч до t2=4 ч. Распределение катионов макросостава модельного раствора соответствует обычным закономерностям и известным значениям ионообменных параметров для рассматриваемой системы. Для зоны Cu2+, находящейся преимущественно на фоне ионов Сa2+, наблюдается практически полное удерживание в начальном (лобовом) слое катионита, что для исследованной продолжительности процесса (t = 32 ч) соответствует значению коэффициента разделения ![]() ³ 41,2, или константы равновесия ионного обмена
³ 41,2, или константы равновесия ионного обмена 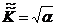 = 6,42. При сравнении этой величины с известными из литературы значениями
= 6,42. При сравнении этой величины с известными из литературы значениями ![]() = 0,5…0,8 [8] очевидно весьма существенное расхождение. Этот эффект может быть обусловлен неизбежным наличием в ионите, наряду с сульфоновыми группами, микропримесей групп с повышенной селективностью к ионам переходных металлов. В этом случае введение в ионит до начала процесса микроколичеств «сильноудерживаемых» ионов, в частности, Cu2+, должно приводить к устранению или ослаблению влияния примесей этих дополнительных функциональных групп. В присутствии микродобавки целевого компонента имеет место заметное смещение его концентрационной зоны вдоль слоя катионита за реальное время эксперимента, а равновесные характеристики ионообменников приближаются к известным из литературы [8], что позволяет использовать эти ионообменники для создания устройств непрерывного контроля динамики загрязнения природных вод.
= 0,5…0,8 [8] очевидно весьма существенное расхождение. Этот эффект может быть обусловлен неизбежным наличием в ионите, наряду с сульфоновыми группами, микропримесей групп с повышенной селективностью к ионам переходных металлов. В этом случае введение в ионит до начала процесса микроколичеств «сильноудерживаемых» ионов, в частности, Cu2+, должно приводить к устранению или ослаблению влияния примесей этих дополнительных функциональных групп. В присутствии микродобавки целевого компонента имеет место заметное смещение его концентрационной зоны вдоль слоя катионита за реальное время эксперимента, а равновесные характеристики ионообменников приближаются к известным из литературы [8], что позволяет использовать эти ионообменники для создания устройств непрерывного контроля динамики загрязнения природных вод.
В настоящее время ведется работа по адаптации этого метода к реальным сточным водам.
Библиографический список
1. , , Трубецков -сорбционный способ контроля состава сточных вод. //Водные ресурсы. 1996. Т.23. № 5.С.575-577
2. , , Горшков обмена щелочных металлов и водорода на ионите КУ-2x8 при малых содержаниях H+// Физ. химии. 1986. Т.60. № 3. С. 715-718.
3. Израэль и контроль состояния природной среды. Л.: Гидрометеоиздат. 19с.
4. О состоянии окружающей природной среды Российской Федерации в 1995 году.- Гос. Доклад Минприроды РФ 1996 г. М., 19с.
5. Патент РФ № 000. Способ сорбционного контроля загрязнения водных объектов /, , - Опубл. 10.11.98, Бюл. № 31.
6. Селективность ионного обмена. // В кн. Ионный обмен. /Под. ред. Я. Маринского. М.: Мир.1968. С. 104-173.
7. Сенявин обмен в технологии и анализе неорганических веществ. М.: Химия.19с.
8. Разделение на ионообменных смолах. М.: Мир.1967.432 с.



