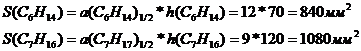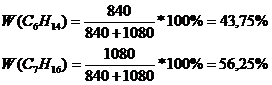Аналитическая химия и физико-химические методы анализа.
1) Написать уравнение реакций, используемые при проведении анализа, и рассчитайте:
а) величину пробы для анализа (г);
б) количество осадителя (мл);
в) величину аналитического множителя (фактор пересчета);
г) содержание определяемого вещества (или элемента) в анализируемом объекте (г или %)
Решение:
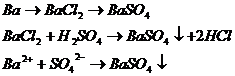
a)
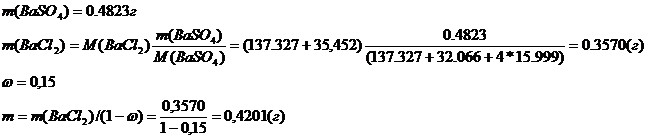
Проба для анализа должна быть 0,4201 г
Б)
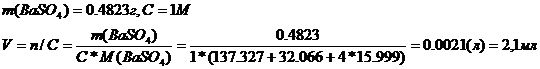
Количество осадителя (1M раствор серной кислоты) 2,1 мл.
В) фактор пересчета
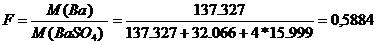
Г) В исходной пробе
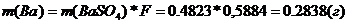
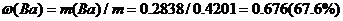
Анализируемый объект | Определеляемое вещество | Схема анализа | Осадитель | Вес весовой формы | Осаждаемая форма осадка |
Технический хлорид бария, содержащий около 15% примесей | Ba | Ba→BaSO4→BaSO4 | 1M раствор серной кислоты | 0,4823 | Кристаллическая |
2)Рассчитать и построить кривую титрования 100 мл раствора указанного вещества. Разбавление раствора при титровании не учитывать. Указать величину скачка и значение рН в точке эквивалентности.
Титруемое вещество | Рабочий раствор | |||
название | формула | концентрация | Кд | |
Молибденовая кислота | Н2Мо2О7 | 0,20 М | 9,5∙10-6 | 0,20 М КОН |
Примечание. Кд –константа диссоциации; её значения взяты из Справочника Лурье. В таблице приведена молярная концентрация эквивалента для всех используемых веществ.
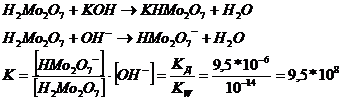
Кислота в реакции одноосновная
В начале титрования концентрации ионов водорода в растворе слабой кислоты вычисляется по формуле
![]()
![]()
![]()
При добавлении щелочи в растворе образуется буферная смесь из неоттитрованной кислоты и ее соли.
До точки эквивалентности (буферный раствор) концентрацию ионов водорода вчисляем по формуле
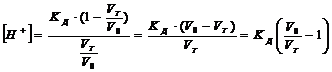
V0 - исходный объем титруемого вещества, мл
Vт - добавленный объем титранта, мл.
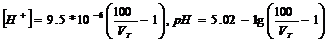
В точке эквивалентности рН раствора определяется концентрацией гидроксид-ионов, полученных при гидролизе соли по аниону А-
А - + Н2О = НА + ОН-
Концентрация гидроксид-ионов без учета изменения объема раствора при титровании
![]() ,
, ![]() .
.
![]()
После точки эквивалентности рН раствора определяется избытком введенного сильного основания и концентрацию ионов водорода вычисляют по формуле ![]()
Сщ - нормальность щелочи, моль экв./л.
![]()
VT | pH |
0 | 2,86 |
5 | 3,74 |
10 | 4,07 |
15 | 4,27 |
20 | 4,42 |
25 | 4,54 |
30 | 4,65 |
35 | 4,75 |
40 | 4,84 |
45 | 4,93 |
50 | 5,02 |
55 | 5,11 |
60 | 5,20 |
65 | 5,29 |
70 | 5,39 |
75 | 5,50 |
80 | 5,62 |
85 | 5,77 |
90 | 5,97 |
95 | 6,30 |
100 | 9,16 |
105 | 12,00 |
110 | 12,30 |
115 | 12,48 |
120 | 12,60 |
125 | 12,70 |
130 | 12,78 |
135 | 12,84 |
140 | 12,90 |
145 | 12,95 |
150 | 13,00 |
155 | 13,04 |
160 | 13,08 |
165 | 13,11 |
170 | 13,15 |
175 | 13,18 |
180 | 13,20 |
185 | 13,23 |
190 | 13,25 |
195 | 13,28 |
200 | 13,30 |
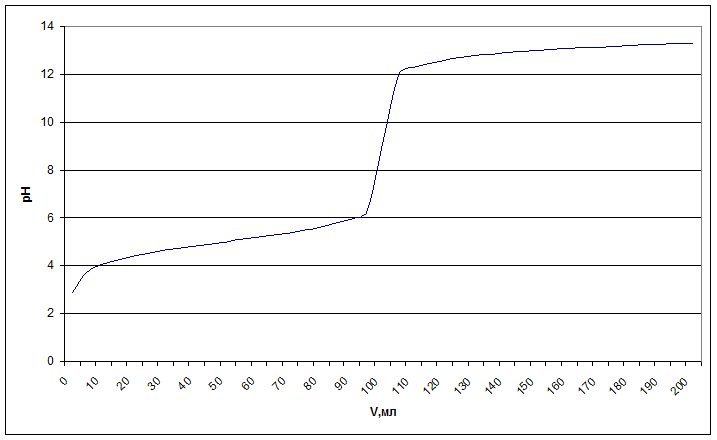
Скачок (0,1%) 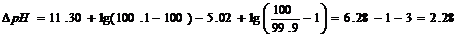
в точке эквивалентности 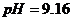
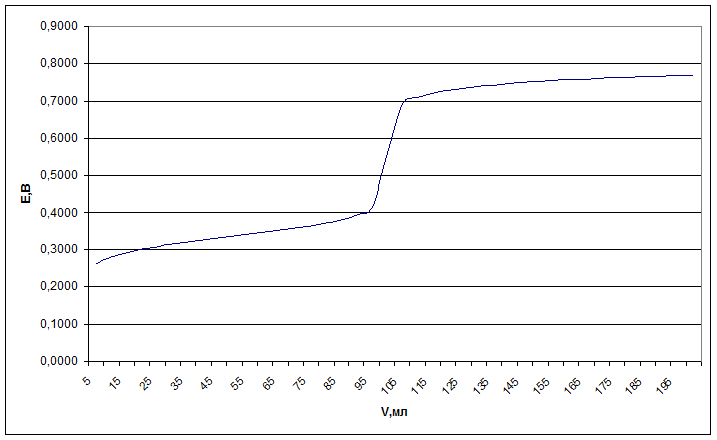
3) Рассчитать и построить кривую титрования 100 мл указанного вещества. Разбавление раствора при титровании в расчетах можно не учитывать. Концентрацию ионов водорода принять равной 1 моль/л (молярная концентрация эквивалента).
Титруемое вещество | Рабочий раствор |
VCl3 0,10 M | FeCl3 0,10M |
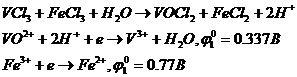
титруемое вещество - восстановитель, то до точки эквивалентности потенциал системы
![]()
![]()
потенциал после точки эквивалентности
![]()
![]()
В точке эквивалентности потенциал рассчитываем по формуле (z1 = z2):
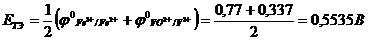
VT | E |
5 | 0,2616 |
10 | 0,2807 |
15 | 0,2926 |
20 | 0,3015 |
25 | 0,3088 |
30 | 0,3153 |
35 | 0,3211 |
40 | 0,3266 |
45 | 0,3319 |
50 | 0,3370 |
55 | 0,3421 |
60 | 0,3474 |
65 | 0,3529 |
70 | 0,3587 |
75 | 0,3652 |
80 | 0,3725 |
85 | 0,3814 |
90 | 0,3933 |
95 | 0,4124 |
100 | 0,5535 |
105 | 0,6932 |
110 | 0,7110 |
115 | 0,7214 |
120 | 0,7288 |
125 | 0,7345 |
130 | 0,7392 |
135 | 0,7431 |
140 | 0,7465 |
145 | 0,7495 |
150 | 0,7522 |
155 | 0,7547 |
160 | 0,7569 |
165 | 0,7590 |
170 | 0,7609 |
175 | 0,7626 |
180 | 0,7643 |
185 | 0,7658 |
190 | 0,7673 |
195 | 0,7687 |
200 | 0,7700 |
4) Пропускание водного раствора с концентрацией вещества 3,75 мг в 100 мл, измеренное в кювете с ℓ=1,00 см при

![]() =480 нм, составляет 54,5%. Рассчитайте удельный коэффициент поглощения этого вещества.
=480 нм, составляет 54,5%. Рассчитайте удельный коэффициент поглощения этого вещества.
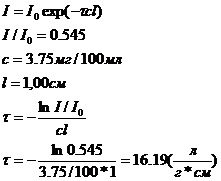
5) Определить концетрацию NH4Cl в растворе (г/л), если при потенциометрическом титровании 20,0 мл раствора NH4Cl раствором Нg2(NO3)2 с молярной концентрацией эквивалента 0,0500 моль/л получили следующие результаты:
V Hg2(NO3)2, мл | 10,0 | 15,0 | 17,0 | 17,5 | 17,9 | 18,0 | 18,1 | 18,5 | 19,0 |
E, мВ | 382 | 411 | 442 | 457 | 498 | 613 | 679 | 700 | 709 |
Конечную точку титрования определить расчетным способом и графически по первой производной.
![]()
V Hg2(NO3)2, мл | 10 | 15 | 17 | 17,5 | 17,9 | 18 | 18,1 | 18,5 | 19 |
E, мВ | 382 | 411 | 442 | 457 | 498 | 613 | 679 | 700 | 709 |
DE/DV | 5,8 | 15,5 | 30 | 102,5 | 1150 | 660 | 52,5 | 18 |
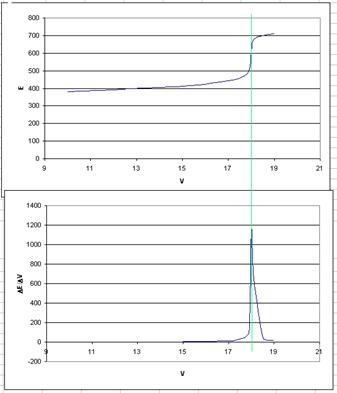
Точка эквивалентности ![]()
Тогда определим концетрацию NH4Cl в растворе (г/л):
![]()
6) Получена хроматографическая кривая с двумя пиками углеводородов – С6Н14, С7Н16. Получены следующие характеристики пиков на хроматограмме:
углевод | h, мм | ℓ, мм | a, мм |
С6Н14 | 70 | 68,9 | 12 |
С7Н16 | 120 | 98,5 | 9 |
Рассчитайте степень разделения RS углеводородов и массовую долю (%) каждого компонента в смеси (методом внутренней нормализации).
Степень разделения рассчитываем по формуле 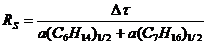 , где
, где ![]() - разность времен удерживания разделяемых компонентов,
- разность времен удерживания разделяемых компонентов, ![]() - полуширина пиков.
- полуширина пиков.
Заменяем время удерживания на расстояние удерживания l, мм
![]() >1, значит, пики разделяются.
>1, значит, пики разделяются.
Массовую долю компонентов находим по методу внутренней нормализации:
![]()
Найдем площадь каждого пика: