Введение
Одной из важных тенденций, проявляющихся на современном этапе в естественных науках, является активное развитие междисциплинарных исследований, в результате чего появляются направления стоящие «на стыке» двух или более традиционных дисциплин. Одна из таких наук – биофизика.
Как отдельная наука биофизика появилась в 50-60-х г-х прошлого века, хотя исследования, которые могут быть названы биофизическими, встречаются еще с 18 века. Это, например, опыты Гальвани, в которых было открыта способность живых объектов к генерации электричества.
Попробуем определить, чем именно занимается биофизика как наука. Одно из наиболее традиционных ее определений формулируется как «биофизика – это наука, изучающая фундаментальные физические закономерности, лежащие в основе биологических процессов». Такое определение, хотя и хорошо коррелирует с названием, дисциплины, является, тем не менее, значительно «зауженным» по сравнению с реальным спектром проблем, изучаемых биофизикой. Так с самого начала своего развития, биофизика была связана не только с физикой, но и с математикой (так математическое моделирование является одним из традиционных инструментов биофизики); с химией (так опирающаяся на химию кинетика является одним из ключевых разделов биофизики); с кибернетикой и т. д.
Таким образом, в качестве предмета изучения биофизики выступает очень широкий спектр проблем, поэтому можно попытаться определить ее как науку о наиболее фундаментальных закономерностях, лежащих в основе функционирования. В настоящее время в биофизике выделяют три наиболее общих направления исследований: биофизика сложных систем, молекулярная биофизика и биофизика клеточных процессов.
Биофизика сложных систем изучает поведение систем, включающих в себя большое количество взаимодействующих компонентов, для исследования которых активно используются методы математического моделирования. К этому разделу биофизики относят такие базовые для биофизики разделы, как термодинамика и кинетика биологических процессов. Молекулярная биофизика изучает физические основы процессов на молекулярном уровне, в частности – пространственную организацию белковых молекул, конформационные переходы в них, ферментативный катализ. Наконец биофизика клеточных процессов изучает физические основы процессов, протекающих на уровне клетки. Это транспортные процессы, процессы биоэлектрогенеза, фотобиологические процессы и др.
Необходимо отметить, что такое разделение достаточно условно, и не всегда может отразить спектр проблем, изучаемых биофизикой.
Кинетика биологических процессов.
Функционирование целостной биологической системы есть результат взаимодействия составляющих ее элементов и отдельных процессов, в ходе которого могут возникать так называемые синергические эффекты, т. е. результат двух совместно протекающих процессов, может качественно отличаться от суммы результатов этих процессов протекающих независимо друг от друга. Следовательно, для изучения такой системы требуется не только знание отдельных реакций в ней протекающих, но и их взаимодействий. Однако, для большинства реальных систем в силу их сложности изучить такое взаимодействие экспериментально практически невозможно, а значит даже зная все протекающие в системе процессы невозможно предсказать ее поведение в целом.
Путем решения этой проблемы является использование методов математического описания систем. Одним из таких путей является кинетический подход, когда поведение системы описывается на основе описания кинетики различных ее компонентов дифференциальными уравнениями. Очевидно, что наиболее адекватно такой подход применим к описанию биохимических реакций, однако существуют примеры его успешного применения и другим областям, например, к популяционной динамике.
Рассмотрим применение кинетического подхода в биофизике подробнее.
Кинетическую систему можно охарактеризовать как совокупность переменных и параметров, выражаемых через измеримые величины, которые в каждый момент времени принимают определенные числовые значения. Параметры — это величины, которые поддерживаются неизменными в течение времени наблюдения над системой; переменные — величины, которые изменяются с течением времени. В разных биологических системах в качестве переменных могут выступать различные измеряемые величины: в биохимии — это концентрации промежуточных веществ, в микробиологии — число микроорганизмов или их суммарная биомасса, в экологии — численность вида, в биофизике мембранных процессов — мембранные потенциалы и т. д. Параметрами могут служить температура, влажность, рН, электрическая проводимость мембраны.
Если допустить, что в системе имеется n различных компонентов, которые для определенности будут считаться химическими соединениями, претерпевающими метаболические превращения, то каждое i-е соединение из общего, их числа n характеризуется значением концентрации ci (i=1, 2, ..., n), которое может изменяться со временем ci = ci(t) в результате взаимодействия i-ro соединения с любым из остальных веществ. Такого предположения достаточно для написания общей математической модели, представляющей собой систему из n дифференциальных уравнений:
d c1 / dt = f 1(c1, c2, …., cN, t)
……………………………….
d cN / dt = f N(c1, c2, …, cN, t)
где с – концентрации компонент системы, f – функции, отражающие зависимость скорости изменения каждой из с от других концентраций и времени. В общем виде, такие функции могут быть нелинейными, их вид зависит от конкретных реакций протекающих в системе.
Если в системе уравнений время в явной форме отсутствует, т. е.:
d c1 / dt = f 1(c1, c2, …., cN)
……………………………….
d cN / dt = f N(c1, c2, …, cN)
То такая система называется автономной (или стационарной), именно такие системы обычно используются в кинетике, за исключением ситуаций, когда на систему действует некая зависящая от времени по отношению к системе внешняя сила. Отметим также, что такая система уравнений является точечной, т. е. значения концентраций являются функцией времени, но не их координаты в пространстве.
Учтем теперь тот факт, что для живых систем характерно явление гомеостаза, т. е. поддержание их показателей (переменных модели) на некотором постоянном уровне. Так при протекании многих цепочек биохимических реакций концентрации промежуточных метаболитов остаются приблизительно постоянными. Например, концентрации продуктов световой и темновой стадии фотосинтеза после длительного освещения постоянной интенсивности и при сохранении неизменными остальных параметров.
Такое постоянство будет соблюдаться в том случае, если скорости изменения всех метаболитов будут равны 0, т. е.:
f 1(c1s, c2s, …., cNs) = 0
……………………………….
f N(c1s, c2s, …, cNs) = 0
В этом случае у нас имеется уже система алгебраических уравнений, где значения концентраций c1s, c2s, …, cNs представляют собой стационарные концентрации метаболитов, т. е. концентрации не меняющиеся со временем. А само такое решение называется стационарным решением системы дифференциальных уравнений.
Учтем, что в реальной системе всегда присутствуют некоторые флуктуации, т. е. случайные отклонения величин показателей (переменных) от текущего значения. В связи с этим весьма актуальным является вопрос об устойчивости стационарных состояний.
Так если после отклонения показателей системы от стационарных значений, происходит ее возвращение в исходное состояние, то такое состояние является устойчивым. И наоборот, если такого возвращения не происходит – это состояние неустойчивое.
Такое свойство удобно проиллюстрировать на примере шарика в профиле потенциальной энергии. В том случае, когда шарик находиться в максимуме потенциальной энергии (РИС), его равновесие является неустойчивым – даже при малом отклоняющем воздействии система необратимо выходит из стационарного состояния. Если шарик находиться в минимуме энергии (РИС) ситуация иная – при любом отклонении, он рано или поздно возвращается в исходное стационарное состояние. Отметим, то в последнем случае речь идет об абсолютной устойчивости, не зависящей от силы отклоняющего воздействия. Однако, этот случай не возможен в реальной системе. Там устойчивость всегда имеет относительный характер – система сохраняет свое стационарное состояние лишь до тех пор, пока воздействие не превысит определенный порог. Это можно иллюстрировать поведением шарика в локальном минимуме потенциальной энергии (РИС).
Знание стационарных состояний системы, а также их устойчивости или неустойчивости может быть очень информативным для качественного анализа ее поведения. Однако прежде чем рассмотреть этот вопрос подробнее рассмотрим – как вообще можно исследовать поведение системы, моделируемой дифференциальными уравнениями?
Аналитическое решение
Наиболее строгим с математической точки зрения, является нахождение зависимости всех ci(t) в явной форме, т. е. аналитическое решение системы уравнений.
В ряде случаев – такое решение может быть достаточно простым, особенно если процесс описывается системой линейных дифференциальных уравнений или отдельным уравнением. Отметим, что линейное дифференциальное уравнение это такое уравнение правая часть которых представляет собой линейную функцию зависимой переменной (переменных).
В качестве простейшего примера такого описания можно привести рост популяции бактерий в не лимитированных условиях.
![]() , где С-концентрация бактерий (или их количество), k - константа скорости, отражающая их деление. Такое уравнение легко решается методом разделения переменных, в результате чего получаем решение вида:
, где С-концентрация бактерий (или их количество), k - константа скорости, отражающая их деление. Такое уравнение легко решается методом разделения переменных, в результате чего получаем решение вида: ![]() , где С0 – начальная концентрация бактерий (если нужно - привести решение).
, где С0 – начальная концентрация бактерий (если нужно - привести решение).
В качестве более сложного примера можно привести реакцию превращения субстрата (S) в продукт (P), в условиях ограниченного количества субстрата 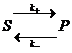 :
:
![]() , где k+ - константа скорости прямой реакции, а k- - константа скорости обратной. Если учесть, что S+P=const=S0 – начальная концентрация субстрата, то можно записать уравнение как
, где k+ - константа скорости прямой реакции, а k- - константа скорости обратной. Если учесть, что S+P=const=S0 – начальная концентрация субстрата, то можно записать уравнение как ![]() . Решение этого уравнения (методом разделения переменных) имеет вид:
. Решение этого уравнения (методом разделения переменных) имеет вид: ![]()
Однако если для простых случаев, подобных приведенным, поиск аналитического решения является несложной задачей, то уже для системы включающей две последовательные биохимические реакции аналитическое ее решение становиться достаточно сложной задачей.
Существуют некоторые приемы, облегчающие ее решение, один из которых – разделение переменных на быстрые и медленные. Так если мы имеем цепочку превращений 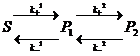 , где k1>>k2, то стационарное распределение в первой реакции будет достигаться намного быстрее, чем во второй.
, где k1>>k2, то стационарное распределение в первой реакции будет достигаться намного быстрее, чем во второй.
Поясним это: учитывая, что k1>>k2, можно выбрать такой интервал времени t – t1<t<t2 (t = 1/(k++k-) – характерное время реакции), на котором можно пренебречь изменениями, связанными с k2. В этом случае мы возвращаемся к предыдущему варианту: 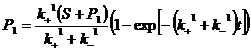 , причем так как t>t1 (
, причем так как t>t1 (![]() ), то соотношение между S и Р1 становиться приблизительно постоянным (
), то соотношение между S и Р1 становиться приблизительно постоянным (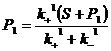 ;
;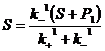 ). Очевидно, что это соотношение не должно меняться и при увеличении t. Однако у нас имеется и вторая реакция – k2 – в ходе которой Р1 превращается в Р2, т. е. субстрат должен постепенно трансформироваться в конечный продукт, а общее количество S+Р1 должно уменьшаться.
). Очевидно, что это соотношение не должно меняться и при увеличении t. Однако у нас имеется и вторая реакция – k2 – в ходе которой Р1 превращается в Р2, т. е. субстрат должен постепенно трансформироваться в конечный продукт, а общее количество S+Р1 должно уменьшаться.
Таким образом S+Р1 у нас меняется, а доля S и Р1 в этой сумме – нет. Отсюда, для описания медленной реакции мы можем ввести новую переменную Х= S+Р1 и записать уравнение в виде: 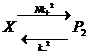 , где N – это доля Х способных к превращению в Р2 , т. е. NХ=Р1, отсюда
, где N – это доля Х способных к превращению в Р2 , т. е. NХ=Р1, отсюда 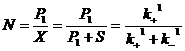 .
.
Реакция 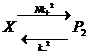 описывается уже не системой, а отдельным дифференциальным уравнением, решение которого мы рассматривали ранее. Если раскрыть в нем N, то получим:
описывается уже не системой, а отдельным дифференциальным уравнением, решение которого мы рассматривали ранее. Если раскрыть в нем N, то получим:
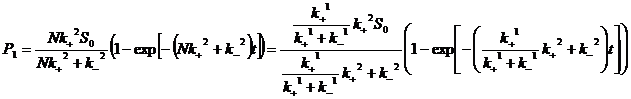
Таким образом, разделение реакций на быстрые и медленные может значительно упростить поиск аналитического решения системы.
Полученный результат, в частности, показывает, что для цепи последовательных реакций динамика выхода ее конечного продукта, будет определяться динамикой самой медленной реакции в цепи, так как остальные реакции достигнут стационарных значений раньше. Этот вывод можно сравнить с широко применяемым в кинетике правилом «узкого места» - в цепи химических реакций общую скорость процесса определяет самая медленная из них.
В то же время, даже применяя описанные упрощения, найти аналитическое решение системы уравнений в некоторых случаях представляется невозможным. В таких ситуациях могут быть применены еще два подхода - качественное описание системы уравнений и ее численное решение.
Качественное исследование кинетических систем
Методы качественного исследования опираются на допущение, что для того чтобы понять принципиальные особенности функционирования системы не обязательно знать ее поведение в каждый момент времени, а достаточно найти стационарный состояния системы, оценить их устойчивость и определить каким путем происходит приближение системы к такому состоянию или ее удаление от него.
В этом случае, на первом этапе исследования уже описанным методом ищутся стационарные состояния исследуемой системы.
На следующем этапе определяется устойчивость найденных состояний, для чего можно использовать критерий устойчивости по Ляпунову. Так пусть у нас есть уравнение ![]() , стационарное решение которого x=xst. По определению
, стационарное решение которого x=xst. По определению ![]() . Добавим к xst некую малую величину ξ, в этом случае:
. Добавим к xst некую малую величину ξ, в этом случае: 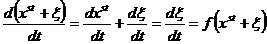 , полученное выражение можно разложить в ряд Тэйлора в точке x:
, полученное выражение можно разложить в ряд Тэйлора в точке x: ![]() , если ξ достаточно мало, то можно пренебречь всеми слагаемыми с порядком ξ выше 1, т. е. получаем
, если ξ достаточно мало, то можно пренебречь всеми слагаемыми с порядком ξ выше 1, т. е. получаем 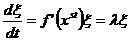 .
.
Решение такого уравнения имеет вид 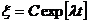 , где С – константа, отражающая отклонение в начальный момент времени. Очевидно, что если λ>0, то такое состояние будет неустойчивым – малое отклонение будет возрастать с течением времени, если λ<0 то устойчивым – система будет возвращаться в исходное состояние. Если λ=0 – то критерий Ляпунова в линейном приближении не может дать ответа об устойчивости системы.
, где С – константа, отражающая отклонение в начальный момент времени. Очевидно, что если λ>0, то такое состояние будет неустойчивым – малое отклонение будет возрастать с течением времени, если λ<0 то устойчивым – система будет возвращаться в исходное состояние. Если λ=0 – то критерий Ляпунова в линейном приближении не может дать ответа об устойчивости системы.
 Рассмотрим в качестве примера уравнение, описывающее динамику количества клеток в проточном культиваторе:
Рассмотрим в качестве примера уравнение, описывающее динамику количества клеток в проточном культиваторе:
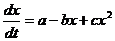 , где x – концентрация клеток, а – скорость их притока, b и c – коэффициенты их гибели и размножения, соответственно. При этом учтем, что a, b, c > 0, также примем, что c = 1. В этом случае система будет иметь два стационарных состояния:
, где x – концентрация клеток, а – скорость их притока, b и c – коэффициенты их гибели и размножения, соответственно. При этом учтем, что a, b, c > 0, также примем, что c = 1. В этом случае система будет иметь два стационарных состояния:
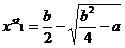 ,
, ![]()
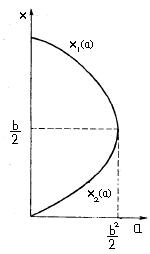
В то же время при b2/4 < a, стационарное состояние не может быть достигнуто системой, так xst1 и xst2 – не являются действительными числами. При b2/4 = a – система имеет одно стационарное состояние, а при b2/4 > a – два. Все это можно представить в виде рисунка (РИС).
Отметим, что такое явление – появление в системе нескольких стационарных состояний при изменении ее параметров называется бифуркацией, а значение параметра b = (4а)0.5 при котором происходит бифуркация – бифуркационное.
Важно отметить, что ветви x1 и x2 различаются по своей устойчивости, так
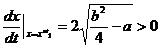 , а
, а ![]()
Т. е. ветвь X1 – неустойчива, а X2 – устойчива. Если порядок дифференциального уравнения равен трем – то система может иметь 3 стационарных состояния и т. д.
Данный анализ был проведен для отдельного дифференциального уравнения, однако похожие принципы могут быть использованы и для системы дифуров. Но там картина может быть значительно сложнее.
Рассмотрим в качестве примера систему из 2-х уравнений:
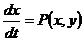
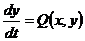
Результат качественного анализа такой системы удобно представлять на фазовой плоскости, т. е. на плоскости где по оси абсцисс отложены значений x, а по оси ординат – y. Каждое состояние системы будет соответствовать на такой плоскости точке с определенными координатами. При этом точка М(x, y), соответствующая текущему состоянию системы называется изображающей точкой, траектория по которой она движется – фазовой траекторией, а совокупность фазовых траекторий – фазовым портретом системы. По сути, для системы дифференциальных уравнений – построить фазовый портрет системы и означает найти ее качественное решение.
Общие этапы нахождения фазового портрета системы близки к этапам анализа отдельного дифференциального уравнения. Так вначале, путем приравнивания левой части к 0 и решения системы алгебраических уравнений, находятся так называемые особые точки системы, т. е. точки на фазовой плоскости, соответствующие стационарным состояниям системы. После этого определяется их устойчивость. Так если координаты особой точки данной ранее системы уравнений равняются xst и yst, то зададим малые смещения x и y из этой точки: ξ = xst – x и η = yst – y, причем | ξ / xst|<<1 и | η / yst| << 1. Если подставить в исходную систему уравнений вместо x и y – xst + ξ и yst + η, после чего разложить ее в ряд Тэйлора, отбросить нелинейные члены и принять P(xst, yst) = Q(xst, yst) = 0, то мы получим систему линенейных дифференциальных уравнений:
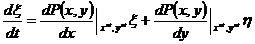
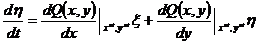
Полученная система называется линеаризованной. Обозначим постоянные коэффициенты как a11, a12, a21, a22 – и будем искать решение этой системы.
Примем, что аналитический общий вид решения будет ![]() , а
, а 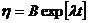 , подставив это решение в предыдущую систему уравнений и сократив экспоненты, получим:
, подставив это решение в предыдущую систему уравнений и сократив экспоненты, получим:
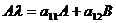
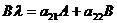
Или2
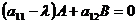
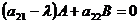
Получаем алгебраическую систему, где А и В – неизвестны. Такая система может иметь ненулевое решение только в том случае, если главный определитель будет равен 0:
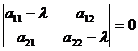
или – раскрыв определитель – ![]()
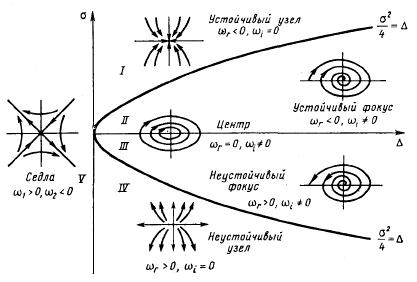
Отсюда:
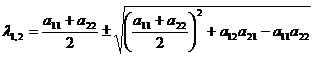
На основании этого мы можем записать уравнения для ξ и η:
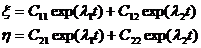
В зависимости от значений λ1 и λ2 особая точка системы будет различной. Так если эти числа действительные возможны следующие варианты:
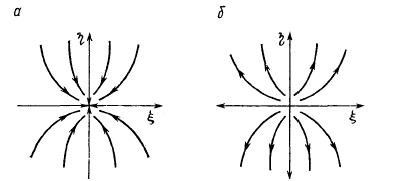
1. λ1 > 0, λ1 > 0 – в этом особая точка будет представлять собой неустойчивый узел (РИС).
2. λ1 < 0, λ2 < 0 – в этом особая точка будет представлять собой устойчивый узел (РИС).
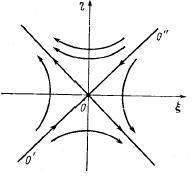
3. λ1 < 0, λ2 > 0 или наоборот – в этом особая точка будет неустойчивой – седло, однако в этом случае будут как траектории входящие в эту точку так и выходящие из нее (РИС)
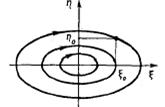
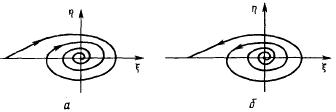
В случае если λ – комплексно сопряженные то все зависит от действительной части. Так если она отрицательна – то в фазовая траектория двигаясь вокруг особой точки приближается к ней – устойчивый фокус (РИС), если положительно – то фазовая траектория движется от особой точки - неустойчивый фокус (РИС), наконец – если действительная часть равна 0, фазовая траектория движется по окружности – центр (РИС).
Как можно видеть и в случае системы из 2-х уравнений особенности стационарного состояния зависят от параметров уравнений. Если ввести параметры σ = — (a11 + a12) и Δ = —a12a21 + a11a22 то можно получить картину зависимости «поведения» стационарного состояния от этих параметров (РИС). 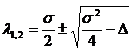
Из такой диаграммы устойчивости особых точек видно, в частности, что и в случае системы из нескольких дифференциальных уравнений возможны параметры, изменение которых приводит к бифуркационным явлениям.
Таким образом, мы видим, что по-крайней мере для систем из двух уравнений произвольного вида можно использовать методы их качественного описание. Такие методы возможны и для более сложных систем уравнений, однако в таком случае имеет место уже не фазовая плоскость, а фазовое пространство, и анализ качественного поведения системы более сложен.
В качестве примера проведем качественный анализ модели Лотке-Волтерра – «хищник-жертва». Ее можно задать системой уравнений
![]()
![]()
Здесь r – скорость размножения, причем для хищников (у) она зависит не только от числа особей данного вида, но и от количества пищи – жертв, d – коэффициент смертности (он пропорционален количеству особей), a - константа отражающая вероятность поедания хищником жертвы при встрече, g=r1-d1 – вводиться для упрощения системы и, по сути, отражает скорость прироста количества жертв.
Найдем стационарные значения х и у:
![]() ,
, 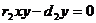 -
-![]() ,
, 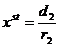 и
и ![]() ,
, ![]() , второй вариант нам не интересен, так как соответствует полному отсутствию и хищников, и жертв.
, второй вариант нам не интересен, так как соответствует полному отсутствию и хищников, и жертв.
Найдем а:
![]() ,
, 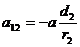 ,
, ![]() ,
, 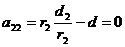
Отсюда:
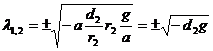
Такая ситуация соответствует нейтральной точке типа центр, которая не является не устойчивой и неустойчивой (РИС). Если нарисовать зависимость количества хищников и жертв от времени, то такая ситуация будет соответствовать колебаниям с амплитудой равной начальному отклонению (РИС).
Следует отметить, что кроме особых точек, в сложных системах могут свойством устойчивости/неустойчивости могут обладать и траектории. В качестве примера можно привести устойчивый и неустойчивый предельный циклы (РИС). Как и центр, такая траектория отражает колебательный процесс, однако, например, в случае устойчивого предельного цикла параметры этого колебательного процесса (частота, амплитуда) зависят не от параметров внешнего воздействия, его индуцирующего, а от свойств самой системы (РИС).
Исследование сложных систем численными методами
Существует еще один подход к описанию сложных кинетических систем, который в последнее время активно развивается, благодаря совершенствованию вычислительной техники, это численное моделирование.
Его принцип можно описать на примере одного из простых методов численного моделирования – методе Рунге-Кутта 1-го порядка или методе Эйлера. Опишем его.
Допустим нам известно значение функции y=f(t0), для того чтобы найти значение у=f(t0+Δt) мы можем разложить ее в ряд Тэйлора:
![]()
Если Δt достаточно мало, то в полученном выражении можно пренебречь членами со степенью выше 1, т. е.:
![]()
Таким образом, зная y(t0) и вид первую производную f(t) по времени, мы можем найти значение y(t=t0+Δt), если Δt достаточно мало. Однако ничего не мешает повторить эту процедур вновь, используя вместо y(t0) - y(t0+Δt). Отсюда повторяя подобную операцию, мы можем получить – численно - зависимость y от t. Причем подобная операция применима и для системы уравнений.
Преимуществом численного метода является его универсальность – он применим практически для всех моделей. Недостатками – ресурсоемкость и невозможность получить общую картину поведения системы: численные решения всегда реализуются лишь для определенных значений параметров.
Системы с распределенными в пространстве параметрами
Таким образом, мы рассмотрели некоторые особенности исследования так называемых точечных систем, т. е. систем в которых процессы рассматривались как бы протекающими в одной точке, а пространственный фактор не учитывался. Однако реальная ситуация бывает зачастую более сложной – и фактор движения компонент системы в пространстве (для химических реагентов – в частности, диффузия) может играть важную роль в функционировании системы. Системы, которые учитывают пространственный фактор, называются системами с распределенными в пространстве параметрами. Для одномерной системы такого типа, описывающие ее уравнения будут выглядеть как:
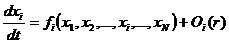
где i = 1, …, N, Q(r) – функция определяющая зависимость переменной (например – концентрации) от пространственной координаты. Полное решение такой системы будет выглядеть как xi = xi (t, r). В том случае, когда пространственное распределение задается диффузией, уравнения для х будут выглядеть:
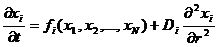
Для анализа таких уравнений необходимо знать начальные условия - функцию x(r) при t = 0, и возможно – граничные условия. Такая система с распределенными параметрами может быть сведена к точечной при выполнении одного из 3-х условий (1) D = 0, что во многих случаях не имеет физического смысла, (2) D очень велико по сравнению со скоростями реакций – в этом случае равномерно частицы перемешиваются по всему реакционному объему и (3) все внешние и начальные условия абсолютно идентичны. Однако такие условия соблюдаются далеко не всегда и во многих случаях при исследовании биосистем приходится анализировать системы уравнений с распределенными в пространстве параметрами.
Такой анализ сопряжен со значительными трудностями, особенно – в общем случае, когда f(x1, x2, …, xN) – имеют нелинейный характер. Поэтому мы рассмотрим лишь некоторые особенности анализа таких систем. Прежде всего, нужно выделить некоторые черты систем с пространственным распределением параметров имеющих биологическую природу. Так, отметим, что биологические распределенные системы относятся к активным распределенным системам. Последние характеризуются рядом свойств. В них существуют распределенные в пространстве источники энергии или богатые энергией вещества; каждый элементарный объем является открытой системой, в которой диссипирует часть энергии, поступающей из распределенного источника; наконец, связь между соседними элементарными объемами осуществляется за счет процессов переноса. Очевидно, целый ряд разнообразных биологических объектов, таких как мембраны, ткани, сообщества живых организмов относятся к классу активных распределенных систем.
В настоящее время существует ряд моделей, любо отражающих реальные распределенные системы, либо теоретических, но позволяющих качественно изучить свойства таких систем. Среди первых можно, например, отметить модель распространения нервного импульса по нервному волокну, среди вторых – так называемый брюсселятор.
Брюсселятор это такая система, в которой протекает следующая совокпность химических реакций:
Его точечная модель выглядит следующим образом:
A → x
2x + y → 3x
B + x → y + D
x → E
Учитывая диффузию метаболитов в одномерном пространстве, система уравнений для брюсселятора:
![]()
![]()
Теоретический анализ такой системы показывает, что в такой системе могут возникать так называемые диссипативные структуры, т. е. неравномерное периодическое распределение концентрации реагентов вдоль брюсселятора (РИС - примерно). Кроме неподвижных диссипативных структур – типа «стоячей волны», в определенных условиях могут возникать структуры типа «бегущей волны» (РИС).
Биологические триггеры
Рассмотрим теперь один частных из более частных вариантов поведения сложной системы имеющий, тем не менее, большое значение для биологических систем.
 Важной особенностью биологических систем является их способность переключаться из одного режима функционирования в другой, что соответствует нескольким устойчивым стационарным состояниям системы. На фазовой плоскости такая система обладает двумя (и более) устойчивыми особыми точками. Области влияния устойчивых особых точек разделяются сепаратрисами, которые обычно проходят через неустойчивую особую точку типа седло (РИС).
Важной особенностью биологических систем является их способность переключаться из одного режима функционирования в другой, что соответствует нескольким устойчивым стационарным состояниям системы. На фазовой плоскости такая система обладает двумя (и более) устойчивыми особыми точками. Области влияния устойчивых особых точек разделяются сепаратрисами, которые обычно проходят через неустойчивую особую точку типа седло (РИС).
Система, обладающая двумя или несколькими устойчивыми стационарными состояниями, между которыми возможны переходы, называется триггерной.
В триггерных системах стационарные значения переменных зависят от начальных условий. Если система функционирует в одном из своих устойчивых режимов, малыми отклонениями ее нельзя вывести из этого режима. Однако в реальных биологических системах существуют способы переключения устойчивых стационарных состояний. Допустим, что система функционирует в устойчивом режиме а и ее необходимо перевести в другой устойчивый режим с. Это можно сделать двумя способами.
За счет внешнего воздействия можно так изменить значения переменных х и у, например, резко увеличив х, что это переведет систему в некую точку с (пояснить на РИС), находящуюся по правую сторону сепаратрисы седла в области притяжения устойчивого узла с: После этого система уже сама по фазовой траектории перейдет в точку с и окажется в требуемом режиме.
Это так называемый силовой способ переключения триггера, он называется также специфическим. В случае химической реакции для такого переключения в систему необходимо добавить некоторое количество определенного химического вещества (в данном случае вещества х).
Другим, более тонким, является способ параметрического неспецифического переключения. Здесь непосредственному воздействию подвергаются не переменные, а параметры системы, что может быть достигнуто разными способами, например изменением температуры, рН или скорости поступления субстрата. Сущность процесса параметрического переключения состоит в использовании характерной зависимости фазового портрета от некоторого управляющего параметра системы (пояснить на РИС).
При изменении фазового портрета сами координаты особой точки с, конечно, также несколько изменятся, поскольку они зависят от параметров системы. При возвращении к прежним значениям управляющего параметра исходный фазовый портрет системы восстановится, но она уже будет работать в требуемом режиме с.
Системы, обладающие триггерными свойствами очень широко распространены в природе. В качестве примеров можно привести системы, включающие в себя два гена, у которых экспрессия каждого подавляется продуктом другого (РИС?); переходы между открыты и закрытым состоянием ионного канала (РИС?); переходы между базовым и адаптированным состояниями при действии стресс-факторов (РИС?) и др. Поэтому исследование средствами кинетического моделирования является весьма важной задачей.
Кинетика ферментативных процессов
Коснемся еще одного частного вопроса биологической кинетики, который, тем не менее, имеет очень большое значение – кинетики ферментативных процессов.
Рассмотрим простейшую схему ферментативной реакции:
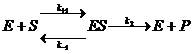
Здесь S – субстрат, Р – продукт, Е – фермент, ES – фермент-субстратный комплекс.

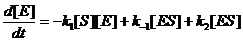
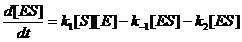
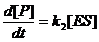
Учтем, что [E]+[ES]=const=[E0], [S]+[P]=const=[S0]; d[E]/dt=d[ES]/dt и перейдем к системе из 2-х уравнений:
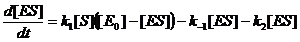
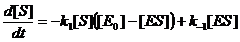
Введем безразмерные величины:
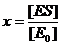 ,
, ![]() ,
, 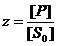 ,
, ![]() ,
, 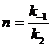 ,
, ![]()
Перейдем к безразмерной форме уравнения:
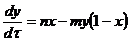
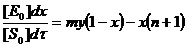
Учтем, что [E0]/[S0] = 10-6 М / 10-2 М =10-4, а обратная величина [S0]/[E0] = 104, перепишем полученные уравнения:
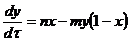
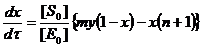
Можно видеть, что x меняется в 10000 раз быстрее, чем y – т. е. его можно рассматривать как быструю переменную. Следовательно, учитывая изложенное ранее мы можем перейти от дифференциального равнения для х, к алгебраическому:
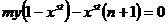
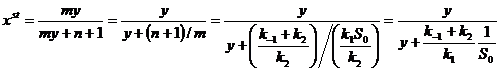
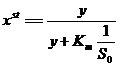
где 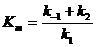 - константа Михаэлиса.
- константа Михаэлиса.
Найдем стационарную концентрацию [ES]:
![]()
Учитывая, что 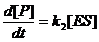 , мы можем найти скорость реакции:
, мы можем найти скорость реакции:
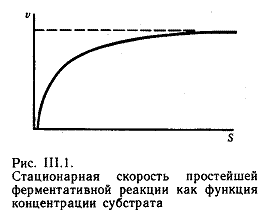
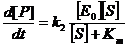
Полученное уравнение называется уравнением Михаэлиса и позволяет найти связь между скоростью реакции и концентрацией ее субстрата (РИС).
Из приведенной зависимости, в частности, видно, что зависимость скорости реакции от концентрации субстрата имеет насыщение, которое связыванием практически всего фермент в фермент-субстратный комплекс. Km – соответствует такой концентрации субстрата, при которой связана половина молекул фермента.
Отсюда можно сделать вывод, то Km отражает сродство фермента к субстрату: чем меньше Km, тем более низкая концентрация субстрата требуется для связывания фермента.
Величина Km сильно варьирует (от 1 до 10-8 М). Например, для лактатдегидрогеназы пировинограднои кислоты 3.5*10-5 М, для инвертазы сахарозы 2.8*10-2 M, для мальтазы-мальтозы 2.l*10-1 M.
Уравнение Михаэлиса представляет собой один из простейших случаев ферментативной кинетики. Возможны и более сложные варианты.
Так, например, фермент может содержать не один, а более активных центров, лишь при заполнении которых, будет происходить образование продукта, т. е. реакция будет протекать по типу:
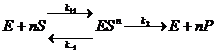
В это случае ее скорость будет описываться формулой:
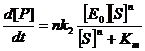
Где n>1. Характерной чертой такой зависимости является ее сигоидный характер (РИС)
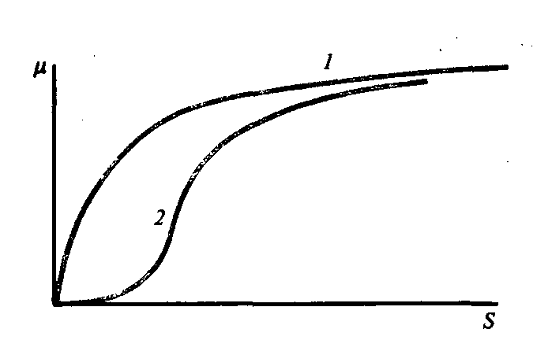
На основе уравнения Михаэлиса можно описать и другие ситуации, связанные с кинетикой биохимических реакций.
В частности можно описать влияние ингибиторов, которые при связывании с ферментом инактивируют его:
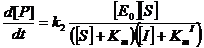
Здесь [I] – концентрация ингибитора, KmI – аналог константы Михаэлиса для связывания фермента и ингибитора. Такая формула применима для описания неконкурентного ингибирования
В целом, кинетика ферментативных процессов является важной частью кинетики биологических процессов в целом, что в первую очередь связано с важностью ферментативных процессов в функционировании живых систем.
Следует отметить, что этот раздел биофизики тесно сближается с биохимией, так как с одной стороны с одной стороны предмет исследования лежит все же в области биохимии, а с другой – используемые при этом теоретические методы приближают раздел к биофизике.
В целом, кинетика биологических процессов является одним из основных и наиболее общих разделов биофизики, дающим в частности подходы применимые к биологическим процессам на разных уровнях организации живой материи.



