![]()
![]() 3
3![]() [
[![]() ] +4
] +4![]()
![]() ]3 + 12 KCl.
]3 + 12 KCl.
4. ![]() Нейтрализация – 2HCl + CaO +
Нейтрализация – 2HCl + CaO +![]() O Ca
O Ca ![]() + 2
+ 2![]() O
O
51. Физико-химические методы очистки: флотация, коагуляция, адсорбция, ионный обмен, обратный осмос, ультрафильтрация, электрохимические методы. Сущность и особенности каждого метода.
Флотация - процесс молекулярного прилипания частиц флотируемого
материала к поверхности раздела двух фаз, обычно газа (чаще воздуха; и жидкости, обусловленный избытком свободной энергии поверхностных пограничных слоев, а также поверхностными явлениями смачивания.
Процесс очистки производственных сточных вод, содержащих ПАВ, нефть, нефтепродукты, масла, волокнистые материалы, методом флотации заключается в образовании комплексов "частицы-пузырьки", всплывании этих комплексов и удалении образовавшегося пенного слоя с поверхности
обрабатываемой жидкости Прилипание частицы, находящейся в ней, к поверхности газового пузырька возможно только тогда, когда наблюдается
несмачивание или плохое смачивание частицы жидкостью. Внешним проявлением способности жидкости к смачиванию является величина поверхностного натяжения ее по границе с газовой фазой, а также разность полярностей на границе жидкой и твердой фаз. Процесс флотации идет
- эффективно при поверхностном натяжении воды не более (60-65)-10-3 Н/м. Большое значение при флотации имеют размер, количество и равномерность распределения воздушных пузырьков в сточной воде. Оптимальные размеры
воздушных пузырьков 15-30 мкм, а максимальные мкм.
Адсорбционный метод - один из наиболее доступных в эффективных методов глубокой очистки от растворенных органических веществ сточных вод предприятий целлюлозно-бумажной, химической, нефтехимической, кстильной и других отраслей промышленности.
Сорбция - это процесс поглощения вещества из окружающей среды твердым телом или жидкостью. Преимуществами этого метода являются возможность адсорбции веществ многокомпонентных смесей и высокая Эффективность очистки, особенно слабо концентрированных сточных вод. Сорбциониые методы весьма эффективны для извлечения из сточных вод ценных растворенных веществ с их последующей утилизацией и использования очищенных сточных вод в системе оборотного водоснабжения промышленных предприятий.
В качестве сорбентов применяют различные искусственные и природные пористые материалы: золу, опилки, торф, коксовую мелочь, силикагели, активные глины и др. Эффективными сорбентами являются активированные угли различных марок. Активность сорбента характеризуется количеством поглощаемого вещества на единицу объема или массы сорбента (кг/м3, кг/кг).
Обратный осмос (гиперфильтрация) - процесс молекулярного разделения растворов путем их фильтрования под давлением через полупроницаемые мембраны, задерживающие полностью или частично Молекулы либо ионы растворенного вещества. При приложении давления выше осмотического (равновесного) осуществляется перенос растворителя в обратном направлении (от раствора к чистому растворителю через мембрану) и обеспечивается достаточная селективность очистки. Необходимое давление, превышающее осмотическое давление растворенного вещества в растворе, составляет при концентрации солей % 0,1-1 МПа и при концентрации солей 20-3 0 г/л 5-10 МПа. Ультрафильтраця - мембранный процесс разделения растворов осмотическое давление которых мало. Этот метод используется при отделении сравнительно высокомолекулярных веществ, взвешенных - коллоидов. Ультрафильтрация по сравнению с обратным осмосом высокопроизводительный процесс, так как высокая проницаемость мембран достигается при давлении 0,2-1 МПа. ^
Коагуляция – способность дисперсных систем выделяться на растворе под влиянием внешних воздействий. Вещества, обуславливающие коагуляцию называются коагулянтами. Центробежное отделение твердой фазы под действием центробежных и центростремительных сил происходит таких аппаратах, как центрифуги и гидроциклоны.
Применяется для очистки стоков от мелкодисперсных и коллоидных примесей.
Al+3 +H2O = Al(OH)2+ + H+
Al(OH)2+ + H2O = Al(OH)2+2 + H+
Al(OH)2+ + H2O = Al(OH)+3 + H+
Коагуляция. Для очистки стоков от мелкодисперсных и коллоид примесей используют их удаление с помощью коагулянтов и флокулянтов. Коагуляцию осуществляют непосредственно после удаления крупных взвесей.
При очистке питьевых и сточных вод в качестве коагулянтов используют соли алюминия, соли железа и их смеси в разных пропорциях. Реже применяют соли магния, цинка и титана. На станциях в специальных баках, защищенных от коррозии, готовят рабочие растворы коагулянтов определенной концентрации и дозируют их в обрабатываемую воду.
Ионообменный метод - процесс обмена ионами, находящимися в
растворе, и ионами, присутствующими на поверхности твердой фазы -
ионита.
Очистка производственных сточных вод методом ионного обмена
позволяет извлекать и утилизировать ценные примеси (соединения мышьяка,
(фосфора, а также хром, цинк, свинец, медь, ртуть и другие металлы), ПАВ и
радиоактивные вещества, очищать сточную воду до предельно допустимых
концентраций с последующим ее использованием в технологических
процессах или в системах оборотного водоснабжения.
По знаку заряда обменивающихся ионов иониты делят на катеониты и аниониты, проявляющие соответственно кислотные и основные свойства. Иониты подразделяются на природные и искусственные или синтетические. Практическое значение имеют неорганические природные и искусственные (алюмосиликаты, гидроокиси и соли многовалентных металлов; применяются также иониты, полученные химической обработкой угля, целлюлозы и лигнина.
Однако ведущая роль принадлежит синтетическим органическим ионитам - ионообменным слюдам.
Важнейшим свойством ионитов является их подготовительная способность, так называемая обменная емкость. (Полная емкость ионита (количество находящихся в сточной воде грамм-эквивалентов ионов, которое может поглотить 1 м3 ионита до полного насыщения. Рабочая емкость ионита - количество находящихся в воде грамм-эквивалентов ионов, которое может поглотить 1 м3 ионита до начала проскока в фильтрат поглощаемых ионов.
Электрохимические методы. Для очистки сточных вод применяют электрохимическое окисление или восстановление, электрофлотацию, электрофорез, электродиализ и электрокоагуляцию.
Общим для всех методов является осуществление электролиза сточных вод, при котором имеет место направленное движение ионов и заряженных дисперсных частиц и протекание реакций окисления на аноде и восстановления на катоде.
Электрохимическое окисление на индифферентном аноде (графит, титан, покрытый оксидами рутения, свинца и др.) различных органических соединений происходит путем образования окислителей С12,О2 ClO
которые способствуют разложению органических веществ
обрабатываемой сточной воды. Электрохимическим окислением можно
удалить фенолы, цианид-ионы и др. Электрохимическим вост. на катоде можно удалить из сточных металлы сполож-ым значением электродного потенциала, такие как Hg2+, Cr2+,Pb2+, Ni2+, можно восстановить непредельные
органические соединения, осуществить восстановление соединений Сr6+ до Сr3+ и др.
процесс электрохимического восстановления и окисления в
значительной степени определяется электролита и величиной рН сточных вод, условиями проведения электролиза.
При электрофлотации на катоде и аноде образуются пузырьки водорода и кислорода, которые оказывают флотационное действие Прилипая к частицам дисперсной фазы, поднимают их на поверхность.
Очистка сточных вод электрофорезом и электродиализам основана на использовании направленного движения ионов и заряженных частиц
процессе электролиза. Осуществляют такую очистку с помощью селективных ионообменных мембран (электродиализ) или фильтрующих материалов (электрофорез).
Электрокоагуляция. В процессе анодного растворения образуется коагулянты - гидроксиды металлов, которые снижают поверхностный заряд частиц под воздействием электрического поля.
В электролитах, содержащих активирующие ионы такие как С1-,Вr-, стальной электрод при наложении электрического поля ионизируется по реакции
Fe° - е + Н20 = Fe(OH)адс + Н+ ;
Fе(ОН)адс - е + Н20= Fe(OH)2адс+ Н+.
В результате анодного растворения и последующего
происходит накопление коагулирующего компонента. Гидроксид Fe(OH)2 образуется при рН > 4,5 и потенциале 0,8 В виде коллоидного раствора.
52. Биологическая очистка сточных вод. Факторы, влияющие на эффективность биологической очистки.
Биологическая очистка. Биологическое окисление осуществляется сообществом микроорганизмов, включающим множество различных бактерий, простейших и ряд более высокоорганизованных организмов, связанных между собой единый комплекс сложными взаимоотношениями. Главенствующая роль в том сообществе принадлежит бактериям.
1. аэробный
2. анаэробный
При термической очистке сжигают, жидки отходы нефтепродуктов и других горючих веществ в печах и горелках.
1. огневое концентрирование
2. огневое обезвреживание
Большое влияние на биологическое окисление оказывает кислородный режим и наличие токсичных веществ в среде. Токсичное действие на биологические процессы могут оказывать органические и неорганические вещества. Биологическая очистка сточных вод может осуществляться как в естественных условиях (поля орошения, поля фильтрации, биологические пруды), так и в специальных сооружениях (аэротенки, метантенки).
Использование бактерий для очистки вод.
Органические вещества + O2 + N + P à(микроорганизмы) + CO2 + H2 + биологически не окисляемые растворимые вещества.
Факторы влияющие на биологическую очистку:
- концентрация водородных ионов (pH)
- кислородный режим и наличие токсичных веществ в среде
53. Литосфера, её состав и строение.
Земля является частью Солнечной системы и имеет форму геоида, т. е. фигуры, ограниченной поверхностью океана, мысленно продолженной через материки таким образом, что она всюду остается перпендикулярной к направлению силы тяжести. От поверхности отсчитывается «высота над уровнем моря». Форма геоида близка к земному эллипсоиду вращения, большая полуось которого (радиус экватора,160 км, малая полуось (полярный радиус,777 км, средний радиус Земли, принимаемой за шар, -6371,032 км, длина окружности по мервдиану - 40008,55 км, площадь поверхности - 510,2 млн км2, объем - 1, км3, масса - 5кг, средняя плотность — 5518 кг/м3.
Земля состоит из центрального тяжелого ядра, мантии и земной коры Или литосферы (рис. ).
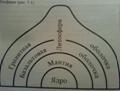 Литосфера - твердая оболочка Земли глубиной 50-100 км, состоит из осадочного слоя - 15-25 км, гранитного - 25-30 км и базальтового — 2-15 км. Земная кора, сложенная осадочными и кристаллическими породами, образует сплошную оболочку, 2/3 которой покрыто водами морей и океанов. Кора Земли глубиной от 7 км (под океаном) до 40 км (под континентом) составляет 0,42 % общей массы и 0,85 % общего объема планеты.
Литосфера - твердая оболочка Земли глубиной 50-100 км, состоит из осадочного слоя - 15-25 км, гранитного - 25-30 км и базальтового — 2-15 км. Земная кора, сложенная осадочными и кристаллическими породами, образует сплошную оболочку, 2/3 которой покрыто водами морей и океанов. Кора Земли глубиной от 7 км (под океаном) до 40 км (под континентом) составляет 0,42 % общей массы и 0,85 % общего объема планеты.
По физическим свойствам земная кора делится на два типа материковый и океанический. Земная кора материкового типа - равнинных и горных районов - богата кремнием и алюминием, характерными для пород группы гранита. Мощность гранитного слоя увеличивается в горах. Океанический тип земной коры представлен породами типа базальта с преобладанием кремния и магния. Здесь гранитный слой отсутствует, а мощность базальтового слоя доходит до 15 км.
У нижней границы земная кора на глубинах 40-100 км приобретает пластический характер из-за большого давления и высоких температур. Ниже расположено подкорковое вещество, которое по физическим свойствам одинаково как под океанами, так и под материками. Эту однородную оболочку называют мантией.
В центральной области Земли на глубине 2900 км расположено ядро, которое, по расчетам и предположениям, состоит из вещества, находящегося в жидком состоянии.
Средняя плотность Земли составляет 5,52 г/см3, причём средняя
плотность осадочных пород - 2,5-2,8, а пород, богатых железом, - 2,9-3,0
г/см3. Высокая средняя плотность Земли объясняется наличием внутри неё
тяжёлого металлического ядра, радиусом порядка 3 000 км и плотностью от 9
до 11 г/см3. На рис. 5.2 представлено распределение плотности вещества
внутри Земли.
54.Почва, состав, плодородие. Почвенный профиль, факторы почвообразования. Типы почв.
Литосфера – внешняя твердая оболочка земли, постепенно, с глубиной переходящая в сферы с меньшей плотностью вещества.
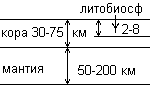
1. Верхняя мантия (200 км).
2. Земная кора: на суше 75 км вглубь, на дне океана 5-10 км вглубь. Состав: 50% - SiO2; 25% - AlO3; 10% - Fe2O3; оксиды K, Ca, Mn, P.
Земельные ресурсы: 30% - суша. S=129 млн. км2. 10% - пашни. 25% - пастбища, сенокосы. 43% - пустыни. 30% - горы. 3.
Верхний слой литосферы – гумус. Гумус – конечный продукт разложения мертвых органических остатков, аморфное вещество, (фенолы, сложные эфиры, карбоновые кислоты) плодородный слой почвы. Гумификация - процесс образования гумуса.
Почва - особое природное образование, сформировавшееся в результате преобразования горных пород растениями и животными, т. е. в результате почвообразовательного процесса. Почва обладает особым свойством - плодородием, она служит основой с/х всех стран. Почва при правильной эксплуатации не только не теряет своих свойств, но и улучшает их, становится плодороднее. Почва - колоссальное природное богатство, обеспечивающее человека продуктами питания, животных - кормами, а промышленность сырьем. Почва образовывалась из выхода на поверхность земли горных пород под действием ветра, атмосферной влаги, в связи с изменением климата и температурными колебаниями горные породы, под действием микроорганизмов, а позднее лишайников и мхов. Микроорганизмы разлагали остатки растений, образуя гумус - основное органическое вещество почвы, содержащее питательные вещества, необходимые высшим растениям. Животные и растения окончательно разрушали горную породу, превращая верхний ее слой в почву. Лучшие почвы, влагоемкие и воздухопроницаемые, имеют мелкокомковатую или мелкозернистую структуру из комочков диаметром от 1 до 10 мм. От состава и свойств горной породы, на которой формируется почва, в значительной степени зависят состав и свойства почвы. Почва состоит из твёрдой, жидкой, газообразной и животной частей. Твердая часть - это минеральные и органические частицы. Они составляют от 80-98 % почвенной массы и состоят из песка, глины, илистых частиц, оставшихся от материнской породы в результате почвообразовательного процесса. Соотношение этих частиц характеризует механический состав почвы. Жидкая часть почвы, или почвенный раствор, вода с растворенными в ней органическими и минеральными соединениями. Воды в почве содержится от долей процента до 40-60 %. Жидкая часть участвует в снабжении растений водой и растворёнными элементами питания. Газообразная часть, почвенный воздух, заполняет поры, не занятые водой. Почвенный воздух содержит больше CO2 и меньше O2, чем атмосферный воздух, а также метан, летучие органические соединения и др. Живая часть почвы состоит из почвенных микроорганизмов (бактерии, грибы, водоросли, актиномицеты и др.), представителей беспозвоночных (простейших, червей, моллюсков, насекомых и их личинок), роющих позвоночных. Они обитают в основном в верхних слоях почвы, около корней растений, где добывают себе пищу. Некоторые почвенные организмы могут жить только на корнях. Почва содержит микроэлементы (азот, фосфор, калий, кальций, сера, железо и др.) и микроэлементы (бор, марганец, молибден, цинк и др.), которые растения потребляют в ограниченных количествах. Их соотношение определяет химический состав почвы. Из физических свойств почвы наибольшее значение имеет влагоемкость, водопроницаемость, скважность.
 Наука изучающая почву называется почвоведением.
Наука изучающая почву называется почвоведением.
Удерживать влагу могут: глина, суглинка, супесь. Переход жизненно важных элементов в неорганические (в почве): Р à фосфаты; С à CO2; N à NO3; N2 à NH4+ (через мочевину).
Рекультивация земель – система мероприятий, направленных на восстановление хозяйственной ценности и комплексного улучшения земель, нарушенных в процессе хозяйственной деятельности человека; один из видов мелиорации. Рекультивация земель предусматривает комплексную перестройку нарушенных земель, что дает возможность восстановить утерянную ими пригодность для непосредственного использования и создать полноценные по структуре и функционированию, экологически сбалансированные ландшафты.
Условия эффективного использования почв: борьба с эрозией; культурная обработка земли; грамотное использование удобрений; проведение мероприятий по мелиорации и рекультивации.
Рекультивация: горнотехническая (засыпка карьеров); биологическая (группы живых организмов, деятельность которых приводит к восстановлению плодородия); лесная (длительное применение до нескольких десятков лет).
55.Деградация почв, причины. Контроль загрязнений. Защита почв.
Состав и свойства почвы постоянно меняются под влиянием жизнедеятельности, климата, деятельности человека. При внесении удобрений почва обогащается питательными для растений веществами, изменяет свои физические свойства. Неправильная эксплуатация может привести к нарушению почвенного покрова - к Деградация почвы: эрозия(снесение верхнего слоя почвы водой или ветром), загрязнение, заболачивание, затопление, опустынивание, отчуждение. Почвообразующие факторы: климат, геологическая основа, рельеф, время, биота. Почва: 50–60% - минеральная основа; 10%- органическая основа; 15% - воздух; 20–30% - вода.
Загрязнение литосферы. Оценка качества литосферы и пищи. Пестициды.
Пестициды (ядохимикаты) - химические препараты для защиты сель-хоз продукции, растений, для уничтожения паразитов у животных, для борьбы с переносчиками опаснх заболеваний и т. п.
Пестициды в зависимости от объекта подразделяются на: Гербициды – для уничтожения сорной растительности; Фунгициды - борьба с грибковыми заболеваниями растений; Зооциды – борьба с вредителями при хранении, борьба с грызунами; Немотоциды – внешние паразиты животных; Дефолианты – для удаления листьев; Дефлоранты - для удаления цветков; Инсектициды – против вредных насекомых.
Токсичные действия: - сильно токсичные ПДК<50мг/кг; - высоко ядовитые ПДК<100 мг/кг; - средние ПДК до 1 г/кг; - мало ядовитые ПДК > 1 г/кг.
Пестициды являются единственным загрязнителем, который сознательно вносится человеком в окружающую среду. Пестициды поражают различные компоненты природных экосистем: уменьшают биологическую продуктивность фитоценозов, видовое разнообразие животного мира, снижают численность полезных насекомых и птиц, а в конечном итоге представляют опасность и для самого человека. Пестициды, содержащие хлор (ДДТ, гексахлоран, диоксин, дибензфуран и др.), отличаются не только высокой токсичностью, но и чрезвычайной биологической активностью и способностью накапливаться в различных звеньях пищевой цепи. Даже в ничтожных концентрациях пестициды подавляют иммунную систему организма, повышая таким образом его чувствительность к инфекционным заболеваниям. В более высоких концентрациях эти примеси оказывают мутагенное и канцерогенное действие на организм человека. ДДТ
Действие: - воздействуют на ЦНС; - аллергены – вызывают аллергические заболевания; - канцерогены – вызывают раковые заболевания; - мутагены - изменяют генокод.
56.Твердые отходы черной и цветной металлургии теплоэлектроэнергетики производств машиностроения: (металлургические шлаки; золошлаковые отходы; золы топлива; шламы; окалина и стружки; сварочные флюсы).
Шлаки цвет. мет. могут быть условно объединены в 3 группы:
1)шлаки никелевых заводов и часть шлаков медных заводов, отличающихся малым содержанием цвет. металлов и железа
2)медные шлаки, отличающиеся значительным содержанием хелеза, малым содержанием меди и менее 5%цинка и свинца
3)оловянные, свинцовые и часть медных шлаков, отличающиеся значительным содержанием цинка, свинца и стронция
Технологическая схема переработки шлаков могут включать гидрометаллургические и пирометаллургические способы извлечения металлов.
Гидрометаллургический связан с восстановлением металлов из водных р-ров их соединений различными методами.
При пирометаллургическом способе осуществляется восстановление металлов из их безводных соединений при высоких температурах.
Шлаки черной и цвет металлургии служат сырьем для получения стройматериалов и изделий различного назначения.
Энергетические установки.
Основные компоненты, выбрасываемые в атмосферу при сжигании топлива в энергоустановках являются СО2 и Н2О, продукты неполного сгорания топлива, оксид углерода, сажа, углеводороды, несгоревшие частицы тв. топлива, зола, шлаки и прочие мех. примеси.
На 80-90%хим. состав золошлаковых отходов представлены оксидами Si, Al, Fe, Ca, Mg; также в них присутствуют соединения Ti, V, Ge, Ga, S, U и несгоревшие частицы топлива.
ТЭС снабжены мокрыми золоуловителями или имеют системы гидроуловления.
Золы и шлаки от сжигания углей, сланцев и торфа могут использоваться в качестве кирпича.
Золы ТЭС используются для получения искусственных пористых заполнителей-гравия, битум. Золошлаковые отходы используют в качестве активной минеральной добавки при производстве цемента; применяют в виде гидравлической добавки к цементу; используют при приготовлении бетонов.
Золы сланца и торфа содержат CaО и использ-ся для известкования кислых почв. Золы также содержат К и Р, микроэлементы; их применяют в с/х как удобрения; некоторые виды золошлаков испльзуют в качестве элементов очистки промстоков.
Пути решения экологической проблемы черной и цвет. металлургии.
-комплексное использование руд цвет. металлов, которые перерабатываются как сырье для получения одного продукта;

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



