- водой Q′п = Gв∙cв (t1 – t2);
- паром Q′п = G ∙r;
- теплопередачей через стенку Q′п = kT F(t1 – t2)τ,
где kT - коэффициент теплопередачи; F – поверхность теплообмена; t1, t2 - температура теплоносителя на входе и выходе соответственно; τ – время.
При определении низшей теплоты сгорания топлива в технических расчетах можно пользоваться формулой :
Qрн = 339,3С + 1256Н – 109(O – S) – 25,2(9Н + W) ( )
где C, H, O, S – содержание в топливе углерода, водорода, кислорода и серы соответственно (в % масс.); W – содержание влаги в рабочем топливе (в% масс.).
Высшая теплота сгорания топлива:
Qрв = Qрн + 25,2(9Н + W) ( )
Теоретический расход воздуха Gтеор (в кг на 1 кг топлива) рассчитывается по уравнению:
Gтеор = 0,116С + 0,348Н + 0,135(S - О) ( )
Количество тепла, вносимое влажным воздухом Iвозд, определяется по формуле:
Iвозд = αGтеор(1,02 + 1,95χ)tвозд ( )
где α - коэффициент избытка воздуха (для твердого топлива α = 1,3-1,7; для жидкого α – 1,1-1,2; для газообразного α – 1,0-1,2); χ – влагосодержание воздуха (кг на 1 кг сухого воздуха); tвозд – температура воздуха, подаваемого в топочное устройство (1,02 и 1,95 – удельная теплоемкость воздуха и водяных паров соответственно).
Пример 4 Котел ПК-10 использует в качестве топлива газ, с которым подводится химическая энергия в количестве 659,86 ГДж/ч. С паром отводится 82,2% тепловой энергии. Остальная часть отводится с отходящими газами и тепловыми потерями в окружающую среду в соотношении 21 : 1. Результаты расчета теплового баланса представить в табличной форме.
Решение
Энергетический баланс котла ПК-10
Таблица
Приход | Расход | ||||
Статья баланса | ГДж/ч | % | Статья баланса | ГДж/ч | % |
Химическая энергия топлива | 659,86 | 100 | Тепло пара Потери с уходящими газами Тепловые потери прочие | 542,40 112,11 5,35 | 82,20 16,99 0,81 |
Всего: | 659,86 | 100 | Всего: | 659,86 | 100 |
Пример 5 Рассчитать теоретическую температуру горения природного газа метана (теплота сгорания 890 310 кДж/моль) при избытке воздуха 25% (α = 1,25).
Решение Реакция горения метана
СН4 +2О2 + 0,5О2 + 2,5∙3,76N2 = CO2 + 2H2O + 0,5О2 + 2,5∙3,76N2
При начальной температуре воздуха 0оС, при заданной температуре горения тепловой баланс выражается уравнением:
Q = 890 310 = ( CCO2 + 2CH2O + 0,5CО2 + 2,5∙3,76N2)∙t
Средняя мольная теплоемкость газов и паров С, кДж/(кмоль∙ оС):
1800 оС | 1900 оС | |
О2 | 34,9 | 35,1 |
CO2 | 53,9 | 54,2 |
N2 | 33,1 | 33,2 |
H2O | 42,8 | 43,2 |
При температуре 1800оС
Q1 = 953,9 + 2∙42,8 + 0,5∙34,9+ 2,5∙3,76∙33,1)∙1800 =467,95∙800 =842 000 кДж
Так как Q1(842 000 кДж) < Q (890 310 кДж) следует выбрать температуру
1900оС:
Q2 = (54,2 + 2∙43,2 + 0,5∙35,1 + 2,5∙3,76∙33,2)∙1900 =470,6∙1900= 906 000 кДж
Q2(906 000 кДж) < Q (890 310 кДж)
Q2 - Q = 906 310 =15 690 кДж
Q - Q1 = 890 000 =кДж
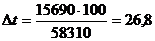 ОС
ОС
![]() ОС
ОС
Пример 6 В реакторе вода массой 5000 кг нагревается острым паром под давлением 2 атм. Определить время, необходимое для нагрева воды от tо =15 ОС до t = 90 ОС, если расход пара G = 0,50 кг/с. Потери тепла в окружающую среду Qп = 15 кВт. Найти закономерность изменения температуры во времени.
Решение
Острый пар конденсируется в воде, поэтому в момент τ количество воды равно М + G∙τ. Уравнение теплового баланса имеет вид:
(М + G∙τ)с∙t = Gi″∙τ + M cto + Qп∙τ
Энтальпия насыщенного водяного пара i″ = 2,71∙103 кДж/кг, удельная теплоемкость воды с = 4,19 кДж/кг∙гр.
Из уравнения теплового баланса определяем время (ч) нагревания воды до заданной температуры:
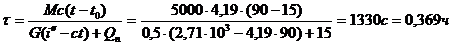
Необходимое для нагревания воды количество пара G (кг) равно:
G′ = G∙τ = 0,5 ∙1330 = 665 кг
Решая уравнение теплового баланса относительно температуры, получим
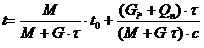
После подстановки в это уравнение числовых значений найдем закон изменения температуры во времени:
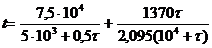
Задачи для самостоятельного решения
1. Составить материальный баланс Q(кг/ч) печи для сжигания серы (S + O2 = SO2) производительностью 60 т/сут. Степень окисления серы 0,95 (остальная сера возгоняется и сгорает вне печи). Коэффициент избытка воздуха α =1,5.
2. Составить материальный баланс производства криолита (m = 1 кг), если процесс описывается суммарным уравнением:
2Al(OH)3 + 12HF + 3Na2CO3 = 2Na3AlF6 + 3CO2 + 9H2O
Плавиковая кислота вводиться в виде 15% раствора HF в вод. Сода берется с 4%-й недостачей от стехиометрического расчета(для
обеспечения необходимой остаточной кислотности).
3. Рассчитать материальный баланс водооборотной охлаждающей системы производительностью 108 000 м3/ч в соответствии с условиями примера 2. Состав оборотной воды Свзв =50 г/м3; Скат = 3,5 г-экв/м3; Сан = 500 г/м3. Состав подпиточной воды Свзв =20 г/м3; Скат = 4 г-экв/м3; Сан = 550 г/м3. Коэффициент α = 0,03.
4. Подсчитать количество теплоты Q (кДж), выделяющееся при образовании 100 л ацетилена из карбида кальция:
СаС2 + Н2О = СаО +С2Н2 +Q
Если теплота образования СаС2 – 62 700 кДж/кмоль; Н2О – кДж/кмоль; С2НкДж/кмоль.
5. Рассчитать теоретическую температуру горения этана (теплота сгорания этана 1,559∙106 кДж/кмоль) при избытке воздуха 20% (α =1,2).
Реакция протекает по уравнению:
C6H6 +3,5O2 + 0,7O2 + 4,2∙(79/21)N2 = 2CO2 + 3H2O + 0,7O2 +4,2∙3,76N2
Значение средней теплоемкости Сср (кДж/кмоль∙гр):
19000С | 20000С | |
СО2 | 54,2∙103 | 54,5∙103 |
О2 | 35,1∙103 | 35,3∙103 |
Н2О (пар) | 43,2∙103 | 43,6∙103 |
N2 | 33,2∙103 | 33,4∙103 |
6. Рассчитать повышение температуры при окислении SO2 на 1% при 5000С для газовой смеси состава: SO2 – 7%; О2 – 12%; N2 – 81%
SO2 + 1/2O2↔ SO3 + 94 400 кДж.
Теплоемкости:
С SO2 – 2,082 кДж/м3∙гр ; С O2 - 1,402 кДж/м3∙гр ; С N2 -1,343 кДж/м3∙гр.
Зависимость теплового эффекта реакции от температуры
рассчитывается по формуле:
Q = 4,187(24,555 – 2,21Т), кДж/кмоль
7. Рассчитать тепловой эффект Q (кДж/моль) конверсии этилена:
С2Н4 + 2Н2О ↔ 2СО + 4Н2 + Q
8. Подсчитать температуру горения мазута, имеющего состав (% масс.):
С – 87; Н2 – 10,8; О2 – 1,0; S – 0,7; N2 - 0,5. Воздух для горения подается с коэффициентом избытка α = 1,36. Температура мазута и воздуха при подаче в топку равна 20оС. Суммарные теплопотери 6,5% от общего прихода теплоты. Теплоемкость мазута – 2,5 кДж/кг∙гр.
Тема 5. Определение количества выделяющихся загрязняющих веществ от различных источников и в некоторых технологических процессах
Работа двигателей автотранспорта
Основная причина загрязнения воздуха разнообразными двигателями, использующими в качестве топлива продукты нефтепереработки, заключается в неполном и неравномерном сгорании топлива. Камера сгорания двигателя – своеобразный химический реактор, синтезирующий загрязняющие вещества, выделяющиеся с выхлопными газами в атмосферу. Основная химическая реакция, протекающая в процессе сгорания топлива, может быть представлена следующим обобщенным уравнением
CхНу + (χ + 0,25y)О2 → χСО2 + 0,5уН2О (….)
Однако эта реакция не проходит полностью даже при стехиометрическом соотношении исходных компонентов. Основными загрязняющими веществами, входящими в состав выхлопных газов практически всех двигателей, являются СО, СnHm, NOx. При определенных условиях в выхлопных газах содержаться также SO2.сажа, бензапирен, соединения свинца. Выбросы ЗВ двигателями осуществляется при прогреве двигателя, холостом ходе, пробеге по территории предприятия и движении по трассе.
Удельные выбросы ЗВ двигателями автотранспорта зависят от категории автомобилей, от их грузоподъемности, типа двигателя, используемого топлива, периода года. Влияние периода года учитывается только для выезжающих с открытых стоянок автомобилей, для остальных расчет выполняется как для постоянного теплого периода года.
Валовое выделение (г/день) ЗВ одним автомобилем в день при выезде с территории и возврате определяется по формулам
![]() (…..)
(…..)
![]() (….)
(….)
Величина времени прогрева tпр принимается одинаковой для различных типов автомобилей, но существенно зависит от температуры воздуха.
Температура воздуха, 0С | Время прогрева, мин | |
Легкового автомобиля | Грузового автомобиля | |
Выше +5 | 3 | 4 |
+5…-5 | 4 | 6 |
-5…-10 | 10 | 12 |
-10…-15 | 15 | 20 |
-15…-20 | 15 | 25 |
-20…-25 | 20 | 30 |
Ниже -25 | 20 | 30 |

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



