Министерство образования и науки Республики Казахстан
Костанайский социально-технический университет
имени академика Зулхарнай Алдамжар

УЧЕБНО-МЕТОДИЧЕСКИЙ КОМПЛЕКС ДИСЦИПЛИНЫ
«ФИЗИКА ТВЕРДОГО ТЕЛА»
Костанай
2014 г.
Учебно-методический комплекс дисциплины «Физика твердого тела» составлен на основании типовой программы, с учетом содержания программы обучения дисциплины для студента – силлабус (Syllabus) – д. ф.-м. н., профессором «Кафедры физики и информационных технологий».
Учебно-методический комплекс дисциплины «Физика твердого тела» рассмотрен и обсужден на заседании кафедры « физика и информационных смистем», протокол № __ от "_____"__________200__г.
Заведующий кафедрой «Кафедры физики и информационных технологий».
Ф. И.О. ________________
(подпись)
Учебно-методический комплекс дисциплины «Физика твердого тела» одобрен и утвержден на заседании методического бюро технического факультета,
протокол № ___ от «___» ________________200___г.
Ф. И.О. председатель ____________
(подпись)
Учебно-методический комплекс дисциплины «Физика твердого тела» предназначен для магистрантов Костанайского социально-технического университета имени академика Зулхарнай Алдамжар 1 курса, специальности: 6M060400 – Физика.
Структура УМКД
1. Типовая учебная программа по дисциплине обязательного
компонента.
2. Программа обучения по дисциплине для студента – силлабус
(Syllabus).
3. Методические рекомендации по изучению дисциплины;
В рекомендациях отразить своевременность и необходимость изучения конкретной дисциплины, чтобы вызвать к ней устойчивый интерес. При характеристике целей и задач выделить самый главный результат, которого студент должен достичь по окончании изучения данной дисциплины. Важно подчеркнуть значимость дисциплины в становлении их как будущих специалистов. Необходимо провести связь с другими дисциплинами. Показать последовательность и преемственность в изучении курсов.
4. Карта учебно-методической обеспеченности дисциплины:
Типовая программа | Силлабус | Методические указания по написанию курсовых работ (проектов) | Тезисы лекций | Тестовый материал | Аудио, видеоматериалы | Наглядный материал |
Автор, издательство, место и год издания | + | Автор, дата утверждения | + | + Кол-во вопросов | перечень | перечень |
Литература.
1. Ч. Киттель. Введение в физику твердого тела. М., Наука, 1978 г.
2. Н. Ашкрофт, Н. Мермин. Физика твердого тела, т.1,2. М., "Мир", 1979г.
3. Дж. Займан. Принципы теории твердого тела. М., "Мир", 1966г.
4. . Кристаллография. М., Высшая школа, 1966г.
Ф. И.О. составителя ______________
Заведующий кафедрой ________________
5. Лекционный комплекс:
1. Определение твердого тела.
Фи́зика твёрдого те́ла — раздел физики конденсированного состояния, задачей которого является описание физических свойств твёрдых тел с точки зрения ихатомного строения. Интенсивно развивалась в XX веке после открытия квантовой механики. Развитие стимулировалось широким спектром важных задач прикладного характера, в частности, развитием полупроводниковой техники.
Кристаллы многих минералов и драгоценных камней были известны и описаны ещё несколько тысячелетий назад.. Кристаллом называли вначале только лёд, а затем и кварц, считавшийся окаменевшим льдом. В конце эпохи средневековья слово «кристалл» стало употребляться в более общем смысле.
Геометрически правильная внешняя форма кристаллов, образующихся в природных или лабораторных условиях, натолкнула ученых ещё вXVII веке на мысль, что кристаллы образуются посредством регулярного повторения в пространстве одного и того же структурного элемента. При росте кристалла в идеальных условиях форма его в течение всего роста остается неизменной, как если бы к растущему кристаллу непрерывно присоединялись бы элементарные кирпичики. Сейчас известно, что такими элементарными кирпичиками являютсяатомы или группы атомов. Кристаллы состоят из атомных рядов, периодически повторяющихся в пространстве и образующих кристаллическую решетку. В XVIII веке минералогами было сделано важное открытие: оказалось, что индексы, определяющие положение в пространстве любой грани кристалла, суть целые числа. Гаюи показал, что это можно объяснить расположением идентичных частичек в ряды, периодически повторяющиеся в пространстве. В 1824 году Зибер из Фрайбурга предположил, что элементарные составляющие кристаллов («кирпичики», атомы)являются маленькими сферами. Он предложил эмпирический закон межатомной силы с учётом как сил притяжения, так и сил отталкивания между атомами, что было необходимо для того, чтобы кристаллическая решетка была стабильным равновесным состоянием системы идентичных атомов.
Пожалуй, наиболее важной датой в истории физики твердого тела является 8 июня 1912 года. В этот день в Баварской Академии наук вМюнхене слушался доклад «Интерференция рентгеновских лучей». В первой части доклада Лауэ выступил с изложением элементарной теории дифракции рентгеновских лучей на периодическом атомном ряду. Во второй части доклада Фридрих и Книппинг сообщили о первых экспериментальных наблюдениях дифракции рентгеновских лучей в кристаллах. Этой работой было показано, что рентгеновские лучи являются волнами, так как они способны дифрагировать. Работа неопровержимо доказала также, что кристаллы состоят из периодических рядов атомов. С этого дня началась та физика твердого тела, какой мы знаем её сегодня. В годы, непосредственно следующие за 1912 годом, в физике твердого тела было сделано много важных пионерских работ. Первыми кристаллическими структурами, определенными У. Л. Брэггом в 1913 года с помощью рентгеновского дифракционного анализа, были структуры кристаллов KCl, NaCl,KBr и KI.
После открытия дифракции рентгеновских лучей и публикации серии простых и весьма успешных работ с расчётами и предсказаниями свойств кристаллических веществ началось фундаментальное изучение атомной структуры кристаллов.
В 1930-е годы работами В. Гейзенберга, Паули, М. Бopна были созданы основы квантово-механической теории твёрдого тела, что позволило объяснить и прогнозировать интересные физические эффекты в твердых телах. Ускоряли формирование физики твердого тела потребности нарождающейся твердотельной электроники в новых сверхчистых материалах. Здесь можно указать важнейшее событие — открытие в 1948 г. У. Шокли, У. Браттейном и Дж. Бардином усилительных свойств транзистора.
В настоящее время методы и теория твёрдого тела, развитые для описания свойств и структуры монокристаллов, широко применяются для получения и исследования новых материалов: композитов и наноструктур, квазикристаллов и аморфных тел. Физика твёрдого тела служит основой для изучения явленийвысокотемпературной сверхпроводимости, гигантского магнетосопротивления и многих других перспективных современных наукоёмких технологий.
Физика твёрдого тела сводится, в сущности, к установлению связи между свойствами индивидуальных атомов и молекул и свойствами, обнаруживаемыми при объединении атомов или молекул в гигантские ассоциации в виде регулярно-упорядоченных систем — кристаллов. Эти свойства можно объяснить, опираясь на простые физические модели твёрдых тел. Реальные кристаллы и аморфные твёрдые тела значительно сложнее, но эффективность и полезность простых моделей едва ли можно переоценить. Предметом данной области науки являются, прежде всего, свойства веществ в твёрдом состоянии, их связь с микроскопическим строением и составом, эвристическое прогнозирование и поиск новых материалов и физических эффектов в них. Фактически физика твёрдого тела служит базой для физического материаловедения.
2. Кристаллические и аморфные тела window. top. document. title = "3.6. Кристаллические и аморфные тела";
По своим физическим свойствам и молекулярной структуре твердые тела разделяются на два класса – аморфные и кристаллические.
Характерной особенностью аморфных тел является их изотропность, т. е. независимость всех физических свойств (механических, оптических и т. д.) от направления внешнего воздействия. Молекулы и атомы в изотропных твердых телах располагаются хаотично, образуя лишь небольшие локальные группы, содержащие несколько частиц (ближний порядок). По своей структуре аморфные тела очень близки к жидкостям (см. §3.5). Примерами аморфных тел могут служить стекло, различные затвердевшие смолы (янтарь), пластики и т. д. Если аморфное тело нагревать, то оно постепенно размягчается, и переход в жидкое состояние занимает значительный интервал температур.
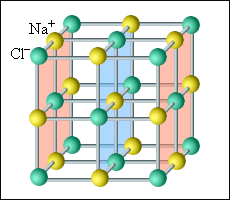
В кристаллических телах частицы располагаются в строгом порядке, образуя пространственные периодически повторяющиеся структуры во всем объеме тела. Для наглядного представления таких структур используются пространственные кристаллические решетки, в узлах которых располагаются центры атомов или молекул данного вещества. Чаще всего кристаллическая решетка строится из ионов (положительно и отрицательно заряженных) атомов, которые входят в состав молекулы данного вещества. Например, решетка поваренной соли содержит ионы Na+ и Cl–, не объединенные попарно в молекулы NaCl (рис. 3.6.1). Такие кристаллы называются ионными.
|
Рисунок 3.6.1. Кристаллическая решетка поваренной соли |
В каждой пространственной решетке можно выделить структурный элемент минимального размера, который называется элементарной ячейкой. Вся кристаллическая решетка может быть построена путем параллельного переноса (трансляции) элементарной ячейки по некоторым направлениям.
Теоретически доказано, что всего может существовать 230 различных пространственных кристаллических структур. Большинство из них (но не все) обнаружены в природе или созданы искусственно.
Кристаллические решетки металлов часто имеют форму шестигранной призмы (цинк, магний), гранецентрированного куба (медь, золото) или объемно центрированного куба (железо).
Кристаллические тела могут быть монокристаллами и поликристаллами. Поликристаллические тела состоят из многих сросшихся между собой хаотически ориентированных маленьких кристалликов, которые называются кристаллитами. Большие монокристаллы редко встречаются в природе и технике. Чаще всего кристаллические твердые тела, в том числе и те, которые получаются искусственно, являются поликристаллами.
В отличие от монокристаллов, поликристаллические тела изотропны, т. е. их свойства одинаковы во всех направлениях. Поликристаллическое строение твердого тела можно обнаружить с помощью микроскопа, а иногда оно видно и невооруженным глазом (чугун).
Многие вещества могут существовать в нескольких кристаллических модификациях (фазах), отличающихся физическими свойствами. Это явление называется полиморфизмом. Переход из одной модификации в другую называется полиморфным переходом. Интересным и важным примером полиморфного перехода является превращение графита в алмаз. Этот переход при производстве искусственных алмазов осуществляется при давлениях 60–100 тысяч атмосфер и температурах 1500–2000 К.
Структуры кристаллических решеток экспериментально изучаются с помощью дифракции рентгеновского излучения на монокристаллах или поликристаллических образцах.
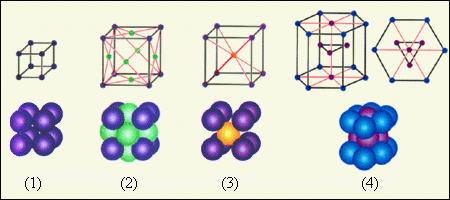
На рис. 3.6.2 приведены примеры простых кристаллических решеток. Следует помнить, что частицы в кристаллах плотно упакованы, так что расстояние между их центрами приблизительно равно размеру частиц. В изображении кристаллических решеток указывается только положение центров частиц.
|
Рисунок 3.6.2. Простые кристаллические решетки: 1 – простая кубическая решетка; 2 – гранецентрированная кубическая решетка; 3 – объемноцентрированная кубическая решетка; 4 – гексагональная решетка |
В простой кубической решетке частицы располагаются в вершинах куба. В гранецентрированной решетке частицы располагаются не только в вершинах куба, но и в центрах каждой его грани. Изображенная на рис. 3.6.1 решетка поваренной соли состоит из двух вложенных друг в друга гранецентрированных решеток, состоящих из Na+ и Cl–. В объемноцентрированной кубической решетке дополнительная частица располагается в центре каждой элементарной кубической ячейки.
Кристаллические структуры металлов имеют важную особенность. Положительно заряженные ионы металла, образующие кристаллическую решетку, удерживаются вблизи положений равновесия силами взаимодействия с «газом свободных электронов» (рис. 3.6.3). Электронный газ образуется за счет одного или нескольких электронов, отданных каждым атомом. Свободные электроны способны блуждать по всему объему кристалла.
3. Моно-и поликристаллы.
Типы кристаллических твердых тел.
Твердые тела (кристаллы) характеризуются правильной геометрической формой, что является результатом упорядоченного расположения атомов и молекул, составляющих кристалл.
Структура, для которой характерно регулярное расположение частиц с периодической повторяемостью в трех измерениях, называется кристаллической решеткой. Точки, в которых расположены частицы называют узлами кристаллической решетки.
Кристаллические тела можно разделить на две группы:
Монокристаллы Поликристаллы
Твердые тела, частицы которых Твердые тела, состоящие из
образуют единую кристаллическую множества беспорядочно
решетку. ориентированных мелких
кристаллических зерен.
Классификация кристаллов:
Кристаллографический признак.
· Пространственная периодичность,
· Симметрия кристаллической решетки,
· Всякая пространственная решетка или решетка Бравэ (трехмерная периодическая структура) может быть составлена повторением в трех различных направлениях одного и того же структурного элемента – элементарной ячейки.
· 14 типов решетки Бравэ.
· 7 классов кристаллической решетки:
Кристаллографическая система параметры элементарной ячейки
1. Кубическая a = b = c α = β = γ
2. Гексагональная a = b ≠ c α = β = 90˚,γ = 60˚
3. Тригональная a = b = c α = β = γ ≠ 90˚
4. Тетрагональная a = b ≠ c α = β = γ = 90˚
5. Ромбическая a ≠ b ≠ c α = β = γ = 90˚
6. Моноклинная a ≠ b ≠ c α = β = 90˚ ≠ γ
7. Триклинная a ≠ b ≠ c α ≠ β ≠ γ
Физический признак:
· Ионные кристаллы – в узлах крист. решетки располагаются
поочередно ионы противоположного
знака. Na(+)Cl(-) – связь ионная.
Решетка – кубическая.
· Атомные кристаллы - в узлах крист. решетки располагаются
нейтральные атомы, алмаз, графит, Si, Ge-
связь ковалентная ( у соседних атомов
обобществлены валентные электроны,
наименее связанные с атомом)
· Металлические кристаллы - в узлах крист. решетки распо – ся
положительные ионы металла. Валентные
электроны слабо связаны с атомами,
отделяются от атомов и принадлежат
всему кристаллу в целом.
· Молекулярные кристаллы - в узлах крист. решетки распо – ся
нейтральные молекулы вещества. Силы
взаимодействия – Ван-дер-ваальсовые.
Инертные газы - Ne, Ar, Kr, Xe, газы-
CO2, O2, N2.
4. Дефекты в кристаллах.
Дефектами кристаллической решетки называются отклонения от упорядоченного расположения частиц в узлах решетки.
Дефекты:
Макроскопические микроскопические
В процессе образования отклонения от периодичности.
и роста кристалла Точечные дефекты: нарушают ближний порядок
(трещины, поры) 1. вакансия – отсутствие атома в крист. решетки
2. междоузельный атом - атом, внедрившийся в междоузельное пространство.
3. примесный атом – атом примеси, либо замещающий атом основного вещества в крист. решетке.
Линейные дефекты: нарушают дальний порядок.
1. дислокации – нарушающие правильное чередование атомных плоскостей.
А. краевые, В – винтовые.
5. Теплоемкость твердых тел.
В качестве модели твердого тела рассмотрим кристаллическую решетку, в узлах которой частицы (атомы, ионы, молекулы), колеблются около своих положений равновесия в трех взаимно перпендикулярных направлениях.
В классической статистической физике
выводится закон Больцмана о равномерном распределении энергии по
степеням свободы молекул:
для статистической системы, находящейся в состоянии термодинамического равновесия, на каждую поступательную и
вращательную степени свободы приходится в сред.
E = ½ кТ (кинет. энергия),
а на каждую колебательную степень свободы – в среднем
E = кТ.
Распределение внутренней энергии по степеням свободы сложных объектов имеющих i степеней свободы имеет вид:
U = i/2 (кТ) (1)
Где i = i (пост) + i (вр) +2i (кол).
(множитель 2 в слагаемом 2i (кол) обусловлен тем, что каждой колебательной степени свободы соответствует кинетическая и потенциальная энергия.
Таким образом, каждой частице кристаллической решетки приписывается
3 колебательных степени свободы, каждая из которых обладает Е=кТ.
Внутренняя энергия 1 моль твердого тела равна
U = 3N(A) kT = 3RT (2),
Где N(A) –постоянная Авогадро;
R = N(A) k – молярная газовая постоянная.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |