Лабораторная работа № 3
Химическое равновесие
Теоретическая часть
Равновесное состояние системы – это такое ее состояние, в котором она может находиться бесконечно долго в отсутствие внешнего воздействия. Для обратимой химической реакции равенство скоростей прямой и обратной реакций – условие сохранения равновесного состояния системы.
Обратимые химические реакции – реакции, которые в данных условиях могут самопроизвольно протекать как в прямом, так и в обратном направлении.
Примером обратимой реакции является реакция синтеза йодоводорода из простых веществ:
H2(г) + I2(г) ⇄ 2HI(г)
Изменение скоростей прямой (v1) и обратной (v2) реакций во времени может быть представлено графически следующим образом:
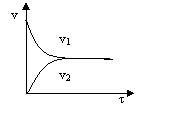
В начальный момент времени в системе присутствуют лишь исходные вещества H2 и I2, и отсутствует HI, поэтому скорость прямой реакции v1 имеет максимальное значение, а скорость обратной реакции v2 равна нулю. С течением времени скорость прямой реакции v1 уменьшается с уменьшением С(H2) и С(I2), а скорость обратной реакции v2 увеличивается с увеличением С(HI). В момент времени, когда скорость прямой реакции станет равна скорости обратной реакции, в системе установится состояние равновесия.
Так как в состоянии равновесия v1 = v2 или k1·[H2]·[I2] = k2·[HI]2, то
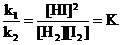 ,
,
где К – константа равновесия.
Закон действующих масс. В равновесной системе отношение произведения равновесных концентраций продуктов обратимой реакции к произведению равновесных концентраций исходных веществ, взятых в степенях, равных стехиометрическим коэффициентам, есть величина постоянная, называемая константой равновесия.
Для обратимой реакции вида mA + nB ⇄ pC +qD константа равновесия равна
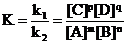 ,
,
а для реакции синтеза аммиака N2 + 3H2 ⇄ 2NH3 константа равновесия имеет вид
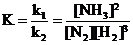 .
.
Константа равновесия зависит от температуры и природы реагирующих веществ и продуктов реакции, так как от этих параметров зависят константы скорости прямой k1 и обратной k2 реакций. Численное значение константы равновесия не зависит от концентраций реагирующих веществ и продуктов реакции, так как K = k1/k2, а константы скорости реакции не зависят от концентрации реагирующих веществ. Численное значение константы равновесия не зависит также от присутствия в системе катализатора, так как катализатор в одинаковой степени увеличивает или уменьшает значения k1 и k2.
Константа равновесия реакции – это количественная мера степени превращения исходных веществ в продукты реакции. Если для какой-либо химической реакции K = 0, то данная реакция не идет; если К > 1, то равновесие в данной системе смещено вправо, а если К < 1 – то равновесие смещено влево.
Закон смещения равновесия (принцип Ле Шателье – Брауна). Если на систему, находящуюся в состоянии равновесия, оказывается внешнее воздействие, то равновесие смещается в направлении, уменьшающем данное воздействие.
Под внешним воздействием понимается изменение температуры, давления, концентраций реагентов или продуктов реакции.
Действие температуры. Увеличение температуры смещает равновесие в сторону эндотермической реакции, а уменьшение температуры – в сторону экзотермической реакции.
Например, повышение температуры будет смещать равновесие в системе
2CO(г) + O2(г) ↔ 2CO2(г ) + Q
влево, так как прямая реакция является экзотермической.
Действие давления. Повышение давления смещает равновесие в сторону меньшего числа молекул газообразных веществ, а понижение давления – в сторону их большего числа. Давление не влияет на равновесие в жидких и твердых системах.
Например, повышение давления сместит равновесие в системе 2CO(г) + O2(г) ↔ 2CO2(г ) + Q вправо (в сторону меньшего числа молекул газообразных веществ), не повлияет на состояние равновесия в системах H2(г) + Cl2(г) ↔ 2HCl(г) (одинаковое число молекул газообразных веществ) и NaCl(р-р) + AgNO3(р-р) ↔ NaNO3(рр) + AgCl(тв) (отсутствуют газообразные вещества).
Действие концентрации. Увеличение концентрации реагента смещает равновесие в сторону прямой реакции, а увеличение концентрации продукта реакции – в сторону обратной реакции.
Например, увеличение концентрации CO и O2 смещает равновесие в системе 2CO(г) + O2(г) ↔ 2CO2(г) вправо, а увеличение концентрации CO2 смещает равновесие в данной системе влево.
Равновесие в гетерогенной системе осадок – насыщенный раствор малорастворимого сильного электролита
В системе, состоящей из осадка какого-либо вещества и его раствора, идут два противоположных по направлению процесса – растворение осадка и осаждение вещества. Равенство скоростей этих двух процессов является условием достижения равновесия в данной системе, а образовавшийся при этом раствор является насыщенным.
1. Термодинамическое и реальное
произведения растворимости
Гетерогенное равновесие между осадком малорастворимого сильного электролита KtmAnn и его ионами Ktn+ и Anm– в насыщенном водном растворе может быть представлено следующим уравнением:
KtmAnn ![]() m Ktn+ + n Anm–
m Ktn+ + n Anm–
(тв) (насыщенный р-р)
Термодинамическая константа равновесия обратимой реакции растворения-осаждения малорастворимого сильного электролита KtmAnn называется термодинамическим произведением растворимости и выражается следующим образом:
KSо(KtmAnn) ![]() ,
,
где ![]() и
и ![]() – активности Ktn+ и Anm– в насыщенном водном растворе, моль/л;
– активности Ktn+ и Anm– в насыщенном водном растворе, моль/л;
![]() – активность твердого вещества KtmAnn, принимаемая равной единице;
– активность твердого вещества KtmAnn, принимаемая равной единице;
m и n – стехиометрические коэффициенты.
Термодинамическое произведение растворимости малорастворимого сильного электролита – это величина, равная произведению активностей его ионов в насыщенном водном растворе данного электролита, взятых в степенях, равных их стехиометрическим коэффициентам.
Для данного малорастворимого сильного электролита KtmAnn величина KSо(KtmAnn) зависит только от температуры. Она отражает истинную энергию связи ионов в соединении.
Константа равновесия приведенной выше реакции растворения-осаждения KtmAnn, выраженная через равновесные концентрации ионов, называется концентрационным произведением растворимости (KSс):
![]()
![]() ,
,
где [Ktn+] и [Anm–] – равновесные концентрации катионов и анионов в насыщенном растворе KtmAnn, моль/л;
f(Ktn+) и f(Аnm-) – коэффициенты активности катионов и анионов;
m и n – стехиометрические коэффициенты.
Величина KSс(KtmAnn) сохраняет постоянство при постоянной температуре и постоянной ионной силе раствора.
Значения термодинамических произведений растворимости большинства малорастворимых в воде сильных электролитов приведены в табл.6 Приложения. Единицы измерения произведения растворимости, равные (моль/л)m+n, обычно опускаются.
2. Условия образования и растворения осадка
Постоянство произведения активностей ионов малорастворимого сильного электролита в насыщенном растворе, находящемся в равновесии с осадком, позволяет решать вопрос о возможности образования или растворения осадка.
Осадок образуется, если произведение активностей ионов малорастворимого соединения в растворе больше величины его термодинамического произведения растворимости:
аm(Ktn+)ּаn(Anm–) > KSо(KtmAnn)
Осадок не образуется или растворяется, если произведение активностей ионов осадка в растворе меньше величины его термодинамического произведения растворимости:
аm(Ktn+)ּаn(Anm-) < KSо(KtmAnn)
При равенстве произведения активностей ионов осадка в растворе величине его термодинамического произведения растворимости раствор является насыщенным. Такое состояние системы можно считать соответствующим моменту начала образования осадка.
3. Связь между произведением растворимости и
растворимостью малорастворимого электролита
Растворимость – это свойство вещества образовывать гомогенные системы (растворы) с растворителем. Количественно растворимость чаще всего выражается в моль/л (молярная растворимость).
Обозначим молярную растворимость малорастворимого сильного электролита KtmAnn через S(KtmAnn). В случае электролита KtmAnn концентрация катионов Ktn+ в растворе будет равна m·S(KtmAnn) моль/л, а концентрация анионов Anm– – n·S(KtmAnn) моль/л.
После подстановки значений [Ktn+] = m·S(KtmAnn) и [Anm–] = n·S(KtmAnn) в выражение для KSо(KtmAnn) и преобразования полученного выражения, получим формулу, связывающую S(KtmAnn) с Ksо(KtmAnn):
S(KtmAnn)=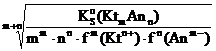
Данная формула используется для расчета молярной растворимости малорастворимых соединений в растворе индифферентного сильного электролита (электролита, не имеющего ионов общих с ионами осадка и химически не взаимодействующего с ними).
Для вычисления молярной растворимости в воде малорастворимых соединений используется формула:
S(KtmAnn) =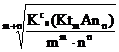
Зная молярную растворимость соединения KtmAnn, легко вычислить его массовую концентрацию (растворимость в г/л) по формуле:
ρ(KtmAnn) = S(KtmAnn)·M(KtmAnn)
и рассчитать массу малорастворимого электролита в любом объеме насыщенного раствора по формуле:
m(KtmAnn) = S(KtmAnn)·M(KtmAnn)·V(ppa),
где S(KtmAnn) – молярная растворимость KtmAnn, моль/л;
M(KtmAnn) – молярная масса KtmAnn, г/моль;
V(ppa) – объем насыщенного раствора KtmAnn, л.
Экспериментальная часть
Опыт 1. Смещение химического равновесия
в гомогенной системе
Смещение химического равновесия вследствие изменения равновесных концентраций реагирующих веществ изучается на примере обратимой реакции между хлоридом железа(III) и тиоцианатом калия. В результате реакции образуется тиоцианат железа(III), окрашивающий раствор в кроваво-красный цвет:
FeCl3 + 3KSCN ⇄ Fe(SCN)3 + 3KCl
Fe3+ + 3SCN– ⇄ Fe(SCN)3
Интенсивность окраски раствора зависит от концентрации Fe(SCN)3.
Смешайте в химическом стакане 20 мл дистиллированной воды с несколькими каплями насыщенных растворов FeCl3 и KSCN. Полученный раствор разделите на три пробирки.
Одну из пробирок оставьте для сравнения. Во вторую пробирку добавьте 5 капель насыщенного раствора FeCl3, а в третью – насыщенного раствора KSCN. Отметьте изменение окраски растворов в каждой из пробирок. Результаты эксперимента занесите в таблицу.
Вещество, концентрация которого увеличивается | Изменение окраски | Направление смещения равновесия |
FeCl3 | ||
KSCN |
Напишите выражение константы равновесия этой реакции и объясните изменение окраски растворов во второй и в третьей пробирках.
Опыт 2. Условия образования и растворения осадков
Налейте в 3 пробирки по несколько капель раствора хлорида бария, затем прилейте в первую из них раствор сульфата натрия, во вторую – раствор карбоната натрия, а в третью – раствор хромата калия до образования осадков. К каждому из осадков добавьте 2 моль/л раствор уксусной кислоты. Запишите Ваши наблюдения.
BaCl2 + Na2SO4 → BaSO4 + 2NaCl
BaCl2 + Na2CO3 → BaCO3 + 2NaCl
BaCl2 + K2CrO4 → BaCrO4 + 2КCl
BaSO4 + СH3COOH →
BaCO3 + 2СH3COOH → (СH3COO)2Ba + H2O + CO2
BaCrO4 + СH3COOH →
Напишите ионно-молекулярные уравнения реакций осаждения соединений бария и уравнение реакции растворения одного из них в уксусной кислоте. Объясните, почему только одна из малорастворимых солей бария растворилась в уксусной кислоте.
Опыт 3. Смещение химического равновесия
в гетерогенной системе
Возьмите в пробирку 5-6 капель раствора нитрата серебра и прибавьте 2-3 капли раствора хромата калия. Обратите внимание на цвет образующегося осадка.
К полученной смеси добавьте 5-6 капель раствора NaCl и перемешайте содержимое пробирки, обратите внимание на изменение цвета осадка.
К содержимому пробирки прибавьте 2-3 капли раствора Na2S и запишите цвет образовавшегося осадка.
Составьте уравнение реакций, описывающих превращение в ряду AgNO3 → Ag2CrO4 → AgCl → Ag2S.
Объясните Ваши наблюдения с использованием значений молярной растворимости соответствующих соединений.



