ИНДИВИДУАЛЬНОЕ ДОМАШНЕЕ ЗАДАНИЕ №2
ТЕМА Химическая кинетика и катализ
Варианты заданий
№ варианта | № задачи | ||
1 | 1 | 16 | 31 |
2 | 2 | 17 | 32 |
3 | 3 | 18 | 33 |
4 | 4 | 19 | 34 |
5 | 5 | 20 | 35 |
6 | 6 | 21 | 36 |
7 | 7 | 22 | 37 |
8 | 8 | 23 | 38 |
9 | 9 | 24 | 39 |
10 | 10 | 25 | 40 |
11 | 11 | 26 | 41 |
12 | 12 | 27 | 42 |
13 | 13 | 28 | 43 |
14 | 14 | 29 | 44 |
15 | 15 | 30 | 45 |
Задачи для самостоятельного решения
1. Скорость реакции ![]() при концентрации вещества А
при концентрации вещества А  и вещества В
и вещества В ![]() равна
равна ![]() . Вычислить константу скорости реакции.
. Вычислить константу скорости реакции.
2. Скорость реакции ![]() при концентрации вещества А
при концентрации вещества А  и вещества В
и вещества В ![]() равна
равна ![]() . Вычислить константу скорости реакции. Результат представить в стандартном виде.
. Вычислить константу скорости реакции. Результат представить в стандартном виде.
3. Скорость реакции ![]() при концентрации вещества А
при концентрации вещества А  равна
равна  . Вычислить константу скорости реакции.
. Вычислить константу скорости реакции.
4. Скорость реакции ![]() при концентрации вещества А
при концентрации вещества А  равна
равна 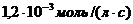 . Вычислить константу скорости реакции. Результат округлить до 4-го знака после запятой.
. Вычислить константу скорости реакции. Результат округлить до 4-го знака после запятой.
5. Скорость реакции ![]() при концентрации вещества А
при концентрации вещества А  и вещества В
и вещества В ![]() равна
равна ![]() . Вычислить константу скорости реакции.
. Вычислить константу скорости реакции.
6. Константа скорости реакции ![]() равна
равна ![]() . Определить скорость реакции при концентрациях вещества А
. Определить скорость реакции при концентрациях вещества А ![]() и вещества В
и вещества В ![]() . Результат выразить в
. Результат выразить в ![]() и представить в стандартном виде.
и представить в стандартном виде.
7. Константа скорости реакции ![]() равна
равна ![]() . Определить скорость реакции при концентрациях веществ:
. Определить скорость реакции при концентрациях веществ: 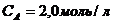 и
и 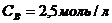 . Результат выразить в
. Результат выразить в ![]() .
.
8. Разложение ![]() на поверхности золота при высоких температурах протекает по уравнению
на поверхности золота при высоких температурах протекает по уравнению ![]()
Константа скорости данной реакции равна ![]() при
при ![]() . Начальная концентрация
. Начальная концентрация ![]()
![]() . Определить скорость реакции при заданной температуре в начальный момент времени. Результат выразить в
. Определить скорость реакции при заданной температуре в начальный момент времени. Результат выразить в ![]() .
.
9. Константа скорости реакции второго порядка
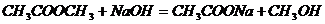
равна  . Определить скорость реакции, если концентрации щелочи и эфира одинаковы и равны
. Определить скорость реакции, если концентрации щелочи и эфира одинаковы и равны 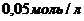 . Результат выразить в
. Результат выразить в ![]() .
.
10. В некоторой химической реакции первого порядка исходная концентрация вещества составляла ![]() . Вычислить скорость этой реакции в начальный момент времени, если константа скорости реакции равна
. Вычислить скорость этой реакции в начальный момент времени, если константа скорости реакции равна 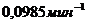 . Результат выразить в
. Результат выразить в ![]() и округлить до 3-го знака после запятой.
и округлить до 3-го знака после запятой.
11. В реакции ![]() константа скорости реакции равна
константа скорости реакции равна 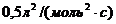 , а начальные концентрации веществ А и В равны соответственно
, а начальные концентрации веществ А и В равны соответственно  и
и  . Вычислить скорость химической реакции в момент, когда концентрация вещества В станет равной
. Вычислить скорость химической реакции в момент, когда концентрация вещества В станет равной ![]() . Результат выразить в
. Результат выразить в ![]() .
.
12. В реакции ![]() константа скорости реакции равна
константа скорости реакции равна 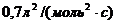 , а начальные концентрации веществ А и В равны соответственно
, а начальные концентрации веществ А и В равны соответственно  и
и  . Вычислить скорость химической реакции в момент, когда концентрация вещества В станет равной
. Вычислить скорость химической реакции в момент, когда концентрация вещества В станет равной ![]() . Результат выразить в
. Результат выразить в ![]() .
.
13. В реакции ![]() константа скорости реакции равна
константа скорости реакции равна 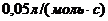 , а начальные концентрации веществ А и В равны соответственно
, а начальные концентрации веществ А и В равны соответственно  и
и  . Вычислить скорость химической реакции в момент, когда концентрация вещества А станет равной
. Вычислить скорость химической реакции в момент, когда концентрация вещества А станет равной ![]() . Результат выразить в
. Результат выразить в ![]() .
.
14. В реакции ![]() константа скорости реакции равна
константа скорости реакции равна 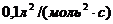 , а начальные концентрации веществ А и В равны соответственно
, а начальные концентрации веществ А и В равны соответственно  и
и  . Вычислить скорость химической реакции в момент, когда концентрация вещества В станет равной
. Вычислить скорость химической реакции в момент, когда концентрация вещества В станет равной ![]() . Результат выразить в
. Результат выразить в ![]() .
.
15. В реакции ![]() константа скорости реакции равна
константа скорости реакции равна 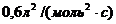 , а начальные концентрации веществ А и В равны соответственно
, а начальные концентрации веществ А и В равны соответственно  и
и  . Вычислить скорость химической реакции в момент, когда прореагирует 50% вещества А. Результат выразить в
. Вычислить скорость химической реакции в момент, когда прореагирует 50% вещества А. Результат выразить в ![]() .
.
16. В реакции ![]() константа скорости реакции равна
константа скорости реакции равна 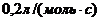 , а начальные концентрации веществ А и В равны соответственно
, а начальные концентрации веществ А и В равны соответственно 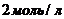 и
и  . Вычислить скорость химической реакции в момент, когда прореагирует 40% вещества А. Результат выразить в
. Вычислить скорость химической реакции в момент, когда прореагирует 40% вещества А. Результат выразить в ![]() .
.
17. В реакции ![]() константа скорости реакции равна
константа скорости реакции равна 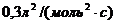 , а начальные концентрации веществ А и В равны соответственно
, а начальные концентрации веществ А и В равны соответственно  и
и 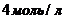 . Вычислить скорость химической реакции в момент, когда прореагирует 60% вещества А. Результат выразить в
. Вычислить скорость химической реакции в момент, когда прореагирует 60% вещества А. Результат выразить в ![]() .
.
18. Определить константу скорости реакции 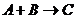 , если начальные концентрации веществ А и В одинаковы и равны
, если начальные концентрации веществ А и В одинаковы и равны  , а скорость реакции к моменту, когда концентрация вещества В уменьшиться на 50%, будет равна
, а скорость реакции к моменту, когда концентрация вещества В уменьшиться на 50%, будет равна ![]() . Результат выразить в
. Результат выразить в ![]() .
.
19. Определить константу скорости реакции 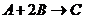 , если начальные концентрации веществ А и В равны соответственно
, если начальные концентрации веществ А и В равны соответственно  и
и 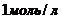 , а скорость реакции к моменту, когда концентрация вещества А уменьшится на 60%, будет равна
, а скорость реакции к моменту, когда концентрация вещества А уменьшится на 60%, будет равна ![]() . Результат выразить в
. Результат выразить в ![]() .
.
20. Определить константу скорости реакции 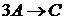 , если начальная концентрация вещества А равна
, если начальная концентрация вещества А равна ![]() , а скорость реакции к моменту, когда концентрация вещества А уменьшится на
, а скорость реакции к моменту, когда концентрация вещества А уменьшится на ![]() , будет равна
, будет равна ![]() . Результат выразить в
. Результат выразить в ![]() .
.
21. Во сколько раз увеличится скорость реакции 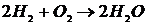 в газовой фазе, если давление увеличить в 3 раза.
в газовой фазе, если давление увеличить в 3 раза.
22. Во сколько раз увеличится скорость реакции 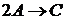 в газовой фазе, если давление увеличить в 3 раза.
в газовой фазе, если давление увеличить в 3 раза.
23. Во сколько раз увеличится скорость реакции 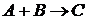 в газовой фазе, если давление увеличить в 2 раза.
в газовой фазе, если давление увеличить в 2 раза.
24. Во сколько раз увеличится скорость реакции 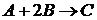 в газовой фазе, если давление увеличить в 2 раза.
в газовой фазе, если давление увеличить в 2 раза.
25. В гомогенной системе протекает химическая реакция 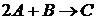 . Определить общий порядок реакции и порядок по веществу В. Реакцию считать идущей в одну стадию.
. Определить общий порядок реакции и порядок по веществу В. Реакцию считать идущей в одну стадию.
26. В гомогенной системе протекает химическая реакция 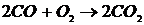 . Определить общий порядок реакции и порядок по веществу
. Определить общий порядок реакции и порядок по веществу ![]() . Реакцию считать идущей в одну стадию.
. Реакцию считать идущей в одну стадию.
27. В гомогенной системе протекает химическая реакция 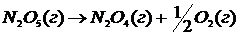 . Определить общий порядок реакции. Реакцию считать идущей в одну стадию.
. Определить общий порядок реакции. Реакцию считать идущей в одну стадию.
28. В гомогенной системе протекает химическая реакция 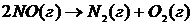 . Определить порядок реакции. Реакцию считать идущей в одну стадию.
. Определить порядок реакции. Реакцию считать идущей в одну стадию.
29. В гомогенной системе протекает химическая реакция 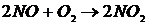 . Определить общий порядок реакции и порядок по кислороду. Реакцию считать идущей в одну стадию.
. Определить общий порядок реакции и порядок по кислороду. Реакцию считать идущей в одну стадию.
30. В некоторой химической реакции первого порядка исходная концентрация вещества составляла ![]() , а его концентрация через
, а его концентрация через 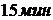 составила
составила 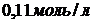 . Вычислить константу скорости реакции. Результат выразить в
. Вычислить константу скорости реакции. Результат выразить в ![]() и округлить до 3-го знака после запятой.
и округлить до 3-го знака после запятой.
31. В реакции первого порядка 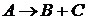 начальная концентрация вещества А составляла
начальная концентрация вещества А составляла ![]() , а его концентрация через 1 час составила
, а его концентрация через 1 час составила 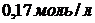 . Вычислить константу скорости реакции. Результат выразить в
. Вычислить константу скорости реакции. Результат выразить в ![]() , представить в стандартном виде и округлить до 1-го знака после запятой.
, представить в стандартном виде и округлить до 1-го знака после запятой.
32. В реакции первого порядка 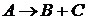 начальная концентрация вещества А составляла
начальная концентрация вещества А составляла ![]() , а его концентрация через 1 час составила
, а его концентрация через 1 час составила 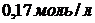 . Вычислить константу скорости реакции. Результат выразить в
. Вычислить константу скорости реакции. Результат выразить в ![]() , представить в стандартном виде и округлить до 1-го знака после запятой.
, представить в стандартном виде и округлить до 1-го знака после запятой.
33. Во сколько раз возрастет скорость реакции при повышении температуры с ![]() до
до 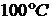 , если температурный коэффициент скорости реакции равен 2.
, если температурный коэффициент скорости реакции равен 2.
34. Температурный коэффициент скорости реакции равен 3,2. Во сколько раз увеличится скорость реакции, если повысить температуру на ![]() ? Результат округлить до целого числа.
? Результат округлить до целого числа.
35. Вычислить, во сколько раз возрастет скорость реакции при повышении температуры с ![]() до
до ![]() , если температурный коэффициент скорости реакции равен 3.
, если температурный коэффициент скорости реакции равен 3.
36. При повышении температуры на 70 К скорость реакции увеличилась в ![]() раз. Вычислить температурный коэффициент скорости. Результат округлить до 2-го знака после запятой.
раз. Вычислить температурный коэффициент скорости. Результат округлить до 2-го знака после запятой.
37. Вычислить температурный коэффициент скорости, если повышение температуры на 38 К вызвало возрастание скорости реакции в 140 раз. Результат округлить до 2-го знака после запятой.
38. Вычислить температурный коэффициент скорости, если повышение температуры на 65 К вызвало возрастание скорости реакции в 200 раз. Результат округлить до 2-го знака после запятой.
39. Рассчитать константу скорости реакции ![]() при температуре (
при температуре (![]() ), используя табличные данные кинетических параметров реакции. Результат выразить в
), используя табличные данные кинетических параметров реакции. Результат выразить в ![]() , представить в стандартном виде и округлить до 2-го знака после запятой.
, представить в стандартном виде и округлить до 2-го знака после запятой.
40. Рассчитать константу скорости реакции ![]() при температуре
при температуре ![]() , используя табличные данные кинетических параметров реакции. Результат выразить в
, используя табличные данные кинетических параметров реакции. Результат выразить в ![]() , представить в стандартном виде и округлить до 2-го знака после запятой.
, представить в стандартном виде и округлить до 2-го знака после запятой.
41. Рассчитать константу скорости реакции ![]() при температуре 300К, используя табличные данные кинетических параметров реакции. Результат выразить в
при температуре 300К, используя табличные данные кинетических параметров реакции. Результат выразить в ![]() , представить в стандартном виде и округлить до 1-го знака после запятой.
, представить в стандартном виде и округлить до 1-го знака после запятой.
42. Рассчитать константу скорости реакции второго порядка 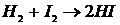 при температуре
при температуре ![]() , используя табличные данные кинетических параметров реакции. Результат выразить в
, используя табличные данные кинетических параметров реакции. Результат выразить в ![]() , представить в стандартном виде и округлить до 2-го знака после запятой.
, представить в стандартном виде и округлить до 2-го знака после запятой.
43. Рассчитать константу скорости реакции второго порядка 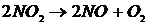 при температуре
при температуре ![]() , используя табличные данные кинетических параметров реакции. Результат выразить в
, используя табличные данные кинетических параметров реакции. Результат выразить в ![]() , представить в стандартном виде и округлить до 2-го знака после запятой.
, представить в стандартном виде и округлить до 2-го знака после запятой.
44. Рассчитать константу скорости реакции ![]() при температуре
при температуре ![]() , используя табличные данные кинетических параметров реакции. Результат выразить в
, используя табличные данные кинетических параметров реакции. Результат выразить в 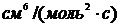 , представить в стандартном виде и округлить до 1-го знака после запятой.
, представить в стандартном виде и округлить до 1-го знака после запятой.
45. Рассчитать константу скорости реакции ![]() при температуре
при температуре ![]() , используя табличные данные кинетических параметров реакции. Результат выразить в
, используя табличные данные кинетических параметров реакции. Результат выразить в 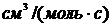 , представить в стандартном виде и округлить до 2-го знака после запятой.
, представить в стандартном виде и округлить до 2-го знака после запятой.



