МАТЕРИАЛ ИЗ
УЧЕБНО-МЕТОДИЧЕСКОГО ПОСОБИЯ
ПО СЕЛЬСКОХОЗЯЙСТВЕННОЙ РАДИОЭКОЛОГИИ
Часть I
ФИЗИЧЕСКИЕ И БИОЛОГИЧЕСКИЕ ОСНОВЫ
ДЕЙСТВИЯ ИОНИЗИРУЮЩИХ ИЗЛУЧЕНИЙ
СОДЕРЖАНИЕ
1. ФИЗИЧЕСКИЕ ОСНОВЫ ДЕЙСТВИЯ ИОНИЗИРУЮЩИХ ИЗЛУЧЕНИЙ | 1 | |
1.1 | Строение атома и изотопы | |
1.2 | Закон радиоактивного распада | |
1.3 | Виды излучений и их проникающая способность | |
1.3.1 | Электромагнитные (фотонные) излучения | |
1.3.2 | Корпускулярные излучения | |
1.4 | Особенности взаимодействия ионизирующих излучений с веществом | |
1.4.1. | Корпускулярные излучения | |
1.4.1.1. | Основные эффекты взаимодействия альфа-излучения с веществом | |
1.4.1.2. | Основные эффекты взаимодействия бета-излучения с веществом | |
1.4.1.3. | Взаимодействие нейтронов с веществом | |
1.4.2. | Электромагнитные излучения | |
Вопросы | ||
Список литературы | 12 | |
Приложение | 13 | |
1. ФИЗИЧЕСКИЕ ОСНОВЫ ДЕЙСТВИЯ ИОНИЗИРУЮЩИХ ИЗЛУЧЕНИЙ
1.1. Строение атома и изотопы
По своему строению атом похож на Солнечную систему в миниатюре: вокруг ядра движутся по орбитам электроны. Размеры ядра чрезвычайно малы по сравнению с пространственными характеристиками самого ядра: если диаметр атома составляет приблизительно 10-8см, то диаметр ядра – порядка 10-13см, т. е. ядро в сто тысяч раз меньше размеров атома. Масса атома настолько мала (10-22 – 10-24г), что ее принято выражать в относительных единицах атомных единицах массы (а. е.м.). 1 а. е.м. равна 1/12 массы атома углерода и соответствует 1,66·10-24г. Плотность ядра велика и масса ядра почти равна массе всего атома, практически вся масса атома заключена в его ядре.
Ядро, как правило, состоит из нескольких более мелких частиц – протонов и нейтронов, которые плотно сцеплены друг с другом. Протоны и нейтроны имеют общее название — нуклоны. Атом состоит из положительно заряженного ядра и оболочки из отрицательно заряженных электронов, которые могут располагаться только на определенных орбитах.
В зависимости от энергии, которая удерживает электроны при вращении вокруг ядра, они группируются на той или иной электронной орбите. Электронную орбиту называют еще уровнем или слоем. Число слоев у разных атомов неодинаково. В атомах с большой массой число орбит достигает семи. Их обозначают или цифрами, или буквами латинского алфавита: K, L,M, N,O, P,Q; K – ближайший к ядру слой. Число электронов в каждом слое строго определенное: K-слой имеет не более двух электронов, L-слой – до 8; M-слой – 18 электронов; N-слой – 32 электрона и т. д. Соответственно числу электронных слоев в Периодической системе химических элементов все элементы размещаются в семи периодах.
Электрон – устойчивая элементарная частица с массой покоя (масса частицы, скорость которой равно 0) равной 0,000548 а. е.м., а в абсолютных единицах массы – 9,1∙ 10-28г. (Энергетический эквивалент 1 а. е.м. составляет 931МэВ). Энергетический эквивалент электрона составляет 0,000548 · 931 = 0,511МэВ.
Электрон несет один элементарный отрицательный заряд электричества, т. е. наименьшее количество электричества, встречающееся в природе – 1,6·10-19Кл. Поэтому в ядерной физике заряд электрона принят за единицу.
Электроны на внутренних оболочках связаны с ядром наиболее прочно, на внешней (валентной) оболочке прочность связи наименьшая, так как взаимное отталкивание электронов в многоэлектронном атоме существенно уменьшает их связь с ядром.
Структура орбит и количество электронов на внешней оболочке определяют химическую индивидуальность элемента — его валентность, степень окисления и другие свойства. Таким образом, каждый электрон несет единичный (элементарный) электрический заряд, а общий отрицательный заряд электронной оболочки атома равен числу электронов.
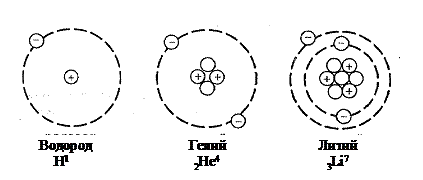
Рис.1 Схема строения атома
Атомы электронейтральны, поэтому ядро должно численно иметь тот же заряд, но со знаком (+). Носителями заряда в ядре являются протоны, каждый из которых обладает одним элементарным положительным зарядом (1,6·10-19Кл), следовательно, число протонов в ядре должно быть равно числу электронов на оболочках атома. Число протонов в ядре строго постоянно для атомов каждого данного элемента и соответствует порядковому номеру в Периодической таблице . Таким образом, число протонов в ядре определяет, к какому химическому элементу относится данный атом. Например (рис.1), 1 протон - в ядре водорода (первый период), 2 протона – в ядре гелия (первый период), 3 протона – в ядре лития (второй период). В ядре цезия (шестой период) – 55 протонов, а уран содержит 92 протона. Находясь вне ядра, протоны стабильны и не испытывают превращений.
Кроме того, в ядре содержатся нейтроны — частицы примерно той же массы, что и протоны, но не имеющие заряда, т. е. электрически нейтральные. Нейтроны в ядрах стабильны, а в свободном состоянии неустойчивы. При распаде нейтрон, испуская электрон и антинейтрино, высвобождает некоторое количество энергии (0,78МэВ) и превращается в протон.
Итак, в каждом атоме число электронов в точности равно числу протонов в ядре; каждый электрон несет отрицательный заряд, равный по абсолютной величине заряду протона, так что в целом атом нейтрален. Присутствие в ядре того или иного числа нейтронов отражается на общей массе атома, но не на его химических свойствах. Сумма числа протонов и нейтронов в ядре атома данного элемента называется его массовым числом, оно близко к значению атомного веса (атомной массы) элемента.
Таким образом, атом содержит всего три вида элементарных частиц, их заряд и масса приведены в таблице 1.
Таблица 1
Элементарные частицы ядра
Название частицы | Обозначение | Масса покоя, а. е.м. | Заряд |
Электрон | ē | 0,000548 = 1/1840 | -1 |
Нуклоны | |||
Протон | р | 1 | +1 |
Нейтрон | n | 1 | 0 |
Так как масса электрона в 1840 раз меньше массы протона или нейтрона, то суммарная масса атома почти целиком (на 99,97 - 99,98%) сосредоточена в ядре, тогда как на все орбитальные электроны приходится чуть больше 0,02% общей массы атома. При этом ядро в атоме занимает чрезвычайно малый объем. Линейные размеры атома имеют порядок 10-10м, а ядра – 10-15 м, т. е. в сотни тысяч раз меньше. Соответственно плотность материи в ядре – 1017кг/м3 (105т/мм3). Все остальное пространство в атоме (кроме ядра и электронов) представляет собой пустоту. Это важно иметь в виду при рассмотрении вопросов взаимодействия и поглощения излучений в веществе, т. е. для оценки вероятности столкновения (и электрического взаимодействия) при пролете частиц через атомы среды.
Атомы, имеющие определенный состав и структуру ядра, называются нуклидами. Индивидуальность нуклида определяется зарядом ядра (числом протонов), Но один и тот же элемент может иметь несколько разновидностей, которые различаются числом нейтронов, следовательно, атомной массой, сохраняя при этом практически одинаковые химические свойства.
Атомы, имеющие ядра с одинаковым числом протонов, но различающиеся по числу нейтронов, относящиеся к разновидностям одного и того же химического элемента, называемым изотопами (isos – одинаковый; topos – место) данного элемента. Такие элементы имеют одинаковый номер в таблице Менделеева, но разное массовf1ое число. Чтобы отличить их друг от друга, к символу элемента приписывают число, равное сумме всех частиц в ядре данного изотопа. Так уран-238 (238U) содержит 92 протона и 146 нейтронов, в уране-235 (235U) тоже 92 протона, но 143 нейтрона.
Каждый отдельный химический элемент может существовать в виде относительно устойчивых ядерных структур – стабильных изотопов, и неустойчивых – радиоактивных изотопов. Стабильность ядра определяется соотношением числа протонов и нейтронов: у большей части стабильных изотопов легких элементов оно составляет 1:1 или близко к этой величине. Но к концу периодической таблицы это соотношение постепенно уменьшается и достигает 1:1,6 (уран), при этом стабильность ядер резко снижается. При недостатке или избытке нейтронов (относительно некоего оптимального для данного элемента соотношения) ядерные структуры оказываются неустойчивыми, что приводит к возникновению радиоактивного распада. Это характерно для радиоактивных элементов, расположенных в конце таблицы Менделеева, образующих радиоактивные семейства (например, семейство 238U, 232Th и др.).
Понятия изотоп и радиоизотоп применимы лишь для обозначения разновидностей атомов одного элемента. Как уже говорилось, если атомы отличаются друг от друга не только массовым числом, но и химическими свойствами, то их называют нуклидами, а в том случае, если они обладают свойствами радиоактивности - радионуклидами. Некоторые нуклиды стабильны, т. е. в отсутствие внешнего воздействия никогда не претерпевают никаких превращений.
Радиоактивный распад происходит самопроизвольно: это внутриядерный процесс, на который обычные физические или химические факторы воздействовать не могут, т. е. не могут задержать или ускорить ход радиоактивных превращений.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



