Автономное профессиональное образовательное учреждение Чувашской Республики «Батыревский агропромышленный техникум» Министерства образования и молодежной политики Чувашской Республики
Методическая разработка
по дисциплине физика в помощь учащимся
по профессиям
190631.01 Автомеханик,
110308.02 Тракторист-машинист сельскохозяйственного производства.
Молекулярная физика
Основы МКТ
Основным положением молекулярно-кинетической теории является утверждение, что все тела состоят из мельчайших частиц (молекул, атомов и т. д.), которые движутся и взаимодействуют между собой. Доказательствами молекулярного строения вещества являются дробление тел, плавление, испарение, диффузия, броуновское движение и т. д.
Молярной массой M вещества называется масса такого количества молекул данного вещества, которое содержится в углероде 12C массой 12 г. Молярную массу вещества можно узнать по таблице Менделеева, сложив атомные массы всех атомов, входящих в молекулу этого вещества. При этом молярная масса будет измеряться в г/моль. Для перевода в систему СИ это значение следует умножить на 10-3. При этом молярная масса измеряется в кг/моль. Так, например, молярная масса водорода H2 равна 2 г/моль=2*103 кг/моль.
В одном моле любого вещества содержится NA = 6,022*1023 моль-1 молекул. Число NA называется постоянной Авогадро. Масса одной молекулы m0 выражается формулой
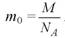
Количеством вещества v называется отношение числа молекул N к числу Авогадро NA :
![]()
Если m — масса вещества, то
![]()
Идеальным газом называется газ, в котором молекулы движутся свободно и взаимодействуют между собой и со стенками сосуда только при столкновениях. Модель идеального газа удовлетворительно описывает достаточно разреженные газы.
Среднеквадратичной скоростью молекул ![]()
называется следующая физическая величин
![]()
где v1, v2, v3,... — скорости молекул: первой, второй, третьей, и так далее до N. Отметим, что средняя скорость молекул равна нулю и не равна ![]()
Концентрацией молекул n называется отношение числа молекул N в объеме V к этому объему V:
![]()
Давление p можно выразить следующей формулой
![]()
Это уравнение носит название основного уравнения молекулярно кинетической теории (МКТ) газов. Это уравнение можно переписать в виде
![]() где ρ— плотность газа,
где ρ— плотность газа, ![]() — средняя кинетическая энергия молекулы газа. Средняя кинетическая энергия
— средняя кинетическая энергия молекулы газа. Средняя кинетическая энергия ![]() связана с температурой T газа формулой
связана с температурой T газа формулой
![]() где k—постоянная Больцмана. Она численно равна
где k—постоянная Больцмана. Она численно равна ![]()
Можно доказать следующую формулу:
![]()
Из нее следует уравнение Менделеева-Клапейрона
![]()
где
![]() — универсальная газовая постоянная.
— универсальная газовая постоянная.
При неизменной массе и составе газа
![]()
Если же постоянна еще и температура, то ![]() (изотермический процесс),
(изотермический процесс),
если давление постоянно, то ![]() (изобарный процесс),
(изобарный процесс),
если объем постоянен, то
![]() (изохорный процесс).
(изохорный процесс).
Водяной пар всегда присутствует в атмосфере Земли, как малая примесь, но он во многом определяет погоду. Влажность воздуха можно характеризовать парциальным давлением пара p или плотностью пара ρ (абсолютная влажность). Насыщенным паром называется пар, находящийся в динамическом равновесии со своей жидкостью. При определенной температуре существует такое давление, при котором водяной пар становится насыщенным. Такое давление рнас называется давлением насыщенного пара. Это давление можно найти по таблице в задачнике. Относительной влажностью φ называется отношение парциального давления пара p к давлению насыщенного пара
![]()
Если pнас — плотность насыщенного пара, то ![]()
В жидкостях имеет место явление поверхностного натяжения. Оно состоит в том, что жидкость стремится уменьшить свою энергию, минимизировав поверхность. Как известно, из всех тел заданного объема минимальной поверхностью обладает шар. Именно поэтому жидкость в невесомости приобретает шарообразную форму. Сила поверхностного натяжения F, действующая на тело длины l, выражается формулой
![]()
где σ — коэффициент поверхностного натяжения.
Пусть имеется твердое тело длинной l с площадью поперечного сечения S, которое под действием силы F удлинилось на Δl. Тогда имеет место формула
![]()
где
![]() напряжение в теле, Е — константа, которая называется модулем Юнга,
напряжение в теле, Е — константа, которая называется модулем Юнга,
![]() — относительное удлинение.
— относительное удлинение.
Молекулярно-кинетическая теория идеального газа. Основные положения
Молекулы в идеальном газе движутся хаотически. Движение одной молекулы характеризуют микроскопические параметры (масса молекулы, ее скорость, импульс, кинетическая энергия). Свойства газа как целого описываются с помощью макроскопических параметров (масса газа, давление, объем, температура). Молекулярно-кинетическая теория устанавливает взаимосвязь между микроскопическими и макроскопическими параметрами.
Число молекул в идеальном газе столь велико, что закономерности их поведения можно выяснить только с помощью статистического метода. Равномерное распределение в пространстве молекул идеального газа является наиболее вероятным состоянием газа, т. е. наиболее часто встречающимся.
Распределение молекул идеального газа по скоростям при определенной температуре является статистической закономерностью.
Наиболее вероятная скорость молекул — скорость, которой обладает максимальное число молекул. Стационарное равновесное состояние газа — состояние, в котором число молекул в заданном интервале скоростей остается постоянным.
Температура тела — мера средней кинетической энергии поступательного движения его молекул:
![]() где черта сверху — знак усреднения по скоростям, k = 1,38 • 10-23 Дж/К — постоянная Больцмана.
где черта сверху — знак усреднения по скоростям, k = 1,38 • 10-23 Дж/К — постоянная Больцмана.
Единица термодинамической температуры — кельвин (К).
При абсолютном нуле температуры средняя кинетическая энергия молекул равна нулю.
Средняя квадратичная (тепловая) скорость молекул газа
![]() где М — молярная масса, R = 8,31 Дж/(К • моль) — молярная газовая постоянная.
где М — молярная масса, R = 8,31 Дж/(К • моль) — молярная газовая постоянная.
Давление газа — следствие ударов движущихся молекул:
![]() где n — концентрация молекул (число молекул в единице объема), Ek — средняя кинетическая энергия молекулы.
где n — концентрация молекул (число молекул в единице объема), Ek — средняя кинетическая энергия молекулы.
Давление газа пропорционально его температуре:
![]()
Постоянная Лошмидта — концентрация идеального газа при нормальных условиях (атмосферное давление р= 1,01 • 105 Па и температура Т = 273 К): ![]()
Уравнение Клапейрона—Менделеева — уравнение состояния идеального газа, связывающее три макроскопических параметра (давление, объем, температуру) данной массы газа.
![]()
Изопроцесс — процесс, при котором один из макроскопических параметров состояния данной массы газа остается постоянным. Изотермический процесс — процесс изменения состояния определенной массы газа при постоянной температуре.
Закон Бойля—Мариотта: для газа данной массы при постоянной температуре:
![]()
где р1, р2, V1, V2 — давление и объем газа в начальном и конечном состояниях
Изотерма — график изменения макроскопических параметров газа при изотермическом процессе. Изобарный процесс — процесс изменения состояния определенной массы газа при постоянном давлении.
Закон Гей-Люссака: для газа данной массы при постоянном давлении
![]()
где V1, V2, T1, Т2— объем и температура газа в начальном и конечном состояниях.
Изобара — график изменения макроскопических параметров газа при изобарном процессе.
Изохорный процесс — процесс изменения состояния определенной массы газа при постоянном объеме. Закон Шарля: для газа данной массы при постоянном объеме
![]()
где p1, р2, T1, Т2 — давление и температура газа в начальном и конечном состояниях.
Изохора — график изменения макроскопических параметров газа при изохорном процессе.
Молекулярная структура вещества. Основные положения
Все вещества состоят из движущихся и взаимодействующих между собой атомов и молекул.
Простые вещества состоят из одинаковых атомов, сложные — из атомов различных химических элементов. Атом — наименьшая часть химического элемента, являющаяся носителем его свойств.
В центре атома находится положительно заряженное ядро, вокруг которого движутся отрицательно заряженные электроны, притягивающиеся к положительно заряженному ядру силами электромагнитного взаимодействия.
Главной характеристикой химического элемента является заряд ядра атома.
Z — зарядовое число ядра, равное числу протонов в ядре, совпадает с порядковым номером химического элемента в периодической системе химических элементов .
Атом электронейтрален: положительный заряд (+Ze) ядра компенсируется отрицательным зарядом (-Ze) электронов.
Кроме протонов, в ядре атомов содержатся нейтроны, связанные с протонами сильным взаимодействием. Общее название протонов и нейтронов, входящих в состав ядра, — нуклоны.
Массовое число А равно числу нуклонов в ядре (суммарное число протонов Z и нейтронов N):
![]()
Изотоп — разновидность одного и того же химического элемента, атом которого содержит одинаковое число протонов в ядре и разное число нейтронов.
В условном обозначении изотопа химического элемента указываются массовое число А и зарядовое число Z:
![]()
Масса атома меньше суммарной массы частиц, входящих в его состав.
Дефект массы — разность суммарной массы отдельных частиц, входящих в состав атома (ядра), и полной массы атома (ядра):
![]()
Дефект массы обусловливается выделением энергии ΔЕ при образовании атома:
![]()
Атомная единица массы (а. е.м.) — средняя масса нуклона в атоме углерода 126С.
Атомная единица массы равна 1/12 массы атома углерода 126С.
![]()
Относительная масса атома Мr — число атомных единиц массы, содержащихся в массе атома:
![]()
Моль — количество вещества, масса которого, выраженная в граммах, численно равна относительной массе атома.
Молярная масса — масса одного моля.
Единица молярной массы — килограмм на моль (кг/моль). Постоянная Авогадро — число атомов (или молекул) в одном моле любого вещества:
![]()
Молярная масса вещества
![]()
Существует четыре агрегатных состояния (или фазы) вещества: твердое, жидкое, газообразное, плазменное.
Фазовый переход — переход системы из одного агрегатного состояния в другое. При фазовом переходе скачкообразно изменяется какая-либо физическая величина (например, плотность, внутренняя энергия) или симметрия системы. Вещество находится в твердом состоянии, если средняя потенциальная энергия притяжения молекул много больше их средней кинетической энергии.
Молекулы в твердом теле располагаются упорядоченно.
Жидкое состояние образуется, если средняя потенциальная энергия притяжения молекул соизмерима с их средней кинетической энергией. Упорядоченное расположение молекул наблюдается в жидкости лишь в пределах нескольких соседних молекулярных слоев.
Вещество находится в газообразном состоянии, если средняя кинетическая энергия молекул превышает среднюю потенциальную энергию их взаимодействия. Молекулы газа движутся хаотически. Условия идеальности газа:
1)диаметр молекул много меньше среднего расстояния между ними;
2)средняя кинетическая энергия молекул много больше средней потенциальной энергии их взаимодействия;
3)молекулы взаимодействуют между собой и со стенками упруго. Плазма — электронейтральная совокупность нейтральных и заряженных частиц.
Ионизация — процесс образования ионов из атомов.



