Муниципальное Образовательное Учреждение лицей при ТПУ
Биохимические и биофизические характеристики коралловой воды
Работу выполнила:
Уразова Ксения, 11 класс
Научный руководитель:
, доцент ТПУ
Томск 2011
Оглавление
Введение………………………………………………………………………...3
Глава 1. Литературный обзор………………………………………………….3
Глава 2. Методы исследования ……………………………………………….5
2.1.Определение окислительно-восстановительного потенциала коралловой воды………………………………………………………............5
2.2.Определение водородного показателя коралловой воды……………………………………………………………………………..6
2.3. Определение поверхностного натяжения методом наибольшего давления образования газовых пузырьков (метод Ребиндера)………………………………………………………………………7
Глава 3. Экспериментальная часть……………………………………….......9
Глава 4.Выводы……………..………………………………………………...16
Глава 5. Список литературы………………………………………………….17
Введение
В настоящее время довольно остро стоит проблема чистой питьевой воды. Множество мировых компаний занимается разработкой альтернативных способов очистки питьевой воды, но, к сожалению, в большинстве случаев для них важнее оказывается прибыль, нежели реальная польза от их товаров.
Одним из способов улучшения качества воды является добавление пищевой добавки коралловый кальций «Alka Mine», которая представляет большой научный интерес, в частности в областях экологии и медицины.
Показано, что коралловая вода улучшает реологические свойства крови, показатели противоинфекционной защиты, обменные процессы.
Актуальность
Окислительно-восстановительный потенциал, pH, поверхностное натяжение, предельная адсорбция, проводимость являются основополагающими критериями для определения качества питьевой воды и её влияния на организм человека.
Глава 1. Литературный обзор
Современная история кораллового кальция началась в 1979 году, когда администрация института Гиннесса командировала британского журналиста на остров Токуносима (близ острова Окинава в Японии) взять интервью у господина Изуми, самого старого в то время жителя Земли. Журналист был удивлен здоровьем этого 115-летнего человека, который к тому же и работал до 105 лет. Оказалось, что источником питьевой воды для жителей островов Токуносима и Окинава является дождевая вода, скапливающаяся в природных резервуарах. Эти острова образовались на коралловых рифах. Впоследствии японское правительство начало разработку коралла.
В последние годы учёные занимаются активным исследованием белого коралла. Известны работы профессора Российского государственного медицинского университета г. Москвы , в которых определяются физико-химические характеристики минеральной композиции «Alka-Mine»[1]. По мнению академика : «Коралловая вода – палеоэкологическое воздействие девственной природы, несущей информацию из глубины веков…»[4].
Цель работы: выявить особенности биохимических и биофизических свойств воды с добавлением кораллового кальция
Задачи:
1) Оценить биохимические характеристики (окислительно-восстановительный потенциал, pH) коралловой, дистиллированной и водопроводной вод.
2) Определить биофизические свойства (поверхностное натяжение, предельная адсорбция, проводимость) коралловой, дистиллированной и водопроводной вод.
3) Рассчитать площадь, занимаемую одной молекулой коралловой воды в насыщенном адсорбционном слое на границе раздела фаз.
Глава 2. Методы исследования
Коралловую воду готовим растворением 1 г порошка белого коралла, приобретённого в Коралловом клубе, в полутора литрах дистиллированной воды.
Биохимические характеристики коралловой воды (pH и ОВП) определялись потенциометрическим методом с помощью стеклянного и хлорсеребряного электродов на приборе анион - 7051, проводимость - с платиновым электродом.
2.1. Определение окислительно-восстановительного потенциала коралловой воды
Принцип метода. В качестве индикаторного электрода обычно используют платиновый (очень редко золотой) электрод, а вспомогательного — хлорсеребряный или каломельный электрод. Платиновый электрод, введенный в среду, содержащую обратимые окислительно-восстановительные системы, приобретает ее потенциал. Скорость установления потенциала зависит от ряда факторов, среди которых главными являются окислительно-восстановительная емкость среды. Окислительно-восстановтиельная емкость — понятие, аналогичное буферной емкости. Она определяется концентрациями окисленных и восстановленных форм элементов с переменной валентностью в растворе. Процесс установления потенциала состоит в приобретении индикаторным электродом определенного заряда за счет окислителей или восстановителей раствора. В зависимости от ОВП среды электрод заряжается положительно или отрицательно. При этом наблюдается адсорбция определенных количеств атомарного кислорода или водорода, образующихся на электроде при разряде воды или ионов гидроксила и водорода.
Ход определения. Пробой воды для определения ОВП наполняют проточную ячейку непосредственно из водоисточника, давая протечь воде через ячейку в течение 5 мин. Ток воды прекращают и измеряют величину о.-в. потенциала. Через 10 и 20 мин производят еще два замера потенциала. Эти два значения ОВП не должны отличаться друг от друга более чем на 3—5 мВ.
Если разность больше 5 мВ, то измерения продолжают с интервалом в 10 мин до установления потенциала. Температуру воды измеряют термометром с точностью до 1° С. Проверка платиновых электродов. Проточную ячейку наполняют стандартным раствором для проверки платиновых электродов и помещают в термостат (25° С). Через 15 мин производят замер потенциала. Электроды, пригодные для работы, дают устойчивые показания, равные 233±5 мВ относительно хлорсеребряного электрода сравнения.
2.2. Определение водородного показателя коралловой воды
Принцип метода. Потенциометрический метод основан на измерении ЭДС электродной системы, состоящей из индикаторного электрода и электрода сравнения. Электрод сравнения иногда называют вспомогательным электродом. Наибольшее практическое применение нашел стеклянный индикаторный электрод, который можно использовать в широком диапазоне pH и в присутствии окислителей.
Стеклянный электрод изготовляется из специальных сортов стекла, обладающих некоторой электропроводностью, достаточной, чтобы тонкую пленку из такого стекла можно было бы включить в качестве составляющей электрической цепи. Для измерения pH используется стекло, электропроводность которого обусловлена перемещением в стекле ионов H+ (электропроводность любого стекла обусловлена способностью к перемещению катионов относительно неподвижного остова - полианиона полимерной кремниевой кислоты).
Ход определения. Для измерения pH стеклянный электрод погружают в испытуемый раствор (тем самым не внося в него никаких посторонних веществ). В этот же раствор напрямую или через электролитический ключ погружают электрод сравнения.
Таким образом, образуется гальванический элемент, состоящий из хлорсеребрянного электрода и электрода сравнения, но внутренняя электролитическая цепь этого элемента включает электропроводную стеклянную пленку, а также исследуемый раствор.
В полученной системе перенос электронов от хлорсеребрянного электрода к электроду сравнения, происходящий под действием непосредственно измеряемой разности потенциалов, неизбежно сопровождается переносом эквивалентного количества протонов из внутренней части стеклянного электрода в испытуемый раствор. Если считать концентрацию ионов H+ внутри стеклянного электрода постоянной, то измеряемая ЭДС является функцией только активности ионов водорода, т. е. pH исследуемого раствора.
2.3. Определение поверхностного натяжения методом наибольшего давления образования газовых пузырьков (метод Ребиндера)
Метод определения. Метод основан на измерении давления, при котором происходит отрыв пузырька газа (воздух), выдуваемого в жидкость через капилляр.
Ход определения.
1) Стеклянный сосуд 1 ополаскивают дистиллированной водой, наливают в него дистиллированную воду до уровня, при котором капилляр 3 только касался бы поверхности воды 2.
2) Открывают кран сосуда 4 и реуляруют скорость вытекания воды их этого сосуда так, чтобы пузырьки, проскакивающие из капилляра 3 в жидкость 2, появлялись через 3-5 секунд.
3) В момент проскока пузырьков фиксируют в мм максимальную разность уровней жидкости (Δh) в манометре 5 (ΔhH2O).
4) Воду из сосуда выливают и приливают в него раствор коллоидного ПАВ самой маленькой концентрации.
5) Аналогичным образом три раза измеряют значение Δh для этого раствора (Δhx).
6) Находят среднее значение Δh для каждого опыта
![]()
Взяв отношение ![]() , получим:
, получим: ![]()
Откуда:
Рис. 1 Экспериментальная установка для определения величины поверхностного натяжения методом наибольшего давления газовых пузырьков
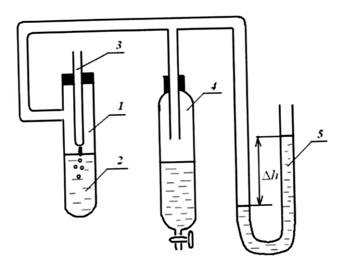
|
2. Жидкость;
3. Капилляр;
4. Стеклянный сосуд с дистиллированной водой;
5. Манометр.
Глава 3. Экспериментальная часть
Основные жизненные среды (кровь, лимфа, межклеточная жидкость и др.) имеют слабощелочную реакцию. При снижении щёлочности этих сред, меняются биохимические процессы, организм закислется. Это ведёт к развитию болезни. Поэтому вода, которую мы пъём, должна быть нейтральной, а лучше слабощелочной. По данным исследования водородный показатель коралловой воды 9,41, что оказывает полезное влияние на орагнизм человека.
Различие ОВП внутренней среды организма человека от -100 до -150 мВ, а питьевой - от 150 до 400 мВ. Это означает, что организм вынужден изменять ОВС питьевой воды. В результате ослабляется энергетический запас организма. ОВП коралловой воды изменяется от 458 до -95 мВ, что приближает её к внутренней среде человеческого организма. При такой ситуации клеткам организма не приходится тратить дополнительную энергию на выравнивание ОВП.
Проводимость определяет концентрацию электролита в воде. По полученным данным таблицы 1 проводимость коралловой воды в 8 раз выше, чем дистиллированной. Этот показатель является ключевым для осуществления биоинформации между клетками организма. Следовательно, коралловая вода улучшает межклеточную связь.
Таблица 1. Биохимические и биофизические характеристики коралловой воды
Проба воды | pH | ОВП(Eh), мВ | Проводимость, мкS/см |
Дистиллированная | 5,80 | 458 | 3,2 |
Alka – Mine | 9,41 | -95 | 24,7 |
Водопроводная | 7,27 | 247 | 602 |
Поверхностное натяжение (σ) исследуемой воды определось на установке Ребиндера (рис.1) по методу наибольшего давления газовых пузырьков. Получили значение 50 мДж/см. Для обычной водопроводной воды эта величина 73 дин/см. Белый коралл понижает поверхностное натяжение воды, делая воду более доступной для организма. По полученным нами данным белый коралл следует отнести к поверхностно – активным веществам (ПАВ). Исследована зависимость поверхностного натяжения (на границе – водный раствор – воздух) от конценрации ПАВ. Построена изотерма поверхностного натяжения σ = f(СПАВ)[2].
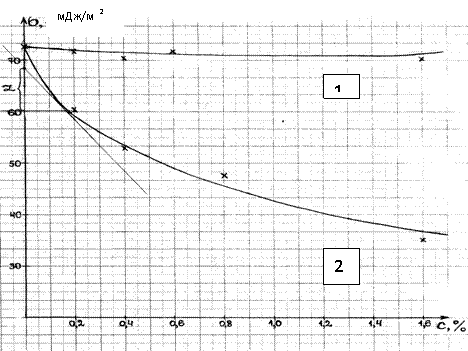
|
Таблица 2. Экспериментальные данные определения поверхностного натяжения раствора коралловой воды
Исследуемое Вещество | Концентрация белого коралла в воде, % | Полученное значение Δn, мм | Поверхностное натяжение σ*103 Дж/м2 | |||
I | II | III | Среднее значение | |||
H2O | 0 | 145 | 145 | 145 | 145 | 72,75 |
БК 1 | 0,2 | 120 | 125 | 120 | 121,67 | 61,04 |
БК 2 | 0,4 | 105 | 106 | 104 | 105 | 52,69 |
БК 3 | 0,8 | 95 | 96 | 95 | 95,3 | 47,81 |
БК 4 | 1,6 | 70 | 70 | 70 | 70 | 35,12 |
H2O | 0 | 70 | 70 | 72 | 70,67 | 72,75 |
Ca(OH)21 | 0,2 | 71 | 73 | 72 | 72 | 74,12 |
Ca(OH)2 2 | 0,4 | 72 | 70 | 71 | 71 | 73,09 |
Ca(OH)2 3 | 0,8 | 71 | 72 | 73 | 72 | 74,12 |
Ca(OH)2 4 | 1,6 | 70 | 71 | 72 | 71 | 73,09 |
Расчёт значений поверхностного натяжения коралловой воды:
Для белого коралла 1: σx=![]()
Для белого коралла 2: σx=![]()
Для белого коралла 3: σx=![]()
Для белого коралла 4: σx=![]()
Для Ca(OH)21: σx= ![]()
Для Ca(OH)22: σx= ![]()
Для Ca(OH)23: σx= ![]()
Для Ca(OH)24: σx= ![]()
С увеличением концентрации ПАВ величина поверхностоного натяжения уменьшается. Значит, белого коралла достаточно для получения «жидкой» воды, легкоусваиваемой организмом.
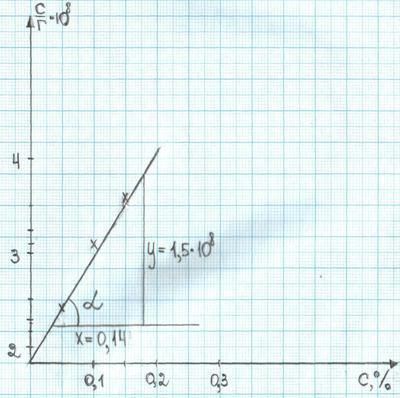
Зная зависимость поверхностного натяжения раствора от концентрации растворённого вещества, можно рассчитать изотерму адсорбции ПАВ методом графического дифференцирования экспериментальной кривой σ=f(C). Для этого в нескольких точках кривой σ=f(C) проводим касательные и определяем тангенсы угла их наклона, которые соответсвуют значениям производных δσ/δс в этих точках (рис.2). Зная значение этих производных, по уравнению адсорции Гиббса рассчитывают величины Г, что позволяет построить изотерму адсорбции Г=f(C).
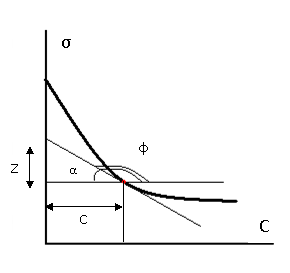 | |
| |
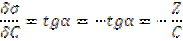
Подставим полученное значение в фундаментальное адсорбционное уравнение Гиббса:
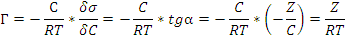
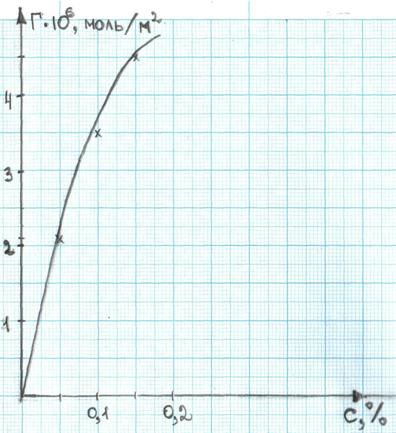
Таким образом, рассчитываем величины адсорбции Г для ряда точек на кривой и по расчитанным данным строим изотерму адсорбции в координатах Г=f(C).
Рассчитываем значение С/Г для каждой концентрации (таблица 3)
Для нахождения величины предельной адсорбции Г∞ строим изотерму адсорбции в координатах линейной формы С/Г=f(c) (рис.2).
|
Рассчитываем ёмкость адсорбционного монослоя Г∞ как котангенс угла наклона прямой.
![]() Г∞=ctgα=
Г∞=ctgα= ![]()
Таблица 3. Экспериментальные данные для расчета величины адсорбции.
С,% | Z*103,Дж/м2 | Г*106, моль/м2 | С/Г, м2/л |
0,05 | 5 | 2,05 | 2,4*108 |
0,10 | 8 | 3,25 | 3,1*108 |
0,15 | 10,5 | 4,25 | 3,5*108 |
Зная значение ![]() Г∞ определяем площадь, занимаемую одной молекулой коралловой воды в насыщенном адсорбционном слое на границе раздела фаз(S0).
Г∞ определяем площадь, занимаемую одной молекулой коралловой воды в насыщенном адсорбционном слое на границе раздела фаз(S0).
S0=![]()
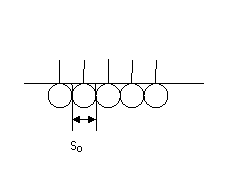 Величина S0 молекулы монослоя, вычисленная в результате эксперимента, позволяет говорить о мелкодисперсном состоянии белого коралла.
Величина S0 молекулы монослоя, вычисленная в результате эксперимента, позволяет говорить о мелкодисперсном состоянии белого коралла.
Таким образом, зная площадь частицы, возможно
рассчитать радиус молекулы кораллового кальция.
Предположим, что молекула исследуемого материала имеет форму шара (хотя данный случай является более идеализированным по сравнению с другими). Запишем: So=4πR2=1,8·10-15м2.
Выразим R=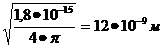
Выводы:
1) Кислотно-щелочное равновесие воды при добавлении белого коралла смещается в щелочную сторону, что приближает её к жидким средам человеческого организма.
2) Значение ОВП коралловой воды указывает на восстановительный характер среды, что важно для создания энергетического баланса в организме (так как клетки организма затрачивают меньшее количество энергии на выравнивание окислительно-восстановительного потенциала).
3) Коралловая вода является поверхностно-активным веществом (ПАВ).
Исследована зависимость поверхностного натяжения от концентрации белого коралла, то есть с увеличением концентрации белого коралла в воде величина поверхностного натяжения понижается. Проводимость коралловой воды в 8 раз выше, чем дистиллированной воды.
4) Размер молекулы монослоя коралловой воды в насыщенном адсорбционном слое на границе раздела фаз составляет 1,8·10-15 м2. Частицы, обладающие такиими размерами могут беспрепятственно проникать через клеточную мембрану человеческого организма, что обуславливает их высокую биологическую активность и высокую совместимость.
Список использованной литературы:
1) Баженков воды. Журнал «Натуральная фармакология и косметология», 2008, №2, стр. 3-6.
2) , Анисимова поверхностного натяжения. Расчёт молекулярных характеристик исследуемого ПАВ. Издательство ТПУ, Томск, 2009 г.;
3) «Вечное движение добра» (из выступлений, книг и статей). Новосибирск: Издатель, 2005: стр. 6,7,16.
4) Осипова оценки качества водных объектов. Изд-во , 2004.



