ЛАБОРАТОРНАЯ РАБОТА № 2
ХИМИЧЕСКИЕ СВОЙСТВА ЭЛЕМЕНТОВ IVA И VA ГРУПП
Теоретическая часть
Элементы IVA группы
Атомы элементов IVA группы (C, Si, Ge, Sn, Pb) в стационарном состоянии имеют электронную конфигурацию ns2np2. Углерод и кремний являются неметаллами, германий, олово, свинец - металлами. В соединениях элементы IVA группы проявляют степени окисления +4, +2, 0, и -4.
Свойства углерода и его соединений
Углерод образует три типа простых веществ: алмаз, графит и карбин. При обычной температуре углерод весьма инертен. При высоких температурах он взаимодействует со многими металлами и неметаллами. В большинстве реакций углерод проявляет восстановительные свойства. Окислительные свойства углерода выражены слабо.
Оксид углерода(II), как и SiO, NO, N2O, является несолеобразующим оксидом. Его можно получить горением углерода в недостатке кислорода:
2С + О2 ® 2СО,
или восстановлением диоксида углерода при нагревании:
CO2 + C ® 2CO.
Монооксид углерода (угарный газ) - сильный восстановитель, при повышенной температуре выделяет металлы из их оксидов:
3СO + Fe2O3 ![]() 2Fe + 3CO2
2Fe + 3CO2
CO + CuO ![]() Cu + CO2
Cu + CO2
Диоксид углерода (углекислый газ) - взаимодействует с водой, образуя слабую неустойчивую угольную кислоту H2CO3:
CO2 + H2O![]() H2CO3
H2CO3![]() H+ + HCO3-
H+ + HCO3-
Оксид углерода(IV) взаимодействует с основаниями, образуя карбонаты и гидрокарбонаты соответствующих металлов:
CO2 + Ca(OH)2 ® CaCO3¯ + H2O
CO2 + CaCO3¯ + H2O ® Ca(HCO3)2
В промышленности CO2 получают обжигом известняка при температуре выше 950оС:
CaCO3 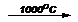 CO2 + CaO
CO2 + CaO
В лаборатории CO2 получают в аппарате Киппа, действуя на мрамор раствором хлороводородной кислоты:
CaCO3 + 2HCl ® CaCl2 + H2O + CO2
Образующийся СО2 очищают от примесей HCl и паров воды, пропуская последовательно через раствор гидрокарбоната натрия и концентрированную серную кислоту:
HCl + NaHCO3 ® NaCl + H2O + CO2
H2O + H2SO4(конц.) ® H2SO4×H2O
В соединениях с металлами углерод проявляет степени окисления -1 (CaC2), -4 (Al4C3) и др. Ацетиленид кальция CaC2 получают при высокой температуре сплавлением оксида кальция с углем:
СаО + 3С 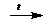 CaC2 + СО
CaC2 + СО
При взаимодействии с водой ацетиленид (“карбид”) кальция образует ацетилен:
CaC2 + 2H2O ® Ca(OH)2 + C2H2,
а карбид алюминия – метан:
Al4C3+ 12H2O ® 4Al(OH)3 + 3CH4
Cвойства кремния и его соединений
В обычных условиях кремний довольно инертен. С простыми веществами (кроме фтора) реагирует лишь при повышенной температуре.
В кислотах кремний пассивируется и растворяется лишь в смеси азотной и плавиковой кислот:
3Si + 4 HNO3 + 18HF ® 3H2SiF6 + 4NO + 8H2O
В растворах щелочей кремний активно растворяется с выделением водорода:
Si + 2NaOH + H2O ® Na2SiO3 + 2H2
Окислительные свойства кремния проявляются лишь в реакциях с некоторыми металлами:
2Mg + Si ® Mg2Si
Оксид кремния(IV) и его галогениды (SiF4, SiCl4 и др.) является кислотными, поэтому взаимодействуют со щелочами:
SiO2 + 2NaOH ® Na2SiO3 + H2O
SiCl4 + 6NaOH ® Na2SiO3 + 4NaCl+ 3H2O
Диоксид кремния, имеющий полимерное строение, не растворяется в воде, а галогениды кремния гидролизуются полностью, образуя соответствующие кислоты:
SiCl4 + 3H2O ® H2SiO3 + 4HCl
Кремниевая кислота очень слабая (слабее угольной) и незначительно растворимая в воде. Она может быть получена при действии более сильных кислот на ее соли - силикаты:
Na2SiO3 + 2HCl ® 2NaCl + H2SiO3¯
Кремниевая кислота при сильном нагревании разлагается на диоксид кремния и воду. Силикаты натрия и калия растворимы в воде, силикаты других металлов в воде не растворяются.
Свойства соединений олова и свинца
Гидроксиды олова и свинца обладают амфотерными свойствами с преобладанием основных свойств в соединениях металлов в степени окисления +2 и кислотных – в соединениях металлов в степени окисления +4:
SnCl2 + 2NaOH ® Sn(OH)2¯ + 2NaCl
Sn(OH)2¯ + 2HCl ® SnCl2 + 2H2O
Sn(OH)2¯ + 2NaOH ® Na2[Sn(OH)4]
SnCl4 + 4NH3 + 3H2O ® H2SnO3¯ + 4NH4Cl
H2SnO3¯ + 2NaOH + H2O ® Na2[Sn(OH)6]
H2SnO3¯ + 4HCl ® SnCl4 + 3H2O
Соединения олова(II) являются сильными восстановителями, а соединения свинца (IV) – сильными окислителями:
SnCl2 + 2FeCl3 ® 2FeCl2 + SnCl4
PbO2 + 4HCl ® PbCl2 + Cl2 + 2H2O
Элементы VA группы
Атомы элементов VA группы в стационарном состоянии имеют электронную формулу ns2np3. Азот, фосфор и мышьяк являются неметаллами, висмут и сурьма имеют металлические свойства. Наиболее характерные степени окисления: +5, +3, 0, -3. Оксиды всех элементов состава Э2О5 обладают кислотными свойствами. Свойства оксидов состава Э2О3 изменяются в зависимости от элемента: кислотные – в случае азота и фосфора, амфотерные – в случае мышьяка и сурьмы и основные – в случае висмута.
Свойства азота и его соединений
При обычных температурах азот химически инертен вследствие большой прочности его двухатомных молекул N2, имеющих тройную связь. Азот в промышленности используется для синтеза аммиака и дальнейшего получения из него азотных удобрений. Синтез аммиака из азота и водорода идет при высоких давлении и температуре в присутствии катализатора согласно уравнению:
N2 + 3H2 ![]() 2NH3
2NH3
Аммиак - бесцветный газ с резким запахом, ядовит, легче воздуха, хорошо растворим в воде (в 1 объеме воды при 20оС растворяется 710 объемов аммиака), В водных растворах аммиак является слабым основанием:
NH3 + H2O ![]() NH4+ + OH -
NH4+ + OH -
Основные свойства аммиака проявляются в его реакциях с кислотами:
NH3 + НСl ® NH4Cl
Аммиак обладает восстановительными свойствами. При горении на воздухе окисляется до азота, а в присутствии платинового катализатора при 600оС - до NO:
4NH3 + 3O2 ® 2N2 + 6H2O
4NH3 + 5O2 ![]() 4NO + 6H2O
4NO + 6H2O
Наличие неподеленной пары электронов на атоме азота молекулы аммиака обусловливает его донорные свойства в реакциях комплексообразования:
CuSO4 + 4NH3 ® [Cu(NH3)4]SO4
Cоли аммония при нагревании разлагаются:
NH4Cl ® NH3 + HCl
NH4NO2 ® N2 + 2H2O
NH4NO3 ® N2O + 2H2O
Оксид азота(II) - бесцветный газ, является восстановителем и легко окисляется кислородом воздуха до оксида азота(IV) - NO2:
2NO + O2 ® 2NO2
Оксида азота(IV) - газ бурого цвета, ядовит. При охлаждении димеризуется в бесцветный оксид N2O4. Диоксид азота - сильный окислитель: уголь, сера и фосфор горят в нем, а оксид серы(IV) окисляется до оксида серы(VI). Оксида азота(IV) взаимодействует с водой и щелочами, проявляя кислотные свойства:
2NO2 + H2O ® HNO3 + HNO2
4NO2 + 2H2O + O2® 4HNO3
2NO2 + 2NaOH ® NaNO3 + NaNO2 + H2O
4NO2 + 4NaOH + O2® 4NaNO3 + 2H2O
Оксид азота (III) N2O3 существует лишь при низких температурах. При 3,5oC кипит и разлагается:
N2O3 ® NO2 + NO
Оксиду азота (III) соответствует слабая азотистая кислота HNO2, которая существует лишь в разбавленных растворах и легко разлагается:
2HNO2 ® NO2 + NO + H2O
Соли азотистой кислоты (нитриты) устойчивы, для них характерны как окислительные, так и восстановительные свойства:
2NaNO2 + 2KI + 2H2SO4 ® I2 + 2NO + K2SO4 + Na2SO4 + 2H2O
2KMnO4 + 3H2SO4 + 5NaNO2® 2MnSO4 + 5NaNO3 + K2SO4 + 3H2O
Оксиду азота(V) соответствует азотная кислота HNO3. Получение азотной кислоты и ее солей основано на синтезе аммиака, его окислении до NO, дальнейшем окислении NО до NO2 и взаимодействии NO2 с водой в присутствии кислорода воздуха:
N2 + 3H2 ![]() 2NH3 ;
2NH3 ;
4NH3 + 5O2 ![]() 4NO + 6H2O
4NO + 6H2O
2NO + O2 ® 2NO2
4NO2 + O2 + 2H2O ® 4HNO3
Азотная кислота - сильная кислота, ее соли хорошо растворимы в воде. Азотная кислота и ее соли (нитраты) являются окислителями. Концентрированная азотная кислота не реагирует с Au и Pt, пассивирует на холоду Fe, Al и Cr, восстанавливается до NO2 в реакциях с тяжелыми металлами и до N2O в реакциях с активными металлами:
Cu + 4HNO3 (конц.) ® Сu(NO3)2 + 2NO2 + 2H2O
4Ca + 10HNO3 (конц.) ® 4Сa(NO3)2 + N2O + 5H2O
Разбавленная кислота восстанавливается до NO в реакциях c тяжелыми металлами и до N2 - c активными металлами. Очень разбавленная азотная кислота в реакциях с активными металлами восстанавливается до NH3 с образованием в качестве продукта реакции соли NH4NO3:
3Cu + 8HNO3 (разб.) ® 3Сu(NO3)2 + 2NO + 4H2O
4Ca + 10HNO3 (оч. разб.) ® 4Сa(NO3)2 + NH4NO3 + 3H2O
Азотная кислота при нагревании окисляет некоторые неметаллы (S, P, C, В) в соответствующую кислоту, восстанавливаясь при этом до NO2 в случае концентрированной и до NO в случае разбавленной кислоты:
S + 6HNO3 (конц.) ® H2SO4 +6NO2 + 2H2O
3P +5HNO3 (разб.) + 2H2O ® 3H3PO4+ 5NO
Нитраты металлов при нагревании разлагаются. Состав продуктов разложения зависит от положения металла в ряду напряжений. При разложении нитратов металлов, стоящих в ряду напряжений левее магния, образуются нитриты и кислород; от магния до меди включительно - оксид металла, оксид азота (IV) и кислород; а после меди - свободный металл, оксид азота (IV) и кислород:
2KNO3 ![]() 2KNO2 + O2
2KNO2 + O2
2Cu(NO3)2 ![]() 2CuO + 4NO2 + O2
2CuO + 4NO2 + O2
2AgNO3 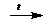 2Ag + 2NO2 + O2
2Ag + 2NO2 + O2
Свойства фосфора и его соединений
Фосфор образует несколько аллотропических модификаций: белый, красный и черный фосфор. Наиболее активен белый фосфор, молекулярная кристаллическая решетка которого построена из тетраэдрических молекул Р4. Красный фосфор имеет атомную кристаллическую решетку.
Фосфор в степени окисления -3 образует водородное соединение фосфин PH3. Фосфин (ядовитый газ с чесночным запахом) может быть получен из фосфида цинка действием кислот или воды:
Zn3P2 + 6HCl ® 2PH3 + 3ZnCl2
Фосфин обладает основными свойствами. Его основные свойства выражены слабее, чем у аммиака:
PH3 + HCl ® PH4Cl
Соли фосфония в водных растворах неустойчивы:
PH4+ + H2O ® PH3 + H3O+
Фосфин проявляет восстановительные свойства. На воздухе горит с образованием пентаоксида фосфора:
2PH3 + 4O2 ® P2O5 + 3H2O
Триоксид фосфора (P2O3 или Р4О6) образуется при окислении фосфора в недостатке кислорода и представляет собой белое кристаллическое вещество, плавящееся при 23,8оС. Он взаимодействует с водой, образуя слабую двухосновную фосфористую кислоту:
Р2О3 + 3Н2О ® Н3РО3,
которая с NaOH образует кислую соль NaH2PO3 и среднюю соль NaHPO3.
Пентаоксид фосфора (P2O5 или P4O10) образуется при горении фосфора на воздухе:
4Р + 5О2 ® 2Р2О5
При взаимодействии с водой оксид фосфора(V) образует на холоду метафосфорную кислоту НРО3, а при нагревании - ортофосфорную кислоту Н3РО4:
P2O5 + H2O ® 2HPO3
P2O5 + 3H2O ![]() 2H3PO4
2H3PO4
В промышленности ортофосфорную кислоту получают действием серной кислоты на фосфорит:
Ca3(PO4)2 + 3H2SO4 ® 3CaSO4 + 2H3PO4
Ортофосфорная кислота - хорошо растворимое в воде кристаллическое вещество (tпл = 42оС). В водных растворах является трехосновной кислотой. В реакциях нейтрализации образует средние и кислые соли. В воде хорошо растворимы все дигидрофосфаты, а также ортофосфаты и гидрофосфаты щелочных металлов и аммония.
Экспериментальная часть
Опыт 1.Адсорбционные свойства угля
Налейте в пробирку 2-3 мл разбавленного раствора красителя индиго и добавьте немного порошка активированного угля. После перемешивания смеси отфильтруйте уголь через бумажный фильтр. Запишите ваши наблюдения и объясните их.
Опыт 2. Получение и свойства оксида углерода (IV)
а) В пробирку поместите немного карбоната кальция, прилейте 1 - 2 мл 2 моль/л раствора соляной кислоты и закройте пробирку пробкой с газоотводной трубкой.
Соберите СО2 в другую пробирку и внесите в неё горящую лучину. Запишите ваши наблюдения и объясните их. Напишите уравнение реакции получения диоксида углерода в молекулярном и ионно-молекулярном виде.
б) Наполните углекислым газом (из подушки с СО2) химический термостойкий стакана на 100 мл и опустите в него, с помощью тигельных щипцов, стружку горящего магния. Происходит образование белого порошка MgO и чёрных частиц углерода. Запишите ваши наблюдения и уравнения реакций:
CaCO3¯ + 2HC1 ® CaC12 + CO2 +H2O
2Mg + CO2 ![]() 2MgO + C
2MgO + C
Реакцию обмена напишите в ионно-молекулярном виде, а окислительно-восстановительную реакцию уравняйте методом электронного баланса.
Опыт 3. Получение карбоната и гидрокарбоната кальция
Налейте в пробирку немного насыщенного раствора гидроксида кальция (известковой воды) и пропустите через него диоксид углерода (из подушки с CO2). Обратите внимание на образование осадка и последующие его растворение.
Запишите ваши наблюдения и соответствующие уравнения реакций в молекулярном и ионно-молекулярном виде:
Ca(OH)2 + CO2 ® CaCO3¯ + H2O
CaCO3¯ + H2O + CO2 ® Ca(HCO3)2
Опыт 4. Сравнение силы угольной и кремниевой кислот
В раствор силиката натрия пропустите оксид углерода (IV). Через некоторое время происходит образование геля кремниевой кислоты. Запишите и объясните ваши наблюдения. Напишите уравнение реакции в молекулярном и ионно-молекулярном виде:
Na2SiO3 + H2O + CO2 ® Na2CO3 + H2SiO3. ¯
Опыт 5. Получение малорастворимых солей кремниевой кислоты
В небольшой стеклянный стакан налейте 20 мл насыщенного раствора силиката натрия и опустите в него по несколько кристаллов следующих солей: CuSO4.5H2O, NiSO4.7H2O, Co(NO3)2.6H2O, FeSO4.7H2O, MnSO4.4H2O.
Обратите внимание на появление и рост окрашенных образований нерастворимых силикатов. Напишите уравнения реакций в молекулярном виде, отвечающих ионно-молекулярному уравнению:
SiO32– + Me2+ ® MeSiO3.
Опыт 6. Свойства аммиака
а) Основные свойства аммиака. Смочите дно и стенки стакана концентрированной соляной кислотой, остаток кислоты слейте. Поставьте тигель с раствором аммиака на основание чашки Петри и накройте тигель стаканом. Запишите ваши наблюдения. Напишите уравнение реакции образования соли аммония.
NH3 + HCl ® NH4Cl
б) Восстановительные свойства аммиака. К 2-3 мл бледно-розового (очень разбавленного) раствора перманганата калия добавьте несколько капель концентрированного раствора аммиака. Полученную смесь слегка подогрейте.
Запишите ваши наблюдения. Напишите уравнение реакции и уравняйте его методом ионно-электронного баланса:
2КMnO4 + 2NH3 ®2MnO2¯ +N2+ 2KOH + 2H2O
в) Качественная реакция на ион аммония. Налейте в пробирку немного раствора хлорида аммония и прибавьте 1-2 мл 2 моль/л раствора гидроксида натрия. Нагрейте раствор на водяной бане и поднесите к отверстию пробирки влажную фенолфталеиновую бумажку.
Запишите ваши наблюдения и напишите уравнение реакции в молекулярном и ионно-молекулярном виде:
NH4Cl + NaOH![]() NH3↑ + H2O + NaCl
NH3↑ + H2O + NaCl
Опыт 7. Окислительно-восстановительные свойства азотистой кислоты (нитритов)
Налейте в одну пробирку 1-2 мл иодида калия, в другую – разбавленного раствора перманганата калия. В каждую из них добавьте такой же объем 2 моль/л раствора серной кислоты и затем немного кристаллического нитрита калия.
Запишите ваши наблюдения. Напишите уравнения реакций и уравняйте их методом полуреакций:
2KI + 2H2SO4 + 2KNO2 ® I2 + 2NO + 2K2SO4 + 2H2O
2KMnO4+3H2SO4 + 5KNO2®2MnSO4 + 5KNO3 + K2SO4 + 3H2O



