Лабораторные работы
1. титриметрия
1.1. правила Работы
Точные объемы растворов в титриметрическом анализе отмеряют с помощью измерительной посуды – мерных колб, пипеток, бюреток. Титрование проводят, приливая титрант из бюретки к раствору определяемого вещества.
Бюретка градуирована в мл с делениями через одну десятую мл. Обычные бюретки имеют емкость 25 мл, а отсчет объема раствора в них дает три цифровых знака – десятки, единицы и десятые доли миллилитра. Сотые доли миллилитра определяют приближенно.
Заполнение бюреток раствором
Чистую бюретку заполняют титрантом, убеждаются в исправности затвора и отсутствии в нем пузырька воздуха. Для этого кончик бюретки поднимают и открывают зажим. Если жидкость идет ровной струей, без пузырьков воздуха, бюретка заполнена правильно. Наклоняя и поворачивая бюретку, смачивают стенки раствором, после чего сливают почти весь раствор через носик. Перед началом титрования бюретку устанавливают строго вертикально и заполняют титрантом до нуля. При этом уровень мениска жидкости вогнутой частью должен совпадать с нулевым делением шкалы (нулевое деление должно находиться на уровне глаз) для бесцветных растворов. Для окрашенных растворов нуль устанавливают по верхнему краю мениска.
Отмеривание растворов пипеткой
Чистую пипетку заполняют раствором до начала расширения, несколько раз поворачивают пипетку, стараясь смочить раствором всю внутреннюю поверхность немного выше метки. Сливают раствор.
Затем заполняют пипетку немного выше метки. «Держа» метку пипетки на уровне глаз, осторожно сливают избыток раствора так, чтобы мениск жидкости вогнутой частью совпадал с меткой. После этого пипетку переносят в другой сосуд и дают жидкости спокойно вытечь. После того как жидкость из пипетки стечет, последние капли сливают, касаясь дна или стенки сосуда, в который выливают жидкость. Выдувать жидкость из пипетки нельзя.
Правила титрования
Место, где проводится титрование, должно быть хорошо освещено. На основание штатива с бюреткой кладут лист белой бумаги. Бюретку укрепляют параллельно стержню штатива.
Титруют малыми порциями – по каплям. Открывают зажим бюретки левой рукой, а колбу для титрования держат правой, постоянно перемешивая ее содержимое вращательными движениями. После вытекания раствора отсчет делений на бюретке производят через 20-30 с, чтобы дать возможность стечь жидкости, оставшейся на стенках бюретки.
Отсчет снимают по нижнему (бесцветные растворы) или по верхнему (окрашенные растворы) краю мениска. Мениск должен находиться на уровне глаз. Для получения достоверных результатов повторяют титрование не менее трех раз. Каждое повторное титрование начинают с нулевого отсчета бюретки.
1.2. ОФОРМЛЕНИЕ ЛАБОРАТОРНЫХ РАБОТ
ПО ТИТРИМЕТРИИ
Лабораторные работы по титриметрии рекомендуется оформлять по нижеприведенной форме.
Определение массы вещества
Способ подготовки титруемого раствора:
Титруемое вещество (Х): Vколбы.= V(Х) = Vпип. =
Титрант (Т): С(1/z Т) =
Индикатор:
Уравнение реакции:
Способ проведения титрования:
Результаты титрования:
№ титрования | V(T), мл | V(T)ср., мл |
1 | ||
2 | ||
3 |
Формулы для расчета и расчет:
Лабораторная работа № 1
ОПРЕДЕЛЕНИЕ МАССЫ ЩЕЛОЧИ И КАРБОНАТА НАТРИЯ ПРИ ИХ СОВМЕСТНОМ ПРИСУТСТВИИ
Определение проводят способом пипетирования (аликвот). Титрантом является стандартизированный раствор НСl.
Взаимодействие смеси NаОН и Nа2СО3 с сильной кислотой можно рассматривать как процесс, протекающий в 3 стадии:
1. NaОН + НСl ® NаСl + Н2О,
ОН– + Н3О+ ® 2Н2О, (рНт. э. = 7)
2. Na2СО3 + НСl ® NaНСО3 + NaСl.
СО32– + Н3О+ ® НСО3– + Н2О, (рНт. э. = 8,32)
3. NаНСО3 + НСl ® NаСl + Н2СО3,
НСО3– + Н3О+ ® Н2СО3 + Н2О, (рНт. э. = 3,88)
При титровании с фенолфталеином (интервал рН изменения окраски 8,2 – 10,0) пройдут 1-й и 2-й процессы, а 3-й процесс может быть проведен с метиловым оранжевым (интервал перехода окраски 3,0 – 4,4).
Эти определения ведут последовательно, не дополняя бюретку кислотой.
Если на титрование с фенолфталеином пошло V1 мл НСl, а на титрование с метиловым оранжевым – V2 мл НСl, то объем кислоты, вступившей в реакцию с НСО3––ионом, равен (V2 – V1) мл; следовательно, с СО32––ионом – 2(V2 – V1) мл. Объем кислоты, прореагировавшей со щелочью, определяется выражением [V2 – 2(V2 – V1)] = (2 V1 – V2) мл.
Масса гидроксида натрия и карбоната натрия рассчитываются по формулам:
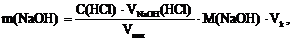
где VNaOH(HCl) = (2V1 – V2)∙10-3 л,
Vпип – аликвота анализируемого раствора, равная вместимости пипетки, л,
Vk – объем анализируемого раствора, равный вместимости мерной колбы, л.
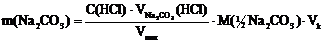
где ![]() = 2(V2 – V1)∙10-3 л.
= 2(V2 – V1)∙10-3 л.
Vпип – аликвота анализируемого раствора, равная вместимости пипетки, л,
Vk – объем анализируемого раствора, равный вместимости мерной колбы, л.
Ход работы
1. Получите у лаборанта раствор смеси NаОН и Nа2СО3 в мерную колбу и добавьте дистиллированной воды до метки. Перемешайте.
2. Заполните бюретку стандартизированной хлороводородной кислотой.
3. Отмерьте пипеткой раствор смеси NаОН и Nа2СО3. Перенесите в колбу для титрования. Добавьте дистиллированной воды и 2-3 капли фенолфталеина.
Оттитруйте аликвоту анализируемого раствора хлороводородной кислотой до исчезновения розовой окраски фенолфталеина. Объем кислоты, пошедшей на титрование, обозначим V1.
4. В этот же раствор добавьте 3-5 капель метилового оранжевого. Раствор станет желтым. Оттитруйте хлороводородной кислотой до оранжевой окраски индикатора. Общий объем кислоты, пошедшей на оба титрования, обозначим V2.
5. Титрование повторите не менее трех раз до получения сходящихся результатов.
6. Рассчитайте массу гидроксида натрия и карбоната натрия в растворе.
Лабораторная работа № 2
ОПРЕДЕЛЕНИЕ МАССЫ ЖЕЛЕЗА(II) В РАСТВОРЕ
МЕТОДОМ ПЕРМАНГАНАТОМЕТРИИ
Определение железа(II) проводят прямым титрованием раствором перманганата калия в присутствии серной кислоты по реакции:
5Fe2+ + MnO4– + 8H3O+ → 5Fe3+ + Mn2+ + 12H2O.
Титрование надо проводить при комнатной температуре, при нагревании происходит окисление железа(II) кислородом воздуха.
В результате реакции образуются окрашенные ионы Fe3+, которые могут мешать определению конечной точки титрования. Изменение цвета раствора в конце титрования наблюдается более отчетливо при добавлении 5 мл 85% фосфорной кислоты. Последняя образует с ионами железа(III) бесцветный комплекс Fe(НРО4)2–, поэтому раствор в конце титрования не желтеет от накопления в нем Fe3+-ионов.
Ход работы
1. Получите у лаборанта мерную колбу с раствором соли железа (II), доведите объем до метки дистиллированной водой, закройте колбу пробкой и хорошо перемешайте.
2. Заполните бюретку стандартизированным раствором КМnО4.
3. Отмерьте пипеткой раствор соли железа (II), перенесите его в колбу для титрования, добавьте 15 мл 1 моль/л Н2SО4, немного воды и 5 мл 85% Н3РО4.
4. Оттитруйте раствор соли железа(II) перманганатом калия до появления неисчезающей розовой окраски. Проведите несколько титрований до получения сходящихся результатов.
5. Рассчитайте массу железа(II) в растворе.
Лабораторная работа № 5
Определение массы кальция в растворе МЕТОДОМ Комплексонометрии
Раствор, содержащий ионы кальция титруют ЭДТА в присутствии аммиачного буфера, индикатор - эриохром черный Т. Титрование проводят методом пипетирования.
Ход работы
1. Получите у лаборанта мерную колбу с раствором смеси CaCl2. Доведите объем раствора до метки дистиллированной водой, хорошо перемешайте.
2. Заполните бюретку стандартизированным раствором ЭДТА.
3. В колбу для титрования отмерьте пипеткой исследуемый раствор, прибавьте 2-3 мл аммиачного буфера, 15 мл воды, немного твердого эриохрома черного Т. Оттитруйте полученный раствор раствором ЭДТА до изменения окраски в синюю. Повторите титрование не менее трех раз.
4. Рассчитайте массу ионов кальция в растворе.
2. ФОТОМЕТРИЯ
2.1. Общие указания к лабораторным работам
по фотометрическому анализу
1. Прежде, чем приступить к выполнению лабораторной работы, необходимо внимательно прочитать методические указания по выполняемой работе, познакомиться с порядком выполнения измерений на приборе.
2. Строго следовать методике приготовления растворов. Особенно важно соблюдать указанный порядок прибавления реагентов.
3. Кюветы, в которых проводят измерение интенсивности поглощения, должны быть чистыми. Их обычно обрабатывают концентрированной хлороводородной кислотой, промывают проточной водой, ополаскивают дистиллированной водой и насухо вытирают снаружи. Перед заполнением кювету ополаскивают небольшой порцией испытуемого раствора во избежание его разбавления.
4. Кюветы заполняют до такого уровня, чтобы поток излучения целиком проходил через слой раствора и устанавливают в кюветное отделение всегда в строго определенном положении. Это позволяет избежать ошибок, связанных с неодинаковым отражением и рассеянием излучения.
5. Измерение на приборе проводят 2-3 раза до получения воспроизводимых результатов.
6. По окончании работы прибор необходимо выключить, как указано в инструкции, и тщательно вымыть кюветы.
Лабораторная работа №1
Фотоэлектроколориметрическое определение
массы меди(II) в растворе
Метод основан на измерении интенсивности окраски аммиачного комплекса меди(II) [Cu(NH3)4]2+, имеющего максимум поглощения при l = 610 нм.
Приготовление эталонных растворов и испытуемого раствора
Ход работы
1. В 5 мерных колб емкостью 50,0 мл градуированной пипеткой емкостью 10,00 или 5,00 мл поместите последовательно 0,5; 1,0; 1,50; 2,00; 2,50 мл стандартного раствора соли меди(II), содержащего 5,0 мг меди в 1 мл. Затем в каждую колбу добавьте по 5 мл раствора аммиака (1:1), доведите водой до метки и тщательно перемешайте.
2. Рассчитайте титр Тi(Cu2+) и молярную концентрацию Сi(Cu2+) полученных эталонных растворов.
3. К полученному у лаборанта анализируемому раствору в мерной колбе емкостью 50,0 мл добавьте 5 мл аммиака (1:1). Доведите объем до метки водой и тщательно перемешайте.
Измерение оптической плотности растворов
Ход работы
1. Измерьте оптическую плотность приготовленных эталонных растворов меди(II) при l = 610 нм в кювете с толщиной слоя 1,0 см. В качестве раствора сравнения возьмите воду. Повторите каждое измерение. Результаты измерений занесите в таблицу.
2. Измерьте оптическую плотность приготовленного раствора (Ах) в тех же условиях, что и эталонных растворов.
Оптические характеристики эталонных растворов меди (II)
(Прибор, l = , толщина слоя 1,0 см)
№ эталонного р-ра | Объем стандартного раствора, мл | Титр эталонного раствора, Тi, мг/мл | Ai1 | Ai2 | Āi |
|
1 | 0,50 | |||||
2 | 1,00 | |||||
3 | 1,50 | |||||
4 | 2,00 | |||||
5 | 2,50 | |||||
Х |
Определение массы меди(II) в растворе
1. Построение градуировочного графика.
По данным таблицы постройте градуировочный график, откладывая на оси абсцисс титр меди(II) в растворе Ti(Cu2+), а на оси ординат - оптическую плотность Āi.
При соблюдении закона Бера получают прямую, проходящую через начало координат.
Вклейте градуировочный график в лабораторную тетрадь.
2. Определение массы меди(II) в анализируемом растворе с помощью градуировочного графика.
По градуировочному графику найдите титр меди(II) Tx(Cu2+) в анализируемом растворе, соответствующий оптической плотности Ах, и рассчитайте массу меди(II) m(Cu2+), в мг в испытуемом растворе по формуле:
m(Cu2+) = Tx(Cu2+)×V(Cu2+),
где V(Cu2+) - общий объем испытуемого раствора, мл.



