Лекции ФХФ. 31 октября 2011
Лекция 10. Оксокислоты галогенов.
§ 1. Характерные степени окисления.
-1
| 0
| +1
| +3
| (+4)
| +5
| (+6)
| +7
|
НГ
| Г2
| НОГ
| НГО2
| | НГО3
| -
| НГО4
|
(а) Степень окисления (СО) – формальное число электронов, которое отдает или принимает частица.
 (b) Характерны нечетные СО.
(b) Характерны нечетные СО.
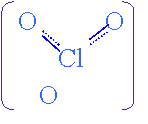
(с) Реальный заряд: КCld O3
d = 0,7
§ 2. Получение.
2.1. Получение HFO:
 F2 + H2O HOF + HF
F2 + H2O HOF + HF
(a) Не диссоциирует
(b) Не образует солей
(c) HOF + H2O = H2O2 + HF
Но: 2F2 + 2H2O 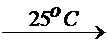 4HF + O2
4HF + O2
2.2. (а) Cl2 + H2O = HCl + HClO
(b) HCl + 2 HgO ® 2 HgO · HgCl2¯

 2Cl2 + H2O + (n + 1)HgO = 2HClO + nHgO · HgCl2 ¯
2Cl2 + H2O + (n + 1)HgO = 2HClO + nHgO · HgCl2 ¯
или
(а) Cl2 + H2O = HCl + HClO
 (b) Na2CO3 + 2HCl = 2NaCl + CO2 + H2O
(b) Na2CO3 + 2HCl = 2NaCl + CO2 + H2O

2Cl2 + H2O + Na2CO3 = 2HClO + 2NaCl + CO2
2.3. HXO3
Ba(XO3)2 + H2SO4 = + BaSO4 ¯
Х = Cl, Br
3I2, ТВ. + 10 HNO3 = + 10 NO2 + 2H2O
2.4. HXO4


KClO4 + H2SO4 HClO4 + KHSO4
NaBrO4 + H2SO4 = HВrO4 + NaHSO4
Ba3(H2IO6)2 + 3H2SO4 = 2H5IO6 + 3BaSO4 ¯
§ 3. Строение

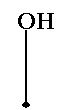
 1. Н – О Ð НОХ = 103о
1. Н – О Ð НОХ = 103о
Х
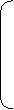
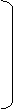


 2. Х ХО
2. Х ХО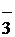 - пирамида
- пирамида



Н – О Cl
Особенность HIO3
HIO3 + HIO3 ⇄ [H(IO3)2]- ; K = 4,
поэтому из кислых растворов
кристаллизуются кислые соли
KH(IO3)2 ; KH2(IO3)3
3.

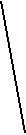 XO
XO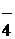 - тетраэдр
- тетраэдр






H – O Cl
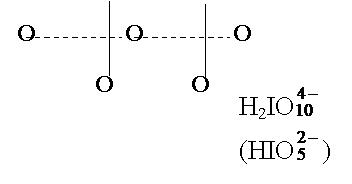
4. Иодная кислота HIO4 × 2H2O = H5IO6

 IO
IO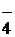 HIO4 + 2H2O = H5IO6
HIO4 + 2H2O = H5IO6 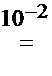 H4IO
H4IO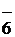
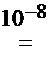 H3IO
H3IO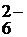
TeO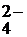 ® H2TeO4 · 2H2O = H6TeO6
® H2TeO4 · 2H2O = H6TeO6
H5IO6 ® За счет водородных связей Н – О Н
октаэдры образуют трехмерный каркас.
H5IO6 = [IO(OH)5] = HIO4 × 2H2O







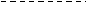


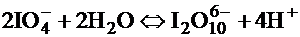
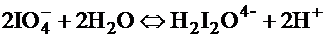
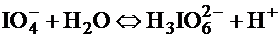
§ 4. Кислотные свойства.
Факторы: а) число концевых атомов кислорода;
b) размер и электроотрицательность атомов галогенов;
с) сила оксокислот галогенов растет справа налево и сверху вниз.
СО

 +1 HOCl HOBr HOI
+1 HOCl HOBr HOI

 +5 HClO3 HBrO3 HIO3
+5 HClO3 HBrO3 HIO3
+7 HClO4 HBrO4 HIO4
(H5IO6)
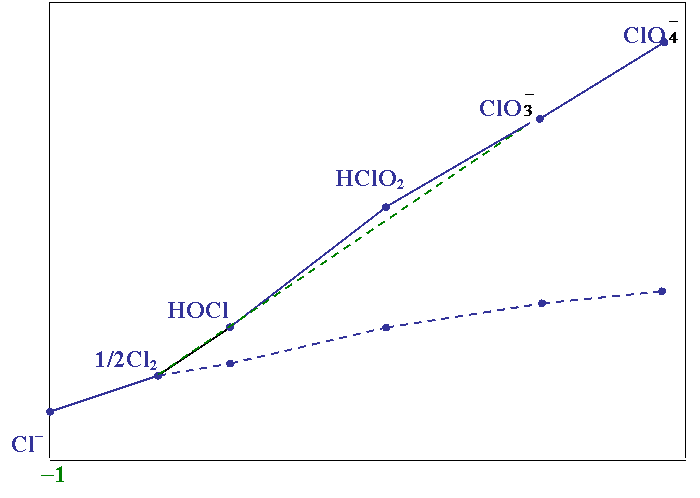
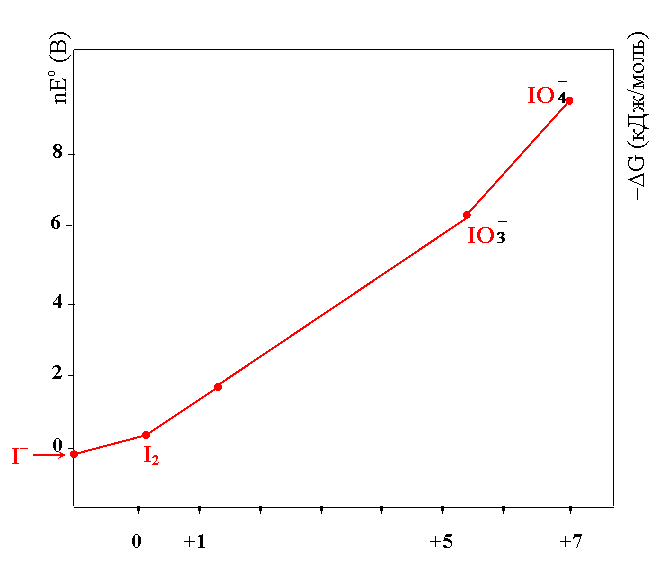
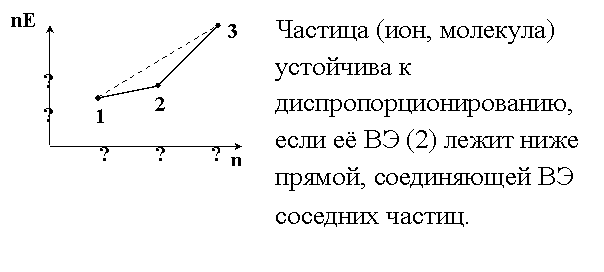
§ 5. Диаграммы окислительных состояний.
(1) А+ + = Ао ; Е ; nEo = ВЭ1 = Е × 1
 (2) А+ + + 2е = Ао ; Е ; nEo = ВЭ2 = Е × 2
(2) А+ + + 2е = Ао ; Е ; nEo = ВЭ2 = Е × 2
(3) nEo = - DGo
Построение
Правила:
1. Наклон (tga) прямой, соединяющей ВЭ двух частиц, равен потенциалу данной пары
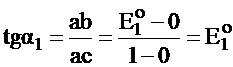
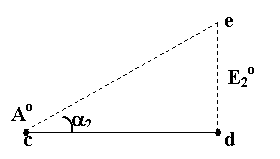
2. Больший наклон соответствует большему окислительному потенциалу,
т. е. tg a2 > tg a1; 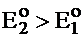 , поэтому
, поэтому
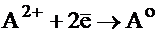 , но
, но
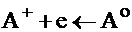
3.
Частица 2 неустойчива по отношению к 1 и 3, если её ВЭ лежит выше прямой (1–3), соединяющей ВЭ соседних частиц:
|
|
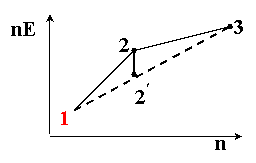 |
DG(2¢) < DG(2)
4.
§ 6.Окислительные свойства оксокислот галогенов
(а) 2KI + Cl2 = I2 + 2KCl
(b) Cl2 + H2O = HClO + HCl
(c) 3HClO = 2HCl + HClO3
(d) HClO3 + I2 = 2HIO3 + Cl2
(e) I2 + 3Cl2 = 2ICl3
Осциллирующие реакции
(а) 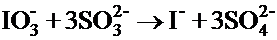
(b) 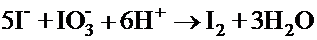
(c) 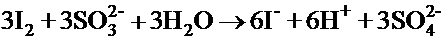
Окраска = f (c /c )
c /c = f (время)
§ 6.Окислительные свойства оксокислот галогенов
(а) 2KI + Cl2 = I2 + 2KCl
(b) Cl2 + H2O = HClO + HCl
(c) 3HClO = 2HCl + HClO3
(d) HClO3 + I2 = 2HIO3 + Cl2
(e) I2 + 3Cl2 = 2ICl3
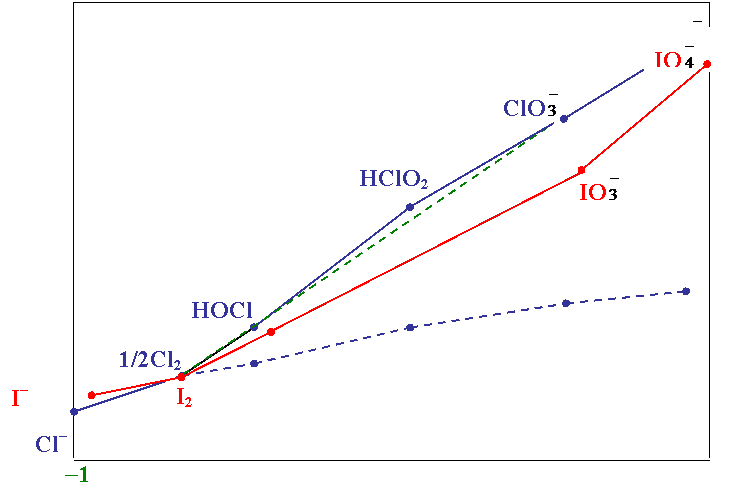
2NaBrO3 + I2 = 2NaIO3 + Br2
NaBrO3 + Cl2 ® не идет
BrO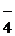
|
|



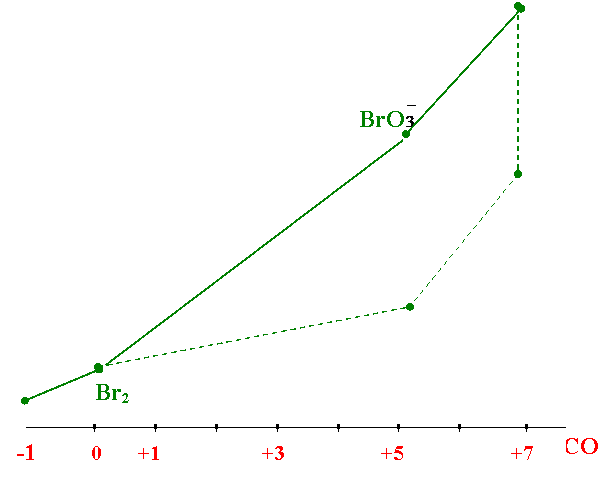
§ 7. Окислительные свойства оксокислот хлора
1. Сильные окислители
2. Термодинамический аспект: DrGo < 0
Cl2 » HClO > HClO2 > HClO3 > HClO4
Fe2+ ® Fe3+ HClO, но не HClO4
Mg + HClO4 = Mg(ClO4)2 + H2
3. Кинетический аспект: скорость реакций с изменением степени окисления:
а) прямой перенос электронов
b) перенос отдельных атомов: Cl+, O



 HOCl + :SO = [HO – Cl–SO3] 2-®OH - + ClSO
HOCl + :SO = [HO – Cl–SO3] 2-®OH - + ClSO
 ClSO + H2O ® SO +2H+ + Cl -
ClSO + H2O ® SO +2H+ + Cl -

с) HClO > HClO2 > HClO3 > HClO4
4. Термодинамический и кинетический прогноз совпадают.
5. V = f (pH): чем ниже рН, тем выше скорость
8KClO3 + C12H22O11 ® 8KCl + 12CO2 + 11H2O
Причины: а) протонирование Р и ослабление Cl–О


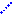
 ¤ + H =
¤ + H =
ClO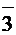
|
|
b) Увеличение электрофильности Сl

 HCl
HCl
6.
HClO4 + KHSO4 +ClO2 + H2O
|
|
 КСlO3
КСlO3

§ 8. Термодинамическая и кинетическая стабильность (ТС и КС)
1. Термодинамическая стабильность – невозможность самопроизвольно превратиться в другие соединения:

 DrGo = - = -RTlnK
DrGo = - = -RTlnK
2. Прогноз с помощью диаграмм ВЭ–СО.
3. (а) 3HClO = HClO3 + 2HCl; E1 > 0; DrG1o < 0; K = 1027
(b) 3HClO2 = 2HClO3 + HCl
(c) 4HClO3 = 3HClO4 + HCl ; K = 1029
(d) 5HClO = 2Cl2 + HClO3 + 2H2O
(e) 7HClO3 = Cl2 + 5HClO4 + H2O
 4. Повышение ТС: HClO ® HClO2 ® HClO3 ® HClO4
4. Повышение ТС: HClO ® HClO2 ® HClO3 ® HClO4
5. Кинетическая стабильность – малые скорости превращения в …
(а) рост энергии связи и аквации в ряду HClO ® HClO4;
Факторы: (b) увеличение экранировки атома хлора в ряду
HClO ® HClO4;
(с) трудность зарождения газовой фазы в
жидкости.
6. Повышение КС в ряду: HClO®HClO2®HClO3®HClO4
(100% р-р)
7. Общие итоги: а) Совпадение тенденций ТС и КС.
b) Все кислоты неустойчивы, но соли более устойчивы: электростатическое взаимодействие К+ + А- повышает энергию кристаллической решетки, а значит, и ТС + КС.
 (b) Характерны нечетные СО.
(b) Характерны нечетные СО. F2 + H2O HOF + HF
F2 + H2O HOF + HF 4HF + O2
4HF + O2 ![]()
 2Cl2 + H2O + (n + 1)HgO = 2HClO + nHgO · HgCl2 ¯
2Cl2 + H2O + (n + 1)HgO = 2HClO + nHgO · HgCl2 ¯![]() (b) Na2CO3 + 2HCl = 2NaCl + CO2 + H2O
(b) Na2CO3 + 2HCl = 2NaCl + CO2 + H2O

![]()

![]() 1. Н – О Ð НОХ = 103о
1. Н – О Ð НОХ = 103о![]()
![]()
![]()
![]()
![]() 2. Х ХО
2. Х ХО![]() - пирамида
- пирамида![]()
![]()
![]()
![]()
![]()


![]() XO
XO![]() - тетраэдр
- тетраэдр
![]()
![]()
![]()
![]()
![]()
![]()

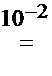 H4IO
H4IO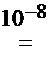 H3IO
H3IO![]() ® H2TeO4 · 2H2O = H6TeO6
® H2TeO4 · 2H2O = H6TeO6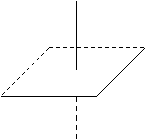




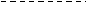

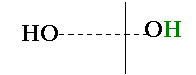
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() +1 HOCl HOBr HOI
+1 HOCl HOBr HOI![]()
![]()
![]()
![]()
![]() +5 HClO3 HBrO3 HIO3
+5 HClO3 HBrO3 HIO3 (2) А+ + + 2е = Ао ; Е ; nEo = ВЭ2 = Е × 2
(2) А+ + + 2е = Ао ; Е ; nEo = ВЭ2 = Е × 2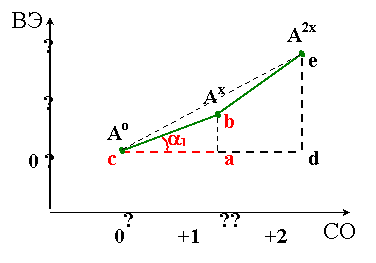
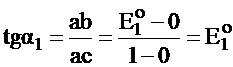
![]() , поэтому
, поэтому![]() , но
, но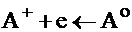



![]()
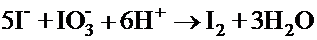
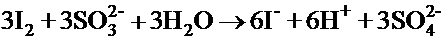






![]()
![]() HOCl + :SO = [HO – Cl–SO3] 2-®OH - + ClSO
HOCl + :SO = [HO – Cl–SO3] 2-®OH - + ClSO ClSO + H2O ® SO +2H+ + Cl -
ClSO + H2O ® SO +2H+ + Cl -
![]()
![]()
![]()
![]() ¤ + H =
¤ + H =


 DrGo = - = -RTlnK
DrGo = - = -RTlnK 4. Повышение ТС: HClO ® HClO2 ® HClO3 ® HClO4
4. Повышение ТС: HClO ® HClO2 ® HClO3 ® HClO4


