Лабораторная работа № 3. Химические свойства элементов VIA и VIIA групп
ЛАБОРАТОРНАЯ РАБОТА № 3
ХИМИЧЕСКИЕ СВОЙСТВА ЭЛЕМЕНТОВ VIA И VIIA ГРУПП
Теоретическая часть
Элементы VIA группы
VIA группу образуют четыре неметалла: кислород, сера селен, теллур, называемые халькогенами, и радиоактивный металл полоний. Атомы элементов VIA группы в стационарном состоянии имеют электронную конфигурацию ns2np4. Для них характерны степени окисления -2, 0, +4, +6.
Химия кислорода и его соединений
Кислород - самый распространенный элемент, на его долю приходится 47,2% по массе литосферы и атмосферы вместе взятых. Кислород О2 представляет собой газ без цвета, без вкуса и без запаха. В промышленности кислород получают при разделении сжиженного воздуха. В лаборатории его обычно получают термическим разложением перманганата калия или хлората калия (бертолетовой соли):
2KMnO4 ![]() K2MnO4 + MnO2 + O2
K2MnO4 + MnO2 + O2
2KClO3 ![]() 2KCl + 3O2
2KCl + 3O2
Известны две аллотропические модификации кислорода: кислород О2 и озон О3. Озон может быть получен из кислорода под действием электрического разряда или ультрафиолетового излучения:
3О2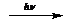 2О3
2О3
Озон О3 является более сильным окислителем в сравнении с кислородом О2, так как при его разложении согласно уравнению
О3 ® О2 + О
образуется атомарный кислород, активность которого выше, чем у молекулярного кислорода.
Молекулярный кислород является сильным окислителем, взаимодействует с большинством химических элементов.
Кислород в низшей степени окисления -2 (в оксидах, гидроксидах, кислотах и солях) обладает только восстановительными свойствами, окисляясь до O2:
2KClO3 ® 2KCl+ 3O2
В промежуточной степени окисления -1 (в пероксидах водорода или металлов) кислород может проявлять как окислительные, так и восстановительные свойства. Пероксид водорода в реакциях с сильными окислителями восстанавливается до кислорода О2:
2KMnO4 + 3H2SO4 + 5H2O2 ® 5O2 + 2MnSO4 + K2SO4 + 8H2O,
а с сильными восстановителями - до H2O в кислой среде:
2KI + H2O2 + H2SO4 ® I2 + K2SO4 + 2H2O
и до OH - - ионов в щелочной среде:
2Na3[Cr(OH)6] + 3H2O2 ® 2Na2CrO4 + 2NaOH + 8H2O.
Получают H2O2 действием кислот на пероксиды металлов:
BaO2 + H2SO4 ® BaSO4 + H2O2
Окислительная активность H2O2, обусловливающая его антисептические свойства, связана с образованием в момент разложения атомарного кислорода:
Н2О2 ® Н2О + О
Химия серы и ее соединений
Элементная сера в обычных условиях - хрупкое кристаллическое вещество желтого цвета. Она образует несколько аллотропических модификаций: ромбическую, моноклинную и пластическую. Аллотропия серы обусловлена различной структурой кристаллов, построенных из восьмиатомных молекул S8. В парах серы в зависимости от температуры обнаружены молекулы S8, S6, S4 и S2.
Сера является типичным неметаллом. При нагревании она окисляет многие простые вещества, проявляя окислительные свойства:
Hg + S ® HgS,
а более активными неметаллами, например, кислородом и галогенами легко окисляется:
S + O2 ® SO2
S + 2Cl2 ® SCl4
В воде при обычной температуре сера не растворяется, но в кипящей воде и значительно лучше в кипящих растворах щелочей она диспропорционирует:
3S + 6NaOH ® 2Na2S+ Na2SO3 + 3H2O
Сульфиды (соединения серы в степени окисления -2), как и оксиды, делятся на основные, кислотные и амфотерные. Сульфиды щелочных и щелочноземельных металов обладают основными свойствами, сульфиды алюминия и хрома(Ш) - амфотерные, а сульфиды неметаллических элементов проявляют кислотные свойства.
Растворимые в воде основные сульфиды в водных растворах гидролизуются обратимо с образованием щелочных растворов:
Na2S + H2O ® NaНS+ NaOH.
Кислотные оксиды в водных растворах образуют соответствующие кислоты:
SiS2+ 3H2O ® H2SiO3+ 2H2S
Амфотерные сульфиды в воде не растворяются, но под действием воды полностью и необратимо гидролизуются:
Al2S3+ 6H2O ® 2Al(OH)3+ 3H2S
Сульфид водорода H2S (сероводород) - бесцветный газ с характерным неприятным запахом. В водных растворах является слабой дипротонной кислотой.
Сероводород является сильным восстановителем. На воздухе горит, окисляясь до оксида серы (IV):
2H2S + 3O2 ® 2SO2 + 2H2O,
а при недостатке кислорода окисляется до свободной серы:
2H2S + O2 ® 2S + 2H2O
В водных растворах в зависимости от условий H2S может окисляться до S, SO2 или H2SO4:
2KMnO4 + 3H2SO4 + 5H2S ® 2MnSO4 + 5S + K2SO4 + 8H2O
H2S + 4Br2 + 4H2O® H2SO4 + 8HBr
Cульфиды тяжелых металлов малорастворимы в воде и окрашены в характерные цвета: ZnS - белый, MnS - розовый, CdS - желтый, Sb2S3 - оранжевый, SnS - коричневый, CuS - черный.
В степени окисления +4 сера образует диоксид SO2, слабую сернистую кислоту H2SO3, и соответствующие ей соли – сульфиты. Оксид серы (IV) SO2 (сернистый газ) получают в промышленности при горении серы или обжигом пирита:
S + O2 ® SO2
4FeS2 + 11O2 ® 2Fe2O3 + 8SO2
В лаборатории SO2 получают действием соляной кислоты на сульфит натрия:
Na2SO3 + 2HCl ® 2NaCl + H2O + SO2
Соединения серы в степени окисления +4 могут проявлять как окислительные, так и восстановительные свойства:
H2SO3 + 2H2S ® 3S + 3H2O
H2SO3 + Cl2 + H2O ® H2SO4 + 2HCl
При кипячении раствора сульфита натрия с порошком серы образуется тиосульфат натрия Na2SO3S:
Na2SO3 + S ® Na2S2O3
Свойства тиосульфатов обусловлены присутствием в них атомов серы в двух степенях окисления: -2 и +6. При взаимодействии с окислителями тиосульфаты проявляют восстановительные свойства:
Na2S2O3+ Cl2 + H2O ® Na2SO4 + S + 2HCl
2Na2S2O3+ I2 ® Na2S4O6 + 2NaI
При действии серной кислоты на тиосульфат натрия образуется неустойчивая тиосерная кислота H2S2O3, распадающаяся на H2SO3 и S в момент образования:
Na2S2O3+ H2SO4® Na2SO4 + H2S2O3
H2S2O3® H2SO3 + S
При окислении оксида серы (IV) кислородом в присутствии катализатора (Pt, V2O5 или NO) образуется оксид серы (VI) SO3. Растворение SO3 в воде приводит к образованию сильной дипротонной серной кислоты H2SO4.
2SO2 + О2 ® 2SO3
SO3 + H2O ® H2SO4
Разбавленная серная кислота реагирует с металлами, стоящими в ряду напряжения до водорода, с образованием соли соответствующего металла и выделением водорода:
Fe + H2SO4 (разб.) ® FeSO4 + H2
Концентрированная серная кислота является сильным окислителем. В реакциях с неметаллами и тяжелыми металлами H2SO4 восстанавливается до SO2, с активными металлами – до S, а со щелочными и щелочноземельными металлами – до H2S:
S + 2H2SO4(конц.) ® 3SO2 + 2H2O
C + 2H2SO4(конц.) ® 2SO2 + CO2 + 2H2O
Сu + 2H2SO4 (конц.) ® СuSO4 + SO2 + 2H2O
3Zn + 4H2SO4 (конц.) ® 3ZnSO4 + S + 4H2O
4Сa + 5H2SO4 (конц.) ® 4СaSO4 + H2S + 4H2O
Концентрированная серная кислота на холоду пассивирует железо, алюминий, хром и не взаимодействует с Pt и Au.
Элементы VIIA группы
VIIA группу образуют водород и галогены. Атомы галогенов (F, Cl, Br, I и At) в стационарном состоянии имеют электронную конфигурацию ns2np5. Простые вещества (F2, Cl2, Br2, I2) – активные неметаллы, сильные окислители. Их активность уменьшается в ряду F2>Cl2>Br2>I2. Характерные степени окисления галогенов в соединениях: -1, 0, +1, +3, +5, +7. Фтор, будучи наиболее активным из всех неметаллов, во всех своих соединениях проявляет степень окисления -1, а в простом веществе – 0.
Электронная формула атома водорода 1s1. С галогенами его объединяет способность принимать один электрон и образовывать стабильную электронную оболочку. Поэтому водород, как правило, располагают вместе с галогенами в VIIA группе.
Химия водорода и его соединений
Водород занимает особое положение среди других элементов Периодической системы. Подобно атомам щелочных металлов, атом водорода способен отдавать один электрон, проявляя восстановительные свойства и образовывая положительно заряженный ион Н+. Подобно галогенам, атом водорода в реакциях с активными металлами отдает электрон, проявляя окислительные свойства и образовывая гидрид-ион Н-. Водород, как и галогены, образует двухатомные молекулы Н2. В органических соединениях атомы галогенов могут замещать атомы водорода: CH4 - CH3Cl - CH2Cl2 и т. д.
В лаборатории водород получают действием соляной кислоты на цинк в аппарате Киппа:
Zn + 2HCl ® ZnCl2 + H2
Окислительные свойства водород проявляет при взаимодействии с активными металлами с образованием ионных солеобразных гидридов:
Н2 + 2Li ® 2LiН
Гидриды активных металлов разлагаются при действии воды или кислот с выделением водорода:
NaH + H2O ® NaOH + H2
CaH2 + 2HCl ® CaCl2 + 2H2
Восстановительные свойства водород проявляет при взаимодействии с неметаллами:
Н2 + Cl2 ® 2HCl
3Н2 + N2 ® 2NH3
Химия фтора и его соединений
Фтор является наиболее активным неметаллом, сильным окислителем. Фтор - зеленовато-желтый газ с резким запахом. В атмосфере фтора горят многие металлы и неметаллы с образованием соответствующих фторидов. Фтор взаимодействует с водородом со взрывом в темноте и при низких температурах:
F2 + H2 ® 2HF
Фтор взаимодействует с водой:
2F2 + 2H2O ® 4HF + O2,
вытесняет хлор из хлоридов:
F2 + 2NaCl ® 2NaF + Cl2
Фтороводородная (плавиковая) кислота является слабой кислотой. Молекулы HF связаны друг с другом водородными связями, образуя молекулы HnFn (n=2-6), поэтому плавиковая кислота может образовывать кислые соли, например, KHF2. Плавиковая кислота нарушает структуру стекла, взаимодействуя с оксидом кремния (IV) с образованием газообразного SiF4:
4HF + SiO2 ® SiF4 + 2H2O
Химия хлора и его соединений
В природе хлор находится в виде хлоридов. В промышленности его получают вместе с водородом и гидроксидом натрия при электролизе водного раствора хлорида натрия:
2NaCl + 2H2O 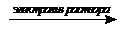 H2 + Cl2 + 2NaOH
H2 + Cl2 + 2NaOH
В лаборатории хлор получают действием концентрированной соляной кислотой на кристаллический перманганат калия:
2KMnO4 + 16HCl ® 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Хлор - тяжелый газ желто-зеленого цвета с резким запахом. Раствор пяти объемов хлора в одном объеме воды называют хлорной водой.
Хлор взаимодействует с водородом на свету с образованием хлороводорода:
Cl2 + H2 ![]() 2HCl
2HCl
Хлороводород - бесцветный газ с резким запахом, хорошо растворим в воде: в 1 объеме воды при 0оС растворяется более 500 объемов хлороводорода. Раствор хлороводорода в воде называют хлороводородной (соляной) кислотой.
При взаимодействии хлора с водой и щелочами происходит его диспропорционирование. При комнатной температуре образуются хлорноватистая кислота HClO или ее соли - гипохлориты:
Cl2 + H2O ® HCl + HClO
2Cl2 + 2Ca(OH)2 ® CaCl2 + Ca(ClO)2 + 2H2O
Cl2 + 2KOH ® KCl + KClO + H2O,
а при пропускании хлора через горячий раствор KOH образуется хлорат калия KClO3 (бертолетова соль):
3Cl2 + 6KOH ® 5KCl + KClO3 + 3H2O
Смесь хлорида CaCl2 и гипохлорита Ca(ClO)2 кальция называют хлорной (белильной) известью и часто записывают как CaCl(ClO). Хлор в количестве 1,5 г на 1 м3 воды используется для ее обеззараживания. Образующаяся в воде хлорноватистая кислота HClO разлагается с образованием атомарного кислорода
HClO ® HCl + O,
который, являясь очень активным окислителем, убивает микроорганизмы, обесцвечивает красители и т. д.
В ряду кислородсодержащих кислот хлора: HClO (хлорноватистая кислота) - HClO2 (хлористая кислота) - HClO3 (хлорноватая кислота) - HClO4 (хлорная кислота) растет сила кислот, а их окислительная активность уменьшается.
Химия брома, йода и их соединений
Простое вещество Br2 - темно-бурая жидкость с резким запахом, а йод - кристаллическое вещество темно-фиолетового цвета. Их получают действием хлора на растворы бромидов и йодидов:
2NaBr + Cl2 ® 2NaCl + Br2
2NaI + Cl2 ® 2NaCl + I2
Бром и йод хорошо растворимы в органических растворителях и экстрагируются ими из водных растворов. Раствор брома в толуоле или тетрахлориде углерода окрашен в оранжевый цвет, а раствор йода - в фиолетовый цвет. С крахмалом йод дает темно-синее окрашивание (качественная реакция на йод), исчезающее при нагревании и появляющееся вновь при охлаждении.
Бром и йод при нагревании взаимодействуют с водородом и многими металлами:
Br2 + H2 ![]() 2HBr
2HBr
I2 + H2 ![]() 2HI
2HI
2Al + 3Br2 ® 2AlBr3
2Al + 3I2 ® 2AlI3![]()
Растворы бромоводорода и йодоводорода в воде являются сильными кислотами. Их соли (бромиды и иодиды) хорошо растворимы в воде. Исключение составляют лишь бромид и иодид серебра:
AgNO3 + NaBr ® AgBr¯ + NaNO3
AgNO3 + NaI ® AgI¯ + NaNO3
Галогенид - ионы (за исключением фторид - ионов) проявляют восстановительные свойства. Их восстановительная способность возрастает в ряду Cl - - Br - - I - , а продуктами окисления являются, как правило, свободные галогены:
10KI + 2KMnO4 + 8H2SO4 ® 5I2 + 2MnSO4 + 6K2SO4 + 8H2O
Экспериментальная часть
Опыт 1. Восстановительные свойства тиосульфатов
a) В пробирку с 1-2 мл 0,1 моль/л раствора Na2S2O3 прибавляйте по каплям хлорную воду до выпадения осадка свободной серы. Затем прилейте избыток хлорной воды до исчезновении мути. Запишите ваши наблюдения.
Напишите уравнения реакций и уравняйте их ионно-электронным методом.
Na2S2O3 + C12 + H2O ® Na2SO4 + 2HC1 + S ¯
S + 3C12 + 4H2O ® Н2SO4 + 6HC1
Na2S2O3 + 4C12 (избыток) + 5H2O® Na2SO4 + 8HC1 + H2SO4
б) Налейте в пробирку 1-2 мл йодной воды и 1-2 капли раствора крахмала. Запишите ваши наблюдения.
Прибавьте в пробирку по каплям 0,1 моль/л раствор тиосульфата натрия (Na2S2O3) до обесцвечивания раствора.
Напишите уравнение реакции и уравняйте его методом ионно-электронного баланса, с учетом окисления тиосульфат-ионов в тетратионат-ионы:
2Na2S2O3 + I2 ® Na2S4O6 + 2NaI
Опыт 2. Растворимость хлора, брома и йода в органических растворителях
Налейте в три пробирки по 1-2 мл растворов: в первую – хлорной воды, во вторую - бромной воды и в третью - иодной воды.
В каждую пробирку добавьте по несколько капель толуола. Пробирки встряхните и отметьте цвет органического слоя в каждой из пробирок. Результаты запишите.
Опыт 3. Сравнение окислительных свойств галогенов
Налейте в три пробирки по 1-2 мл растворов: в первую - бромида калия, во вторую и третью - иодида калия. В каждую пробирку добавьте по несколько капель толуола. Затем в первые две пробирки прибавьте хлорной, а в третью - бромной воды, пробирки встряхните. Объясните окрашивание слоя толуола. Напишите уравнения реакций и уравняйте их.
2KBr + Cl2 ® Br2 + 2KCl
2KI + Cl2 ® I2 + 2KCl
2KI + Br2 ® I2 + 2KBr
Опыт 4. Образование галогенидов серебра и свинца
В три пробирки возьмите по несколько капель растворов KCl, KBr и KI. Затем в каждую пробирку прибавьте по несколько капель раствора нитрата серебра. Обратите внимание на цвет образовавшихся осадков. Наблюдения запишите.
Ag+ + Cl - → AgCl↓ | Pb2+ + 2Cl - → PbCl2↓ |
Ag+ + Br - → AgBr↓ | Pb2+ + 2Br - → PbBr2↓ |
Ag+ + I - → AgI↓ | Pb2+ + 2I - → PbI2↓ |
Повторите опыт с раствором нитрата свинца. Отметьте цвет образовавшихся осадков.
Составьте уравнения реакций. Сравните растворимость в ряду галогенидов серебра и свинца в воде с использованием значений их констант растворимости: Кs0(AgC1) = 1,78.10-10; Кs0(AgBr) = 5,3.10-13; Кs0(AgI) = 8,3.10-17; Кs0(PbC12) = 1,6.10-5 ; Кs0(PbBr2) = 9,1.10-6 ; Кs0(PbI2) = 1,1.10-9.
Опыт 5. Восстановительные свойства галогенидов
В две пробирки возьмите по 1-2 мл раствора хлорида железа (III) и по несколько капель толуола.
В первую пробирку добавьте несколько капель раствора бромида калия, во вторую - раствора иодида калия. Пробирки встряхните.
В какой пробирке слой толуола окрасился? Напишите уравнение реакции.
2FeCl3 + 2KI → 2FeCl2 + I2 + 2KCl
FeCl3 + KBr ≠
Объясните различия в результатах опыта, используя следующие значения стандартных редокс-потенциалов:
Ео(Fe3+/Fe2+) = +0,77B; Ео(Br2/2Br-) = +1,09B; Ео(I2/2I-) = +0,54B



