Всероссийская олимпиада школьников по химии
(школьный этап)
11 класс, 2011-12 учебный год
Задача 11-1.
Что такое «тяжелая вода»? Сколько, примерно, протонов, нейтронов и электронов содержит образец такой воды массой 10 г? Какой газ выделится при взаимодействии этой порции «тяжелой воды» с избытком натрия? Напишите уравнение реакции и определите массу газа. (10 баллов)
Задача 11-2.
Смесь карбида алюминия и сульфида алюминия обработали избытком раствора гидроксида натрия, при этом смесь полностью растворилась, и выделилось 6,72 л газа (н. у.) Через полученный раствор пропустили углекислый газ до прекращения выпадения осадка, масса которого после прокаливания составила 40,8 г. Напишите уравнения реакций. Определите массовые доли веществ в исходной смеси (10 баллов)
Задача 11-3.
Напишите уравнения реакций, соответствующих следующей схеме
Cu2O ![]() Х1
Х1 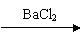 Х2
Х2  Х3
Х3  Cu2O
Cu2O
Для окислительно-восстановительных реакций укажите окислитель и восстановитель. Напишите структурную формулу органического вещества, полученного на последнем этапе, и назовите его (8 баллов)
Задача 11-4.
Вещество А (C7H8O) взаимодействует с металлическим натрием, но не взаимодействует с раствором NaOH. При окислении оно образует вещество Б (C7H6O), которое при обычных условиях не взаимодействует ни с натрием, ни с раствором щелочи, но легко окисляется до вещества В (C7H6O2). Вещество В взаимодействует и с натрием и с NaOH. В присутствии серной кислоты вещество В реагирует и с этанолом, образуя вещество Г (C9H10O2).
Предложите три наиболее вероятных изомера для состава C7H8O. Объясните, какой из них по свойствам является веществом А. Определите все вещества А-Г (структурные формулы и названия), напишите уравнения соответствующих реакций. (10 баллов)
Задача 11-5.
После занятия химического кружка восьмиклассников в лаборатории осталось пять колб с растворами. На первой колбе было написано "иодид калия", на второй – "карбонат калия", на третьей – "соляная кислота", на четвертой – "хлорид меди" и на пятой – "гидроксид бария". Десятиклассники Маша и Саша сразу увидели, что что-то здесь не так – колба с хлоридом меди была подписана неправильно. «Надо проверить и другие растворы» - решили друзья, и поспорили, кто это сделает быстрее.
Маша взяла немного раствора из первой колбы, и прилила к ней раствор из второй. Выделился газ. Тогда Маша к раствору из первой колбы прилила раствор из третьей – выпал белый осадок. «Этого достаточно» - решила Маша и подошла к Саше.
А Саша к этому времени уже налил немного растворов из четырех колб в четыре пробирки и прибавил к ним уже известный раствор хлорида меди. В одной пробирке у него раствор стал темно-коричневым и выпал желтый осадок, в другой был осадок синего цвета, еще в одной – зеленоватый, и только в одной – ничего не произошло. «Мне тоже все понятно!» - сказал он. А у восьмиклассников остались вопросы:
а) Как Маша и Саша сразу поняли, что хлорид меди подписан неправильно?
б) Какие реакции провела Маша? Напишите молекулярные и ионные уравнения реакций. На основании ее опытов определите, в какой колбе находился какой раствор.
в) Какие реакции провел Саша? Напишите уравнения и этих реакций.
г) Есть ли среди проведенных реакций окислительно-восстановительные? Если да, укажите окислитель и восстановитель, напишите электронные уравнения. (10 баллов)
Решение и критерии оценивания
Задача 11-1. «Тяжелая вода» - оксид дейтерия, D2O. (2 балла)
Дейтерий - изотоп водорода, в состав ядра атома которого входит 1 протон и 1 нейтрон, относительная атомная масса дейтерия равна 2. Молярная масса D2O равна 20 г/моль, следовательно, предложенный образец содержит n = m/M = 10/20 = 0,5 моль тяжелой воды. (2 балла)
Число молекул N= n·NA, следовательно: N(D2O) = 3·1023 молекул.
Состав атома дейтерия D(1p+1n+1e) кислорода O(8p+8n+8e), следовательно, в состав одной молекулы входит по 10 протонов, нейтронов и электронов. Значит, в образце тяжелой воды массой 10 г будет содержаться по 3·1024 этих частиц. (2 балла)
Уравнение реакции 2Na + 2D2O = D2↑ + 2NaOD
Выделяется «тяжелый водород» с молярной массой 4 г/моль. (2 балла)
По уравнению:
n(D2) = n(D2O)/2 = 0,25 моль; m(D2) = M·n = 0,25·4 = 1 г (2 балла)
Всего 10 баллов.
Задача 11-2. Карбид и сульфид алюминия полностью гидролизуются водой:
Al4C3 + 12H2O = 4Al(OH)3 + 3CH4 (1) (1 балл)
Al2S3 + 6H2O = 2Al(OH)3 + 3H2S (2) (1 балл)
Гидроксид алюминия и сероводород тут же реагируют со щелочью:
Al(OH)3 + NaOH = Na[Al(OH)4] (3) (1 балл)
H2S + 2NaOH = Na2S + 2H2O (4) (1 балл)
При пропускании в раствор углекислого газа:
Na[Al(OH)4] + CO2 = Al(OH)3↓ + NaHCO3 (5) (1 балл)
При прокаливании: 2Al(OH)3 = Al2O3 + 3H2O (6) (1 балл)
Количество вещества метана: n(CH4)=V/VM = 6,72/22,4 = 0,3 моль
По уравнению 1: n(Al4C3) = n(CH4)/3 = 0,1 моль
n(Al2O3) = m/M = 40,8/102 = 0,4 моль
n(Al)общее = n(Al2O3)·2 = 0,8 моль; n(Al)карбид = n(Al4C3)·4 = 0,4 моль
n(Al)сульфид = n(Al)общее - n(Al)карбид = 0,8-0,4 = 0,4 моль
n(Al2S3) = n(Al)сульфид / 2 = 0,4/2 = 0,2 моль (2 балла)
Массы (m=M·n): m(Al4C3) = 144·0,1 = 14,4 г;
m(Al2S3) = 150·0,2 = 30 г; m(смеси) = 14,4+30 = 44,4 г.
ω(Al4C3) = 14,4/44,4 = 0,324 = 32,4%;
ω(Al2S3) = 100% - 32,4% = 67,6% (2 балла)
Всего 10 баллов.
Задача 11-3.
Уравнения реакций:
Cu2O + 3H2SO4 = 2CuSO4 +SO2+3H2O
Cu2O – восстановитель, H2SO4 – окислитель 2 балла
CuSO4 + BaCl2 = CuCl2 + BaSO4¯; 1 балл
CuCl2 + 2KOH = 2КCl + Cu(OH)2¯ 1 балл
2Cu(OH)2 + CH2(OH)-(CHOH)4-CHO = Cu2O + CH2(OH)-(CHOH)4-COOH + 2H2O
глюкоза – восстановитель, Cu(OH)2 – окислитель 2 балла
образуется глюконовая кислота CH2(OH)-(CHOH)4-COOH 2 балла
Всего 8 баллов.
Задача 11-4.
Сравнив формулу вещества А (C7H8О) с формулой соответствующего алкана C7H14 видим, что она подчиняется формуле (CnHn-6О). Это показывает, что в состав структуры входит фенильный фрагмент. В соответствии с этим веществу с составом C7H8О можно предложить три наиболее вероятных структуры:
CH3-C6H4ОН (1), CH3-O-C6H5 (2), C6H5-CH2-OH (3) 3 балла
Из них первое относится к классу фенолов (реагирует с Na и NaOH), второе – к простым эфирам (не реагирует ни с Na, ни с NaOH), и только третье – бензиловый спирт удовлетворяет условиям задачи и реагирует только с натрием:
2C6H5-CH2-OH + 2Na → 2C6H5-CH2-ONa + H2↑ 2 балла
Окисление спирта приводит к соответствующему альдегиду Б:
C6H5-CH2-OH + CuO → C6H5-CHO + Cu + H2O (бензойный альдегид) 1 балл
Альдегид легко окисляется до бензойной кислоты В:
2C6H5-CH2-OH + O2 → 2C6H5-COOH + H2O 1 балл
Уравнения реакций бензойной кислоты:
C6H5-COOH + NaOH → C6H5-COONa + H2O 1 балл
2C6H5-COOH + 2Na → 2C6H5-COONa + H2↑ 1 балл
C6H5-COOH + C2H5OH → C6H5-COOC2H5 + H2O
В последней реакции образуется сложный эфир, этилбензоат – вещество Г. 1 балл
Всего 10 баллов.
Задача 11-5.
а) Растворы всех веществ бесцветны, а разбавленный раствор хлорида меди(II) имеет голубую окраску, поэтому определить, в какой колбе он находился, не составляло труда. (1 балл)
б) Реакция с выделением газа могла пройти только такая:
K2CO3 + 2HCl = 2KCl + CO2↑ + H2O; CO32– + 2H+ = H2O + CO2↑
значит, в первых двух колбах находятся K2CO3 и HCl. Соляная кислота не может дать осадок ни с одним из растворов. А карбонат калия может дать белый осадок только с гидроксидом бария:
K2CO3 + Ba(OH)2 = BaCO3↓ + 2 KOH; CO32– + Ba2+ = BaCO3↓
Следовательно, в первой колбе - карбонат калия, во второй - соляная кислота, в третьей – гидроксид бария. CuCl2 не может быть в четвертой колбе – он был подписан неправильно, значит он в пятой колбе. А в четвертой – раствор иодида калия. (3 балла)
в) Реакции с раствором хлорида меди(II):
2CuCl2 + 4KI = 2CuI↓ + 4KCl + I2; 2Cu2+ + 4I–= 2CuI↓ + I2;
Иод придает раствору бурый цвет, осадок CuI белого цвета, но из-за поглощенного иода кажется желтым. (1 балл)
CuCl2 + Ba(OH)2 = Cu(OH)2↓ + BaCl2; Cu2+ + 2OH – = Cu(OH)2↓;
синий осадок гидроксида меди. (1 балл)
2CuCl2 +2K2CO3 + H2O = (CuOH)2CO3+ 4KCl +CO2;
2Cu2+ +2CO32– + H2O = (CuOH)2CO3↓ + CO2; (1 балл)
зеленоватый осадок основного карбоната меди.
г) Окислительно-восстановительной является только реакция хлорида меди(II) с иодидом калия. При этом иодид-ион является восстановителем:
2I-1 – 2e = I20, ион меди – окислителем: Cu+2 + 1e = Cu+1 (3 балла)
Всего 10 баллов.
Максимальное количество баллов – 48
Время выполнения - 3 часа



