Согласовано Утверждаю
Декан фармацевтического факультета Директор УД «Фармация»
____________ _____________
«______»___________2014 г. «______»____________ 2014 г.
Экзаменационные вопросы по дисциплине
«Общая химическая технология» для студентов 3 курса по специальности
5В074800 - «Технология фармацевтического производства» на 2013-2014 учебный год
1. Промышленный способ получения кальцинированной соды. Назначение стадий аммонизации, карбонизации, бикарбонизации.
2. Укажите современные методы умягчения воды.
3. Ионообменное умягчение и обессоливание воды
4. Сравнить известково-содовый и фосфатный способы устранения жесткости.
5. Физико-химические основы производства азотной кислоты.
6. Производство этилового спирта. Применение этилового спирта в промышленности.
7. Производство дивинила. Значение дивинила в народном хозяйстве.
8. Синтез метилового спирта. Применение метилового спирта.
9. Производство кальцинированной соды по аммиачному способу.
10. Методы переработки нефти.
11. Особенности и основные физико-химические закономерности нитрозного способа производства серной кислоты.
12. Какие продукты получают при химической переработке нефти?
13. Теоретические основы синтеза аммиака.
14. Производство поливинилового спирта. Свойства и применение.
15. Технология производства простых и сложных эфиров целлюлозы.
16. Перечислите основные способы фиксации азота.
17. Основные технологические характеристики твердых катализаторов.
18. При получении серной кислоты образовался 1 моль воды и 1 моль ![]() . Рассчитать концентрацию полученной кислоты.
. Рассчитать концентрацию полученной кислоты.
19. Каково влияние катализаторов на скорость технологических процессов?
20. Опишите два способа получения серной кислоты.
21. Какие реакции лежат в основе получаемые серной кислоты двумя способами?
22. Укажите технологические особенности производства перманганата калия.
23. Какие методы переработки нефти Вы знаете?
24. Производство едкого натра электолизом водных разтворов хлористого натрия.
25. Каковы физико-химические основы и оптимальные условия обжига колчедана?
26. Назначение процесса коксования угля.
27. Физические и химические способы получения бензинов из нефти.
28. Контактное окисление сернистого газа.
29. Назовите способы получения простого и двойного суперфосфата.
30. Преимущества электрохимических методов получения продуктов.
31. К 500 кг серной кислоты прибавили 30 кг воды. Определите концентрацию получившейся кислоты и повышение температуры в результате разбавления.
32. Рассчитайте обьем сухого воздуха, необходимый для сжигания 100 кг колчедана, и объем обжигового газа, если колчедан содержит 43% S, влажность колчедана 6.8%, ![]() в обжиговом газе 11% по объему. Коэффициент избытка воздуха a=1.5%. Состав воздуха: 21% кислорода и 79М азота по объему.
в обжиговом газе 11% по объему. Коэффициент избытка воздуха a=1.5%. Состав воздуха: 21% кислорода и 79М азота по объему.
33. Определите теоретическую теплотворную способность (теплоту горения в кДж/кг) углистого колчедана, содержащего 42% серы и 5% углерода. Известно, что 1 кг чистого пирита при сгорании дает 7060 кДж/кг, а 1 кг углерода – 32700 кДж/кг.
34. В олеумный абсорбер поступает 30500 ![]() газа, содержащего 10%
газа, содержащего 10% ![]() ; вытекающий олеум содержит 21.5%
; вытекающий олеум содержит 21.5% ![]() . Определите массу олеума, необходимую для орошения абсорбера в кг/ч, если степень абсорбции
. Определите массу олеума, необходимую для орошения абсорбера в кг/ч, если степень абсорбции ![]() составляет 40%.
составляет 40%.
35. Рассчитайте состав газа на входе и выходе из колонны синтеза при производстве аммиака. На входе и выходе соответственно 4 и 16% по объему.
36. С хлорного электролизера дифрагменного типа нагрузкой 40 кА за сутки получен щелок объемом 10.6 ![]() , содержащий 130 кг/
, содержащий 130 кг/![]() едкого натра. Определите выход щелочи по току.
едкого натра. Определите выход щелочи по току.
37. При каталитическом крекинге керосина массаовая доля газа равна 18% от сырья. Определите массу метана, которая получится из 1 т керосина, если объемные доли компонентов газа крекина: 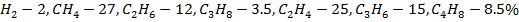 .
.
38. В качестве побочных продуктов при окислении ацетальдегида в уксусную кислоту получаются метилацетат, этилидендиацетат, муравьиная кислота, оксид углерода (2) и др. Рассчитайте массу метилацетата, которая получается в сутки на установке производительностью 2000 кг/ч уксусной кислоты, если в метилацетат превращается 1% ацетальдегида, а выход уксусной кислоты на стадии окисления составляет 97% на ацетальдегид.
39. Для производства поливинилхлорида суспензионным методом использованы следующие вещества ( в массовых долях): винилхлорида 100, воды 150, других ингредиентов 2. Рассчитайте массовую долю полимера в латексе, если конверсия составила 85%, а автоклав загружается 24 т сырьевых компонентов.
40. Вычислите степень полимеризации полипропилена, если средняя молекулярная масса его образца равна 357·10 3 .
41. Определите массу аммиака и воздуха, необходимую для производства 1000 кг азотной кислоты. Степень превращения аммиака в NО 0.97, а степень абсорбции 0.92. Концентрация аммиака в аммиачно-воздушной смеси 11.5%.
42. В реакцию с водородом взято 8 ![]() хлора. Определить количество полученной соляной кислоты, если ее концентрация 80%.
хлора. Определить количество полученной соляной кислоты, если ее концентрация 80%.
43. Какое количество ![]() по весу и объему потребуется для получения 50л 3М
по весу и объему потребуется для получения 50л 3М ![]() ?
?
44. Определить объем 70% ![]() (g=1.6), который можно получить из 16 кг серы?
(g=1.6), который можно получить из 16 кг серы?
45. При сухой перегонке 12 г древесины было выделено 5 мл 0,7 Н уксусной кислоты. Определить содержание уксусной кислоты в древесине в процентах.
46. Подсчитать суточную производительность завода, перерабатывающего на серу 4500 ![]() ас газа, содержащего 5% об.
ас газа, содержащего 5% об. ![]() , если степень использвания
, если степень использвания ![]() составляет 90%.
составляет 90%.
47. Какое количество аммиака по весу и объему потребуется для получения 15 л азотной кислоты концентрации 0,6 моль/л, если степень использования аммиака в этом процессе составляет 97%? Расчет вести по балансному уравнению: 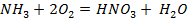 .
.
48. Сколько двусернистого железа FeS2 содержится в природном колчедане, если по данным анализа серы в нем 42%?
49. Сколько тонн бурого железняка потребуется для выплавки 5000 т передельного чугуна, содержащего 92% железа? По аналитическим данным, бурый железняк сдержит 80% лимонита 2Fe 2O 3 . 3H 2O.
50. Жесткость воды равна 5,4 мг-экв ионов кальция в 1 л воды. Какое количество тринатрийфосфата Na3PO4 необходимо взять, чтобы понизить жесткость 1 т воды практически до нуля.
51. В 5 м 3 воды содержится 250 г ионов кальция и 135 г ионов магния. Определить общую жесткость воды.
52. Определить расходный коэффициент аммиака в производстве азотной кислоты (без учета производственных потерь).
53. Теоретически 17 кг аммиака NH3 при окислении дают 63 кг азотной кислоты HNO3. Практически же получено 54 кг кислоты. Определить выход азотной кислоты.
54. Из 320 т колчедана FeS2, содержащего 45% серы S, было получено 270 т сернистого газа SO2. Вычислить расходный коэффициент и выход SO2 по сере.
55. В контактном аппарате в течение 12 ч окисляется 180 т ангидрида SO2, степень окисления 98,5%. Определить производительность аппарата в кг/ч.
56. Определить годовую (365 дней) производительность колонны синтеза аммиака в расчете на 100%-ный NH3 (в тыс. т), если за 8 ч вырабатывается 60000 кг 99%-ного аммиака.
57. Производительность печи КС равна 8,33 т/ч (по флотационному колчедану). Определить интенсивность процесса обжига в кг/м 3 в сут и сравнить с интенсивностью этого процесса в печи ВХЗ. Площадь решетки печи - 20 м2, высота кипящего слоя (h) — 1,5 м.
58. Карбонатная жесткость воды равна 5 мг-экв/л. Определить содержание бикарбоната кальция в 10 м3 воды.
59. Определить общую жесткость воды методом комплексометрического титрования, если на 100 мл исследуемой воды пошло 8,5 мл 0,1н. раствора трилона. Поправочный коэффициент трилона равен 1,05. Установлено, что 1 мл 0,1 н раствора трилона Б соответствует 0,1 мг-экв ионов Ca 2+ и Mg 2+
60. Вычислить процентное содержание фтораппатита 3Ca3(PO4)2, CaF2 и примесей в хибинской руде, если, по данным анализа, в ней содержится 32% окисла P2O5.
Экзаменационные вопросы по дисциплине «Общая химическая технология» для студентов 3-го курса обсуждены на заседании модуля «Фармацевт-аналитик»
от «__» _________ 2014 г. протокол №
Руководитель модулем
«Фармацевт-аналитик», профессор




