Лабораторная работа №2
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ БЕЛКОВ
Для количественного определения белков применяют физические, химические и биологические методы.
Из физических методов простейшим кажется взвешивание чистого белка. Однако белки очень гигроскопичны, и полностью удалить из их состава воду столь трудно, что этот способ количественного определения белков применяют редко. Кроме того, выделить весь белок из препарата практически невозможно.
Наибольшее распространение из физических методов количественного определения белков получили три: рефрактометрический (по показателю преломления белковых растворов), спектрофотометрический (по поглощению в ультрафиолетовой области спектра) и полярографический (по кривым, показывающим зависимость между силой тока и напряжением, приложенным к системе, содержащей белок.
Химические методы количественного определения белков разнообразны. Наиболее простым химическим методом определения белка является количественное определение общего или белкового азота. Умножая величину процентного содержания общего азота на коэффициент 6,25 (среднее содержание азота в белках - 16%, отсюда 100∙16 = 6,25), получают данные о содержании сырого протеина. Проделывая ту же операцию с величиной, характеризующей содержание белкового азота, получают данные о количестве белка.
На том же принципе основаны два других метода химического определения белков: по содержанию металла и по содержанию той или иной аминокислоты. Например, в гемоглобине содержится 0,34% железа. Если в изучаемом на содержание гемоглобина препарате нет других железосодержащих соединений, то определение в препарате железа дает возможность рассчитать содержание гемоглобина. Аналогично рассуждают, если в составе препарата определено содержание какой-либо аминокислоты, доля которой в белке хорошо известна. Оба перечисленных метода применяются лишь в отдельных случаях.
Самым распространенным химическим методом количественного определения белков является колориметрический метод. Он основан на измерении интенсивности цветных реакций, развивающихся при взаимодействии белков с тем или иным специфическим реагентом. Чтобы рассчитать концентрацию белка, в этом случае строят калибровочный график.
Биологические методы количественного определения белков применимы лишь к белкам, обладающим ферментативной и гормональной активностью. Измеряя степень биологической активности препарата, можно составить представление о содержании в нем белка, обладающего данной активностью.
Оборудование, реактивы. Фотоколориметра КФК-2, кюветы для фотометрирования, рН-метр, магнитная мешалка, альбумин (для построения калибровки), биуретовый реактив, яичный белок, молоко, 1% фенолфталеин, 0,1 моль/дм3, 2,5% раствор сульфата кобальта, формалин 40%, 0,05 моль/дм3 серная кислота, коническая колба вместимостью 100 и 200 см3; пипетка вместимостью 20 см3; бюретка вместимостью 25 см3; прибор для автоматического отмеривания формалина вместимостью 1 см3, цилиндр мерный вместимостью 100 см3; бюретка вместимостью 25 см3 с ценой деления 0,10 см3; мерная пипетка вместимостью 50 см3; стаканы на 50 мл, воронка; бумажный фильтр, фильтровальная бумага.
Работа 1. Количественное определение белка по биуретовой реакции
Метод основан на образовании в щелочной среде окрашенного в фиолетовый цвет комплекса пептидных связей с ионами двухвалентной меди. Чувствительность метода составляет от 2 до 10 мг белка в пробе.
Оптическую плотность растворов определяют с помощью фотоколориметра КФК-2 (рис. 1)
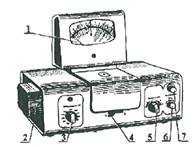
Рис. 1. Общий вид колориметра КФК-2:
1 - микроамперметр типа М907; 2 - осветитель; 3 - ручка для введения светофильтров в световой поток; 4 - ручка для ввода кювет в световой поток; 5 - ручка «ЧУВСТВИТЕЛЬНОСТЬ» для включения фотоприемников; 6 - ручка «УСТАНОВКА 100 ГРУБО»; 7 - ручка «ТОЧНО»
Как известно, зависимость между интенсивностью проходящего светового потока I0 и содержанием в растворе окрашенного вещества описывается законом Бугера-Ламберта-Бера:
I = I0∙10-ξ∙c∙l ,
где I - интенсивность светового потока после прохождения через раствор окрашенного вещества;
ξ - молярный коэффициент поглощения (экстинкции); константа для данного вещества;
с - молярная концентрация окрашенного вещества, моль/дм ;
l - толщина светопоглощающего слоя раствора, см.
Из вышеуказанного уравнения можно получить оптическую плотность раствора D:
![]()
Следовательно, оптическая плотность раствора прямо пропорциональна концентрации вещества в растворе. Прямая пропорциональная зависимость соблюдается только при низких концентрациях раствора и определенных значениях рН (рН = 2,3 ±0,1), которые создаются буферными растворами.
Принципиальная оптическая схема КФК-2, представленная на рис. 2, показывает ход светового потока в приборе. Нить лампы изображается конденсором в плоскости диафрагмы. Это изображение переносится объективом через систему светофильтров в кювету с исследуемым раствором. Для выделения узких участков спектра из сплошного спектра излучения лампы имеются цветные светофильтры, Теплозащитный светофильтр вводится в световой пучок при работе в видимой области спектра (400...490 им). Для ослабления светового потока при работе в спектральном диапазоне (400...540 нм) установлен нейтральный светофильтр.
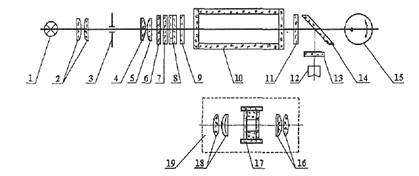
Рис. 2. Принципиальная оптическая схема КФК-2:
1 - галогенная малогабаритная лампа; 2 - конденсор; 3 - диафрагма (d=2 мм); 4, 5 - объектив; 6 - теплозащитный светофильтр; 7 - нейтральный светофильтр; 8 - цветные светофильтры; 9, 11 - защитные стекла; 10 - кювета с исследуемым раствором; 12 - фотодиод ФД-24К для работы и области спектра 590 ...980 нм; 13 - светофильтр из цветного стекла СЗС-16; 14 - пластинка, разделяющая световой поток; 15 - фотоэлемент Ф-26 для работы в области спектра 315...540 нм; 16 - линзы; 17 - кюветы малой емкости; 18 - линзы; 19 - приставка микроанализатора
Прошедший через кювету световой поток попадает на пластину, которая делит его на две части: около 10% потока направляется на фотодиод и около 90% - на фотоэлемент.
Для уравнивания фототоков, снимаемых с фотодиода при работе с различными цветными светофильтрами, перед ним установлен светофильтр.
Таким образом, световой поток, пройдя через исследуемый раствор, воздействует одновременно и на фотодиод, и на фотоэлемент. Вход усилителя постоянного тока подключен к одному из них. Ток подключенного светоприемника проходит через усилитель и попадает на измерительный прибор - микроамперметр. Он имеет шкалу, оцифрованную в коэффициентах пропускания (Т) от 100% до 0% и оптической плотности (D) от 0 до 3,0.
Фотоэлемент обеспечивает изменение чувствительности электрической схемы в соотношениях 1 : 1, 1 : 3 и 1 ; 9 (положения переключателя соответственно «3», «2» и «1», обозначенные черным цветом). Фотодиод - 1 : 9, 1 : 3 и 1 : 1 (положения переключателя соответственно «1»:, «2» и «3», обозначенные красным цветом). При работе фотоэлемента отключается фотодиод и наоборот.
Примечание. Жидкость в кювету необходимо наливать до метки на ее боковой стенке, не следует наклонять кювету при установке в кюветодержатель. Перед каждым измерением рабочие поверхности кювет необходимо протирать спирто-эфирной смесью. При установке кювет в кюветодержатели нельзя касаться пальцами рабочих участков поверхностей (ниже уровня жидкости в кювете), так как наличие загрязнений или капель раствора на рабочих поверхностях кюветы приводит к получению неверных результатов измерений.
Порядок работы на колориметре КФК-2. Колориметр включают в сеть за 15 мин до начала измерений. Во время прогрева кюветное отделение должно быть открыто.
Устанавливают светофильтр с длиной волны (590 ± 10) нм. На лицевой панели колориметра он отмечен красным цветом.
Ручку «ЧУВСТВИТЕЛЬНОСТЬ» переводят в положение «1», также отмеченное красным цветом, ручки «УСТАНОВКА 100 ГРУБО» и «ТОЧНО» - в крайнее левое положение.
Проверяют установку стрелки на «0» по шкале коэффициентов пропускания «Т» при открытом кюветном отделении. При смещении стрелки ее подводят к нулю с помощью потенциометра «НУЛЬ».
В заднее гнездо кюветодержателя в световой поток помещают кювету с опытной пробой, в переднее - с контрольной. Крышку кюветного отделения закрывают. (В случае проверки оптической плотности рабочего раствора красителя в заднее гнездо кюветодержателя помещают кювету с дистиллированной водой.)
Ручками «ЧУВСТВИТЕЛЬНОСТЬ», «УСТАНОВКА 100 ГРУБО» и «ТОЧНО» устанавливают стрелку прибора на «0» по шкале оптической плотности «0». Ручка «ЧУВСТВИТЕЛЬНОСТЬ» может находиться в одном из трех положений: «1» «2» или «3», отмеченных красным цветом.
Поворотом ручки кюветодержателя кювету с опытной пробой заменяют на кювету с контрольной. Снимают показание разности оптической плотности по шкале «0».
Измерения проводят 3 раза. Среднее значение используют для расчета массовой доли белка в исследуемом образце.
Построение калибровочной кривой. Готовят ряд растворов исследуемого вещества с известными концентрациями. Измеряют оптические плотности каждого из этих растворов и строят график (калибровочную кривую), откладывая по горизонтальной оси (абсциссе) известные концентрации, а по вертикальной оси (ординате) - соответствующие им значения оптической плотности (экстинкцию) (рис. 3).
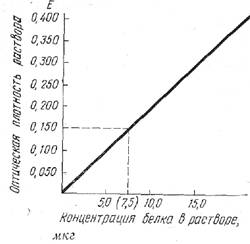
Рис. 3. Калибровочная кривая, построенная со стандартным растворам белка.
Пользуясь калибровочной кривой, определяют неизвестную концентрацию вещества в исследуемом растворе. Для этого исследуемый раствор наливают в ту же кювету, для которой построена кривая и, включив тот же светофильтр, определяют оптическую плотность раствора. Затем по калибровочной кривой находят концентрацию, соответствующую измеренному значению оптической плотности.
Ход работы. К 1 мл исследуемого раствора, содержащего от 2 до 10 мг белка, добавляют 4 мл биуретового реактива. Пробы перемешивают и оставляют при комнатной температуре на 30 мин, после чего колориметрируют на ФЭКе при 540 нм.
Содержание белка в исследуемых растворах рассчитывают по калибровочному графику.
Результаты представить в виде калибровочной прямой с экстраполяцией данных по исследуемому раствору. Сделать выводы.
Определение массовой доли белка в молоке методом формального титрования
Данный титриметрический метод основан на нейтрализации карбоксильных групп моноаминодикарбо-новых кислот белков раствором гидроксида натрия. Объем гидроксида натрия, затраченный на нейтрализацию, пропорционален массовой доле белка в молоке.
Известно, что в состав белков молока входят моноаминомонокарбоновые (нейтральные), моноаминодикарбоновые (кислые) и диаминомонокарбоновые (основные) кислоты. На долю кислых аминокислот - аспарагиновой и глутаминовой - приходится до 30%, а на долю основных - лизина, аргинина - до 9% от общего количества аминокислот. Поэтому в целом белки молока кислые.
Карбоксильные и аминные группы аминокислот способны к ионизации, в связи с чем белки молока несут отрицательные и положительные заряды.
В методе формольного титрования массовую долю белка в молоке определяют по количеству ионизированных аминных групп, находящихся на поверхности мицелл казеина и молекул сывороточных белков,
Ионизированные аминные группы способны разрушаться формальдегидом с выделением ионов водорода в раствор. Количество последних определяют, оттитровывая их щелочью.
Поскольку исходное молоко имеет слабокислую реакцию среды (рН = 6,7...6,8), то, во избежание ошибок при определении массовой доли белка, молоко вначале нейтрализуют.
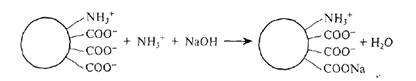 Основные реакции, характеризующие сущность метода, представлены следующими уравнениями:
Основные реакции, характеризующие сущность метода, представлены следующими уравнениями:
Нейтрализация молока:
Взаимодействие ионизированных аминных групп с формальдегидом с образованием дигидроксиметилпроизводных белка:
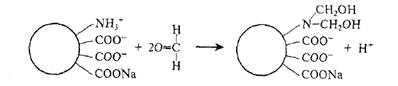
Повторная нейтрализация раствора:
Н+ + ОН - →Н2О
Таким образом, титриметрический метод определения массовой доли белка основан на измерении объема титранта (раствора щелочи), вступающего в реакцию с определяемым ионом (Н+). Момент окончания реакции (точку эквивалентности) устанавливают с помощью потенциометрического анализатора или в упрощенной методике - по изменению окраски индикатора (индикаторный способ).
Работа 2. Определение массовой доли белка индикаторным способом
В качестве индикатора используют фенолфталеин, приобретающий окраску в нейтральной и щелочной среде.
Ход работы. В колбу вместимостью 100 см3 отмеривают 20 см3 молока, 0,25 см3 (10...12 капель) 1%-го раствора фенолфталеина и титруют раствором гидроксида натрия с концентрацией 0,1 моль/дм3 до появления розовой окраски, соответствующей цвету эталона (смешивают 20 см3 молока и 0,5 см3 2,5%-ного раствора сульфата кобальта). Затем вносят прибором для автоматического отмеривания 4 см3 (4 объема) нейтрализованного 40%-ного формалина и вновь титруют раствором гидроксида натрия с концентрацией 0,1 моль/дм3 до появления окраски эталона. Количество щелочи, пошедшее на второе титрование (при первом титровании она расходуется на нейтрализацию веществ, обусловливающих кислотность молока), умножают на коэффициент 0,959 и получают массовую долю белков в молоке в процентах.
Для перевода количества раствора гидроксида натрия с концентрацией 0,1 моль/дм3 в проценты белка можно пользоваться табл. 1.
Таблица 1. - Зависимость массовой доли белков от объема раствора щелочи (Сэ = 0,1 моль/дм3), затраченного на титрование проб молока в присутствии формалина
Расход раствора NaОН, см3 | Массовая доля белков в молоке, % | Расход раствора NaОН, см3 | Массовая доля белков в молоке, % | Расход раств NaОН, см3 | Массовая доля белков в молоке, % |
2,45 | 2,35 | 2,95 | 2,83 | 3,45 | 3,31 |
2,50 | 2,40 | 3,00 | 2,88 | 3,50 | 3,35 |
2,55 | 2,44 | 3,05 | 2,93 | 3,55 | 3,40 |
2,60 | 2,49 | 3,10 | 2,98 | 3,60 | 3,45 |
2,65 | 2,54 | 3,15 | 3,03 | 3,65 | 3,50 |
2,70 | 2,59 | 3,20 | 3,07 | 3,70 | 3,55 |
2,75 | 2,64 | 3,25 | 3,12 | 3,75 | 3,60 |
2,80 | 2,69 | 3,30 | 3,16 | 3,80 | 3,65 |
2,85 | 2,73 | 3,35 | 3,21 | ||
2,90 | 2,78 | 3,40 | 3,25 |
Оформить результаты определения массовой доли белки в исследуемых образцах молока, сделать выводы.
Работа 3. Определение массовой доли белка с использованием потенциометрического анализатора
Ход работы. В стакан вместимостью 50 см3 пипеткой вносят 20 см3 молока и стержень магнитной мешалки
Электроды мономера и термокомпенсатор обсушивают фильтровальной бумагой и погружают в стакан с молоком. Стакан помещают на магнитную мешалку, включают двигатель мешалки. Следят за тем, чтобы электроды не препятствовали вращению стержня.
Включают режим измерения.
Затем начинают медленно титровать молоко раствором гидроксида натрия (Сэ = 0,1 моль/дм3). Титрование осуществляют из бюретки.
Вначале рН изменяется незначительно. Это связано с наличием молока буферных свойств, то есть способности препятствовать изменению рН при добавлении кислоты или щелочи. После насыщения буферной емкости рН раствора резко изменяется.
Титрование проводят до достижения точки эквивалентности, соответствующей рН = 9,0. Записывают объем щелочи (V1), пошедшей на нейтрализацию молока.
Не выключая прибор, вносят в стакан 5 см3 раствора формалина массовой долей формальдегида 30% (40%). Формалин ядовит, поэтому его отмеряют с помощью автоматической пипетки. '
После добавления формалина рН среды смещается в кислую сторону. Содержимое стакана вновь титруют щелочью до рН = 9,0. Записывают общий объем израсходованной щелочи (V).
Выключают режим измерения рН метра.
Стакан снимают с магнитной мешалки. Электроды и термокомпенсатор промывают дистиллированной водой, обсушивают фильтровальной бумагой и погружают в стакан с раствором формалина (5 см3 формалина и 20 см3 дистиллированной воды).
Нажимают режим измерения рН метра и содержимое стакана титруют щелочью до рН = 9,0.
Записывают объем щелочи, пошедшей на нейтрализацию раствора формалина (V2).
Выключают рН метр.
Убирают стакан с формалином. Электроды и термокомпенсатор промывают дистиллированной водой и помещают в стакан вместимостью 50 см3 с дистиллированной водой.
Обработка результатов. Массовую долю белка (Б) рассчитывают по формуле:
![]()
где V - общий объем израсходованного раствора гидроксида натрия, см3;
V1 - объем раствора гидроксида натрия, пошедшего на нейтрализацию молока, см3;
V2 - объем раствора гидроксида натрия, пошедшего на нейтрализацию формалина, см3;
19,2 - эмпирический коэффициент пересчета объема раствора гидроксида натрия на массовую долю белка;
m - объем молока, взятого для испытания, см3 (m - 20 см').
Расхождения между двумя параллельными измерениями не должны превышать 0,2% массовой доли белка.
Оформить результаты определения массовой доли белки в исследуемых образцах молока, сделать выводы.
Работа 4.Определение массовой доли казеина в молоке методом кислотного осаждения
Казеин молока обладает кислыми свойствами, и поэтому способен взаимодействовать со щелочью. Поэтому массовую долю казеина можно определить по разнице объемов щелочи, пошедшей на нейтрализацию молока и бесказеинвой сыворотки.
В основе получения бесказеиновой сыворотки лежит кислотная коагуляция казеина в изоэлектрической точке (ИТ), соответствующей рН 4,6...4,7. Механизм процесса заключается в том, что при подкислении молока происходит постепенная нейтрализация отрицательных групп (карбоксильных и фосфатных) казеина и удаление из состава казеиновых мицелл коллоидного фосфата кальция. При рН 4,9 наступает потеря частицами всего коллоидного фосфата кальция и полное разрушение мицеллярной структуры. Дальнейшее понижение рН раствора до ИТ приводит к нейтрализации казеиновых частиц и снижению степени их гидратации. Изоэлектрическое состояние сопровождается конформационными изменениями полипептидных цепей макромолекул казеина внутри субмицелл, а это приводит к частичной гидрофобизации их поверхности и образованию нерастворимых в водной среде агрегатов.
Дальнейшее объединение субмицелл за счет гидрофобных, водородных и, в меньшей степени, ионных связей приводит к образованию геля.
Примечание. Следует помнить, что казеин осаждается только в изоэлектрической точке (ИТ). Так, при недостатке кислоты мицеллы имеют отрицательный заряд и, следовательно, гидратированы, что препятствует их осаждению. Избыток кислоты приводит к перезарядке частиц казеина, их гидратации и повторному растворению. Схемы поверхности казеиновых частиц при рН выше, ниже и в ИТ представлена на рис. 4
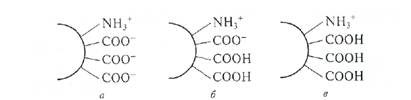
Рис. 4. Схема поверхности казеиновых частиц при различных значениях рН;
а - выше изоэлектрической точки: б - в изоэлектрической точке; в - ниже изоэлектрической точки
Ход работы.
1 этап. В коническую колбу вместимостью 200 см3 пипеткой вносят 20 см3 молока и цилиндром 80 см3 дистиллированной воды с температурой 20°С; содержимое колбы перемешивают и титруют из бюретки раствором серной кислоты (Сэ = 0,05моль/дм3) при слабом постоянном помешивании до тех пор, пока казеин не выпадет в осадок большими хлопьями. Для контроля полноты выпадения казеина определяют рН, пользуясь индикаторной бумажкой, ИТ казеина соответствует рН = 4,6,..4,7.
Объем раствора серной кислоты (Vк), пошедшей на осаждение казеина, записывают.
Через 3...5 мин после образования осадка казеина жидкость фильтруют через сухой складчатый фильтр в коническую колбу вместимостью 200 см3. Далее 50 см3 фильтрата мерной пипеткой переносят в коническую колбу вместимостью 100 см3; добавляют сюда 3...5 капель 1%-ного раствора фенолфталеина и титруют раствором гидроксида натрия (С, = 0,1 моль/дм3) до слабо-розового окрашивания, не исчезающего в течение 30 с.
Объем щелочи (V1,), пошедшей на титрование, записывают.
2 этап. В коническую колбу вместимостью 200 см3 пипеткой вносят 20 см3 молока, цилиндром - 80 см3 дистиллированной воды температурой 20°С, из бюретки - столько же серной кислоты (Сэ = 0,05 моль/дм3), сколько потребовалось на осаждение казеина на первом этапе, и 3...5 капель 1%-ного раствора фенолфталеина. Содержимое колбы, перемешивают и титруют раствором гидроксида натрия так же, как описано выше.
Объем раствора щелочи (V2), пошедшей на титрование, записывают.
Обработка результатов. Поскольку на первом этапе работы брали только 50 см3 фильтрата, то вначале рассчитывают объем щелочи (X), который пошел бы на титрование всего раствора (молоко + вода + кислота). Пользуются расчетной формулой,
![]()
где Vк - объем раствора серной кислоты, израсходованной на осаждение казеина, см3;
V1 - объем раствора гидроксида натрия, израсходованного на титрование 50 см3 фильтрата, см3;
50 - исходный объем раствора, см3.
Массовую долю казеина К (в %) рассчитывают по формуле.
![]()
где V2 - объем раствора гидроксида натрия, израсходованного на титрование на втором этапе работы, см3;
X - рассчитанный объем раствора гидроксида натрия, израсходованного на титрование на первом этапе, см1;
0,1131 — масса казеина, соответствующая 1 см3 раствора гидроксида натрия с эквивалентной концентрацией 0,1 моль/дм3, г;
m — объем молока, взятого на исследование, см3 (m = 20 см3).
Оформить результаты определения массовой доли казеина в исследуемых образцах молока, сделать выводы.



