Федеральное агентство по образованию
Государственное образовательное учреждение
высшего профессионального образования
Тульский государственный университет
Кафедра оборудование и технология сварочного и литейного производства
ФИЗИКО–ХИМИЧЕСКИЕ ОСНОВЫ ЛИТЕЙНОГО ПРОИЗВОДСТВА
Методические указания
по проведению практических занятий для студентов
направления: 150200 “Машиностроительные технологии и оборудование”
специальности: 150204 “Машины и технология литейного производства”
очной формы обучения
Тула 2005 г.
Разработал:
кандидат технических наук, доцент
ВВЕДЕНИЕ
Учебная дисциплина “Физико-химические основы литейного производства “ изучается студентами специальности 150204 в 9-ом семестре как продолжение курса “Термодинамические и физико-химические основы высокотемпературных металлургических процессов ”.
Практические занятия по этой дисциплине проводятся с целью более глубокого усвоения студентами материала, излагаемого в лекционном курсе, приобретения навыков определения основных термодинамических параметров и функций физико-химических процессов литейного производства.
При составлении методических указаний к практическим занятиям учтено, что студенты освоили основы программирования на ЭВМ.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ №1
ОПРЕДЕЛЕНИЕ ЭНТРОПИИ МОЛЯ ИДЕАЛЬНОГО ГАЗА ПРИ РАЗЛИЧНЫХ ПРОЦЕССАХ
1. Цель и задачи практического занятия.
Практическое ознакомление с методом определения энтропии моля идеального газа при различных процессах.
2. Основные теоретические положения.
Энтропия S является однозначной функцией состояния термодинамической системы: S = f /T, Р, V/. Изменение энтропии dS в равновесном изотермическом процессе равно отношению изменения теплоты системы dQ к температуре системы Т, т. е. dS = dQ / Т.
Неравновесные процессы в изолированной системе сопровождаются ростом энтропии, они приближают систему к состоянию равновесия, в котором энтропия максимальна.
Так как dS является полным дифференциалом, то изменение энтропии в любом физико-химическом процессе зависит только от начального и конечного состояния системы и не зависит от пути перехода: ∆S = S2 – S1.
Энтропия является аддитивной величиной, т. е. энтропия сложной системы равна сумме энтропий ее отдельных частей.
Основное уравнение для определения энтропии моля идеального газа dS= Cv* dT/ T+ R* dV/ V или
dS= Cv* dlnT+ R*dlnV (1)
Для изобарного процесса (p = const, dp = 0):
dS= Cv*dln T+ R*dln V; ![]()
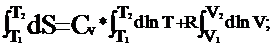
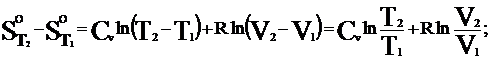
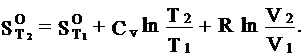
Так как при постоянном р для идеальных газов dT/ T= dV/V, то
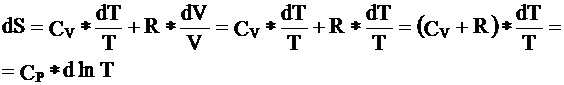
dS= CP* dlnT (2)
или
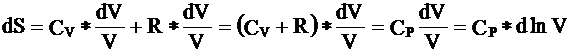
dS= CP*dlnV (3)
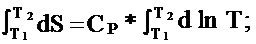
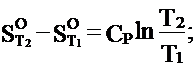
![]()
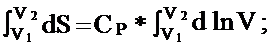
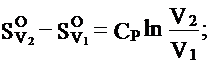
Для изохорного процесса / V= const, dV=0/:
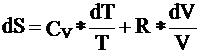
Так как dV= 0 , то
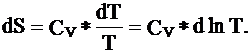 (4)
(4)
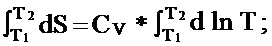
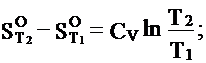
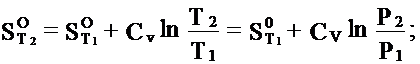
(из: рV= RT ; T=рV/ R= V/ R* р= const* р ).
Для изотермического процесса / T= const, dT= 0 /:
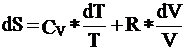 .
.
Так как dT= 0, то
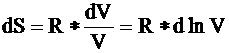 (5)
(5)
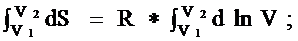
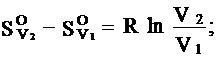
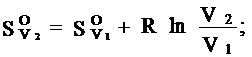
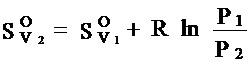 (6)
(6)
(из: pV= RT; RT= const; pV= p1V1= p2V2= const ; V2/ V1= p1/ p2).
3. Выполнение практической работы.
Задание: определить энтропию моля водорода как идеального газа при 1000 К и изменение энтропии ΔS0 = S01000 - S0298:
1- в изобарном процессе / p= 0,1МПа= const /;
2- в изохорном процессе / V0= 22, 43*10-3нм3 / моль Н2= const;
3- в изотермическом процессе / T= 1000 K= const / при повышении давления с 0,1 МН/м2 или при уменьшении объема в 10 раз.
Определение энтропии моля водорода при 1000 К и изменение его энтропии в интервале от 298 К до 1000 К выполняются:
в изобарном процессе по уравнению (1) или (2) , (3);
в изохорном процессе по уравнению (4);
в изотермическом процессе по уравнению (5) или (6), а также по справочным данным [2, 3].
Результаты определения объема водорода при 298 К, средней теплоемкости водорода в температурном интервале 298 К - 1000 К, энтропии водорода при 298 К, а также при 1000 К и изменение энтропии водорода в интервале от 298 К до 1000 К занести в табл.1.
Таблица 1
Процессы |
нм3/моль |
Дж/(моль*К) |
298-1000 К, Дж/(моль*К) | S01000, Дж/(моль*К) |
-S0298 , Дж/(моль*К) |
Изобарный | |||||
Изохорный | |||||
Изотерми- ческий |
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ № 2
ОПРЕДЕЛЕНИЕ ЭНТРОПИИ МОЛЯ ИДЕАЛЬНОГО
ГАЗА В СМЕСИ
1. Цель и задачи практического занятия.
Практическое ознакомление с методом определения энтропии моля идеального газа в смеси.
2. Основные теоретические положения.
Образование газовой смеси в результате самопроизвольного необратимого процесса взаимной диффузии исходных газов сопровождается увеличением энтропии:
ΔSсм=-R*(NA*lnNA+NB*lnNB) , (1)
ΔSсм = 4.69
где ΔSсм – изменение энтропии при смешивании газов А и В на один моль смеси этих газов, Дж/ (моль*К); R – универсальная газовая постоянная, R= 8,31434 Дж/моль*К; NA и NB – мольные доли компонентов А и В в газовой смеси:
NA=nA/nA+nB; NB=nB/nA+nB; NA+ NB=1
Для n молей газовой смеси:
ΔSсм=-n*R*(NA*lnNA+NB*lnNB) (2)
Энтропия моля газовой смеси равна:
Sсм=NA* SА+NB* SВ+ ΔSсм=
= NA* SА+NB* SВ –R*(NA*lnNA+NB*lnNB), (3)
ΔSсм=152
где SА и SВ – энтропия моля газа А и В соответственно, Дж/(моль*К).
Энтропия n молей газовой смеси:
Sсм=n*(NA* SА+NB* SВ+ ΔSсм)=
=n*[ NA* SА+NB* SВ –R*(NA*lnNA+NB*lnNB)] (4)
Для эквимолярной газовой смеси NA= NB= 0,5 и поэтому для нее ΔSсм
максимальна и составляет 5,77 Дж/(моль* К) – рис.2.1.
Для моля газовой смеси, содержащей любое число компонентов, Sсм равно:
ΔSсм=-R*(NA*lnNA+NB*lnNB + NС*lnNС +…) , (5)
где NA=nA/(nA+nB+nC+…); NB=nB/(nA+nB+nC +…);
NС=nС/(nA+nB+nC+…); NA+ NB +NC+…=1
Для n молей смеси, содержащей любое число компонентов, ΔSсм равно:
ΔSсм=-n*R*(NA*lnNA+NB*lnNB + NС*lnNС +…) (6)
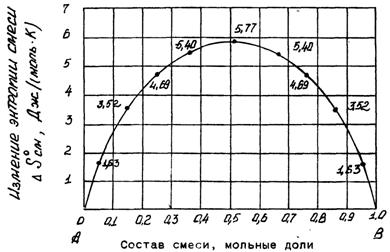
Рис.1. Зависимость изменения энтропии смеси идеальных газов
от состава смеси
3. Выполнение практической работы.
Задание: определить ΔSсм и энтропию Sсм моля газовой смеси, содержащей 0,25 доли окиси углерода СО и 0,75 мольной доли водорода Н2, при 1000К в изобарном процессе /р = 0,1 Мн/м2= const/. Такая смесь образуется при конверсии природного газа по реакции СН4+Н2О=СО+3Н2.
Определения ΔSсм и Sсм моля газовой смеси СО и Н2 при 1000К в изобарном процессе выполняются соответственно по уравнениям (1) и (3) после предварительного определения энтропии СО и Н2 при той же температуре по уравнению (1) или по уравнениям (2), (3) из практического занятия № 1, а также по справочным данным [2,3].
Результаты выбора и определения стандартных значения энтропии компонентов газовой смеси, энтропии этих компонентов при 1000К, а также ΔS0см и S0см при 1000К занести в табл.1.
Таблица 1
Процесс | Стандартнаяэнтропия ком-тов газовой смеси, Дж/(моль*К) | Энтропия ком-товгазовой смеси при 1000К, Дж/(моль*К) | ΔS0см, Дж/(моль*К) | S0см, Дж/ (моль*К) | ||
СО | H2 | СО | Н2 | |||
Изобарный | 197.54 | 130.57 | 234.43 | 166.14 | 4.69 | 152 |
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ № 3
РАСЧЕТЫ РАВНОВЕСИЯ ФИЗИКО-ХИМИЧЕСКИХ ПРОЦЕССОВ ЛИТЕЙНОГО ПРОИЗВОДСТВА С ПОМОЩЬЮ АБСОЛЮТНЫХ ЗНАЧЕНИЙ ЭНТАЛЬПИИ И ЭНТРОПИИ
1. Цель и задачи практического занятия.
Практическое ознакомление с методом расчетов равновесия физико-химических процессов литейного производства с помощью абсолютных значений энтальпии и энтропии.
2. Основные теоретические положения.
На основе экспериментальных и теоретических работ созданы справочные таблицы термодинамических свойств многих элементов и индивидуальных веществ (газов и химических соединений) для температур от 293К до 3000К и выше [4].
Изменение энергии Гиббса реакции аА+вВ=сС+dD при заданной температуре с использованием этих справочных данных определяют по следующему уравнению:
ΔG0T = ΔН0Т - ΔS0Т *T, (1)
где ΔGoT - изменение энергии Гиббса реакции при заданной температуре Т, Дж/моль; ΔН0Т - изменение энтальпии реакции при заданной температуре Т, Дж/моль; ΔS0Т - изменение энтропии реакции при заданной температуре Т, Дж/(моль*К); T - заданная температура реакции, К.
Изменение энтальпии реакции (тепловой эффект реакции) при заданной температуре Т определяют по уравнению:
ΔН0Т = сΔН0ТС + dΔН0ТD - a ΔН0ТA - bΔН0ТB, (2)
где А, В и C, D - исходные и конечные вещества реакции соответственно;
а, в и c, d - стехиометрические коэффициенты у исходных и конечных веществ реакции соответственно; ΔН0ТA, ΔН0ТB и ΔН0ТС, ΔН0ТD - полные энтальпии исходных и конечных веществ реакции соответственно, Дж/моль (в справочнике [4] полные энтальпии веществ обозначены как J0T);
ΔН0ТА= ΔН0f298A+( Н0ТA-Н0OA)-(Н0298A-Н0OA)=
= ΔН0f298A +( Н0ТA - Н0298A), (3)
где ΔН0f298A - теплота образования вещества А из простых веществ (например, Н2 из 2Н, Н20 из Н2 и 0,5 О2 и т. д.), Дж/моль; Н0OA - энтальпия вещества А при ОК, Дж/моль; Н0ТA-Н0OA -изменение энтальпии вещества А при повышении температуры от О до Т К, Дж/моль; Н0298A-Н0OA - изменение энтальпии вещества А при повышении температуры от 0 до 298 К, Дж/моль; Н0ТA - Н0298A -изменение энтальпии вещества А при повышении температуры от 298К до Т, Дж/моль.
Изменение энтропии реакции при заданной температуре:
ΔS0Т= cS0TC+ dS0ТD-aS0TA-bS0TB, (4)
где S0TA, S0TB, S0TC, S0ТD - энтропии исходных и конечных веществ реакции при заданной температуре соответственно, Дж/(моль*К).
При отрицательном значении ΔG0Т реакция идет слева направо, т. е. в cторону образования конечных веществ С и D, при положительном значении, наоборот - справа налево, т. е. в сторону исходных веществ А и В. Чем больше абсолютное значение ΔG0Т, тем более реакция смещена от положения равновесия. При ΔG0Т = 0 реакция находится в состоянии динамического равновесия.
Температура равновесия реакции:
ТРАВН = ΔН0Т /ΔS0Т (5)
Константа равновесия реакции определяется по уравнению:
lnКр = - ΔG0Т/ RT= -ΔG0Т/8,31434Т; (6)
lnКр = 2,30258 lgКр ; lgКр = lnКр/ 2,30258 ;
lgКр = - ΔG0Т/ 2,30258 RT = - ΔG0Т/ 19,14 Т (7)
3. Выполнение практической работы.
Задание: определить изменение энергии Гиббса, температуру равновесия и константу равновесия реакции конверсии природного газа СН4+Н2О = = СО+ЗН2 при 1000К в изобарном процессе (р= 0,1 Mн/м2 = const) с использованием справочных таблиц термодинамических свойств индивидуальных веществ [4].
Определение ΔН01000 реакции конверсии природного газа при 1000К выполняются по уравнению (2.2.), ΔS01000 - по (2.4.), ΔG01000 - по (2.1.) , ТРАВН - по (2.5.), Кр1000 -по (2.6.) или (2.7.).
Результаты определений изменения энтальпии, энтропии, энергии Гиббса, температуры равновесия и константы равновесия реакции конверсии природного газа при 1000К занести в табл.1.
Таблица 1
Реакция | ΔН01000, Дж/моль | ΔS01000, Дж/ (моль*К) | ΔG01000, Дж/моль | ТРАВН, К | Кр1000 | Направление реакции |
СН4+Н2О= СО+ЗН2 |
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ № 4
ОПРЕДЕЛЕНИЕ КОНСТАНТЫ РАВНОВЕСИЯ В ГОМОГЕННОЙ ГАЗОВОЙ СРЕДЕ И ВЫХОДА ПРОДУКТОВ РЕАКЦИИ
1. Цель и задачи практического занятия.
Практическое ознакомление с методом определения константы равновесия в гомогенной газовой среде и выхода продуктов реакции.
2. Основные теоретические положения.
Равновесным называется такое состояние системы, которое не изменяется во времени. Важнейшим из различных видов равновесных состояний в физико-химических процессах литейного производства является устойчивое динамическое равновесие. Оно устанавливается вследствие протекания процесса в двух противоположенных направлениях с одинаковой скоростью.
Условием устойчивого равновесия являются следующие соотношения:
dG= 0, d2G>0, (1)
отвечающие точкам минимума ΔG0т в физико-химическом процессе.
Различают гомогенные и гетерогенные реакции. Гомогенными называются такие реакции, в которых исходные и конечные вещества находятся в одной фазе. Простейшими из них являются газовые реакции.
Константа равновесия газовой реакции A+2B=3D+E выражаются уравнением lgКр=-ΔG0т /19,14*Т или через парциальные давления конечных и исходных газов:
Кр= РD3*РE /(РA*РB2), (2)
где РA, РB, РD, РE - парциальные давления газов A, B,D, E соответственно; РA+ РB+ РD+ РE =1 (в изобарных процессах).
Для реакций, протекающих без изменения числа молей, КР=КN=КС, где С - концентрация, равная n/ V.
Значение величины константы равновесия позволяют определять полноту протекания реакции:
при КР/КN, КC/>1-реакция смещена от положения равновесия вправо;
при Кр >>1 - система состоит в основном из продуктов реакции;
при КР <1 - реакция смещена от положения равновесия влево;
при КР<<1 - система состоит в основном из исходных веществ;
при КР = 1 - состояние динамического равновесия.
При подстановке в уравнение (2) вместо парциальных давлений газов мольных долей этих газов получаем:
Кр=ND 3*NE /(NA*NB2 ). (3)
Выход продуктов реакции можно определить по уравнению (3) после подстановки в него значения Кр, рассчитанного по (7) из практического занятия №3, и мольных долей конечных и исходных газов.
3.Выполнение практической работы.
Задание: определить константу равновесия гомогенной реакции Гана CO+ H2O= CO2 + H2, протекающей в сырой песчано-глинистой форме во время заливки ее металлом, при 1000К и выход продуктов реакции.
Определение константы равновесия КР1000 выполняется по уравнению (7), а выход продуктов реакции по уравнению (3) после подстановки в него КР1000 и мольных долей исходных и конечных газов из предварительно заполненной табл.1.
Таблица 1
Компоненты, моли | СО | Н2О | СО2 | Н2 |
Было до начала реакции | ||||
Ушло в реакцию | ||||
В реакции при 1000К | ||||
Общее число молей в реакции при 1000К | ||||
Мольные доли в реакции при 1000К |
Результаты определений ΔH01000, ΔS01000, ΔG01000, KР1000, nCO2, nH2, nCO, nH2O занести в табл.2.
Таблица 2
Реакция | ΔH01000, Дж/моль | ΔS01000, Дж/ (моль*К) | ΔG01000, Дж/ (моль*К) | KР1000 | nCO2, моль | nH2, моль | nCO, моль | nH2O, моль |
СО+ Н2О= СО2+ Н2 |
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ № 5
ОПРЕДЕЛЕНИЕ КОНСТАНТЫ РАВНОВЕСИЯ В ГЕТЕРОГЕННОЙ РЕАГИРУЮЩЕЙ СИСТЕМЕ И ВЫХОДА ПРОДУКТОВ РЕАКЦИИ
1. Цель и задачи практического занятия.
Практическое ознакомление с методом определения константы равновесия в гетерогенной реагирующей системе и выхода продуктов реакции.
2. Основные теоретические положения.
Гетерогенными называются такие системы, в которых содержится более одной фазы. В состав их могут входить фазы и в различных агрегатных состояниях.
Константа равновесия гетерогенной реакции вида AГ +BК=DК +ЕГ (индекс "к"- конденсированное состояние), как и любой другой реакции, определяется по уравнению LgKp= -ΔGТ/l9,14*Т, а также выражается через парциальные давления газовых фаз
Кр= РЕ /РА (1)
и мольные доли газовых фаз
КN= NЕ /NА (2)
Как и в случае гомогенных реакций, по значению константы равновесия гетерогенной реакции КP = КN можно рассчитать выход продуктов реакции.
3. Выполнение практической работы.
Задание: определить константу равновесия гетерогенной реакции взаимодействия паров воды с магнием и магниевыми сплавами при 1000К Мgж+Н2Ог =МgOт +Н2Г и выход продуктов этой реакции.
Определение ΔН01000 и ΔS01000 указанной выше реакции наиболее быстро можно выполнить с использованием справочных таблиц термодинамических свойств индивидуальных веществ [4], Кр1000 - по уравнению (7) из практического занятия №3 и выход продуктов реакции - по уравнению (2) после подстановки в него Кр1000 и мольных долей газовых фаз из предварительно заполненной табл.1.
Таблица 1
Компоненты, моли | Мgж | Н20г | Н2г | МgОг |
Было до реакции | ||||
Ушло в реакцию | ||||
В реакции при 1000К | ||||
Общее число молей газа в реакции при 1000К | ||||
Мольные доли газов в реакции при 1000К |
Результаты определений ΔН01000, ΔS01000, ΔG01000, Кр1000, nH2г, nМgОт, nН20г, Мgж занести в табл.2.
Таблица 2
Реакция | ΔН01000, | ΔS01000, | ΔG01000, | Кр1000, | nH2г, моль | nМgОт, моль | nМgж, моль | nН20г, моль |
Мgж+ Н2Ог = МgОт + Н2г |
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ № 6
ОПРЕДЕЛЕНИЕ ТЕМПЕРАТУР КИПЕНИЯ И КРИСТАЛЛИЗАЦИИ РАЗБАВЛЕННЫХ РАСТВОРОВ
1. Цель и задачи практического занятия.
Практическое ознакомление с методом определения температур кипения и кристаллизации разбавленных растворов.
2. Основные теоретические положения.
Температура кипения растворов определяется условием, при котором парциальное давление паров над раствором равно внешнему давлению. При постоянном внешнем давлении температура кипения зависит от концентрации раствора.
В соответствии с законом Рауля давление паров над раствором рi меньше, чем над чистым растворителем p0i(pi =p0i*N, где Ni - мольная доля растворителя).
Для повышения давления паров над раствором до внешнего давления необходимо поднять температуру раствора на ΔTкип (рис.1).
ΔTкип= (R*T2кип*А/ (Lкип*А)) *Nв, (1)
где ΔTкип - повышение температуры кипения раствора (А-В) по сравнению с температурой кипения растворителя (компонента) А, К; R- универсальная газовая постоянная (R = 8,31434 Дж/(моль*К)); Ткип А - температура кипения растворителя А, К; Lкип А - мольная теплота кипения (испарения) растворителя А; Nв - мольная доля растворенного вещества В в растворителе А.
Ткип (А-В) = Ткип А + ΔТкип. (2)
Кристаллизация раствора обычно происходит в интервале температур ТL-ТS. Температуру начала кристаллизации (температуру ликвидуса ТL) называют также температурой замерзания раствора Т3, когда она ниже комнатной температуры.
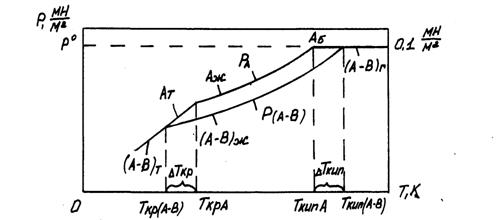
Рис.1. Повышение температуры кипения и понижение температуры кристаллизации растворов:
А - растворитель; В - растворенное вещество; /А-В/ - раствор; т, ж, г - твердое, жидкое и газообразное состояние вещества соответственно
Понижение температуры кристаллизации раствора пропорционально мольной доле в нем растворенного вещества (рис.1).
ΔTкр= (R*T2кр*А/ (Lкр*А)) *Nв, (3)
где ΔТкр - понижение температуры кристаллизации раствора (А-В) по сравнению с температурой кристаллизации растворителя А, К; ТкрА - температура кристаллизации растворителя А, К; LкpA - мольная теплота кристаллизации растворителя А, Дж/моль.
Ткр(А-В) = ТкрА -ΔТкр (4)
3. Выполнение практической работы.
Задание: определить температуру кипения и температуру начала кристаллизации сплава цинка с 5% (по массе) алюминия.
Определение Ткип и ТL сплава Zn - 5% AI выполняются соответственно по уравнениям (2) и (4) после предварительного перевода массовых процентов алюминия в мольную долю его в сплаве по уравнению
Nв= В% /[ В%+ (МВ/ МА)*А%], (5)
где МА и МВ - соответственно молекулярные масcы растворителя А и растворенного вещества В.
Рассчитанное значение температуры начала кристаллизации ТL сплава Zn – 5% А1 сравнить с TL на диаграмме состояния сплавов системы “Цинк-алюминий” [5] с определением погрешности расчетов в процентах.
Результаты определений ΔТкип, Ткип, ΔТкр, ТLэксп, ТLрасч и δTL для сплава Zn – 5% А1 занести в табл.1.
Таблица 1
Сплав | ΔТкип, К | Ткип, К | ΔТкр, К | ТLэксп, К | ТLрасч, К | δTL, % |
Zn – 5%Al |
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ № 7
ОПРЕДЕЛЕНИЕ РАСТВОРИМОСТИ ВОДОРОДА В ТВЕРДЫХ И ЖИДКИХ МЕТАЛЛАХ
1. Цель и задачи практического занятия.
Практическое ознакомление с методом определения растворимости водорода в твердых и жидких металлах.
2. Основные теоретические положения.
Зависимость растворимости водорода и других двухатомных газов, образующих с металлами эндотермические растворы внедрения, от температуры и давления выражается объединенным уравнением Сивертса и Борелиуса.
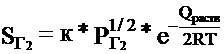 , (1)
, (1)
где SГ2 - растворимость двухатомного газа в металлах и сплавах, см3/100 г металла; к - константа, зависящая от свойств металла и газа; рг2 - парциальное давление двухатомного газа над металлом, H/м2; е - основание натуральных логарифмов (е = 2,718282); Qраств - теплота растворения моля двухатомного газа в металле, Дж/моль; R-универсальная газовая постоянная (R = 8,31434 Дж/моль* К); Т - абсолютная температура, К.
Наиболее часто уравнение (1) применяют в логарифмическом виде
lg Sг2= lgk+ 1/2 lgpг2- (Qраств/2RT)*lge;
lg Sг2= - (Qраств* lge /2R)*1/T+1/2 lgpг2+lgk;
lg Sг2= - А/Т+1/2 lgpг2+В (2)
где А и В - константы /А= (Qраств* lge /2R); В=lgk/.
Теплоты растворения моля водорода в твердом и жидком алюминии соответственно равны 79496 Дж/моль и 105667 Дж/моль.
Поэтому логарифмические уравнения для определения растворимости водорода в твердом и жидком алюминии принимают следующий вид:
lgSн2вAlт =- 2080/T+ 1/2 lgpн2- 1,712, (3)
lgSн2вAlж =- 2760/T+ 1/2 lgpн2- 0,296, (4)
где pн2 - парциальное давление водорода над металлом, Н/м2 (для изобарных процессов в обычных атмосферных условиях р равно 105 Н/м2 ).
При подстановке р =760 мм рт. ст. коэффициент В в уравнении (3) принимается равным - 0,652, а в уравнении (4) равным 1,356.
3. Выполнение практической работы.
Задание: определить растворимость водорода в твердом и жидком алюминии при температуре плавления, а также при Т3 =Тпл + 100К.
Определение растворимости водорода в твердом алюминии при температуре плавления выполняется по уравнению (3), а в жидком алюминии - по уравнению (4).
Результаты определения Sн2 в твердом и жидком алюминии занести в табл.1.
Таблица 1
Металл | Sн2, см3/100 г металла при | 1 Sн2ТплЖ/Sн2ТплТ | ||
ТплТ | ТплЖ | Тпл + 100К | ||
Al |
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
1. Васильев -химические основы литейного производства.- М.: Изд-во МГТУ, 1994.-320c.
2. Олкокк термохимия. - М.: Металлургия, 1982.- 392 с.
3. , Гуляницкий превращения металлургических реакций.- М.: Металлургия, 1975.-416 с.
4. Термодинамические свойства индивидуальных веществ. Т.2.Таблицы термодинамических свойств /, , и др.- М.: Издательство АН СССР, 1962. - 916 с.
5. и Структуры двойных сплавов. Т.1,2.-М.: Металлургиздат, 1962. - 1488 с.
Рассмотрено на заседании кафедры Нормоконтролер, ответственный
протокол № 1 от 30 августа 2005 г. по стандартизации на кафедре
Зав. кафедрой ____________ ______________



